خطر پیشرفت به سمت عقب
اصل کلی: پیگیری و مشاهده
اندیکاسیون لیزر باریکید: گسترش پیشرونده، نزدیکی به قطب خلفی
هدف درمان: جلوگیری از پیشرفت بیشتر به سمت عقب

رتینوشیزیس (retinoschisis) وضعیتی است که در آن شبکیه عصبی در لایه شبکهای داخلی یا خارجی جدا میشود. این بیماری از نظر پاتوفیزیولوژی با جداشدگی شبکیه که در آن لایه سلولهای گیرنده نور از لایه اپیتلیوم رنگدانهای جدا میشود، کاملاً متفاوت است.
| نوع بالینی | سن و جنس شایع | محل شایع | شیوع و بروز |
|---|---|---|---|
| رتینوشیزیس وابسته به سن (اکتسابی) | بالای ۴۰ سال؛ در هر دو جنس | ناحیه محیطی تحتانی-گیجگاهی (۷۰%) | ۷ تا ۳۰٪ افراد بالای ۴۰ سال |
| جداشدگی شبکیه وابسته به X (مادرزادی) | سن مدرسه؛ تقریباً فقط در مردان | فووآ (تقریباً در همه موارد) + محیطی (حدود نیمی از موارد) | یک نفر از هر ۵٬۰۰۰ تا ۲۵٬۰۰۰ نفر2) |
| جداشدگی مرکزی شبکیه در نزدیکبینی | میانسالی به بعد؛ نزدیکبینی شدید | قطب خلفی و ناحیه ماکولا | درصد مشخصی از چشمهای با نزدیکبینی شدید |
رتینوشیزیس وضعیتی است که در آن جداشدگی در «داخل لایه» شبکیه عصبی رخ میدهد و کاملاً با جداشدگی شبکیه (جداشدگی تمام لایه شبکیه از اپیتلیوم رنگدانهای) متفاوت است. در رتینوشیزیس، ارتباط با اپیتلیوم رنگدانهای شبکیه حفظ میشود، بنابراین پیشآگهی بینایی معمولاً بهتر از جداشدگی شبکیه است. با این حال، اگر در هر دو لایه داخلی و خارجی سوراخ ایجاد شود، ممکن است به جداشدگی شبکیه پیشرفت کند.
جداشدگی شبکیه مرتبط با سن، وضعیتی است که در آن دژنراسیون کیستیک فیزیولوژیک (کیستهای بلس-ایوانف) در شبکیه محیطی بزرگسالان، با هم ادغام و بزرگ شده و باعث جداشدگی در لایه شبکهای خارجی یا لایه دانهدار داخلی میشود.
شیوع آن ۱٫۶۵ تا ۷٪2) گزارش شده است، بیشتر در افراد بالای ۴۰ سال دیده میشود و در حدود ۷۰٪ موارد دوطرفه است. ۷۰٪ موارد در ناحیه تحتانی-گیجگاهی محیطی شبکیه رخ میدهد و سطح برجستگی صاف است. این وضعیت ارثی نیست و با افزایش سن ایجاد میشود.
رتینوشیز ثانویه ممکن است به دلیل غشاهای پرولیفراتیو، کشش زجاجیه، تغییرات کیستیک، خونریزی داخل شبکیه، اگزودا یا التهاب ایجاد شود. بیماریهای زمینهای خاص شامل رتینوپاتی دیابتی، جداشدگی مزمن شبکیه، دژنراسیون ماکولای وابسته به سن، رتینوپاتی نارسی (ROP) و بیماری کوتس هستند.
اکثر موارد بدون علامت هستند و پیشرفت به قطب خلفی نادر است؛ بینایی معمولاً طبیعی است. هنگامی که ضایعه از خط استوا عبور کند، ممکن است علائمی مانند نقص میدان بینایی ایجاد شود.
| یافته | ویژگی | اهمیت در تشخیص افتراقی |
|---|---|---|
| برآمدگی گنبدی شکل | نیمکرهای صاف و شفاف؛ ثابت و بیحرکت | با تغییر وضعیت بدن جابهجا نمیشود |
| ظاهر ابریشم آبی | درخشش موجدار لایه داخلی | مشخصه این بیماری |
| snowflakes (کدورتهای دانهبرفی) | کدورتهای دانهدار زرد-سفید در سطح داخلی لایه جدا شده | نشانگر دژنراسیون |
حتی اگر سوراخ لایه خارجی ایجاد شود و جداشدگی لایه خارجی شبکیه رخ دهد، خطر کم است. در صورت ایجاد سوراخ داخلی و خارجی و پیشرفت به جداشدگی، درمان جراحی مشابه جداشدگی معمولی شبکیه ناشی از پارگی ضروری است.
پاتوفیزیولوژی اصلی، همجوشی و گسترش تغییرات کیستیک در الیاف هنله لایه پلکسیفرم خارجی به دلیل افزایش سن است. مکانیسم اسکوتوم مطلق این است که جداشدگی بین لایهای در لایه پلکسیفرم خارجی منجر به پارگی بافتی در محل اتصالات سیناپسی شده و انتقال سیگنال تحریک نوری را مسدود میکند1).
عوامل خطر شامل افزایش سن و دوربینی هستند2). استعداد ژنتیکی شناسایی نشده است2).
تشخیص با OCT نقش اصلی را ایفا میکند2). گسترش، عمق حفره جداشدگی و ساختارهای ستونی عمودی بین لایهها (پلهای بافتی عمودی) را نشان میدهد و جداشدگی بین لایهای در لایه پلکسیفرم خارجی را مستقیماً تأیید میکند.
تشخیص افتراقی از جداشدگی شبکیه بسیار مهم است.
| ویژگی | رتینوشیزیس | جداشدگی شبکیه |
|---|---|---|
| تحرک برجستگی | ثابت و غیرمتحرک | با تغییر وضعیت حرکت میکند |
| شفافیت | بالا (شفاف) | پایین (کدر) |
| ماهیت اسکوتوم | اسکوتوم مطلق | اسکوتوم نسبی |
| ویژگی سطح | صاف (ابریشمی) | نامنظم و موجدار |
اصولاً پیگیری (تحت نظر داشتن) انجام میشود. خطر پیشرفت به جداشدگی شبکیه حدود ۰.۰۵٪ در سال است که پایین بوده و اکثر موارد بدون علامت و پایدار هستند.
خطر پیشرفت به سمت عقب
اصل کلی: پیگیری و مشاهده
اندیکاسیون لیزر باریکید: گسترش پیشرونده، نزدیکی به قطب خلفی
هدف درمان: جلوگیری از پیشرفت بیشتر به سمت عقب
تشکیل سوراخ لایه خارجی
اصل راهنما: پیگیری و مشاهده
نکته مهم: پارگی لایه خارجی خطر جداشدگی را افزایش میدهد
ارزیابی دقیق اندیکاسیون: در صورت وجود همزمان سوراخ لایه داخلی باید احتیاط کرد
جداشدگی ناشی از رتینوشیزیس
اصل کلی: جراحی مشابه جداشدگی معمولی شبکیه (رگماتوژن)
اندیکاسیون جراحی: در صورت ایجاد سوراخ در هر دو لایه داخلی و خارجی و پیشرفت جداشدگی
پیشآگهی: به طور کلی خوب
مورد نفوذ ماکولا
اصل درمان: بررسی جراحی ویترکتومی
روش جراحی: جداسازی ILM + تزریق گاز
شواهد: سطح گزارش موردی1)
جدایی بین لایهها در لایه شبکهای خارجی منجر به پارگی بافتی در محل اتصالات سیناپسی میشود و اسکوتوم مطلق ایجاد میکند1). تصور میشود که الیاف هنله به دلیل همجوشی دژنراسیون کیستیک مرتبط با افزایش سن از هم جدا میشوند و این علت جدایی است. ارزیابی سهبعدی با SD-OCT امکان اندازهگیری دقیق گسترش حفره جدایی و نازکشدن لایههای داخلی و خارجی را فراهم کرده است و شناسایی سیر طبیعی طولانیمدت و عوامل پیشبینیکننده پیشرفت در حال پیشرفت است2).
در رتینوشیزیس وابسته به سن، جدایی بین لایهها در لایه شبکهای خارجی رخ میدهد. در این ناحیه، اتصالات سیناپسی بین سلولهای گیرنده نور و سلولهای گانگلیونی وجود دارد و اگر سیناپسها به دلیل جدایی قطع شوند، تحریک نوری به سلولهای دوقطبی و گانگلیونی منتقل نمیشود1). بنابراین، در ناحیه جدایی، حتی با تابش نور، سیگنال الکتریکی هدایت نمیشود و به صورت اسکوتوم مطلق احساس میشود.
بیشتر موارد جداشدگی شبکیه وابسته به سن سیر پایدار دارند. خطر پیشرفت به جداشدگی شبکیه بسیار کم و حدود ۰٫۰۵٪ در سال است. با این حال، در صورت ایجاد سوراخ در هر دو لایه داخلی و خارجی، خطر جداشدگی افزایش مییابد، بنابراین پیگیری منظم با معاینه فوندوسکوپی مهم است2).
جداشدگی شبکیه وابسته به X (XLRS) یک بیماری مادرزادی شبکیه با وراثت مغلوب وابسته به X ناشی از جهش در ژن RS1 است. این یک بیماری نادر دژنراتیو زجاجیهای-شبکیهای است که شیوع آن ۱ در ۵۰۰۰ تا ۲۵۰۰۰ نفر تخمین زده میشود2). معمولاً فقط مردان مبتلا میشوند و زنان ناقل هستند.
معمولاً فقط مردان مبتلا میشوند. از آنجا که این بیماری با وراثت مغلوب وابسته به X منتقل میشود، زنانی که تنها در یک کروموزوم X جهش دارند، ناقل بوده و معمولاً بدون علامت هستند. به ندرت، به دلیل عدم تعادل در غیرفعالسازی کروموزوم X یا دیزومی تکوالدی، فنوتیپ خفیف در زنان نیز گزارش شده است2).
علائم ذهنی:
یافتههای بالینی:
یافتههای ناحیه ماکولا
جداشدگی حفرهای (تقریباً در همه موارد): تغییرات کیستیک همراه با چینهای شعاعی (کیستها و ساختارهای پلمانند در OCT)
آتروفی ماکولا: با افزایش سن، تغییرات کیستیک消退 و به آتروفی تبدیل میشوند؛ در بسیاری از موارد شبیه ادم ماکولای کیستیک ساده به نظر میرسد
آنژیوگرافی فلورسئین: برخلاف ادم ماکولای کیستیک، نشت فلورسئین وجود ندارد (فووآ طبیعی است یا نقص پنجرهای دارد)
یافتههای محیطی
جداشدگی شبکیه محیطی (حدود نیمی از موارد): شایع در ناحیه تحتانی-گیجگاهی؛ ممکن است با سوراخ بزرگ داخل شبکیه همراه باشد
رفلکس طلایی: یافته مشخص در شبکیه محیطی؛ همراه با سفید شدن رگهای شبکیه
حجاب زجاجیه: در موارد شدید دیده میشود؛ زجاجیه جدا نشده و به شدت به شبکیه چسبیده است
عوارض: جداشدگی شبکیه (۵-۲۰٪)، خونریزی زجاجیه، خونریزی درون حفره جداشدگی
در صورت مشاهده ادم ماکولار کیستیک دوطرفه در پسران، باید به این بیماری مشکوک شد که نقطه شروع مهمی برای تشخیص است.
تشخیص افتراقی:
| بیماری | نکات افتراقی |
|---|---|
| جداشدگی شبکیه رگماتوژن | معمولاً یک طرفه؛ تشکیل خط مرزی؛ همراه با دژنراسیون لتیس |
| ادم ماکولای کیستیک | نشت گلبرگی در آنژیوگرافی فلورسین؛ در XLRS نشتی وجود ندارد |
| جداشدگی شبکیه وابسته به سن (دژنراتیو) | در افراد مسن رخ میدهد؛ محدود به محیط؛ موج b طبیعی |
| سندرم گلدمن-فاور | همراه با شبکوری و رسوب رنگدانه |
در ادم ماکولار کیستیک (CME)، آنژیوگرافی فلورسئین نشت و تجمع فلورسئین به شکل گلبرگ را نشان میدهد. در مقابل، در XLRS حفرههای جداشدگی فووئال وجود دارد اما سد خونی-شبکیه طبیعی است و در آنژیوگرافی فلورسئین نشتی دیده نمیشود و تنها نقص پنجرهای (window defect) مشاهده میگردد. این تفاوت در تشخیص افتراقی با ترکیب OCT و آنژیوگرافی فلورسئین اهمیت دارد.
هیچ درمان قطعی و اثباتشدهای وجود ندارد.
دارودرمانی:
درمان جراحی:
مدیریت بیمار:
با رشد، تغییرات کیستیک در ناحیه فووآ ممکن است به طور خودبهخود کاهش یابد2). با این حال، برخی موارد به آتروفی ماکولا تبدیل میشوند و کاهش لزوماً به معنای بهبود بینایی نیست. در برخی موارد، پس از ایجاد جداشدگی خلفی زجاجیه، جداشدگی محیطی کاهش یافته است.
رتینوشیزین، پروتئین ترشحی کدگذاریشده توسط ژن RS1، از ۲۲۴ اسید آمینه تشکیل شده و از طریق دامنه دیسکوئیدین، کمپلکسهای هماولیگومری را تشکیل میدهد 2). این پروتئین با اتصال به سلولهای گیرنده نور و سلولهای دوقطبی، یکپارچگی ساختاری و سیناپسی شبکیه را حفظ میکند. جهش در RS1 باعث فروپاشی کمپلکس شده و منجر به ایجاد حفرههای جداشدگی مشخص و اختلال در انتقال سیگنال شبکیه میشود 2).
از نظر هیستوپاتولوژی، جداشدگی شبکیه عمدتاً در لایه فیبرهای عصبی رخ میدهد. در OCT، جداشدگی در لایه شبکهای خارجی و لایه گرانولار داخلی در ناحیه فووه و اطراف آن مشاهده میشود. حتی اگر جداشدگی مورفولوژیک محدود باشد، الکتروفیزیولوژی وجود اختلال عملکردی در کل شبکیه را نشان میدهد که با موج b منفی مشخص میشود.
همبستگی ژنوتیپ-فنوتیپ (کوهورت ۸۳ نفری کرهای، Lee et al. 2025) 2):
در مطالعهای که مایع حفره جداشدگی در XLRS را تحلیل کرد، پروتئین متصلشونده به رتینوئید بین گیرندههای نوری (IRBP) در مایع حفره شناسایی شد که نشاندهنده اختلال متابولیسم شبکیه در داخل حفره است 2). همچنین مواردی از ماکولوپاتی اگزوداتیو که معمولاً در XLRS دیده نمیشود، گزارش شده است که وجود فنوتیپهای متنوع تحت یک تشخیص را نشان میدهد 2).
ژن درمانی RS1 در حال انجام کارآزمایی بالینی است2)3). در مدلهای حیوانی و کارآزماییهای بالینی اولیه، بهبود نسبی پاسخ الکترورتینوگرام و بهبود آناتومی شبکیه گزارش شده است.
کارآزماییهای بالینی اصلی:
چالش فعلی: در XLRS، شکنندگی شبکیه افزایش یافته و جداشدن غشای زجاجیه خلفی و تزریق زیر شبکیه از نظر فنی بسیار دشوار است 3). تزریق داخل زجاجیه ممکن است ترجیح داده شود، اما باید خطر التهاب زجاجیه را پذیرفت.
ژن درمانی برای XLRS هنوز در مرحله کارآزمایی بالینی است و به عنوان درمان در بیمارستانهای عمومی تأیید نشده است. برخی کارآزماییهای بالینی چالشهای ایمنی مانند التهاب داخل چشمی را آشکار کردهاند و برخی مطالعات متوقف شدهاند 3). برای شرکت در این مطالعات، مشاوره با مراکز تخصصی ضروری است.
جداشدگی لایههای داخلی شبکیه در ناحیه فووآ (myopic foveoschisis) یک جداشدگی لایههای داخلی شبکیه در قطب خلفی چشم است که با نزدیکبینی شدید همراه است. این وضعیت از دیرباز به عنوان جداشدگی شبکیه قطب خلفی همراه با نزدیکبینی شدید توصیف شده است و امروزه موارد همراه با سوراخ ماکولا را نیز شامل میشود.
عوامل زیر به طور ترکیبی در پاتوفیزیولوژی نقش دارند:
علائم: کاهش بینایی، اسکوتوم مرکزی، دگرسانیبینی (metamorphopsia)، تیرگی دید. در نزدیکبینی شدید، ممکن است علائم کمی وجود داشته باشد.
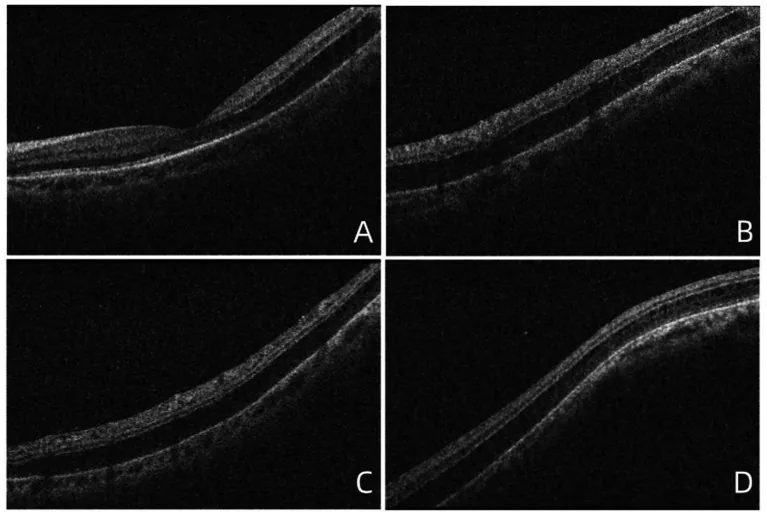
تشخیص (OCT):
درمان: جراحی ویتره (ویترکتومی) اساس درمان است.
پیشآگهی: