망막분리증은 신경망막 이 내망상층 또는 외망상층에서 분리된 상태로, 망막박리 (시세포 층이 색소상피층에서 박리)와는 병태가 다릅니다.
세 가지 유형이 있습니다. ① 연령 관련성(40세 이상의 730%에서 발생, 70%가 아래관자쪽 주변부에 호발), ② X-연관성(남아/학령기, 5,00025,000명 중 1명), ③ 근시 성 중심와 분리증(고도 근시 안).
연령 관련성 망막분리증은 대부분 무증상으로 경과 관찰만 하며, 망막박리 로 진행할 위험은 연간 약 0.05%로 매우 낮습니다 2) .
X-연관성 망막분리증(XLRS)은 RS1 유전자 돌연변이에 의한 X-연관 열성 유전 질환입니다. ERG 에서 음성 b파(b파 진폭 < a파)가 진단에 특징적입니다 2) .
XLRS에 대해 탄산탈수효소 억제제(도르졸라미드 점 안액, 아세타졸라미드 경구)로 분리강 개선이 보고되었으나, 확립된 근치 치료법은 없습니다.
근시 성 중심와 분리증은 고도근시 안에서 발생하며, 유리체절제술 (ILM 박리)이 기본 치료입니다.XLRS에 대한 RS1 유전자 치료 는 임상시험 단계에 있으며, 안내 염증 등의 안전성 문제가 남아 있습니다3) .
망막분리증은 신경망막 이 내망상층 또는 외망상층에서 분리된 상태입니다. 시세포 층이 색소상피층에서 박리되는 망막박리 와는 병태가 근본적으로 다릅니다.
병형 호발 연령 및 성별 호발 부위 유병률/발생률 연령 관련(후천성) 망막분리증 40세 이상; 남녀 모두 아래관자쪽 주변부(70%) 40세 이상의 7~30% X-연관(선천성) 망막분리증 학령기; 거의 남성만 중심와 (거의 모든 경우) + 주변부(약 절반)5,000~25,000명당 1명2) 근시 성 중심와 분리증중년 이후; 고도 근시 후극부, 황반부 고도 근시 안의 일정 비율
Q
망막분리증과 망막박리는 다른 질환인가요?
A
망막분리증은 신경망막 의 ‘층 내’에서 분리가 발생하는 병태이며, 망막박리 (망막 전층이 색소상피에서 박리)와는 완전히 다릅니다. 분리증에서는 망막색소상피 와의 연결이 유지되므로 망막박리 에 비해 시력 예후가 일반적으로 좋습니다. 그러나 내외 두 층에 구멍이 생기면 망막박리 로 진행할 가능성이 있습니다.
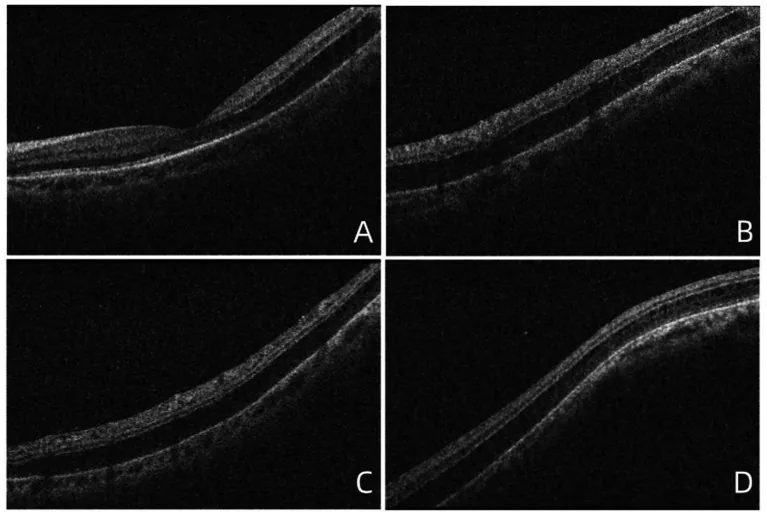
망막분리증의 OCT 영상 Wang N, et al. Case Report: A case of unexplained retinoschisis. Front Med (Lausanne). 2025. Figure 1. PM
CI D: PMC12518284. License: CC BY.
OCT 영상은 망막분리증을 보여줍니다: (A) 황반부 외망상층의 분리, (B) 상측 망막 혈관궁 근처의 분리, (C) 하측 망막 혈관궁 근처의 분리, (D) 황반 이측의 망막 분리. 이는 본문 “2. 후천성(연령 관련) 망막분리증” 항목에서 다루는 망막 분리에 해당합니다.
연령 관련 망막분리증 은 성인 주변부 망막 의 생리적 낭포성 변성(Blessig-Iwanoff 낭포)이 융합 및 확장되어 외망상층 또는 내과립층에 분리가 발생하는 병태입니다.
유병률은 1.65~7%2) 로 보고되며, 40세 이상에서 흔하고 약 70%에서 양안성입니다. 70%가 하이측 망막 주변부에 호발하며, 융기 표면은 매끄럽습니다. 유전성은 없으며 노화에 따라 발생합니다.
이차성 망막분리증은 증식막 , 유리체 견인, 낭성 변화, 망막 내 출혈, 삼출 또는 염증에 의해 발생할 수 있습니다. 구체적인 원인 질환으로는 당뇨망막병증 , 오래된 망막박리 , 연령관련 황반 변성, 미숙아 망막병증 (ROP ), 코츠병 이 알려져 있습니다.
대부분 무증상이며, 후극부까지 진행하는 경우는 드물고 시력 은 정상인 경우가 많습니다. 병변이 적도부를 넘으면 시야 결손 등의 자각 증상이 나타날 수 있습니다.
소견 특징 감별 진단의 의의 돔 모양 융기 매끄럽고 투명한 반구형; 고정되어 움직이지 않음 체위 변경 시 이동하지 않음 물결 비단 모양 내층의 물결치는 광택 본 질환의 특징적 소견 눈송이 모양 혼탁 (snowflake opacities) 분리층 내층 표면의 황백색 과립상 혼탁 변성 지표
외층공이 발생하여 외층 망막박리 가 생겨도 위험성은 낮습니다. 내·외층공이 생겨 박리로 진행된 경우에는 일반적인 열공성 망막박리 에 대한 수술적 치료가 필요합니다.
노화로 인한 외망상층의 Henle 섬유의 낭포성 변성이 융합·확대되는 것이 주요 병태입니다. 절대 암점 의 기전은 외망상층에서의 층간 분리가 시냅스 연결부의 조직 파열을 초래하여 광자극의 신호 전달이 차단되기 때문입니다1) .
위험 요인으로는 노화와 원시 가 있습니다2) . 유전적 소인은 확인되지 않았습니다2) .
OCT 진단2) . 분리강의 범위, 깊이, 층 사이의 기둥 구조(수직 조직 다리)를 묘사하여 외망상층에서의 층간 분리를 직접 확인할 수 있습니다.
망막박리 와의 감별
특징 망막분리증 망막박리 융기의 이동성 고정, 부동 체위 변경 시 이동 투명도 높음(투명) 낮음(혼탁) 암점 의 성질 절대 암점 상대 암점 표면 성상 매끄러움 (물결 모양) 불규칙, 물결 모양
원칙적으로 경과 관찰입니다. 망막박리 로 진행될 위험은 연간 약 0.05%로 낮으며, 대부분의 증례는 무증상으로 안정적입니다.
배리어 레이저 광응고술 : 후방 진행을 막기 위해 시행합니다. 적응증은 진행성 확대, 후방 경계가 후극에 근접, 내외층 모두 열공이 있는 경우입니다.황반 침윤 예의 유리체 절제술유리체 절제술(ILM 박리, 가스 충전)로 시력 개선이 얻어졌습니다1) . 황반부 로 진행된 증례에서는 수술이 선택지가 됩니다.
후방 진행 위험
기본 방침 : 경과 관찰
배리케이드 레이저 적응증 : 진행성 확대, 후극으로의 접근
치료 목적 : 추가 후방 진행 차단
외층 열공 형성
기본 방침 : 경과 관찰
주의점 : 외층 열공은 박리 위험을 높임
적응증을 신중히 평가 : 내층 구멍이 동시에 있는 경우 주의 필요
분리증성 박리
기본 방침 : 일반적인 열공성 망막박리 에 준한 수술
수술 적응증 : 내·외 양층에 구멍이 생기고 박리가 진행된 경우
예후 : 일반적으로 양호
황반 침범 예
기본 방침 : 유리체 절제술 고려
수술 방법 : ILM 박리 + 가스 충전
근거 : 증례 보고 수준1)
외망상층에서의 층간 분리는 시냅스 연결부에서 조직 파열을 초래하여 절대 암점 을 유발합니다1) . Henle 섬유가 노화 관련 낭포성 변성의 융합으로 인해 분리되는 것이 분리의 원인으로 생각됩니다. SD-OCT 를 이용한 3차원 평가로 분리강의 범위와 내외층의 얇아짐을 정밀하게 평가할 수 있게 되어 장기적인 자연 경과와 진행 예측 인자의 규명이 진행되고 있습니다2) .
Q
절대 암점이 왜 발생하나요?
A
노화 관련 망막분리증에서는 외망상층에서 층간 분리가 발생합니다. 이 부위에는 광수용체와 신경절 세포 사이의 시냅스 연결이 존재하며, 분리로 인해 시냅스가 단절되면 빛 자극이 양극 세포와 신경절 세포로 전달되지 않습니다1) . 따라서 분리 영역에서는 빛을 비추어도 전기 신호가 전도되지 않아 절대 암점 으로 인지됩니다.
Q
노화 관련 망막분리증은 앞으로 반드시 악화되나요?
A
대부분의 노화 관련 망막분리증은 안정적인 경과를 보입니다. 망막박리 로 진행될 위험은 연간 약 0.05%로 매우 낮습니다. 그러나 내외 두 층 모두에 구멍이 생기면 박리 위험이 증가하므로 정기적인 안저 검사를 통한 경과 관찰이 중요합니다2) .
X-연관 망막분리증(XLRS)은 RS1 유전자 돌연변이에 의한 X-염색체 열성 유전의 선천성 망막 질환입니다. 비교적 드문 유리체 망막 변성 질환으로, 유병률은 5,000~25,000명당 1명으로 알려져 있습니다2) . 일반적으로 남성만 발병하고 여성은 보인자가 됩니다.
원인 유전자 : RS1 유전자 (Xp22.2) 2) 코드 단백질 : 레티노스키신 (retinoschisin; RS)기능 : 광수용체와 양극 세포에서 발현되는 세포외 기질 단백질; 동종올리고머 복합체를 형성하여 세포 부착, 시냅스 형성, 망막 분화 및 기능에 중요한 역할을 합니다2) 돌연변이 수 : 200개 이상의 질병 원인 돌연변이가 확인됨표현형 : 표현형의 다양성이 현저함; 동일 돌연변이 내에서도 중증도가 다름; 비증후군성 질환(망막 에만 국한)
Q
여성이 X-연관 망막분리증에 걸릴 수 있나요?
A
일반적으로 남성만 발병합니다. X-연관 열성 유전이므로, 여성은 하나의 X 염색체에만 돌연변이가 있으면 보인자가 되어 보통 무증상입니다. 드물게 X 염색체 불활성화의 편향이나 단친 이염색체성으로 인해 여성에서도 경미한 표현형이 나타날 수 있다고 보고되었습니다2) .
자각 증상 :
시력 저하10세경)에 시력 저하(0.30.8 정도)를 자각하는 경우가 많습니다2) . 중증 예에서는 출생 후부터 시력 이 나쁩니다.원시 가 많은 것으로 알려져 있음; 약시 , 사시 , 안진 (영아기~취학 전에 나타날 수 있음).시력 0.6 정도면 일반 대학 진학이 가능. 나이가 들면서 황반 위축이 오면 시력 0.1로 저하.중등도 시력 (0.2~0.7)을 장기간 유지하는 경우가 많음.
임상 소견 :
황반부 소견
중심와 분리(거의 전례)OCT 상 낭종과 교량 구조).
황반 위축황반 부종처럼 보이는 경우가 많음
형광 조영술 : 낭포성 황반 부종과 달리 형광 누출 없음 (중심와 는 정상 또는 window defect)
주변부 소견
주변부 망막 분리 (약 절반): 아래관자쪽에 호발; 큰 망막 내층 구멍을 동반할 수 있음
금박 반사 : 주변 망막 의 특징적 소견; 망막 혈관의 백선화를 동반함
유리체 베일유리체 는 박리되지 않고 망막 에 강하게 부착됨
합병증 : 망막박리 (5~20%), 유리체출혈 , 분리강내출혈
유전적 배경 : RS1 유전자 돌연변이로 인한 레티노스키신의 동종올리고머 복합체 붕괴가 특징적인 분리강과 망막 신호전달 장애를 초래합니다2) 합병증 위험 :
망막박리 (내층공이 전층공으로 진행; 증례의 5~20%)유리체출혈 (망막 분리 진행으로 혈관 파열; 신생아의 유리체출혈 은 본 질환을 의심하는 계기가 됩니다)2) 약시 (유리체 출혈 또는 수술 후 형태감각 차단으로 인한)
남아 양안의 낭포성 황반 부종이 보이면 본 질환을 의심 하는 것이 중요한 진단의 첫걸음입니다.
OCT 중심와 낭종, 교량 구조(기둥 모양의 뮐러 세포 잔해), 분리 범위를 평가합니다. 한국인 83명의 코호트 연구에서 SD-OCT , ffERG , 안저 사진의 종합 평가가 유용한 것으로 보고되었습니다2) ERG (망막전위도 )2) . a파는 보존되지만 b파 진폭이 a파보다 작음(음성 b파); 유아기부터 나타나며 안저 전체의 망막 중층 기능 장애를 반영; 일부 환자에서는 정상~준정상 파형을 보임.형광 안저 조영술 : 낭포성 황반 부종과의 감별에 유용; XLRS에서는 꽃잎 모양의 형광 누출 없음.유전자 검사 : RS1 유전자 변이 분석으로 확진; 200개 이상의 질병 원인 변이가 확인됨.
감별 진단 :
질환 감별 포인트 열공성 망막박리 보통 단안성; 경계선 형성; 격자변성 동반 낭포황반부종 형광조영술에서 꽃잎모양 누출; XLRS에서는 누출 없음 연령 관련(변성성) 망막분리증 노인에서 발생; 주변부 국한; b파 정상 Goldman-Favre 증후군 야맹 및 색소 침착 동반
Q
낭포황반부종과의 차이점은 무엇인가?
A
낭포황반부종 (CME )에서는 형광안저조영술 에서 꽃잎 모양의 형광 누출 및 저류가 관찰됩니다. 반면 XLRS에서는 중심와 의 분리강이 존재하지만 혈액-망막 장벽 은 정상이며, 형광조영술에서 누출이 없고 창문 결손(window defect)만 나타납니다. 이 차이는 OCT 와 형광조영술을 결합한 감별 진단에서 중요합니다.
확립된 근치 치료법은 없습니다.
약물 요법 :
탄산탈수효소 억제제(CAI) : OCT 상 분리강을 개선시키는 효과가 보고됨
도르졸라미드 점 안액(국소 투여)아세타졸라미드 경구(전신 투여)효과에는 개인차가 있으며, 시력 과 OCT 상 낭포성 액체의 변화로 모니터링 필요
외과적 치료 :
유리체절제술
주변부 망막 분리가 망막박리 로 진행된 경우 (주요 적응증)
중심와 큰 낭종의 편평화 (시력 및 ERG 개선 기대 어려움)후유리체박리 유발 (향후 주변부 망막 분리 예방 가능성)소아에서는 유리체 와 망막 이 광범위하게 유착되어 수술이 위험하므로 신중히 적응증 판단
공막 돌륭술망막박리 예에 적용레이저 광응고술 : 망막박리 예방 목적으로 고려될 수 있으나, 의인성 열공의 위험이 있어 논란이 있습니다.
환자 관리 :
10세 미만: 소아안과 전문의 또는 망막 전문의에 의한 연 1회 이상 정기 평가.
약시 치료원시 , 유리체 출혈, 수술 후 약시 가 발생한 경우 안경 처방 및 가림 요법 .저시력 관리 유전 상담
아세타졸아미드 경구 복용은 전해질 이상, 신석회화, 혈구 감소 등의 전신 부작용을 일으킬 수 있습니다. 장기 복용 시 정기적인 혈액 검사가 필요합니다.
유리체 절제술은 시력 이나 ERG 의 근본적인 개선을 기대하기 어려운 경우가 많습니다. 수술의 목적과 기대할 수 있는 결과에 대해 수술 전 충분한 설명이 필요합니다.미성년 환자는 망막 과 유리체 의 유착이 강하여 수술 위험이 성인보다 높습니다.
Q
나이가 들면 분리가 사라지나요?
A
성장과 함께 중심와 의 낭포양 변화가 자연적으로 감소하는 경우가 있습니다2) . 그러나 황반 위축으로 이행하는 예도 있어, 소실이 반드시 시력 개선을 의미하지는 않습니다. 일부 증례에서는 후유리체 박리 발생 후 주변부 분리가 감소하기도 한다고 보고되었습니다.
RS1 유전자가 코딩하는 레티노스키신은 224개의 아미노산으로 구성된 분비 단백질로, 디스코이딘 도메인을 통해 동종 올리고머 복합체를 형성합니다2) . 광수용체와 양극세포에 결합하여 망막 의 구조적 및 시냅스 완전성을 유지합니다. RS1 돌연변이로 인해 복합체가 붕괴되면 특징적인 분리강과 망막 신호전달 장애가 발생합니다2) .
조직병리학적으로 망막 분리는 주로 신경섬유층에서 발생합니다. OCT 에서는 중심와 와 그 주변에서 외망상층과 내과립층의 분리가 관찰됩니다. 형태학적 분리가 국한되어 있더라도 전기생리학적으로는 망막 전체의 기능 장애가 존재하며, 이는 음성 b파로 나타납니다.
유전자형-표현형 상관관계 (한국인 83명 코호트, Lee et al. 2025)2) :
RS1 단백질 분비 능력을 가진 돌연변이군은 비분비군보다 최종 BCVA가 유의하게 우수함 (P=0.021)
비분비군에서 타원체대 (EZ ) 손상 빈도가 유의하게 높음 (P=0.030)
절단 변이와 미스센스 변이 간 BCVA, OCT , ERG 매개변수에 유의한 차이 없음
RS1 단백질의 분비 능력이 변이 유형보다 표현형을 결정하는 중요한 요인이 될 수 있음
XLRS의 분리강액을 분석한 연구에서 광수용체간 레티노이드 결합 단백질(IRBP)이 분리강액에서 확인되었으며, 분리강 내 망막 대사 이상 가능성이 보고되었습니다2) . 또한 XLRS에서 일반적으로 나타나지 않는 삼출성 황반 병증이 동반된 사례도 보고되어, 동일 진단 하에 다양한 표현형이 존재함을 시사합니다2) .
RS1 유전자 치료 의 임상 시험이 진행 중입니다2) 3) . 동물 모델 및 초기 임상 시험에서 망막 전도도 반응의 부분적 회복과 망막 해부학적 개선이 보고되었습니다.
주요 임상 시험:
NEI 시험(NCT 02317887) : AAV-RS1 벡터의 유리체 내 투여 안전성 평가. 고용량 투여군 1례에서 분리강 폐쇄가 관찰되었으나, 안내 염증도 유발되었습니다.AGTC 시험(NCT 02416622) : rAAV2tYF-CB-hRS1 벡터의 안전성 및 유효성 시험. 염증 발생과 임상적 치료 효과 부족으로 시험이 중단되었습니다. 고용량군을 중심으로 투여 후 초기 안내 염증이 관찰되어 안전성 측면에서 과제가 남아 있습니다3) .
현재 과제: XLRS에서는 망막 취약성이 증가하여 후유리체 막 박리와 망막 하 주사가 기술적으로 매우 어렵습니다3) . 유리체 내 투여가 바람직할 수 있지만, 유리체 염의 위험을 감수해야 합니다.
Q
유전자 치료를 현재 받을 수 있나요?
A
XLRS에 대한 유전자 치료 는 아직 임상 시험 단계에 있으며, 일반 병원에서의 치료로 승인되지 않았습니다. 일부 임상 시험에서는 안내 염증 등의 안전성 문제가 밝혀져 일부 시험이 중단되었습니다3) . 참여를 원할 경우 전문 기관에 상담이 필요합니다.
근시 성 망막 중심와 분리증(myopic foveoschisis)은 고도 근시 안에 동반된 후극부 망막 내층 분리입니다. 오래전부터 고도 근시 안에 동반된 후극부 망막 박리로 기술되었으며, 현재는 황반 원공을 동반하는 경우도 포함하는 개념입니다.
병태에는 다음 요소가 복합적으로 관여합니다:
안축 연장 및 후부 포도종 형성망막 이 늘어나고 안쪽으로 당기는 힘이 작용합니다.유리체 , 내경계막 (ILM ) 및 망막 혈관의 견인유리체 막, 경화된 내경계막 및 적도부에 비해 상대적으로 짧은 망막 혈관이 후극부의 망막 내층을 잡아당기는 방향으로 작용합니다.
자각 증상 : 시력 저하, 중심 암점 , 변시증 (metamorphopsia), 안개시. 고도 근시 에서는 자각 증상이 미미할 수 있습니다.
진단(OCT ) :
망막 내층 분리와 망막 간극에 교량 구조(내경계막 및 뮐러 세포의 잔해)가 관찰됩니다.황반원공 이나 황반 박리를 동반할 수 있습니다.감별 진단: 황반원공 망막박리 (전층 박리)
치료 : 유리체절제술 이 기본입니다.
수술법 : ILM 박리가 기본; 역전 ILM 플랩 기법, 수정체 형성 ILM 플랩법 등수술 후 망막 재유착까지 수개월 이상 걸릴 수 있습니다.
예후 :
수술 전 황반 박리를 동반한 경우 시력 예후가 가장 좋습니다
수술 전 황반원공 또는 수술 후 황반원공 형성은 시력 예후가 불량합니다
적절한 시기의 수술적 중재가 시기능 예후를 좌우합니다
Desjarlais EB , Barineau W, Shah CP. Surgical treatment of macula-involving degenerative retinoschisis. Retin Cases Brief Rep. 2022;16(1):73-76.
Yang YP, Chen YP, Yang CM. Clinical manifestation and current therapeutics in X-linked juvenile retinoschisis. J Chin Med Assoc. 2022;85(3):276-278. doi:10.1097/JCMA.0000000000000666.
van der Veen I, Stingl K, Kohl S, et al. The road towards gene therapy for X-linked retinoschisis: a systematic review of preclinical and clinical findings. Int J Mol Sci. 2024;25(2):1267. doi:10.3390/ijms25021267.
글 전문을 복사해 원하는 AI 도우미에 붙여 넣고 질문할 수 있습니다.
아래 AI 도우미를 열고 복사한 내용을 채팅창에 붙여 넣으세요.