ความเสี่ยงของการลุกลามไปทางด้านหลัง
หลักการพื้นฐาน: การสังเกตอาการ
ข้อบ่งชี้ของการเลเซอร์กั้น: การขยายตัวที่ดำเนินไป, ใกล้ถึงขั้วหลัง
เป้าหมายการรักษา: ป้องกันการลุกลามไปทางด้านหลังเพิ่มเติม

จอประสาทตาฉีกขาด (retinoschisis) คือภาวะที่จอประสาทตาชั้นประสาทแยกออกจากกันที่ชั้น plexiform ชั้นในหรือชั้นนอก ซึ่งแตกต่างโดยพื้นฐานจากจอประสาทตาลอกที่ชั้นเซลล์รับแสงหลุดออกจากชั้นเยื่อบุผิวเม็ดสี
| รูปแบบ | อายุและเพศที่พบบ่อย | ตำแหน่งที่พบบ่อย | ความชุกและอุบัติการณ์ |
|---|---|---|---|
| จอประสาทตาฉีกขาดจากอายุ (ที่ได้มา) | อายุ 40 ปีขึ้นไป; ทั้งชายและหญิง | บริเวณขอบตาด้านล่างขมับ (70%) | 7–30% ของผู้ที่มีอายุ 40 ปีขึ้นไป |
| จอประสาทตาฉีกขาดแบบเชื่อมโยง X (แต่กำเนิด) | วัยเรียน; เฉพาะเพศชายเกือบทั้งหมด | รอยบุ๋มจอตา (เกือบทั้งหมด) + ขอบตา (ประมาณครึ่งหนึ่ง) | 1 ใน 5,000–25,000 คน2) |
| จอประสาทตาลอกบริเวณรอยบุ๋มจากสายตาสั้น | วัยกลางคนขึ้นไป; สายตาสั้นมาก | ขั้วหลัง / จุดภาพชัด | สัดส่วนหนึ่งของดวงตาที่มีสายตาสั้นรุนแรง |
จอประสาทตาหลุดลอกชั้นใน (Retinoschisis) เป็นภาวะที่มีการแยกตัวภายในชั้นของจอประสาทตาส่วนประสาท ซึ่งแตกต่างอย่างสิ้นเชิงจากจอประสาทตาลอก (Retinal detachment) ที่จอประสาทตาทุกชั้นหลุดออกจากชั้นเยื่อบุผิวสี ในจอประสาทตาหลุดลอกชั้นใน การเชื่อมต่อกับชั้นเยื่อบุผิวยังคงอยู่ ดังนั้นการพยากรณ์โรคทางสายตาโดยทั่วไปดีกว่าจอประสาทตาลอก อย่างไรก็ตาม หากเกิดรูขึ้นทั้งในชั้นในและชั้นนอก อาจลุกลามไปสู่จอประสาทตาลอกได้
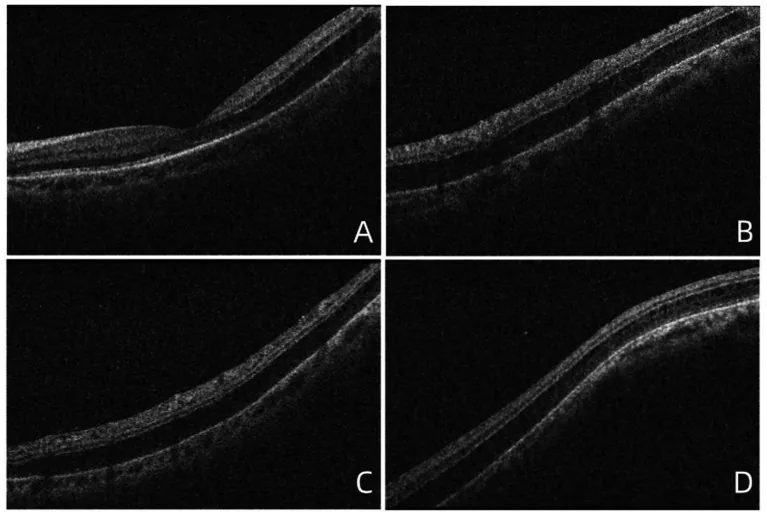
ภาวะจอประสาทตาฉีกขาดที่เกี่ยวข้องกับอายุเป็นภาวะที่การเสื่อมแบบถุงน้ำทางสรีรวิทยาของจอประสาทตาส่วนปลายในผู้ใหญ่ (ถุงน้ำ Blessig-Iwanoff) รวมตัวและขยายใหญ่ขึ้น ทำให้เกิดการแยกในชั้นเพล็กซิฟอร์มชั้นนอกหรือชั้นนิวเคลียสชั้นใน
ความชุกอยู่ที่ 1.65–7%2) พบมากในผู้ที่มีอายุมากกว่า 40 ปี พบทั้งสองข้างประมาณ 70% ของกรณี 70% เกิดขึ้นที่จอประสาทตาส่วนปลายด้านล่างขมับ พื้นผิวนูนเรียบ ไม่มีการถ่ายทอดทางพันธุกรรม และเกิดขึ้นตามอายุที่เพิ่มขึ้น
จอประสาทตาหลุดลอกแบบทุติยภูมิอาจเกิดจากเยื่อเจริญ แรงดึงของวุ้นตา การเปลี่ยนแปลงแบบถุงน้ำ เลือดออกในจอประสาทตา สารน้ำรั่ว หรือการอักเสบ สาเหตุเฉพาะที่ทราบ ได้แก่ จอประสาทตาจากเบาหวาน จอประสาทตาหลุดลอกเก่า จอประสาทตาเสื่อมตามอายุ จอประสาทตาในทารกคลอดก่อนกำหนด (ROP) และโรคคาทส์
ส่วนใหญ่ไม่มีอาการ ไม่ค่อยลุกลามถึงขั้วหลัง และการมองเห็นมักปกติ เมื่อรอยโรคเกินเส้นศูนย์สูตร อาจเกิดอาการเช่นข้อบกพร่องของลานสายตา
| อาการแสดง | ลักษณะ | ความสำคัญในการวินิจฉัยแยกโรค |
|---|---|---|
| การนูนเป็นรูปโดม | ครึ่งทรงกลมเรียบใส; คงที่ ไม่เคลื่อนที่ | ไม่เคลื่อนที่เมื่อเปลี่ยนท่าทาง |
| ลักษณะคล้ายแพรน้ำ | ชั้นในเป็นมันระยิบระยับ | ลักษณะเฉพาะของโรคนี้ |
| snowflakes (ความขุ่นคล้ายเกล็ดหิมะ) | ความขุ่นแบบเม็ดสีเหลือง-ขาวบนพื้นผิวด้านในของชั้นที่แยกออก | ตัวบ่งชี้การเสื่อม |
แม้จะเกิดรูในชั้นนอกและจอประสาทตาชั้นนอกหลุดลอก ความเสี่ยงก็ต่ำ หากเกิดรูทั้งชั้นในและชั้นนอกและลุกลามเป็นการหลุดลอก จำเป็นต้องรักษาด้วยการผ่าตัดสำหรับจอประสาทตาหลุดลอกชนิดมีรูฉีกขาดตามปกติ
กลไกหลักคือการรวมตัวและขยายตัวของถุงน้ำเสื่อมของเส้นใยเฮนเลในชั้นเพล็กซิฟอร์มชั้นนอกเนื่องจากการสูงวัย กลไกของจุดบอดสัมบูรณ์คือการแยกชั้นในชั้นเพล็กซิฟอร์มชั้นนอกทำให้เกิดการฉีกขาดของเนื้อเยื่อที่จุดเชื่อมต่อซินแนปส์ ส่งผลให้การส่งสัญญาณกระตุ้นแสงถูกขัดขวาง1).
ปัจจัยเสี่ยง ได้แก่ อายุที่มากขึ้นและสายตายาว 2) ยังไม่พบปัจจัยทางพันธุกรรม 2).
การวินิจฉัยด้วย OCT มีบทบาทสำคัญ 2) สามารถแสดงขอบเขตและความลึกของโพรงที่ฉีกขาด และโครงสร้างแนวตั้งระหว่างชั้น (สะพานเนื้อเยื่อแนวตั้ง) ยืนยันการแยกชั้นในชั้นเพล็กซิฟอร์มชั้นนอกได้โดยตรง
การแยกความแตกต่างจากจอประสาทตาลอก เป็นสิ่งที่สำคัญที่สุด
| ลักษณะ | จอประสาทตาฉีกขาด | จอประสาทตาลอก |
|---|---|---|
| การเคลื่อนที่ของส่วนนูน | คงที่ ไม่เคลื่อนที่ | เคลื่อนที่เมื่อเปลี่ยนท่า |
| ความโปร่งใส | สูง (ใส) | ต่ำ (ขุ่น) |
| ลักษณะของจุดบอด | จุดบอดสัมบูรณ์ | จุดบอดสัมพัทธ์ |
| ลักษณะพื้นผิว | เรียบ (water silk) | ไม่สม่ำเสมอ / เป็นคลื่น |
หลักการคือการสังเกตอาการ ความเสี่ยงในการลุกลามไปสู่จอประสาทตาลอกต่ำประมาณ 0.05% ต่อปี และผู้ป่วยส่วนใหญ่มีอาการคงที่โดยไม่มีอาการ
ความเสี่ยงของการลุกลามไปทางด้านหลัง
หลักการพื้นฐาน: การสังเกตอาการ
ข้อบ่งชี้ของการเลเซอร์กั้น: การขยายตัวที่ดำเนินไป, ใกล้ถึงขั้วหลัง
เป้าหมายการรักษา: ป้องกันการลุกลามไปทางด้านหลังเพิ่มเติม
การเกิดรูฉีกขาดของชั้นนอก
หลักการพื้นฐาน: การสังเกตอาการ
ข้อควรระวัง: การฉีกขาดของชั้นนอกเพิ่มความเสี่ยงต่อการหลุดลอก
ประเมินข้อบ่งชี้อย่างรอบคอบ: ต้องระวังหากมีรูในชั้นในร่วมด้วย
จอประสาทตาหลุดลอกจากภาวะแยกชั้น
หลักการพื้นฐาน: การผ่าตัดตามแนวทางการรักษาจอประสาทตาหลุดลอกจากรอยฉีกขาดทั่วไป
ข้อบ่งชี้ในการผ่าตัด: เมื่อมีรูทั้งในชั้นในและชั้นนอกและการหลุดลอกดำเนินไป
การพยากรณ์โรค: โดยทั่วไปดี
กรณีที่มีการแทรกซึมของจอประสาทตา
แนวทางพื้นฐาน: พิจารณาการผ่าตัดน้ำวุ้นตา
เทคนิคการผ่าตัด: การลอก ILM + การอัดแก๊ส
หลักฐาน: ระดับรายงานผู้ป่วย1)
การแยกชั้นในชั้นเพล็กซิฟอร์มชั้นนอกทำให้เกิดการฉีกขาดของเนื้อเยื่อที่จุดเชื่อมต่อซินแนปส์ ส่งผลให้เกิดจุดบอดสัมบูรณ์1) เชื่อว่าเส้นใยเฮนเลถูกแยกออกเนื่องจากการรวมตัวของภาวะเสื่อมแบบถุงน้ำที่เกี่ยวข้องกับอายุ ซึ่งเป็นสาเหตุของการแยกตัว การประเมินสามมิติด้วย SD-OCT ช่วยให้สามารถประเมินการแพร่กระจายของโพรงแยกและความบางของชั้นในและชั้นนอกได้อย่างแม่นยำ ทำให้ความเข้าใจเกี่ยวกับประวัติธรรมชาติระยะยาวและการระบุปัจจัยทำนายการดำเนินโรคก้าวหน้าขึ้น2)
ในภาวะจอประสาทตาฉีกขาดที่เกี่ยวข้องกับอายุ จะเกิดการแยกชั้นในชั้นเพล็กซิฟอร์มชั้นนอก ในบริเวณนี้มีจุดเชื่อมต่อซินแนปส์ระหว่างเซลล์รับแสงและเซลล์ปมประสาท และเมื่อซินแนปส์ขาดเนื่องจากการแยกตัว สิ่งเร้าแสงจะไม่สามารถส่งต่อไปยังเซลล์สองขั้วและเซลล์ปมประสาทได้1) ดังนั้น ในบริเวณที่แยกตัว แม้จะส่องแสง สัญญาณไฟฟ้าก็ไม่ถูกนำส่ง และผู้ป่วยจะรับรู้ถึงจุดบอดสัมบูรณ์
ภาวะจอประสาทตาฉีกขาดที่เกี่ยวข้องกับอายุส่วนใหญ่มีแนวโน้มคงที่ ความเสี่ยงในการลุกลามไปสู่จอประสาทตาลอกต่ำมาก ประมาณ 0.05% ต่อปี อย่างไรก็ตาม หากเกิดรูทั้งในชั้นในและชั้นนอก ความเสี่ยงในการลอกจะเพิ่มขึ้น ดังนั้น การติดตามผลเป็นระยะด้วยการตรวจอวัยวะรับภาพจึงมีความสำคัญ2)
โรคจอประสาทตาหลุดลอกแบบ X-linked (XLRS) เป็นโรคจอประสาทตาแต่กำเนิดที่ถ่ายทอดแบบด้อยบนโครโมโซม X เกิดจากการกลายพันธุ์ของยีน RS1 เป็นโรคความเสื่อมของวุ้นตาและจอประสาทตาที่พบได้ค่อนข้างน้อย โดยมีความชุกประมาณ 1 ใน 5,000 ถึง 25,000 คน 2) โดยปกติแล้วจะเกิดเฉพาะในเพศชาย ส่วนเพศหญิงเป็นพาหะ
โดยปกติแล้วจะมีผลเฉพาะเพศชายเท่านั้น เนื่องจากเป็นโรคถอยที่ถ่ายทอดทางโครโมโซม X ผู้หญิงที่มีการกลายพันธุ์บนโครโมโซม X เพียงหนึ่งแท่งจะเป็นพาหะและมักไม่มีอาการ พบได้น้อยที่ผู้หญิงมีฟีโนไทป์เล็กน้อยเนื่องจากการไม่ทำงานของโครโมโซม X ที่เบี่ยงเบนหรือ uniparental disomy2).
อาการที่ผู้ป่วยรู้สึก:
อาการทางคลินิก:
ลักษณะของจอประสาทตาส่วนกลาง
การแยกชั้นของรอยบุ๋มจอตา (เกือบทุกกรณี): การเปลี่ยนแปลงแบบถุงน้ำร่วมกับรอยพับรูปซี่ล้อ (ถุงน้ำและสะพานเชื่อมโครงสร้างในการตรวจ OCT)
ฝ่อจอประสาทตา: เมื่ออายุมากขึ้น การเปลี่ยนแปลงแบบถุงน้ำจะหายไปและเปลี่ยนเป็นฝ่อ; มักมีลักษณะคล้ายจอประสาทตาบวมน้ำแบบถุงน้ำธรรมดา
การตรวจหลอดเลือดด้วยฟลูออเรสซีน: ไม่มีการรั่วของฟลูออเรสซีนแตกต่างจากจอประสาทตาบวมชนิดซิสตอยด์ (โฟเวียปกติหรือมีข้อบกพร่องแบบหน้าต่าง)
การตรวจพบบริเวณรอบนอก
จอประสาทตาหลุดลอกส่วนปลาย (ประมาณครึ่งหนึ่ง): มักเกิดบริเวณขมับด้านล่าง; อาจมีรูขนาดใหญ่ในชั้นในของจอประสาทตาร่วมด้วย
การสะท้อนแสงสีทอง: ลักษณะเฉพาะที่พบในจอประสาทตาส่วนรอบ; ร่วมกับเส้นเลือดจอประสาทตามีสีขาว
ม่านน้ำวุ้นตา: พบในกรณีรุนแรง; น้ำวุ้นตาไม่หลุดลอกและยึดติดแน่นกับจอประสาทตา
ภาวะแทรกซ้อน: จอประสาทตาลอก (5-20%), เลือดออกในน้ำวุ้นตา, เลือดออกในช่องแยก
เมื่อพบจอประสาทตาบวมแบบถุงน้ำในเด็กชายทั้งสองข้าง ให้สงสัยโรคนี้ เป็นจุดเริ่มต้นการวินิจฉัยที่สำคัญ.
การวินิจฉัยแยกโรค:
| โรค | จุดที่ใช้แยก |
|---|---|
| จอประสาทตาลอกชนิดมีรอยฉีกขาด | มักเป็นข้างเดียว; มีเส้นแบ่งเขต; ร่วมกับจอประสาทตาเสื่อมแบบ lattice |
| จอประสาทตาบวมน้ำชนิดถุงน้ำ | มีการรั่วซึมรูปกลีบดอกไม้ในการฉีดสี fluorescein; ไม่มีการรั่วซึมใน XLRS |
| จอประสาทตาลอกตามอายุ (เสื่อม) | เกิดในผู้สูงอายุ; จำกัดบริเวณรอบนอก; คลื่น b ปกติ |
| กลุ่มอาการโกลด์แมน-ฟาฟร์ | ร่วมกับตาบอดกลางคืนและการสะสมของเม็ดสี |
ในจอประสาทตาบวมชนิดซิสตอยด์ (CME) การตรวจหลอดเลือดด้วยฟลูออเรสซีนจะพบการรั่วและการสะสมของฟลูออเรสซีนเป็นรูปกลีบดอกไม้ ในทางตรงกันข้าม ใน XLRS จะมีโพรงแยกที่รอยบุ๋มจอตา แต่กำแพงกั้นเลือด-จอตาปกติ และการตรวจหลอดเลือดด้วยฟลูออเรสซีนไม่พบการรั่ว มีเพียงข้อบกพร่องแบบหน้าต่าง (window defect) ความแตกต่างนี้สำคัญในการวินิจฉัยแยกโรคโดยใช้ OCT ร่วมกับการตรวจหลอดเลือดด้วยฟลูออเรสซีน
ยังไม่มีการรักษาที่หายขาดที่ได้รับการยอมรับ
การรักษาด้วยยา:
การรักษาด้วยการผ่าตัด:
การจัดการผู้ป่วย:
การเปลี่ยนแปลงคล้ายถุงน้ำที่รอยบุ๋มจอประสาทตาอาจลดลงตามธรรมชาติเมื่อเติบโตขึ้น2) อย่างไรก็ตาม บางรายอาจเปลี่ยนเป็นจอประสาทตาฝ่อ และการหายไปไม่ได้หมายถึงการมองเห็นดีขึ้นเสมอไป ในบางราย มีรายงานว่าภาวะจอประสาทตาฉีกขาดบริเวณรอบนอกลดลงหลังจากเกิดภาวะวุ้นตาหลุดลอกส่วนหลัง
เรติโนสคิซินที่ถูกเข้ารหัสโดยยีน RS1 เป็นโปรตีนที่ถูกหลั่งออกมาซึ่งประกอบด้วยกรดอะมิโน 224 ตัว และสร้างสารประกอบเชิงซ้อนโฮโมโอลิโกเมอร์ผ่านโดเมนดิสคอยดิน 2) โดยการจับกับเซลล์รับแสงและเซลล์ไบโพลาร์ โปรตีนนี้จะรักษาความสมบูรณ์ของโครงสร้างและซินแนปส์ของจอประสาทตา การกลายพันธุ์ของ RS1 ทำให้สารประกอบเชิงซ้อนสลายตัว ส่งผลให้เกิดช่องว่างแยกตัวที่มีลักษณะเฉพาะและการรบกวนการส่งสัญญาณจอประสาทตา 2)
ทางจุลพยาธิวิทยา การแยกตัวของจอประสาทตาเกิดขึ้นส่วนใหญ่ในชั้นเส้นใยประสาท ในการตรวจ OCT จะพบการแยกตัวในชั้นเพล็กซิฟอร์มชั้นนอกและชั้นนิวเคลียร์ชั้นในที่บริเวณรอยบุ๋มจอตาและรอบๆ แม้ว่าการแยกตัวทางสัณฐานวิทยาจะจำกัดอยู่เฉพาะที่ แต่การตรวจทางไฟฟ้าสรีรวิทยาแสดงให้เห็นความผิดปกติของจอประสาทตาทั้งหมด ซึ่งบ่งชี้โดยคลื่น b ที่เป็นลบ
ความสัมพันธ์ระหว่างจีโนไทป์และฟีโนไทป์ (กลุ่มตัวอย่างผู้ป่วยชาวเกาหลี 83 ราย, Lee et al. 2025) 2):
ในการศึกษาที่วิเคราะห์ของเหลวในช่องแยกของ XLRS พบโปรตีนจับเรตินอยด์ระหว่างเซลล์รับแสง (IRBP) ในของเหลวในช่องแยก ซึ่งอาจบ่งชี้ถึงความผิดปกติของการเผาผลาญจอประสาทตาภายในช่องแยก2) นอกจากนี้ยังมีรายงานกรณีของจอประสาทตาอักเสบชนิด exudative ที่ไม่พบปกติใน XLRS แสดงให้เห็นถึงการมีอยู่ของฟีโนไทป์ที่หลากหลายภายใต้การวินิจฉัยเดียวกัน2)
การบำบัดด้วยยีน RS1 กำลังอยู่ในระหว่างการทดลองทางคลินิก2)3) แบบจำลองสัตว์และการทดลองทางคลินิกระยะแรก รายงานการฟื้นตัวบางส่วนของการตอบสนองของคลื่นไฟฟ้าจอประสาทตาและการปรับปรุงกายวิภาคของจอประสาทตา
การทดลองทางคลินิกหลัก:
ความท้าทายในปัจจุบัน: ใน XLRS ความเปราะบางของจอประสาทตาเพิ่มขึ้น ทำให้การลอกของเยื่อวุ้นตาส่วนหลังและการฉีดใต้จอประสาทตาทำได้ยากมากในทางเทคนิค3) การฉีดเข้าช่องว่างน้ำวุ้นตาอาจเป็นที่ต้องการในบางกรณี แต่ต้องยอมรับความเสี่ยงของภาวะวุ้นตาอักเสบ
การบำบัดด้วยยีนสำหรับ XLRS ยังอยู่ในขั้นตอนการทดลองทางคลินิก และยังไม่ได้รับการอนุมัติให้เป็นการรักษาในโรงพยาบาลทั่วไป การทดลองทางคลินิกบางรายการพบปัญหาด้านความปลอดภัย เช่น การอักเสบภายในลูกตา และบางการทดลองถูกยุติ 3) หากต้องการเข้าร่วม จำเป็นต้องปรึกษาที่สถานพยาบาลเฉพาะทาง
ภาวะจอประสาทตาชั้นในแยกตัวจากสายตาสั้น (myopic foveoschisis) คือการแยกตัวของชั้นในของจอประสาทตาบริเวณขั้วหลังที่สัมพันธ์กับสายตาสั้นรุนแรง เดิมทีถูกอธิบายว่าเป็นจอประสาทตาลอกบริเวณขั้วหลังที่สัมพันธ์กับสายตาสั้นรุนแรง และปัจจุบันแนวคิดรวมถึงกรณีที่มีรูที่จุดรับภาพร่วมด้วย
พยาธิสรีรวิทยาเกี่ยวข้องกับปัจจัยต่อไปนี้ร่วมกัน:
อาการ: การมองเห็นลดลง, จุดบอดกลาง, ภาพบิดเบี้ยว (metamorphopsia), มองเห็นพร่ามัว ในสายตาสั้นมาก อาการอาจน้อย
การวินิจฉัย (OCT):
การรักษา: การผ่าตัดน้ำวุ้นตาเป็นพื้นฐาน
การพยากรณ์โรค: