Rischio di progressione posteriore
Linee guida generali: osservazione
Indicazione per laser barriera: progressione, vicinanza al polo posteriore
Obiettivo del trattamento: prevenire l’ulteriore estensione posteriore

La retinoschisi è una condizione in cui la retina neurale si separa a livello dello strato plessiforme interno o esterno. È fondamentalmente diversa dal distacco di retina, in cui lo strato dei fotorecettori si stacca dall’epitelio pigmentato.
| Tipo | Età e sesso più comuni | Sede più frequente | Prevalenza e incidenza |
|---|---|---|---|
| Retinoschisi senile (acquisita) | ≥40 anni; entrambi i sessi | Periferia infero-temporale (70%) | 7-30% delle persone ≥40 anni |
| Retinoschisi X-linked (congenita) | Età scolare; quasi esclusivamente maschi | Fovea (quasi tutti i casi) + periferia (circa metà) | 1 su 5.000-25.000 persone2) |
| Retinoschisi foveale miopica | Età media o avanzata; miopia elevata | Polo posteriore e macula | Una certa percentuale di occhi con miopia elevata |
La retinoschisi è una condizione in cui si verifica una separazione all’interno degli strati della retina neurosensoriale, ed è completamente diversa dal distacco di retina (in cui l’intero spessore della retina si stacca dall’epitelio pigmentato). Nella retinoschisi, la connessione con l’epitelio pigmentato retinico è preservata, quindi la prognosi visiva è generalmente migliore rispetto al distacco di retina. Tuttavia, se si formano fori sia nello strato interno che in quello esterno, può progredire verso un distacco di retina.
La retinoschisi senile è una condizione in cui la degenerazione cistica fisiologica della retina periferica adulta (cisti di Blessig-Iwanoff) si fonde e si espande, causando una separazione nello strato plessiforme esterno o nello strato granulare interno.
La prevalenza è dell’1,65-7%2), più comune dopo i 40 anni, con bilateralità in circa il 70% dei casi. Il 70% si verifica nella retina periferica inferotemporale, con superficie rialzata liscia. Non è ereditaria e insorge con l’invecchiamento.
La retinoschisi secondaria può essere causata da membrane proliferative, trazione vitreale, alterazioni cistiche, emorragia intraretinica, essudazione e infiammazione. Le malattie causali specifiche includono la retinopatia diabetica, il distacco di retina cronico, la degenerazione maculare legata all’età, la retinopatia del prematuro (ROP) e la malattia di Coats.
La maggior parte dei casi è asintomatica, raramente si estende al polo posteriore e spesso l’acuità visiva è normale. Quando la lesione supera l’equatore, possono manifestarsi sintomi soggettivi come difetti del campo visivo.
| Reperto | Caratteristica | Significato per la diagnosi differenziale |
|---|---|---|
| Rialzo a cupola | Emisferica liscia e trasparente; fissa e immobile | Non si sposta con i cambi di posizione |
| Aspetto a seta d’acqua | Riflesso ondulato dello strato interno | Caratteristico di questa condizione |
| snowflakes (opacità a fiocchi di neve) | opacità granulosa giallo-biancastra sulla superficie interna dello strato di separazione | indicatore di degenerazione |
Anche se si forma un foro nello strato esterno causando un distacco dello strato retinico esterno, il rischio è basso. Se si formano fori sia interni che esterni e progredisce verso un distacco, è necessario un trattamento chirurgico come per il distacco di retina regmatogeno standard.
Il principale meccanismo patologico è la fusione e l’espansione della degenerazione cistica delle fibre di Henle nello strato plessiforme esterno dovuta all’invecchiamento. Il meccanismo dello scotoma assoluto è che la separazione degli strati a livello dello strato plessiforme esterno provoca una rottura tissutale nelle giunzioni sinaptiche, interrompendo la trasmissione del segnale luminoso1).
I fattori di rischio includono l’invecchiamento e l’ipermetropia2). Non sono state identificate predisposizioni genetiche2).
La diagnosi mediante OCT svolge un ruolo centrale 2). Consente di visualizzare l’estensione, la profondità della cavità di separazione e le strutture colonnari (ponti tissutali verticali) tra gli strati, confermando direttamente la separazione a livello dello strato plessiforme esterno.
La diagnosi differenziale con il distacco di retina è della massima importanza.
| Caratteristiche | Retinoschisi | Distacco di retina |
|---|---|---|
| Mobilità del rigonfiamento | Fisso/immobile | Si sposta con il cambiamento di posizione |
| Trasparenza | Alta (trasparente) | Bassa (opaca) |
| Natura dello scotoma | Scotoma assoluto | Scotoma relativo |
| Aspetto superficiale | Liscio (water silk) | Irregolare, ondulato |
In linea di principio si tratta di osservazione. Il rischio di progressione verso il distacco di retina è basso, circa lo 0,05% annuo, e la maggior parte dei casi è asintomatica e stabile.
Rischio di progressione posteriore
Linee guida generali: osservazione
Indicazione per laser barriera: progressione, vicinanza al polo posteriore
Obiettivo del trattamento: prevenire l’ulteriore estensione posteriore
Formazione di foro nello strato esterno
Linee guida generali: osservazione nel tempo
Attenzione: i fori dello strato esterno aumentano il rischio di distacco
Valutare attentamente l’indicazione: prestare particolare attenzione in caso di foro dello strato interno concomitante
Distacco da retinoschisi
Linee guida generali: intervento chirurgico simile a quello per il distacco di retina regmatogeno standard
Indicazioni chirurgiche: quando si formano fori in entrambi gli strati (interno ed esterno) e il distacco progredisce
Prognosi: generalmente buona
Caso di infiltrazione maculare
Linee guida generali: considerazione della vitrectomia
Tecnica chirurgica: peeling della ILM + tamponamento gassoso
Evidenze: livello di case report1)
La separazione degli strati nella plessiforme esterna provoca una rottura tissutale a livello delle giunzioni sinaptiche, determinando uno scotoma assoluto 1). Si ritiene che la separazione sia causata dalla fusione di degenerazioni cistiche legate all’età delle fibre di Henle. La valutazione tridimensionale con SD-OCT ha permesso di misurare con precisione l’estensione della cavità di separazione e lo spessore degli strati interni ed esterni, favorendo l’identificazione del decorso naturale a lungo termine e dei fattori predittivi di progressione 2).
Nella retinoschisi senile si verifica una separazione degli strati nella plessiforme esterna. In questa sede sono presenti sinapsi tra fotorecettori e cellule gangliari; quando la separazione interrompe le sinapsi, lo stimolo luminoso non viene trasmesso alle cellule bipolari e gangliari 1). Di conseguenza, nell’area di separazione, anche se esposta alla luce, il segnale elettrico non viene condotto, e il paziente percepisce uno scotoma assoluto.
La maggior parte dei casi di retinoschisi acquisita (senile) ha un decorso stabile. Il rischio di progressione verso il distacco di retina è estremamente basso, circa lo 0,05% all’anno. Tuttavia, se si formano fori sia nello strato interno che in quello esterno, il rischio di distacco aumenta, pertanto è importante un monitoraggio regolare con esame del fondo oculare 2).
La retinoschisi legata all’X (XLRS) è una malattia retinica congenita a ereditarietà recessiva legata all’X causata da mutazioni nel gene RS1. È una malattia vitreoretinica degenerativa relativamente rara, con una prevalenza stimata di 1 su 5.000-25.000 persone 2). Di solito colpisce solo i maschi, mentre le femmine sono portatrici.
Di solito colpisce solo i maschi. Poiché è una malattia recessiva legata all’X, le donne con mutazione su un solo cromosoma X sono portatrici e generalmente asintomatiche. Raramente, a causa di inattivazione sbilanciata del cromosoma X o disomia uniparentale, è stato riportato un fenotipo lieve anche nelle donne2).
Sintomi soggettivi:
Reperti clinici:
Reperti maculari
Separazione foveale (quasi tutti i casi): alterazioni cistiche con pieghe a raggiera (cisti e ponti strutturali alla OCT)
Atrofia maculare: con l’età, le alterazioni cistiche regrediscono e progrediscono verso l’atrofia; spesso appare come semplice edema maculare cistoide
Angiografia con fluoresceina: a differenza dell’edema maculare cistoide, non c’è perdita di fluoresceina (la fovea è normale o presenta un difetto finestra)
Reperti periferici
Schisi retinica periferica (circa la metà dei casi): predilige il quadrante temporale inferiore; può essere associata a grandi rotture retiniche interne
Riflesso a foglia d’oro: reperto caratteristico nella retina periferica; associato a sbiancamento dei vasi retinici
Velo vitreale: presente nei casi gravi; il vitreo non è distaccato e aderisce fortemente alla retina
Complicanze: distacco di retina (5-20%), emorragia vitreale, emorragia intra-cavitaria
Se si osserva edema maculare cistoide bilaterale in un bambino maschio, sospettare questa malattia è un importante punto di partenza diagnostico.
Diagnosi differenziale:
| Malattia | Punti chiave per la diagnosi differenziale |
|---|---|
| Distacco di retina regmatogeno | Solitamente unilaterale; formazione di linea di demarcazione; associato a degenerazione a reticolo |
| Edema maculare cistoide | Fluoresceinografia mostra perdita a petalo; nella XLRS nessuna perdita |
| Retinoschisi degenerativa (senile) | Si verifica negli anziani; localizzato alla periferia; onda b normale |
| Sindrome di Goldmann-Favre | Associata a cecità notturna e pigmentazione |
Nell’edema maculare cistoide (CME), l’angiografia con fluoresceina mostra una perdita e accumulo di fluoresceina a forma di petalo. Nella XLRS, invece, è presente una cavità di separazione foveale, ma la barriera emato-retinica è normale e all’angiografia non si osserva perdita, ma solo un difetto finestra. Questa differenza è importante per la diagnosi differenziale combinando OCT e angiografia.
Non esiste una terapia curativa consolidata.
Terapia farmacologica:
Trattamento chirurgico:
Gestione del paziente:
Con la crescita, le alterazioni cistiche della fovea possono ridursi spontaneamente 2). Tuttavia, in alcuni casi si verifica una transizione verso l’atrofia maculare, e la regressione non significa necessariamente un miglioramento della vista. In alcuni casi, è stato riportato che la schisi periferica si riduce dopo il distacco del vitreo posteriore.
La retinoschisina, codificata dal gene RS1, è una proteina secretoria di 224 aminoacidi che forma complessi omo-oligomerici attraverso il dominio discoidina 2). Legandosi ai fotorecettori e alle cellule bipolari, mantiene l’integrità strutturale e sinaptica della retina. La mutazione di RS1 causa la disgregazione del complesso, portando alla formazione di cavità schisiche caratteristiche e a un’alterazione della trasduzione del segnale retinico 2).
Istopatologicamente, la schisi retinica si verifica principalmente nello strato delle fibre nervose. All’OCT si osserva una separazione a livello dello strato plessiforme esterno e dello strato granulare interno nella fovea e nelle aree circostanti. Anche quando la separazione morfologica è limitata, l’elettrofisiologia mostra una disfunzione retinica diffusa, come evidenziato dall’onda b negativa.
Correlazione genotipo-fenotipo (coorte di 83 coreani, Lee et al. 2025) 2):
Uno studio che ha analizzato il liquido di scollamento nella XLRS ha identificato la proteina legante il retinoidi tra i fotorecettori (IRBP) nel liquido di scollamento, suggerendo un possibile metabolismo retinico anomalo all’interno della cavità di scollamento 2). Inoltre, sono stati riportati casi di XLRS complicati da maculopatia essudativa, che di solito non si osserva, indicando l’esistenza di fenotipi variabili sotto la stessa diagnosi 2).
Terapia genica RS1 è in corso in studi clinici2)3). Modelli animali e studi clinici precoci hanno riportato un parziale recupero della risposta elettroretinografica e un miglioramento dell’anatomia retinica.
Studi clinici principali:
Sfida attuale: nell’XLRS la fragilità retinica è aumentata, rendendo il distacco della membrana vitreale posteriore e l’iniezione sottoretinica tecnicamente molto difficili 3). La somministrazione intravitreale può essere preferibile, ma è necessario accettare il rischio di vitrite.
La terapia genica per l’XLRS è ancora in fase di sperimentazione clinica e non è approvata come trattamento negli ospedali generali. Alcuni studi clinici hanno evidenziato problemi di sicurezza come l’infiammazione intraoculare, e alcuni studi sono stati interrotti 3). Per partecipare, è necessario consultare un centro specializzato.
La foveoschisi miopica (myopic foveoschisis) è una separazione degli strati interni della retina nella regione del polo posteriore associata a miopia elevata. Storicamente descritta come distacco retinico del polo posteriore in occhi con miopia elevata, oggi il concetto include anche i casi complicati da foro maculare.
La patogenesi coinvolge molteplici fattori:
Sintomi soggettivi: riduzione dell’acuità visiva, scotoma centrale, metamorfopsia e visione offuscata. Nella miopia elevata, i sintomi soggettivi possono essere scarsi.
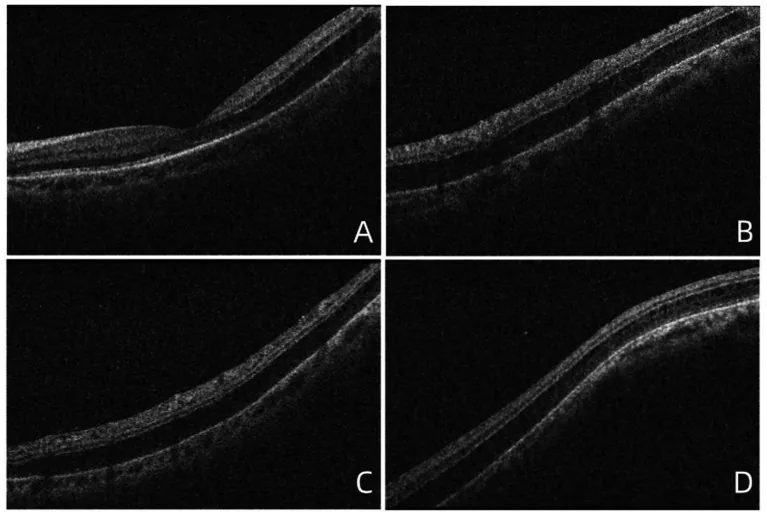
Diagnosi (OCT):
Trattamento: la vitrectomia è il trattamento di base.
Prognosi: