其他构成疾病①
先天性遗传性角膜内皮营养不良(CHED):一种常染色体隐性遗传病,出生至1-2岁左右出现双眼对称性角膜水肿。由SLC4A11基因突变引起,眼压不升高。
后部多形性角膜营养不良(PPCD):一种角膜内皮和Descemet膜的常染色体显性遗传病。表现为角膜水肿,但角膜直径不增大。角膜内皮检查有助于诊断。

前段发育异常(anterior segment developmental anomalies; ASDA),也称为前段发育不全(anterior segment dysgenesis; ASD),是角膜、虹膜、晶状体、前房角等前段结构先天性发育障碍的总称1)。
这些疾病在表型和遗传学上极为多样,但基于房水流出通路(小梁网和Schlemm管)发育异常导致的眼压升高,即发育性青光眼,是常见的重要并发症1,2)。
ASDA包括的主要疾病有:后胚胎环、Axenfeld-Rieger综合征(ARS)、Peters异常、原发性先天性青光眼(PCG)、无虹膜症、先天性遗传性角膜内皮营养不良(CHED)、后部多形性角膜营养不良(PPCD)、硬化性角膜、巨角膜、虹膜角膜内皮(ICE)综合征等。
前段的发育涉及神经嵴来源的间充质细胞,这些细胞也参与小梁网和Schlemm管的发育。当前段形成异常时,房水流出通路的结构也常同时受损,导致房水流出阻力增加,眼压升高。因此,发育性青光眼是ASDA的常见并发症。
ARS是一种常染色体显性遗传病,表现为眼部症状和全身症状。眼部表现包括后胚胎环(Schwalbe线前移和增厚)、虹膜发育不全、多瞳症、虹膜偏位。突出的Schwalbe线与虹膜粘连称为Axenfeld异常,进一步出现虹膜和实质萎缩称为Rieger异常。伴有骨骼发育异常或牙齿异常等全身表现时称为Rieger综合征。角膜通常正常,内皮结构也正常,但残留物引起的物理接触可导致继发性混浊。PITX2(4号染色体)和FOXC1(6号染色体)转录因子基因突变是病因,50-75%合并青光眼1)。青光眼可能从婴儿期发病,但多数在儿童期至青年期发病。FOXC1突变和PITX2突变的表型不同,有报道FOXC1突变中角膜异常占50%,PITX2突变中占16%2)。
一种先天性疾病,特征为角膜中央混浊和角膜内皮及Descemet膜缺损。80%为双眼性,可伴有虹膜角膜粘连或晶状体角膜粘连。PAX6、PITX2、CYP1B1突变相关。彼得斯-普拉斯综合征伴有唇裂、身材矮小、精神发育迟滞等全身异常,由B3GLCT基因突变(常染色体隐性)引起3)。重症病例需角膜移植,但合并晶状体角膜粘连时预后不良3)。
一种由小梁网发育异常引起的常染色体隐性遗传病。CYP1B1基因(GLC3A位点,2p21)突变最常见4)。在日本儿童青光眼队列中,约20%检测到CYP1B1突变,也发现FOXC1突变4)。在日本,发病率约为十万分之一,75%为双眼性,65%为男性,80%在出生后一年内发病。婴幼儿高眼压导致角膜直径增大(牛眼)、角膜水肿混浊、Descemet膜破裂(Haab纹)。
一种以虹膜发育不全为主的常染色体显性遗传病,由PAX6基因(11号染色体)突变引起5)。除虹膜部分至完全缺损外,可伴有晶状体脱位、角膜混浊、黄斑发育不全导致的视力障碍。合并邻近WT1基因缺失时,有WAGR综合征(Wilms瘤、无虹膜症、泌尿生殖器异常、精神发育迟滞)的风险,需评估WT1。WT1缺失病例建议每3个月进行肾脏超声检查至8岁,并随访小儿肿瘤科5)。
其他构成疾病①
先天性遗传性角膜内皮营养不良(CHED):一种常染色体隐性遗传病,出生至1-2岁左右出现双眼对称性角膜水肿。由SLC4A11基因突变引起,眼压不升高。
后部多形性角膜营养不良(PPCD):一种角膜内皮和Descemet膜的常染色体显性遗传病。表现为角膜水肿,但角膜直径不增大。角膜内皮检查有助于诊断。
其他构成疾病②
巩膜化角膜:不透明的巩膜组织非炎症性、非进行性地侵入周边角膜,使角膜与巩膜的边界模糊。与FOXE3、PAX6等基因突变相关。
大角膜:角膜直径扩大至12.5mm以上的疾病,多为CHRDL1基因突变导致的X连锁隐性遗传。眼压和内皮细胞通常正常。先天性大角膜无Haab纹和视盘凹陷扩大,可与PCG鉴别。
发育性青光眼的初始症状是眼压升高引起的角膜上皮水肿刺激症状。具体表现为无分泌物的流泪、畏光和眼睑痉挛。如果高眼压持续,角膜上皮水肿加重,导致角膜混浊。此外,眼球被膜(尤其是角巩膜缘)被拉伸,导致角膜直径增大(牛眼)和前房深度增加。
角膜被拉伸时,弹性较低的Descemet膜发生破裂(Haab纹),房水流入角膜基质,使角膜水肿和混浊迅速恶化。Haab纹留下永久性混浊,导致视力障碍。
| 所见 | 正常值/标准 |
|---|---|
| 新生儿角膜直径 | 9.5-10.5mm(1岁时10.0-11.5mm)。出生后立即超过12.0mm时怀疑PCG |
| 视盘杯盘比(C/D比) | 婴儿中0.3以上怀疑青光眼。双眼差0.2以上也提示青光眼 |
确认每种疾病特征性的前节表现。后胚胎环(Schwalbe线前移和增厚)与ARS和Alagille综合征相关。虹膜发育不全、多瞳症和虹膜偏位是ARS的特征。中央角膜混浊和虹膜角膜粘连提示Peters异常。
根据青光眼诊疗指南(第5版)6)和国际儿童青光眼研究网络(CGRN)分类7),满足以下5项中的2项或以上即可诊断为儿童青光眼。
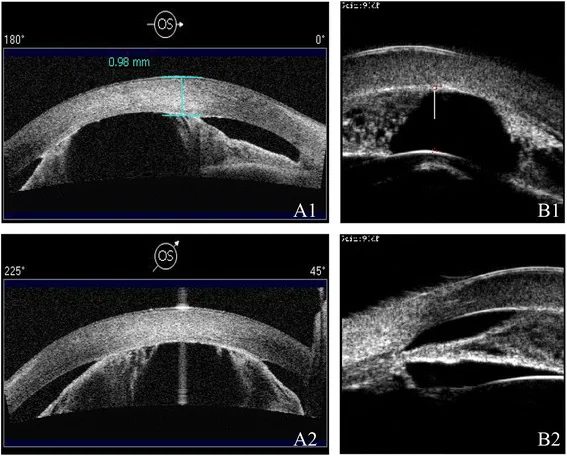
5岁以下儿童常需要在镇静或全身麻醉下进行检查。全身麻醉下眼压较清醒时降低,因此解读测量值需谨慎。房角检查使用手持裂隙灯和Koeppe透镜等直接型房角镜。当角膜混浊导致房角镜观察困难时,超声生物显微镜(UBM)很有用。
在分型诊断中,根据前节表现进行鉴别。检查是否存在后胚胎环、虹膜异常(ARS)和白内障(彼得斯异常)。如果怀疑遗传性,考虑对亲属进行青光眼检查和基因检测。
全身麻醉所用的所有药物都会降低眼压(唯一的例外是氯胺酮,可能轻微升高)。因此,仅凭全身麻醉下的眼压测量值不能排除青光眼。尽可能在清醒时进行测量,并综合评估角膜直径、Haab纹、视盘凹陷等非眼压指标非常重要。
早发型发育性青光眼是一种基本需要手术治疗疾病,药物治疗定位为术前短期降眼压和术后辅助治疗。由于患者是婴幼儿,需要向家长充分解释再次手术并不罕见,并获得理解。
初次手术通常进行房角切开术(goniotomy)或小梁切开术(trabeculotomy)。这些手术直接干预房水流出道的发育异常。如果不成功,则考虑滤过手术或引流管植入手术。
即使眼压得到控制,也常需要弱视治疗。屈光参差、不规则散光、角膜混浊和Haab纹可导致弱视,因此术后应定期检查视力和屈光。
在角膜混浊严重的彼得斯异常中,角膜移植(穿透性角膜移植术)是适应症,但在合并晶状体角膜粘连的重症病例中,移植失败的风险很高。
在前节发育中,表面外胚层来源的角膜上皮和晶状体、神经外胚层来源的视网膜色素上皮与神经嵴来源的间充质细胞相互作用,形成正常的前节结构。神经嵴细胞参与角膜基质、角膜内皮、小梁网和虹膜基质的形成。其迁移或分化异常导致前节发育不良。
已有超过50个基因被发现与ASDA相关,但仍有40%–75%的病例未确定遗传原因。
| 基因 | 染色体 | 相关疾病 | 遗传方式 |
|---|---|---|---|
| PITX2 | 4q25 | ARS、彼得斯异常 | 常染色体显性 |
| FOXC1 | 6p25 | ARS、虹膜角膜角发育不全 | 常染色体显性 |
| PAX6 | 11p13 | 无虹膜症、彼得斯异常 | 常染色体显性 |
| CYP1B1 | 2p21 | 原发性先天性青光眼 | 常染色体隐性 |
在ARS中,FOXC1和PITX2物理相互作用,对神经嵴细胞的正常分化至关重要。任一基因的突变都可能因这种相互作用而产生相似的表型。