眼部并发症

巩膜化角膜
一目了然的要点
Section titled “一目了然的要点”1. 什么是巩膜化角膜?
Section titled “1. 什么是巩膜化角膜?”巩膜化角膜(sclerocornea)是一种罕见的先天性疾病,由于神经嵴细胞迁移异常导致角膜缘原基(limbal anlage)未能正常形成,角膜呈巩膜样白色混浊。非进行性,双眼发病且不对称。与炎症或感染无关,无性别差异。
角膜混浊呈白色,伴有血管侵入,角膜缘边界不清。在欧洲常被称为扁平角膜(cornea plana),在美国则多称为巩膜化角膜(sclerocornea)。
Waring分类
Section titled “Waring分类”| 分类 | 特征 |
|---|---|
| 孤立周边型 | 仅周边部巩膜化,不伴其他异常 |
| 扁平型 | 伴有扁平角膜(角膜屈光力<38 D)和高度远视 |
| 前房异常合并型 | 合并虹膜角膜粘连等前节异常 |
| 全型 | 整个角膜弥漫性混浊 |
50%的病例表现为常染色体显性(AD)或常染色体隐性(AR)遗传。其余50%为散发性。
2. 主要症状和临床所见
Section titled “2. 主要症状和临床所见”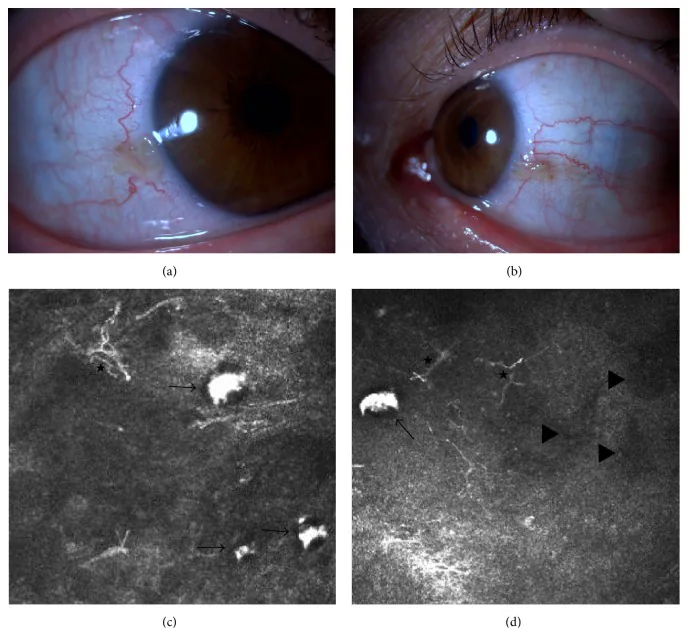
临床所见(医生检查确认的所见)
Section titled “临床所见(医生检查确认的所见)”- 角膜混浊:从周边向中央呈巩膜样白色混浊。全型累及整个角膜,但中央混浊密度稍低。部分型中央区域可能透明。
- 角膜缘消失:角膜与巩膜的边界变得不清晰。周边混浊病例难以准确评估角膜直径。
- 角膜扁平:从侧面裂隙灯观察可一目了然地确认角膜扁平。
- 角膜新生血管:可见来自上巩膜和结膜的血管侵入角膜全层。
全身并发症
智力障碍:作为神经嵴细胞异常的全身性影响而出现。
听力损失:作为前段发育异常综合征的一部分合并出现。
颅面异常:与神经嵴细胞来源的组织形成异常相关。
心血管畸形:罕见合并。
泌尿生殖器畸形:罕见合并。
皮肤异常:与神经嵴细胞异常相关。
在巩膜化角膜中,角膜扁平化和前房狭窄增加了继发性青光眼的风险。发育性青光眼通常在青少年期后发病。常染色体隐性突变的病例风险更高。常伴有房角异常,定期眼压评估至关重要。
3. 原因与风险因素
Section titled “3. 原因与风险因素”巩膜化角膜是由于胚胎期神经嵴细胞迁移异常所致。正常发育中,胚胎7-10周时形成角膜缘原基,决定角膜曲率和角膜-巩膜边界。该结构未能形成导致巩膜与角膜的正常边界紊乱,角膜曲率变平。
- CNA1(扁平角膜1型):常染色体显性遗传。基因座位于12号染色体长臂,但致病基因尚未确定。
- CNA2(扁平角膜2型):常染色体隐性遗传。由12q22-q23区域的KERA基因突变引起。KERA基因编码角膜透明性重要的硫酸角质素蛋白聚糖——角蛋白聚糖(keratocan)。CNA2伴有更严重的角膜扁平化和前节异常。
- PAX6、FOXC1、PITX2:突变可能伴有虹膜角膜粘连、瞳孔异位、虹膜萎缩。
- RAD21:在巩膜化角膜家系中发现的突变。通过WNT9B信号调控神经嵴细胞向角膜角质细胞或巩膜基质细胞的分化方向。
4. 诊断与检查方法
Section titled “4. 诊断与检查方法”眼科检查
全身检查
遗传学检查:检测KERA、PAX6、FOXC1、PITX2、RAD21等基因的突变。与遗传咨询一起进行。
全身评估:检查是否存在相关的全身异常,如智力障碍、听力损失、心血管畸形和泌尿生殖器畸形。
- Peters异常:中央角膜混浊伴有Descemet膜和角膜内皮缺损。表现为虹膜角膜粘连或虹膜晶状体粘连。
- 先天性青光眼:角膜水肿导致的混浊,通过角膜直径增大(牛眼)和Descemet膜破裂(Haab纹)进行鉴别。
- 先天性遗传性角膜内皮营养不良(CHED):双侧弥漫性角膜水肿和混浊,但角膜缘清晰。
- 分娩外伤:通常为单侧,伴有Descemet膜破裂。
5. 标准治疗方法
Section titled “5. 标准治疗方法”对于影响视轴的角膜混浊,穿透性角膜移植术(PKP)是首选。为避免形觉剥夺性弱视,应尽早进行手术。然而,视力预后较差,且移植排斥率较高。
关于移植结果的报告:
- 巩膜化角膜的全层角膜移植显示约75%的失败率,主要原因是角膜缘区域的新生血管形成。
- 一项包括15只全型和12只部分型眼的病例系列报告了1年移植片存活率为70%。
- 在儿童病例中,1年后的移植片透明维持率据报道仅为约37%。
在角膜移植失败的病例中,周边新生血管形成是危险因素,同时可能需要前段重建手术(如房角重建术、瞳孔成形术、晶状体摘除术、人工晶状体复位术等)1)。
在视轴保留的部分型中,应尽早进行光学矫正(眼镜),以预防高度远视引起的弱视。合并青光眼的病例需要滴眼液或手术进行眼压管理。
巩膜化角膜的角膜移植预后不良。据报道,1年移植片存活率为37-70%,最终失败率为75%。主要失败因素是角膜缘区域的新生血管形成。儿童病例预后更差,可能需要多次再移植。
6. 病理生理学与详细发病机制
Section titled “6. 病理生理学与详细发病机制”眼部发育与神经嵴细胞的作用
Section titled “眼部发育与神经嵴细胞的作用”正常前段发育涉及三个重要过程:前脑神经外胚层的形成、晶状体泡从表面外胚层的分离,以及神经嵴来源的间充质前体细胞向前迁移。
在正常发育中,妊娠4周晶状体泡分离后,表面外胚层分化为角膜上皮。妊娠6周,视杯前缘附近的神经嵴细胞进入角膜上皮和晶状体之间,形成Bowman层和角膜内皮。随后,神经嵴细胞再次进入Bowman层和角膜内皮之间,形成角膜基质。妊娠7周,神经嵴细胞开始形成巩膜,从前向后进展,妊娠5个月时到达后极部。
在巩膜化角膜中,胚胎7-10周时角膜缘原基未能形成,因此角膜和巩膜之间的正常边界无法建立。结果导致角膜曲率变平,角膜基质呈现巩膜样特性。
- 上皮:免疫组织化学染色显示角蛋白3和12阳性(角膜上皮标志物),证实其来源于角膜。未见杯状细胞。
- Bowman层:缺失或伴有不规则的玻璃样物质斑块。
- 基质:胶原纤维的层状结构紊乱,排列不规则。纤维直径不一致,深层纤维较细(巩膜样特征)。然而,硫酸角质素等糖胺聚糖和I型胶原的存在表明基质来源于角膜而非巩膜。前部和中部基质有来自上巩膜和结膜的血管侵入。
- Descemet膜:缺失或变薄(0.8-1.5 μm),伴有均质物质和成纤维细胞增殖。
- 内皮:部分病例报告内皮完全缺失。
在巩膜化角膜中,角膜基质的胶原纤维排列不规则,层状结构紊乱,因此无法维持角膜的透明性。正常角膜中均匀胶原纤维的规则排列控制光干涉并保持透明,但在巩膜化角膜中这种结构被破坏。此外,全层角膜的血管侵入也是混浊的原因。
7. 最新研究与未来展望
Section titled “7. 最新研究与未来展望”在一个巩膜化角膜家系中发现了RAD21基因突变。RAD21是黏连蛋白复合体的组成部分,参与基因表达的调控。研究发现,在受RAD21表达影响的过程中,WNT9B在决定神经嵴细胞分化为角膜角质细胞或巩膜基质细胞的方向上起着至关重要的作用。
这一发现为理解角膜和巩膜基质细胞虽均来源于神经嵴细胞却具有不同组织特性的原因提供了线索。未来有望通过调控WNT9B信号通路开发新的治疗策略。
8. 参考文献
Section titled “8. 参考文献”- American Academy of Ophthalmology. Corneal Edema and Opacification Preferred Practice Pattern. Ophthalmology. 2024.
