眼部併發症

鞏膜化角膜
一目了然的要點
Section titled “一目了然的要點”1. 什麼是鞏膜化角膜?
Section titled “1. 什麼是鞏膜化角膜?”鞏膜化角膜(sclerocornea)是一種罕見的先天性疾病,由於神經嵴細胞遷移異常導致角膜緣原基(limbal anlage)未能正常形成,角膜呈鞏膜樣白色混濁。非進行性,雙眼發病且不對稱。與發炎或感染無關,無性別差異。
角膜混濁呈白色,伴有血管侵入,角膜緣邊界不清。在歐洲常被稱為扁平角膜(cornea plana),在美國則多稱為鞏膜化角膜(sclerocornea)。
Waring分類
Section titled “Waring分類”| 分類 | 特徵 |
|---|---|
| 孤立周邊型 | 僅周邊部鞏膜化,不伴其他異常 |
| 扁平型 | 伴有扁平角膜(角膜屈光力<38 D)和高度遠視 |
| 前房異常合併型 | 合併虹膜角膜粘連等前節異常 |
| 全型 | 整個角膜瀰漫性混濁 |
50%的病例表現為體染色體顯性(AD)或體染色體隱性(AR)遺傳。其餘50%為散發性。
2. 主要症狀與臨床所見
Section titled “2. 主要症狀與臨床所見”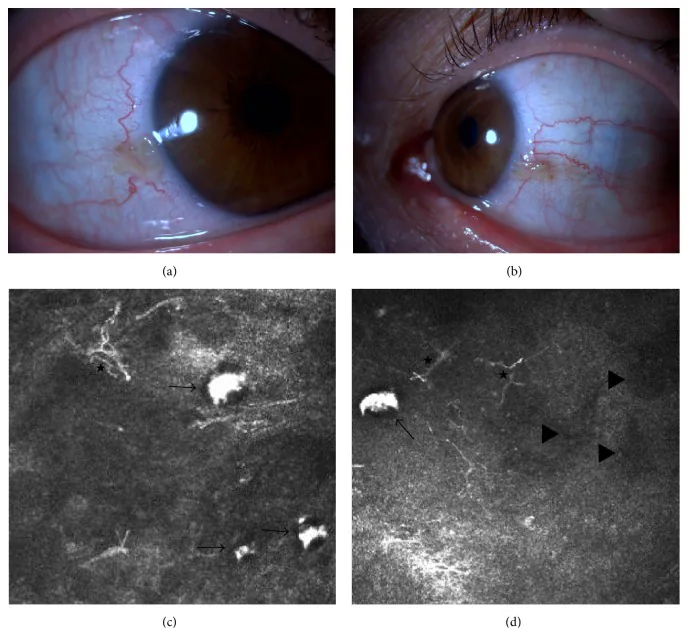
臨床所見(醫師檢查確認的所見)
Section titled “臨床所見(醫師檢查確認的所見)”- 角膜混濁:從周邊向中央呈鞏膜樣白色混濁。全型累及整個角膜,但中央混濁密度稍低。部分型中央區域可能透明。
- 角膜緣消失:角膜與鞏膜的邊界變得不清晰。周邊混濁病例難以準確評估角膜直徑。
- 角膜扁平:從側面裂隙燈觀察可一目瞭然地確認角膜扁平。
- 角膜新生血管:可見來自上鞏膜和結膜的血管侵入角膜全層。
全身併發症
智力障礙:作為神經嵴細胞異常的全身性影響而出現。
聽力損失:作為前段發育異常症候群的一部分合併出現。
顱面異常:與神經嵴細胞來源的組織形成異常相關。
心血管畸形:罕見合併。
泌尿生殖器畸形:罕見合併。
皮膚異常:與神經嵴細胞異常相關。
在鞏膜化角膜中,角膜扁平化和前房狹窄增加了續發性青光眼的風險。發育性青光眼通常在青少年期後發病。常染色體隱性突變的病例風險更高。常伴有隅角異常,定期眼壓評估至關重要。
3. 原因與風險因素
Section titled “3. 原因與風險因素”鞏膜化角膜是由於胚胎期神經嵴細胞遷移異常所致。正常發育中,胚胎7-10週時形成角膜緣原基,決定角膜曲率和角膜-鞏膜邊界。該結構未能形成導致鞏膜與角膜的正常邊界紊亂,角膜曲率變平。
- CNA1(扁平角膜1型):體染色體顯性遺傳。基因座位於第12號染色體長臂,但致病基因尚未確定。
- CNA2(扁平角膜2型):體染色體隱性遺傳。由12q22-q23區域的KERA基因突變引起。KERA基因編碼角膜透明性重要的硫酸角質素蛋白聚醣——角蛋白聚醣(keratocan)。CNA2伴有更嚴重的角膜扁平化和前節異常。
- PAX6、FOXC1、PITX2:突變可能伴有虹膜角膜粘連、瞳孔異位、虹膜萎縮。
- RAD21:在鞏膜化角膜家系中發現的突變。通過WNT9B信號調控神經嵴細胞向角膜角質細胞或鞏膜基質細胞的分化方向。
4. 診斷與檢查方法
Section titled “4. 診斷與檢查方法”眼科檢查
全身檢查
遺傳學檢查:檢測KERA、PAX6、FOXC1、PITX2、RAD21等基因的突變。與遺傳諮詢一起進行。
全身性評估:檢查是否有相關的全身異常,如智能障礙、聽力損失、心血管畸形和泌尿生殖器畸形。
- Peters異常:中央角膜混濁伴有Descemet膜和角膜內皮缺損。表現為虹膜角膜沾黏或虹膜水晶體沾黏。
- 先天性青光眼:角膜水腫導致的混濁,通過角膜直徑增大(牛眼)和Descemet膜破裂(Haab紋)進行鑑別。
- 先天性遺傳性角膜內皮營養不良(CHED):雙側瀰漫性角膜水腫和混濁,但角膜緣清晰。
- 分娩外傷:通常為單側,伴有Descemet膜破裂。
5. 標準治療方法
Section titled “5. 標準治療方法”對於影響視軸的角膜混濁,穿透性角膜移植術(PKP)是首選。為避免形覺剝奪性弱視,應盡早進行手術。然而,視力預後較差,且移植排斥率較高。
移植成績的報告:
- 鞏膜化角膜的全層角膜移植顯示約75%的失敗率,主要原因是角膜緣區域的新生血管形成。
- 一項包括15隻全型和12隻部分型眼的病例系列報告了1年移植片存活率為70%。
- 在兒童病例中,1年後的移植片透明維持率據報導僅約37%。
在角膜移植失敗的病例中,周邊新生血管形成是危險因子,同時可能需要前段重建手術(如隅角重建術、瞳孔成形術、水晶體摘除術、人工水晶體復位術等)1)。
在視軸保留的部分型中,應儘早進行光學矯正(眼鏡),以預防高度遠視引起的弱視。合併青光眼的病例需要眼藥水或手術進行眼壓管理。
鞏膜化角膜的角膜移植預後不良。據報導,1年移植片存活率為37-70%,最終失敗率為75%。主要失敗因素是角膜緣區域的新生血管形成。兒童病例預後更差,可能需要多次再移植。
6. 病理生理學與詳細發病機轉
Section titled “6. 病理生理學與詳細發病機轉”眼部發育與神經嵴細胞的角色
Section titled “眼部發育與神經嵴細胞的角色”正常前段發育涉及三個重要過程:前腦神經外胚層的形成、水晶體泡從表面外胚層的分離,以及神經嵴來源的間質前驅細胞向前遷移。
在正常發育中,妊娠4週水晶體泡分離後,表面外胚層分化為角膜上皮。妊娠6週,視杯前緣附近的神經嵴細胞進入角膜上皮和水晶體之間,形成Bowman層和角膜內皮。隨後,神經嵴細胞再次進入Bowman層和角膜內皮之間,形成角膜基質。妊娠7週,神經嵴細胞開始形成鞏膜,從前向後進展,妊娠5個月時到達後極部。
在鞏膜化角膜中,胚胎7-10週時角膜緣原基未能形成,因此角膜與鞏膜之間無法建立正常邊界。結果導致角膜曲率變平,角膜基質呈現鞏膜樣特性。
- 上皮:免疫組織化學染色顯示角蛋白3和12陽性(角膜上皮標誌物),證實其來源於角膜。未見杯狀細胞。
- Bowman層:缺失或伴隨不規則的玻璃樣物質斑塊。
- 基質:膠原纖維的層狀結構紊亂,排列不規則。纖維直徑不一致,深層纖維較細(鞏膜樣特徵)。然而,硫酸角質素等糖胺聚醣和I型膠原的存在表明基質來源於角膜而非鞏膜。前部和中部基質有來自上鞏膜和結膜的血管侵入。
- Descemet膜:缺失或變薄(0.8-1.5 μm),伴有均質物質和纖維母細胞增殖。
- 內皮:部分病例報告內皮完全缺失。
在鞏膜化角膜中,角膜基質的膠原纖維排列不規則,層狀結構紊亂,因此無法維持角膜的透明性。正常角膜中均勻膠原纖維的規則排列控制光干涉並保持透明,但在鞏膜化角膜中這種結構被破壞。此外,全層角膜的血管侵入也是混濁的原因。
7. 最新研究與未來展望
Section titled “7. 最新研究與未來展望”在一個鞏膜化角膜家系中發現了RAD21基因突變。RAD21是黏連蛋白複合體的組成部分,參與基因表現的調控。研究發現,在受RAD21表現影響的過程中,WNT9B在決定神經嵴細胞分化為角膜角質細胞或鞏膜基質細胞的方向上扮演至關重要的角色。
這一發現為理解角膜和鞏膜基質細胞雖均來源於神經嵴細胞卻具有不同組織特性的原因提供了線索。未來有望透過調控WNT9B訊息傳導路徑開發新的治療策略。
8. 參考文獻
Section titled “8. 參考文獻”- American Academy of Ophthalmology. Corneal Edema and Opacification Preferred Practice Pattern. Ophthalmology. 2024.
