기타 구성 질환①

전안부 발생 이상
한눈에 보는 포인트
섹션 제목: “한눈에 보는 포인트”1. 전안부 발생 이상이란?
섹션 제목: “1. 전안부 발생 이상이란?”전안부 발생 이상(anterior segment developmental anomalies; ASDA)은 전안부 형성 이상(anterior segment dysgenesis; ASD)이라고도 불리며, 각막, 홍채, 수정체, 전방각 등 전안부 구조에 발생하는 선천성 발생 장애를 총칭하는 개념입니다1).
이러한 질환들은 표현형 및 유전학적으로 매우 다양하지만, 방수 유출로(섬유주 및 슐렘관)의 발육 이상에 기반한 안압 상승, 즉 발달 녹내장이 공통적인 중요한 합병증이 됩니다1,2).
ASDA에 포함되는 주요 질환으로는 후태생환, Axenfeld-Rieger 증후군(ARS), Peters 이상, 원발 선천 녹내장(PCG), 무홍채증, 선천 유전 각막 내피 이영양증(CHED), 후부 다형 각막 이영양증(PPCD), 공막화 각막, 거대 각막, 홍채각막내피(ICE) 증후군 등이 있습니다.
전안부의 발생에는 신경능선 유래 간엽 세포가 관여하며, 이 세포군은 섬유주와 슐렘관의 발생에도 기여합니다. 전안부의 형성 이상이 발생하는 경우, 방수 유출로의 구조도 동시에 손상되는 경우가 많아 방수 유출 저항이 증가하여 안압이 상승합니다. 따라서 발달 녹내장은 ASDA의 공통적인 합병증이 됩니다.
2. 주요 구성 질환
섹션 제목: “2. 주요 구성 질환”Axenfeld-Rieger 증후군(ARS)
섹션 제목: “Axenfeld-Rieger 증후군(ARS)”ARS는 안구 증상과 전신 증상을 나타내는 상염색체 우성 질환이다. 안구 소견으로는 후부 태생환(전방으로 전위되고 비후된 슈발베선), 홍채 저형성, 다동공증, 홍채 편위가 나타난다. 돌출된 슈발베선과 홍채 유착을 보이는 것을 악센펠트 이상, 추가로 홍채 및 실질 위축을 보이는 것을 리거 이상이라고 한다. 전신 소견으로 골 발육 이상이나 치아 이상 등을 동반하는 경우를 리거 증후군이라고 부른다. 각막은 일반적으로 정상이고 내피 구조도 정상이나, 잔류물에 의한 물리적 접촉으로 이차적으로 혼탁을 초래할 수 있다. PITX2(4번 염색체) 및 FOXC1(6번 염색체)의 전사인자 유전자 변이가 원인이 되며, 5075%에서 녹내장이 합병된다1). 녹내장은 유아기부터 발병하는 경우도 있지만, 대부분 소아기청년기에 발병한다. FOXC1 변이와 PITX2 변이는 표현형이 달라, FOXC1 변이에서는 각막 이상이 50%, PITX2 변이에서는 16%라는 보고가 있다2).
피터스 이상
섹션 제목: “피터스 이상”각막 중앙 혼탁과 각막 내피 및 데스메막 결손을 특징으로 하는 선천성 질환이다. 80%가 양안성이며, 홍채각막 유착이나 수정체각막 유착을 동반할 수 있다. PAX6, PITX2, CYP1B1의 변이가 관련된다. 피터스 플러스 증후군에서는 구순열, 저신장, 정신 발달 지연 등의 전신 이상을 동반하며, B3GLCT 유전자의 변이(상염색체 열성)가 원인이다3). 중증 예에서는 각막 이식이 필요하지만, 수정체각막 유착을 합병하는 경우의 예후는 불량하다3).
원발 선천 녹내장(PCG)
섹션 제목: “원발 선천 녹내장(PCG)”섬유주 발달 이상을 원인으로 하는 상염색체 열성 질환이다. CYP1B1 유전자(GLC3A 유전자좌, 2p21)의 변이가 가장 많다4). 일본 소아 녹내장 코호트에서는 CYP1B1 변이가 약 20%에서 검출되었고, FOXC1 변이도 인정된다고 보고되었다4). 일본에서는 약 10만 명당 1명의 빈도로, 75%가 양안성, 65%가 남아에서 발병하며, 80%가 생후 1년 이내에 발병한다. 영유아의 높은 안압은 각막 직경 증가(우안), 각막 부종·혼탁, 데스메막 파열(Haab 선조)을 유발한다.
무홍채증
섹션 제목: “무홍채증”홍채 저형성을 주체로 하는 상염색체 우성 질환으로, PAX6 유전자(11번 염색체)의 변이가 원인이다5). 홍채의 부분적~전주위 결손에 더해, 수정체 탈구, 각막 혼탁, 황반 저형성에 의한 시력 장애를 동반할 수 있다. 인접한 WT1 유전자의 결실을 합병하면 WAGR 증후군(윌름스 종양·무홍채증·비뇨생식기 이상·정신 지체)의 위험이 있어, WT1 평가가 필요하다. WT1 결실 예에서는 8세까지 3개월마다 신장 초음파 검사와 소아 종양과의 추적 관찰이 권장된다5).
기타 구성 질환②
공막화각막: 불투명한 공막 조직이 비염증성·비진행성으로 주변부 각막에 침입하여 각막과 공막의 경계가 불명확해진다. FOXE3, PAX6 등의 돌연변이가 관련된다.
거대각막: 각막 직경이 12.5mm 이상으로 확대되는 질환으로, CHRDL1 유전자 돌연변이에 의한 X-연관 열성 유전이 많다. 안압과 내피 세포는 일반적으로 정상이다. 선천 거대각막은 Haab 선조나 유두 함몰 확대를 보이지 않는다는 점에서 PCG와 감별된다.
3. 증상과 임상 소견
섹션 제목: “3. 증상과 임상 소견”영유아 발달 녹내장
섹션 제목: “영유아 발달 녹내장”발달 녹내장의 초발 증상은 안압 상승에 따른 각막 상피 부종의 자극 증상이다. 구체적으로는 눈곱을 동반하지 않는 눈물흘림, 눈부심, 눈꺼풀 경련이 나타난다. 높은 안압이 지속되면 각막 상피 부종이 심해져 각막 혼탁을 초래한다. 또한 안구 피막(특히 각결막 이행부)이 신장되어 각막 직경의 증가(소안)와 전방 깊이의 증가를 보인다.
각막이 신장되면 탄력성이 낮은 데스메막에 파열이 발생하고(Haab 선조), 전방수가 각막 실질로 유입되어 각막 부종·혼탁이 급속히 악화된다. Haab 선조는 영구적인 혼탁을 남겨 시력 장애의 원인이 된다.
| 소견 | 정상치·기준 |
|---|---|
| 신생아 각막 직경 | 9.5 |
| 시신경 유두 함몰비(C/D비) | 영아에서는 0.3 이상이면 녹내장 의심. 좌우차 0.2 이상도 녹내장 시사 |
전안부 형성 이상과 관련된 소견
섹션 제목: “전안부 형성 이상과 관련된 소견”각 질환에 특징적인 전안부 소견을 확인한다. 후부 태생환 (Schwalbe선의 전방 전위 및 비후)은 ARS 및 Alagille 증후군과 관련된다. 홍채 저형성, 다동공증, 홍채 편위는 ARS에 특징적이다. 각막 중심 혼탁과 홍채각막 유착은 Peters 이상을 시사한다.
4. 진단과 검사
섹션 제목: “4. 진단과 검사”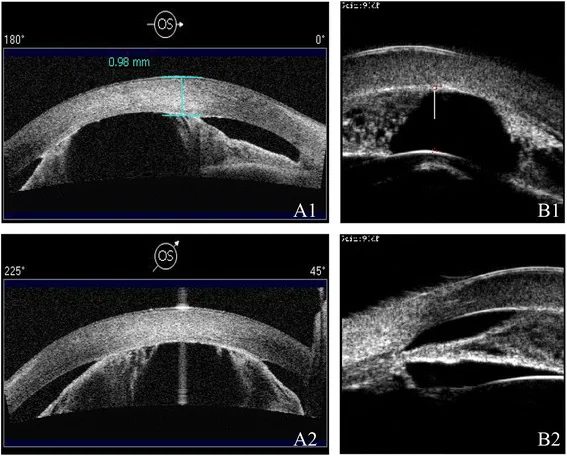
소아 녹내장의 진단 기준
섹션 제목: “소아 녹내장의 진단 기준”녹내장 진료 가이드라인 (제5판) 6) 및 국제 소아 녹내장 연구 네트워크 (CGRN) 분류 7)에 따르면, 다음 5개 항목 중 2개 이상을 충족할 때 소아 녹내장으로 진단된다.
- 안압이 21 mmHg를 초과
- 시신경 유두 함몰비 (C/D비) 증가의 진행, 좌우 비대칭 증가, 테두리 얇아짐
- 각막 소견 (Haab 선조, 신생아에서 각막 직경 11mm 이상, 1세 미만에서 12mm 이상, 전 연령에서 13mm 이상)
- 안축장의 정상 발달을 초과한 신장으로 인한 근시화
- 녹내장성 시신경병증에 부합하는 재현성 있는 시야 결손
검사 시 주의사항
섹션 제목: “검사 시 주의사항”5세 이하 소아에서는 진정 또는 전신 마취 하에 검사가 필요한 경우가 많습니다. 전신 마취 하에서는 안압이 각성 시보다 낮아지므로 측정값 해석에 주의가 필요합니다. 전방각 검사는 휴대용 세극등과 Koeppe 렌즈 등의 직접형 전방각경을 사용합니다. 각막 혼탁으로 전방각경 관찰이 어려운 경우 초음파 생체현미경(UBM)이 유용합니다.
병형 진단에서는 전안부 소견에 따라 감별을 시행합니다. 후부 태생환, 홍채 이상(ARS), 백내장(피터스 이상)의 유무를 확인합니다. 유전성이 의심되는 경우 혈연자의 녹내장 검사와 유전자 검사를 고려합니다.
전신 마취에 사용되는 모든 약물은 안압을 낮춥니다(유일한 예외는 케타민으로 약간 상승시킬 수 있음). 따라서 전신 마취 하의 안압 측정값만으로는 녹내장을 배제할 수 없습니다. 가능한 한 각성 시 측정을 시행하고, 각막 직경, Haab 선조, 시신경 유두 함몰 등 안압 외 소견을 종합적으로 평가하는 것이 중요합니다.
5. 치료
섹션 제목: “5. 치료”치료 방침
섹션 제목: “치료 방침”조기 발현 발달성 녹내장은 기본적으로 수술적 치료가 필요한 질환으로, 약물 요법은 수술 전 단기간의 안압 하강 및 수술 후 보조적 치료로 위치 지어집니다. 환자가 영유아이므로 재수술이 필요한 경우가 드물지 않음을 보호자에게 충분히 설명하고 이해를 얻는 것이 중요합니다.
수술 치료
섹션 제목: “수술 치료”초회 수술로는 전방각 절개술(고니오토미) 또는 섬유주 절개술(트라베큘로토미)이 시행됩니다. 이 수술들은 방수 유출로의 발달 이상에 직접 개입하는 술식입니다. 실패할 경우 여과 수술이나 튜브 션트 수술이 고려됩니다.
안압이 조절된 후에도 약시 치료가 필요한 경우가 많습니다. 굴절 부등시, 불규칙 난시, 각막 혼탁 및 Haab 선조는 약시의 원인이 되므로, 수술 후에도 시력 및 굴절 검사를 정기적으로 시행합니다.
각막 혼탁이 심한 피터스 이상에서는 각막 이식(전층 각막 이식)이 적응이 되지만, 수정체 각막 유착을 동반한 중증 예에서는 이식편 부전의 위험이 높습니다.
6. 병태생리학 및 상세한 발병 기전
섹션 제목: “6. 병태생리학 및 상세한 발병 기전”신경능선 세포와 전안부 발생
섹션 제목: “신경능선 세포와 전안부 발생”전안부 발생에서 표면 외배엽 유래 각막 상피와 수정체, 신경외배엽 유래 망막색소상피가 신경능선 유래 간엽 세포와 상호작용하여 정상적인 전안부 구조를 형성합니다. 신경능선 세포는 각막 실질, 각막 내피, 섬유주, 홍채 실질 등의 형성에 관여합니다. 이들의 이동이나 분화 이상이 전안부 형성 이상을 유발합니다.
주요 관련 유전자
섹션 제목: “주요 관련 유전자”50개 이상의 유전자가 ASDA와 관련된 것으로 밝혀졌지만, 여전히 40~75%의 증례에서 유전적 원인이 확인되지 않았습니다.
| 유전자 | 염색체 | 관련 질환 | 유전 양식 |
|---|---|---|---|
| PITX2 | 4q25 | ARS, 피터스 이상 | 상염색체 우성 |
| FOXC1 | 6p25 | ARS, 홍채각막각형성부전 | 상염색체 우성 |
| PAX6 | 11p13 | 무홍채증, 피터스 이상 | 상염색체 우성 |
| CYP1B1 | 2p21 | 원발 선천성 녹내장 | 상염색체 열성 |
ARS에서 FOXC1과 PITX2는 물리적으로 상호작용하며 신경능선 세포의 정상적인 분화에 필수적입니다. 이 상호작용으로 인해 두 유전자 중 하나의 돌연변이가 유사한 표현형을 유발할 수 있습니다.
모든 경우에서 확진할 수 있는 것은 아닙니다. 4075%의 증례에서는 현재 유전적 원인이 확인되지 않았습니다. 그러나 유전자 검사는 질환 유형 감별(예: 무홍채증의 PAX6 돌연변이와 인접 WT1 유전자 평가를 통한 WAGR 증후군 배제), 가족 내 선별검사, 유전 상담에 유용합니다. 특히 ARS에서는 친척의 5075%가 녹내장을 발병할 수 있으므로 유전자 검사와 가족의 안압 및 녹내장 검사가 권장됩니다.
7. 참고문헌
섹션 제목: “7. 참고문헌”- Michels K, Bohnsack BL. Ophthalmological manifestations of Axenfeld-Rieger syndrome: current perspectives. Clin Ophthalmol. 2023;17:819-828.
- Prem Senthil M, Knight LSW, Taranath D, et al. Comparison of anterior segment abnormalities in individuals with FOXC1 and PITX2 variants. Cornea. 2022;41(8):1009-1015.
- Khasnavis A, Fernandes M. Peters anomaly: an overview. Taiwan J Ophthalmol. 2023;13(4):434-442.
- Fuse N, Kimura M, Shimizu A, et al. Mutations of CYP1B1 and FOXC1 genes for childhood glaucoma in Japanese individuals. Jpn J Ophthalmol. 2024;68(6):688-701.
- Moosajee M, Hingorani M, Moore AT. PAX6-Related Aniridia. In: Adam MP, et al, eds. GeneReviews®. Seattle: University of Washington; updated 2018.
- Kiuchi Y, Inoue T, Shoji N, et al. The Japan Glaucoma Society guidelines for glaucoma 5th edition. Jpn J Ophthalmol. 2023;67(2):189-254.
- Thau A, Lloyd M, Freedman S, et al. New classification system for pediatric glaucoma: implications for clinical care and a research registry. Curr Opin Ophthalmol. 2018;29(5):385-394.
- Choe S, Lee KS, Ha A, et al. Association of maternal exposure to fine particulate matter during pregnancy with anterior segment dysgenesis risk: a matched case-control study. J Clin Med. 2025;14(9):3003.
