밸브형 (Valved)

녹내장 배액 장치(관 션트 수술)
한눈에 보는 포인트
섹션 제목: “한눈에 보는 포인트”1. 녹내장 배액 장치란?
섹션 제목: “1. 녹내장 배액 장치란?”녹내장 배액 장치(GDD)는 방수 션트(aqueous shunt) 또는 튜브 션트라고도 불리는 임플란트입니다. 실리콘 튜브와 플레이트로 구성되며, 튜브를 안구 내에 삽입하고 플레이트를 안구 적도부 근처의 공막 위에 고정합니다. 방수는 튜브를 통해 안구 외부의 플레이트로 유도되며, 수술 후 4~6주에 플레이트 주변에 형성되는 섬유성 피막(fibrous capsule)을 통해 주변 조직에 흡수됩니다1).
기존의 여과 수술(섬유주 절제술)로 안압 조절이 어려운 녹내장 증례에 대한 치료 선택지로 자리 잡고 있습니다. 튜브는 전방 내 삽입과 유리체강 내 삽입으로 나뉘며, 유리체의 유무와 목표 안압에 따라 선택합니다.
국내에서는 바르벨트® 녹내장 임플란트와 아메드® 녹내장 밸브의 두 종류가 건강보험 진료에서 사용 가능합니다(2012년 건강보험 적용). 플레이트가 없는 익스프레스® 녹내장 여과 장치도 승인되었습니다12).
적응증
섹션 제목: “적응증”GDD의 적응증은 다음과 같습니다12).
- 항대사약물 병용 섬유주절제술 실패 사례: 권장 등급 1B
- 결막 반흔화가 심한 사례: 수술 과거력으로 인한 광범위한 결막 유착
- 섬유주절제술 성공이 어려운 사례: 신생혈관녹내장, 포도막염 속발녹내장, ICE 증후군(홍채각막내피증후군)
- 다른 여과 수술이 기술적으로 어려운 사례
- 난치성 소아 녹내장: 각수술이 효과가 없는 경우3)
- 외상성 녹내장, 무수정체안/인공수정체안 녹내장, 각막이식 후 녹내장2)
원발개방각녹내장(POAG)의 경우 첫 수술로 권장되지 않습니다. 재수술 사례에서 적응증을 고려합니다. 또한 정상안압녹내장(NTG)에 대한 증거는 불충분하며 향후 검토가 필요합니다12).
주요 적응증은 항대사약물을 병용한 섬유주절제술이 실패한 사례나 수술 과거력으로 결막 반흔화가 심한 사례입니다(권장 등급 1B)12). 신생혈관녹내장, 포도막염 속발녹내장, ICE 증후군 등 섬유주절제술 성공이 어려운 질환형에서도 적응됩니다. 원발개방각녹내장에서는 첫 수술로 권장되지 않으며 재수술 사례에서 고려합니다.
2. 주요 증상과 임상 소견
섹션 제목: “2. 주요 증상과 임상 소견”관류관 단락 수술이 고려되는 병태
섹션 제목: “관류관 단락 수술이 고려되는 병태”GDD는 녹내장 자체의 치료법이므로 적응증 판단에 관련된 임상 양상의 이해가 중요합니다. 다음 질환형이나 배경 인자를 가진 사례에서는 섬유주절제술의 성공률이 낮아 GDD가 고려됩니다.
섬유주절제술이 효과가 적은 질환형:
- 포도막염 속발 녹내장: 염증으로 인한 결막 반흔화가 여과포 유지를 어렵게 합니다.
- 신생혈관 녹내장: 홍채 및 전방각의 신생혈관으로 인한 여과포 폐쇄 위험이 높습니다.
- ICE 증후군: 각막 내피세포 증식으로 여과포가 덮입니다.
내안 수술 과거력이 있는 증례:
환자 배경 인자:
- 젊은 환자(상처 치유 반응이 강함)
- 여러 차례 수술 과거력이 있는 증례
수술 후 주의해야 할 임상 소견
섹션 제목: “수술 후 주의해야 할 임상 소견”GDD 수술 후 다음 소견이 나타나면 합병증으로 대처가 필요합니다.
- 수술 후 고안압기(Baerveldt® 특유): 수술 후 약 1개월간 20 mmHg 전후의 고안압으로 경과합니다.
- 튜브 노출: 패치 이식편 아래에서 튜브가 결막 밖으로 노출된 상태입니다.
- 저안압: 특히 비밸브형에서 수술 후 조기에 발생할 수 있습니다.
- 복시: 플레이트 위치로 인한 외안근의 기계적 제한
3. 원인 및 위험 요인
섹션 제목: “3. 원인 및 위험 요인”GDD 수술이 필요한 난치성 녹내장의 배경 요인은 다음과 같습니다.
- 다수의 내안 수술 병력: 결막 반흔화가 진행되어 여과포 형성 및 유지가 어려움
- 젊은 연령: 섬유아세포 활동이 활발하여 상처 치유 반응이 강하고 여과 수술 실패율이 높음
- 포도막염, 신생혈관녹내장 등의 속발성 녹내장: 염증이나 신생혈관이 여과포를 파괴함
- 결막 반흔화: 화학 외상, 스티븐스-존슨 증후군, 다수의 결막 수술 등으로 인함
PTVT 연구(첫 수술안 비교)에서 튜브군의 실패율이 재수술안을 대상으로 한 TVT 연구보다 높았던 점은 연구군의 연령이 낮고 흑인 비율이 높은 것이 영향을 미친 것으로 고려됩니다12).
4. 장치 종류 및 선택
섹션 제목: “4. 장치 종류 및 선택”밸브형 vs 비밸브형
섹션 제목: “밸브형 vs 비밸브형”GDD는 안압 조절 밸브의 유무에 따라 두 가지로 분류됩니다.
논밸브형
대표: Baerveldt® 녹내장 임플란트
기전: 밸브 기전 없음. 수술 중 흡수성 봉합사(Vicryl®)로 튜브를 완전 결찰하고, 여러 개의 Sherwood slit(일시적 누출공)을 만들어 초기 부분 유출을 확보합니다.
장점: 장기적인 안압 하강에 우수함 (5년째 안압 18 mmHg 미만 유지: 약 70%). 도달 가능한 안압이 더 낮음 15)
단점: 수술 후 약 1개월간의 고안압기가 있음. 저안압 위험이 밸브형보다 높음 (4.5% vs 0.4%) 12)
수술 후 관리: 흡수성 봉합사가 녹을 때까지 약 1개월간 녹내장 점안약을 병용하여 안압을 관리합니다.
국내 승인 기기의 사양
섹션 제목: “국내 승인 기기의 사양”국내에서 승인된 플레이트형 GDD 목록은 다음과 같습니다 12).
| 기기 | 모델 | 플레이트 면적 | 삽입 부위 | 비고 |
|---|---|---|---|---|
| 바벨트® | BG101-350 | 350 mm² | 전방 | 표준 크기 |
| 바벨트® | BG103-250 | 250 mm² | 전방 | 소아/짧은 안축장 |
| 바벨트® | BG102-350 | 350 mm² | 모양체 평면부 | 유리체 수술 과거력이 있는 눈 |
| Ahmed® | FP7 | 184 mm² | 전방 | 조압밸브 내장, 가장 범용적 |
| Ahmed® | FP8 | 96 mm² | 전방 | 소아, 짧은 안축장 |
플레이트가 없는 GDD로 Ex-PRESS® 녹내장 여과 장치(전장 2.6 mm, 내강 50 μm, 스테인리스 스틸)가 있습니다. 공막판 아래에서 전방 내로 삽입합니다. 폐쇄각 녹내장, 포도막염, 금속 알레르기는 금기입니다. 3테슬라까지의 MRI 검사는 안전한 것으로 간주됩니다12).
장치 선택 기준
섹션 제목: “장치 선택 기준”Baerveldt®와 Ahmed®의 선택은 다음 기준에 따라 결정됩니다.
- 더 낮은 안압을 목표로 하는 경우: Baerveldt®가 적합합니다. 수술 후 합병증 위험을 고려하더라도 장기적인 안압 조절에 우수합니다.
- 수술 직후부터 안압을 낮추고 싶거나 저안압이 위험한 경우: Ahmed®가 적합합니다. 무수정체안, IOL 봉합안, 박출성 출혈 과거력안, 포도막염 속발 녹내장 등이 해당됩니다.
장기적인 안압 조절은 플레이트 표면적에 의존합니다. 플레이트 면적이 클수록 주변 섬유성 피막도 크게 형성되어 더 많은 방수를 흡수할 수 있습니다. 이중 플레이트 Molteno는 단일 플레이트보다 안압 조절이 우수했으며, 350 mm²와 500 mm² Baerveldt의 비교에서는 350 mm² 모델이 더 우수했습니다1).
수술 후 합병증 위험을 고려하더라도 더 낮은 안압을 목표로 하는 증례에서는 Baerveldt®(비밸브형)를 선택합니다. 수술 직후부터 안압을 낮추고자 하는 증례나 저안압이 위험한 증례(무수정체안, 포도막염 속발 녹내장 등)에서는 Ahmed®(밸브형)를 선택합니다. 메타분석에서 Baerveldt®의 수술 후 평균 안압(13.2 mmHg)이 Ahmed®(15.8 mmHg)보다 유의하게 낮았지만15), 저안압 발생률은 Baerveldt®가 더 높습니다(4.5% vs 0.4%)12).
5. 수술 술기와 합병증 관리
섹션 제목: “5. 수술 술기와 합병증 관리”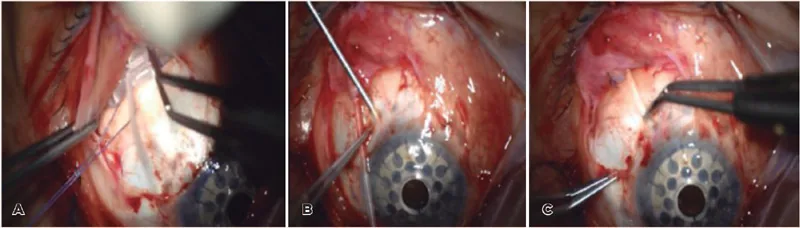
Baerveldt® 녹내장 임플란트(전방 내 튜브 삽입법)
섹션 제목: “Baerveldt® 녹내장 임플란트(전방 내 튜브 삽입법)”- 설치 부위 선택: 상이측을 첫 번째 선택으로 합니다. 기존 수술 창으로 인해 설치가 불가능한 경우 비측이나 하측을 고려하지만, 하측은 감염 위험이 높고 비측은 안구 운동 장애가 발생하기 쉬우므로 가능한 한 피합니다.
- 결막 절개: 원개부 기저로 절개하고, 인접한 두 직근이 노출될 수 있는 범위에서 시행합니다. 결막과 결막하 조직을 가능한 한 후방까지 박리합니다.
- 플레이트 고정: 플레이트 양 끝을 인접한 두 직근 아래에 삽입하고, 윤부에서 8~10 mm 위치에 나일론 봉합사로 공막에 봉합합니다.
- 튜브 결찰(저안압 예방): 플레이트 2~4 mm 앞에서 흡수성 봉합사(Vicryl®)로 튜브를 완전 결찰합니다.
- Sherwood slit 생성(고안압 예방): 바늘이나 메스로 튜브에 일시적인 누출공을 여러 개 내어 수술 직후의 고안압을 완화합니다.
- 튜브 트리밍: 전방 내에 2~3 mm 삽입할 수 있는 길이로 베벨 업(bevel-up) 상태에서 트리밍합니다.
- 튜브 삽입: 각공막 윤부에 23게이지 바늘로 홍채면과 평행하게 천자공을 만들고 튜브를 전방 내에 삽입합니다.
- 튜브 고정 및 피복: 나일론 봉합사로 공막에 고정하고, 보존 공막이나 보존 각막 등의 패치 재료로 튜브를 덮습니다(권장 등급 1A)12).
- 결막 봉합: 흡수성 봉합사로 결막을 봉합하여 덮고 종료합니다.
Ahmed® 녹내장 밸브의 추가 요점
섹션 제목: “Ahmed® 녹내장 밸브의 추가 요점”기본 수기는 Baerveldt®와 동일하지만, 다음 사항이 다릅니다.
- 프라이밍: 튜브 끝에서 관류액을 주입하여 조압밸브가 열리는지 확인합니다.
- 결막 절개 범위: 플레이트 크기가 작기 때문에 Baerveldt®보다 좁은 절개로 시행 가능합니다.
- 결찰 및 누출공 불필요: 조압밸브로 수술 직후 저안압이 방지되므로 튜브 결찰이나 Sherwood slit 생성이 필요하지 않습니다.
유리체강 내 튜브 삽입법 (편평부 튜브)
섹션 제목: “유리체강 내 튜브 삽입법 (편평부 튜브)”유리체 수술 과거력이 있는 눈에서는 전방 대신 모양체 편평부에서 튜브를 삽입하는 방법이 있습니다.
- 각막 윤부에서 3.5 mm 떨어진 모양체 편평부 위치에 20게이지 바늘 또는 20G V-랜스로 유리체강 내로 천자합니다.
- Hoffmann® 엘보를 삽입하고 나일론 봉합사로 공막 위에 고정합니다.
- 패치 재료로 덮고 결막을 봉합합니다.
Baerveldt® BG102-350이 이 삽입법에 대응합니다. Ahmed®에는 모양체 편평부에서 삽입하는 모델이 국내에서 판매되지 않습니다.
수술 후 관리
섹션 제목: “수술 후 관리”- 항생제 점안액: 하루 3회, 2주간.
- 스테로이드 점안액: 점감하며 약 6개월간 지속합니다.
- Baerveldt® 수술 후 고안압기: 관을 결찰한 흡수성 봉합사가 녹을 때까지 약 1개월간 안압이 20mmHg 전후로 높게 유지됩니다. 녹내장 점안약 또는 경구약으로 안압을 조절하며, 1~2개월 후 안압이 하강하는 경우가 많습니다. 나일론 봉합사를 관에 통과시켜 조기 고안압 시 나일론 봉합사를 제거하여 안압을 조절하는 방법도 있습니다.
논밸브형 저안압 예방법
섹션 제목: “논밸브형 저안압 예방법”논밸브형 장치에서는 수술 후 조기 저안압을 방지하기 위해 다음과 같은 방법이 사용됩니다.
- 관내 스텐트: 4-0 또는 5-0 봉합사를 관 내강에 삽입하고, 피막 형성 후 세극등 하에서 제거합니다.
- 외부 결찰: 흡수성 봉합사(7-0 또는 8-0 Vicryl®)로 관을 결찰합니다. 조기 부분 유출을 위해 벤팅 슬릿을 병용하기도 합니다.
- 2단계 수술: 첫 단계에서 플레이트만 고정하고, 4~6주 후 피막 형성을 기다려 관을 전방에 삽입합니다.
주요 합병증
섹션 제목: “주요 합병증”관 노출: GDD 특유의 합병증으로, 4.3~14.3%의 빈도로 발생합니다7). 결막 미란을 통해 관이 노출되며, 안내염 위험이 있으므로 조기 복구가 필요합니다8). 패치 이식편 추가 또는 공막 터널 피복이 시행됩니다. 관 노출 방지를 위해 보존 공막이나 보존 각막 등의 패치 재료를 사용하거나, 자가 공막 반층판으로 관을 덮어야 합니다(권고 수준 1A)12).
저안압: 특히 논밸브형에서 많습니다1). Baerveldt®의 저안압 발생률은 4.5%, Ahmed®는 0.4%입니다12). 전방 깊이가 유지되면 보존적으로 관리 가능하지만, 수정체-각막 접촉이 있는 경우 점탄물질 주입으로 전방 재형성이 필요합니다.
관 폐쇄: 피브린, 홍채, 출혈, 유리체에 의한 폐쇄가 발생할 수 있습니다. 전방 내 관은 Nd:YAG 레이저, 유리체강 내 관은 유리체 절제술로 대처합니다6). 각막 혼탁 예에서는 안내 내시경이 원인 확인과 치료에 유용합니다6).
복시 및 안구 운동 장애: 수술 후 약 5%에서 발생합니다. 플레이트의 상비측 삽입은 피하는 것이 바람직합니다. 6개월 경과 관찰 후 프리즘 안경 또는 수술로 대응합니다.
각막 내피 손상: 관 끝이 각막 내피에 근접한 경우 장기적인 각막 내피 세포 감소와 수포성 각막병증을 초래할 수 있습니다1). 고령자에서는 백내장 동시 수술을 권장하기도 합니다.
테논 낭종(피막화): 플레이트 주변의 섬유성 피막이 비후되어 안압이 상승합니다. AGV에서의 빈도는 4080%, 논밸브형에서는 2030%로 알려져 있습니다10). 수술 후 3주~3개월의 ‘고안압기(hypertensive phase)‘로 나타나는 경우가 많습니다.
거대 여과포: 드물게 플레이트 주변에 거대 여과포가 형성됩니다5). 전방 확대형(이물감, 미용 문제)과 후방 확대형(안구 편위, 복시, T2 강조 MRI 평가 유용)으로 분류됩니다5). GDD 제거 후 포도막염이 발생한 보고도 있습니다11).
TVT 연구의 5년 데이터에 따르면, 심각한 합병증 발생률은 튜브군에서 34%, 섬유주절제술군에서 36%였습니다13). 주요 합병증으로는 튜브 노출(4.3~14.3%)7), 저안압(Baerveldt® 4.5%, Ahmed® 0.4%)12), 복시(약 5%)가 있습니다. 합병증의 내용은 두 수술법 간에 다릅니다: 튜브 션트 쪽에서는 각막내피손상과 튜브 노출이, 섬유주절제술 쪽에서는 여과포 누출, 저안압 황반병증, 여과포 감염이 많습니다13).
6. 비교 연구와 근거
섹션 제목: “6. 비교 연구와 근거”CQ4: 튜브 션트 수술을 섬유주절제술 대신 권장하는가?
섹션 제목: “CQ4: 튜브 션트 수술을 섬유주절제술 대신 권장하는가?”녹내장 진료 가이드라인(제5판)의 CQ4에서는 튜브 션트 수술과 섬유주절제술의 선택에 대해 다음과 같은 권고를 제시하고 있습니다12).
- 권고문: 두 수술법의 선택에 있어서는 치료안·환자 배경, 술자의 수술법 숙련도 등을 고려하여 선택하는 것이 권장됩니다.
- 권고의 강도: ‘시행하지 않음’을 약하게 권장함
- 근거의 강도: C (약함)
안압 조절 성적에서는 두 수술법 간에 유의한 차이가 없었고, 시기능을 손상시키는 심각한 합병증의 발생 빈도에도 유의한 차이가 없었습니다. 다만 저안압에 따른 합병증과 수술 후 감염은 섬유주절제술에 많고, 임플란트 노출과 각막내피손상은 튜브 션트 수술에 많습니다12).
섬유주절제술과의 비교
섹션 제목: “섬유주절제술과의 비교”섬유주절제술이 유리한 점
임플란트 불필요: 이물질이 없고, 튜브 노출 위험이 없습니다1).
각막 내피: 장기적인 각막 내피 손상 위험이 낮음
비용: 보존적 치료와 비교한 QALY당 비용은 섬유주절제술 $8,289, 바르벨트® $13,896로, 섬유주절제술이 저비용임12)
GDD의 유리한 점
여과수술 고위험군: 결막 반흔, 속발녹내장에 적합함1)
수술 후 관리: 수술 후 관리 부담이 상대적으로 적음
재수술: TVT 연구 5년 결과, 추가 녹내장 수술이 섬유주절제술군에서 유의하게 많음 (p=0.025)13)
주요 비교 연구 결과
섹션 제목: “주요 비교 연구 결과”| 연구 | 비교 | 주요 결과 |
|---|---|---|
| TVT 연구 (5년) | Baerveldt 350 vs TLE+MMC (기수술안) | 누적 실패율: 튜브 29.8% vs TLE 46.9% (p=0.02)13) |
| PTVT 연구 (3년) | Baerveldt 350 vs TLE+MMC (초회수술안) | 누적 실패율: 튜브 33% vs TLE 28% (유의한 차이 없음)14) |
| ABC/AVB 통합 (5년) | Ahmed 대 Baerveldt | Baerveldt 13.2 mmHg vs Ahmed 15.8 mmHg (p<0.001) 15) |
TVT 연구(Tube Versus Trabeculectomy Study)는 백내장 수술 또는 섬유주절제술 병력이 있는 눈을 대상으로 한 다기관 RCT입니다13). 5년 추적에서 관군의 성공률이 섬유주절제술군을 상회했습니다. 안압 감소, 약물 사용, 중증 합병증, 시력 상실은 유사했으나, 추가 녹내장 수술 횟수는 섬유주절제술군에서 유의하게 많았습니다(p=0.025)13). NEI VFQ-25를 이용한 수술 후 삶의 질 평가에서는 두 군 간 유의한 차이가 없었습니다12).
PTVT 연구(Primary TVT Study)는 초회 수술안을 대상으로 한 RCT입니다14). 3년 시점에서 성공률은 두 군 간 유사했으나, 섬유주절제술군에서 더 적은 약물 수로 더 낮은 안압이 달성되었습니다14).
ABC/AVB 연구는 Ahmed와 Baerveldt를 비교한 다기관 RCT입니다15). 5년 추적에서 Baerveldt군은 Ahmed군에 비해 안압 하강 및 약물 감소에 우수했으나, 중증 합병증은 Ahmed군에서 적었습니다15). Baerveldt 수술 후 저안압 발생률(4.5%)은 Ahmed(0.4%)에 비해 유의하게 높았습니다(p=0.002)12).
Ahmed 대 섬유주절제술 비교 연구에서 누적 성공률(41~52개월 후)은 Ahmed군 69.8%, 섬유주절제술군 68.1%로 유의한 차이가 없었습니다. 관 노출은 Ahmed군에서 많았고, 여과포 누출 및 여과포 감염은 섬유주절제술군에서 많은 경향을 보였습니다16).
항섬유화제의 역할
섹션 제목: “항섬유화제의 역할”GDD에서 마이토마이신 C(MMC)의 수술 중 사용은 여러 RCT에서 검토되었으나 성공률 향상은 입증되지 않았습니다1). 저안압 기간 연장과 합병증 증가가 보고되었으며, GDD에서 항섬유화제는 일반적으로 사용되지 않습니다.
소아 녹내장에서의 GDD
섹션 제목: “소아 녹내장에서의 GDD”소아 녹내장에서는 각도 수술(전방각절개술/섬유주절개술)이 일차 선택이나, 속발 녹내장에서는 효과가 제한적이며 GDD가 일차 치료로 사용되기도 합니다3).
Stallworth 등은 32개 연구(1,221안, 885명의 소아)를 대상으로 체계적 문헌고찰 및 메타분석을 시행했습니다3). 수술 전 평균 안압은 31.8±3.4 mmHg였습니다. 수술 후 12개월의 통합 평균 안압은 16.5 mmHg(95% CI: 15.5–17.6), 성공률은 0.87(95% CI: 0.83–0.91)이었습니다. 24개월에는 평균 안압 17.6 mmHg, 성공률 0.77(95% CI: 0.71–0.83)이었습니다. 48개월 성공률은 0.54, 60개월 0.60, 120개월 0.37로 감소했습니다. Ahmed와 Baerveldt 사이에 12개월 및 24개월 성공률의 유의한 차이는 없었습니다. 가장 흔한 합병증은 전방압박(13.6%), 저안압(11.7%), 맥락막박리(8.3%)였습니다. 연구의 90%가 Ahmed를 사용했으며, 소아에서 Baerveldt의 데이터는 제한적입니다.
소아에서는 튜브-플레이트 노출 위험이 높습니다. 눈을 자주 비비는 행동과 강한 면역 반응이 원인으로 꼽힙니다. 소아 속발성 녹내장, 특히 백내장 수술 후 녹내장에서 수술 성적이 좋지 않으며, 결국 GDD가 필요할 수 있습니다12).
어느 것이 최적인지는 환자의 상태에 따라 다릅니다. 초회 수술인 원발개방각녹내장에서는 PTVT 연구에서 섬유주절제술이 더 낮은 안압을 달성했습니다14). 반면, 이전 수술력이 있는 눈이나 속발성 녹내장에서는 TVT 연구에서 튜브 션트 수술이 유리했습니다13). 녹내장 진료 가이드라인에서는 치료 눈, 환자 배경, 술자의 숙련도를 고려하여 선택할 것을 권장합니다12).
7. 최신 연구와 향후 전망
섹션 제목: “7. 최신 연구와 향후 전망”새로운 수술 기법
섹션 제목: “새로운 수술 기법”패치 이식편이 필요 없는 자가 공막 터널을 이용한 튜브 피복법이 개발되었습니다.
Tanito 등은 1mm 폭의 초승달 칼을 사용하여 미세절개 공막 터널(MIST)을 만들고, 전방, 섬모체고랑, 유리체강의 세 부위로의 튜브 삽입에 적용했습니다4). 봉합이 필요 없어 수술 시간 단축이 가능하며, 수술 후 튜브 노출도 관찰되지 않았습니다.
Miura 등은 22게이지 바늘을 이용한 공막 터널 생성법을 보고했으며, 최장 21개월의 추적 관찰에서 튜브 노출이 관찰되지 않았습니다7).
이러한 기법들은 패치 이식편 재료의 확보 어려움과 바이러스 감염 위험을 피할 수 있는 장점이 있습니다.
합병증에 대한 새로운 접근법
섹션 제목: “합병증에 대한 새로운 접근법”Kawashima 등은 각막 혼탁으로 세극등 관찰이 어려운 AGV 실패 증례에서 안내 내시경을 통해 튜브 끝의 섬유 조직 폐쇄를 확인하고 조직 제거로 안압을 낮추었습니다6). 각막 혼탁을 동반한 증례에서 GDD 실패 진단에 내시경이 유용함이 입증되었습니다.
안압 안정화를 위한 새로운 적응증
섹션 제목: “안압 안정화를 위한 새로운 적응증”Katsev 등은 유출로 장애와 방수 생성 감소가 병발하고 점안약 치료 범위가 매우 좁은 증례에 AGV를 삽입하여 순응성 유출로를 만들어 불안정한 안압을 안정화시켰습니다9). 15개월 동안 무투약으로 안압 8–10 mmHg를 유지했습니다.
8. 병태생리학·상세한 발병 기전
섹션 제목: “8. 병태생리학·상세한 발병 기전”방수 유출의 메커니즘
섹션 제목: “방수 유출의 메커니즘”GDD에 의한 안압 하강은 다음 경로를 통해 실현됩니다.
- 튜브: 안내 방수를 플레이트로 유도하는 실리콘관
- 플레이트: 안구 적도부 근처에 고정. 튜브를 통해 유도된 방수를 저장하는 공간을 제공합니다.
- 섬유성 피막: 수술 후 4–6주에 플레이트 주위에 형성되는 결합 조직. 피막의 외면에서 주변 조직(테논낭·결막하 조직)으로 방수가 흡수됩니다.
- 플레이트 면적의 영향: 면적이 클수록 주위에 형성되는 피막도 커져 더 많은 방수를 흡수할 수 있습니다.
Baerveldt® 수술 후 경과의 기전
섹션 제목: “Baerveldt® 수술 후 경과의 기전”- 수술 직후: 튜브가 흡수 봉합사로 결찰되어 있으므로 플레이트로의 방수 유출이 없습니다. Sherwood slit에서의 미량 누출만 있습니다.
- 수술 후 약 1개월: 흡수 봉합사가 용해되어 플레이트로의 방수 유출이 시작됩니다. 이 시기부터 안압이 하강하기 시작합니다.
- 수술 후 2–3개월: 플레이트 주위의 섬유성 피막이 성숙하여 방수의 유출 저항이 안정됩니다.
- 장기: 피막 섬유화가 진행되면 유출 저항이 증가하여 안압이 상승할 수 있습니다 (테논 낭종).
Ahmed® 조압변의 기전
섹션 제목: “Ahmed® 조압변의 기전”Ahmed® 조압변은 벤추리 효과를 이용한 단방향 밸브로, 이론적으로 안압 8 mmHg 이하에서 밸브가 닫힙니다. 이는 수술 직후 과도한 여과를 방지하고 저안압 관련 합병증(맥락막 박리, 저안압 황반병증 등)의 위험을 줄입니다. 그러나 플레이트 면적이 Baerveldt®보다 작기 때문에 도달 가능한 최종 안압은 Baerveldt®에 비해 다소 떨어집니다.
9. 참고문헌
섹션 제목: “9. 참고문헌”- European Glaucoma Society. European Glaucoma Society Terminology and Guidelines for Glaucoma, 6th Edition. Br J Ophthalmol. 2025;109(Suppl 1):1-230.
- American Academy of Ophthalmology. Primary Open-Angle Glaucoma Preferred Practice Pattern. San Francisco: AAO; 2020.
- Stallworth JY, O’Brien KS, Han Y, Oatts JT. Efficacy of Ahmed and Baerveldt glaucoma drainage device implantation in the pediatric population: A systematic review and meta-analysis. Surv Ophthalmol. 2023;68(4):578-590.
- Tanito M, Ohtani H, Ida C, et al. Tube Insertion of Ahmed Glaucoma Valve Using a Micro-incision Scleral Tunnel Technique. Cureus. 2024;16(12):e75899.
- Ugarte R, Sugihara K, Sano I, et al. Two different types of giant bleb formation following Ahmed Glaucoma valve implantation. Am J Ophthalmol Case Rep. 2024;33:102008.
- Kawashima R, Baba K, Matsushita K, et al. Intraocular Endoscopy Resolved Tube Occlusion of an Ahmed Glaucoma Valve. Case Rep Ophthalmol. 2021;12:706-711.
- Miura Y, Fukuda K, Yamashiro K. A Novel Scleral Tunnel Technique for the Prevention of Ahmed Glaucoma Valve Tube Exposure. Cureus. 2025;17(2):e79290.
- Mansoori T. Management of Ahmed glaucoma valve tube exposure after scleral patch graft shrinkage. Indian J Ophthalmol. 2022;70(9):3432.
- Katsev B, Campagna G, Liu JC. Ahmed glaucoma valve implantation in a case of volatile intraocular pressure and preoperative hypotony. Am J Ophthalmol Case Rep. 2025;38:102285.
- Goel R, Gaonker T, Arya D, Golhait P. Outcome of combined single-loop fixation of intraocular lens with Ahmed glaucoma valve implantation. BMJ Case Rep. 2023;16:e254240.
- Kolipaka PG, Krishnamurthy R, Bagga B. Unusual sequelae of staphyloma following Ahmed glaucoma valve explantation and its management. BMJ Case Rep. 2021;14:e239585.
- 日本緑内障学会緑内障診療ガイドライン改訂委員会. 緑内障診療ガイドライン(第5版). 日眼会誌. 2022;126(2):85-177.
- Gedde SJ, Schiffman JC, Feuer WJ, et al; Tube versus Trabeculectomy Study Group. Treatment outcomes in the Tube Versus Trabeculectomy (TVT) study after five years of follow-up. Am J Ophthalmol. 2012;153(5):789-803.
- Gedde SJ, Feuer WJ, Lim KS, et al; Primary Tube Versus Trabeculectomy Study Group. Treatment outcomes in the primary tube versus trabeculectomy study after 3 years of follow-up. Ophthalmology. 2020;127(3):333-345.
- Christakis PG, Zhang D, Budenz DL, et al; ABC-AVB Study Groups. Five-year pooled data analysis of the Ahmed Baerveldt comparison study and the Ahmed versus Baerveldt study. Am J Ophthalmol. 2017;176:118-126.
- Wilson MR, Mendis U, Paliwal A, Haynatzka V. Long-term follow-up of primary glaucoma surgery with Ahmed glaucoma valve implant versus trabeculectomy. Am J Ophthalmol. 2003;136(3):464-470.
