非感染性
貝西氏病:眼部炎症發作時容易發生UME。
Vogt-小柳-原田病:發病初期伴有漿液性視網膜剝離。
類肉瘤病:伴有視網膜靜脈炎、脈絡膜肉芽腫。
幼年特發性關節炎:通過慢性虹膜睫狀體炎導致UME。

葡萄膜炎性黃斑水腫(uveitic macular edema; UME)是指葡萄膜炎導致黃斑部液體蓄積的狀態。葡萄膜炎在先進國家占全盲原因的15% 2)。其最常見的併發症是UME,約三分之一的葡萄膜炎患者因此出現視力障礙 2)。
約8.3%的非感染性葡萄膜炎患者發生UME 1)。囊樣黃斑水腫(CMO)見於10%–70%的葡萄膜炎患者,前葡萄膜炎為5.1%,中間葡萄膜炎為40.7% 5)。結節病、中間葡萄膜炎和貝西氏症是UME合併率特別高的類型。
囊樣黃斑水腫是指黃斑部視網膜神經元間隙中組織液蓄積,導致黃斑部出現囊樣水腫的狀態。葡萄膜炎透過血-視網膜屏障(BRB)破壞導致囊樣黃斑水腫,特徵為外叢狀層和內顆粒層的囊樣改變。囊壁由Müller細胞和軸索纖維形成。白內障手術或玻璃體手術後發生的術後囊樣黃斑水腫稱為Irvine-Gass症候群,需與葡萄膜炎性黃斑水腫區分 7)。
炎症控制後水腫仍可能持續,因此需要對炎症和水腫兩方面進行干預 2)。如果存在感染性葡萄膜炎,應優先治療病原體。葡萄膜炎診療指南將囊樣黃斑水腫列為活動性葡萄膜炎的嚴重併發症,推薦早期治療介入 7)。
炎症消退後黃斑水腫可能遷延。因此可能需要針對水腫本身的額外治療。詳見「標準治療方法」一節。
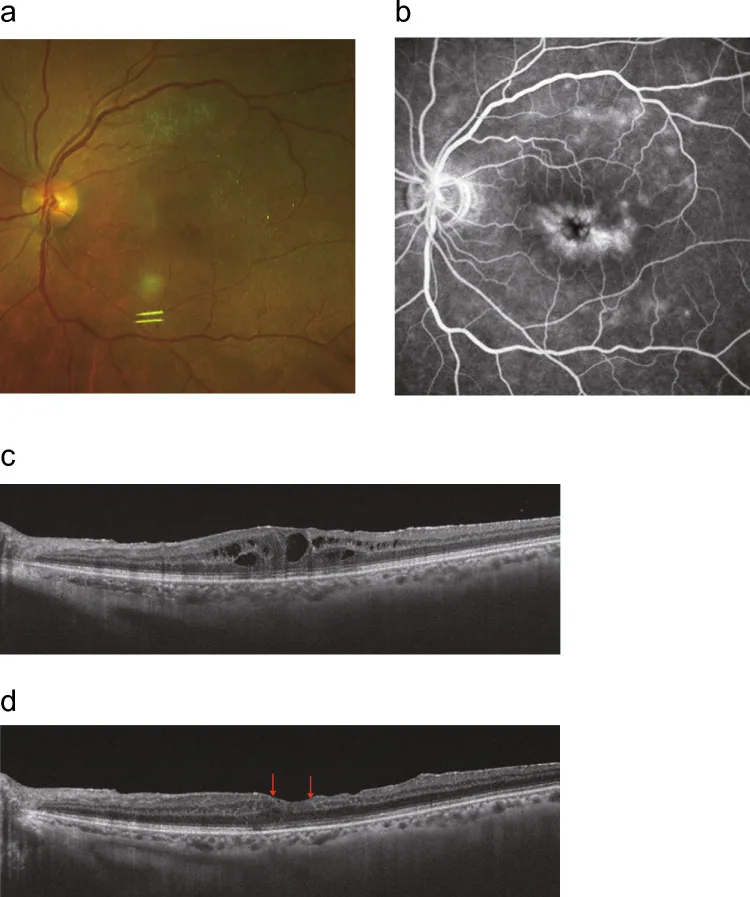
UME的主要自覺症狀是中心視力下降。
在葡萄膜炎中,前房或玻璃體細胞浸潤、角膜混濁、併發性白內障等也可導致視力下降。如果視力下降程度超過這些所見,應懷疑囊樣黃斑水腫。視力下降通常為中度至重度,黃斑部的詳細評估必不可少。
UME的臨床所見因葡萄膜炎的類型和炎症活動性而異。
UME的根本原因是眼內炎症,其病因多種多樣。
非感染性
貝西氏病:眼部炎症發作時容易發生UME。
Vogt-小柳-原田病:發病初期伴有漿液性視網膜剝離。
類肉瘤病:伴有視網膜靜脈炎、脈絡膜肉芽腫。
幼年特發性關節炎:通過慢性虹膜睫狀體炎導致UME。
感染性
UME的風險因素包括以下內容:
光學同調斷層掃描(OCT)是診斷UME最重要的檢查。結合前置鏡和裂隙燈顯微鏡進行詳細眼底檢查、OCT和螢光眼底血管攝影進行診斷。
需要鑑別的疾病包括糖尿病黃斑水腫、視網膜靜脈阻塞伴黃斑水腫、年齡相關性黃斑變性、以及由視網膜前膜引起的牽引性黃斑水腫。白內障術後黃斑水腫(Irvine-Gass症候群)也需鑑別。
在UME的追蹤中,OCT對黃斑部的評估不可或缺。主治醫師會根據發炎活動性和治療階段判斷頻率,但治療期間通常每1~3個月檢查一次。
UME的治療複雜,每位患者的最佳方法不同1)。感染性葡萄膜炎優先治療病因,非感染性UME則以類固醇為中心進行治療。葡萄膜炎診療指引推薦對持續性囊樣黃斑水腫進行Tenon囊下類固醇注射,對於類固醇抵抗的難治病例,將玻璃體手術作為選項之一7)。
這是控制後段慢性發炎的首選局部操作,適用於黃斑水腫、視網膜血管炎及玻璃體混濁等。
葡萄膜炎性黃斑水腫可能反覆發作,因此可能需要多次注射。重複給藥時建議間隔至少2個月。但每次注射前應測量眼壓,並檢查有無眼壓升高或白內障。如果眼壓升高成為問題,考慮改用其他治療方法,如玻璃體內注射。
玻璃體內給藥可獲得高藥物濃度,但存在眼內感染和眼壓升高的風險。
| 藥物 | 作用持續時間 | 特點 |
|---|---|---|
| 曲安奈德(4 mg) | 約3個月 | 廣泛使用。需要重複給藥。 |
| Ozurdex(地塞米松植入劑 0.7 mg) | 約4-6個月 | 緩釋型。已證實對UME有效。 |
| Iluvien(氟輕鬆 0.19 mg) | 約36個月 | 長效。白內障和青光眼風險高。 |
| Retisert(氟輕鬆 0.59 mg) | 約30個月 | 長效作用。青光眼手術率40% |
玻璃體內注射曲安奈德:給予4 mg可使約50%的患者視力改善1)。白內障進展與注射次數相關,注射4-5次後幾乎必然發生。眼壓升高見於20-45%的患者,但多數可透過眼藥水控制1)。
地塞米松玻璃體內植入劑(Ozurdex):這是一種緩釋0.7 mg地塞米松的聚合物植入物。HURON試驗(III期)中,Ozurdex 0.7 mg組在26週時42%的患者玻璃體混濁評分為零(安慰劑組12%,p<0.001)9)。在8週時確認了中心凹視網膜厚度顯著降低和玻璃體混濁改善9)。
Fan等人(2023)的系統性回顧和統合分析顯示,單次DEX植入後,BCVA在1個月時改善-0.15 logMAR,3個月時改善-0.22 logMAR,6個月時改善-0.24 logMAR3)。中心黃斑厚度(CMT)在1個月時減少-179.77 μm,3個月時減少-179.13 μm,6個月時減少-140.25 μm。
DEX植入後眼壓升高(IOP>21 mmHg)的發生率為13.6%,白內障形成為5.4%,均可用眼藥水控制3)。
POINT試驗直接比較了眼周曲安奈德(PTA)、玻璃體內曲安奈德(ITA)和玻璃體內DEX植入劑(IDI),中心凹視網膜厚度減少率分別為23%、39%和46%1)。玻璃體內給藥優於眼周給藥,但玻璃體內給藥組的眼壓升高風險也更高。
氟輕鬆玻璃體內植入劑:有Iluvien(0.19 mg,持續36個月)和Retisert(0.59 mg,持續30個月)。可獲得長期效果,但有晶體眼中73.8%(Iluvien)至90%以上(Retisert)需要白內障手術,青光眼手術分別需要11.9%和40%1)。
曲安奈德脈絡膜上腔注射懸浮液(Xipere; SCS-TA)是首個獲批用於治療UME的藥物,也是首個獲批用於脈絡膜上腔給藥的製劑2)。
上脈絡膜腔(SCS)是位於脈絡膜與鞏膜之間的潛在空間,藥物可選擇性分布於眼後段2)。動物實驗顯示,與玻璃體內注射相比,上脈絡膜給藥使眼後段藥物暴露量高出12倍,而眼前段暴露量降低96%2)。此特性降低了白內障和眼壓升高的風險。
在PEACHTREE試驗(第三期)中,SCS-TA 4 mg組在24週時達到BCVA改善≥15個字母的患者比例為46.9%(假手術組15.6%,p<0.001)2)。中心凹視網膜厚度平均減少152.6 μm對比17.9 μm(p<0.001),從第4週起即觀察到顯著差異。
在MAGNOLIA延伸研究中,SCS-TA組50%的患者在第二次注射後長達9個月內無需救援治療2)。48週內至救援的中位時間,SCS-TA組為257天,假手術組為55.5天。
SCS-TA的療效不受是否合併全身性類固醇使用、葡萄膜炎的解剖位置或病程長短的影響2)。非救援患者中類固醇相關眼壓升高的發生率為10.8%,低於假手術組接受救援治療患者的21.7%2)。
VEGF抑制劑在UME中為仿單外使用1)。合併脈絡膜新生血管時為第一線選擇。對於類固醇不耐受或類固醇反應者(易眼壓升高者)是強有力的選擇。然而,針對UME的明確給藥方案尚未建立1)。
玻璃體切除術適用於藥物治療抵抗或類固醇抵抗的囊樣黃斑水腫7)。聯合內界膜剝離的玻璃體切除術、聯合囊切開術的玻璃體切除術用於持續性囊樣黃斑水腫。視網膜前膜、黃斑裂孔、玻璃體出血也是手術適應症。最好在炎症穩定期進行,並考慮術前術後補充類固醇。
術後炎症可能惡化,因此需仔細評估風險效益比1)。玻璃體切除術後,曲安奈德的半衰期從18.6天縮短至3.2天,因此建議使用長效藥物1)。
首先嘗試用降壓眼藥水控制。多數情況下眼藥水可以控制。如果眼藥水和口服藥物不足,則考慮青光眼手術如小樑切開術。小樑切開術對類固醇性青光眼特別有效。
內層和外層血-視網膜屏障(BRB)的破壞在UME的發生中扮演核心角色。
正常情況下,BRB由視網膜血管內皮細胞(內側)和視網膜色素上皮細胞(外側)的緊密連接維持。在葡萄膜炎中,發炎性細胞因子(TNF-α、IL-1β、IL-6)降低緊密連接蛋白(ZO-1、occludin、claudin)的表現,導致血管通透性增加5)。VEGF也促進血管通透性增加和新生血管形成2)。液體積聚主要發生在內核層和Henle纖維層,表現為外叢狀層和內顆粒層的囊樣變化。
葡萄膜炎引起的發炎觸發以下連鎖反應:
後玻璃體膜對黃斑的牽引也可能導致UME的發生。在視網膜前膜和玻璃體黃斑牽引症候群中,玻璃體牽引可引起黃斑水腫。與葡萄膜炎相關的玻璃體混濁和玻璃體纖維化容易對黃斑產生牽引。
曲安奈德與細胞內糖皮質激素受體結合,促進脂皮質素產生,抑制促炎性花生四烯酸的釋放2)。它抑制免疫細胞浸潤和活化,降低VEGF表現,從而改善血管通透性並減輕水腫2)。如果治療有效且水腫消退,可預期視力改善;但在慢性葡萄膜炎中,水腫的復發或持續存在可能惡化視力預後。
Muya等人使用兔子的研究顯示,與玻璃體內注射曲安奈德製劑相比,SCS-TA在注射時的滑動力較低且變異性較小2)。這有助於安全地將藥物遞送到上脈絡膜腔。上脈絡膜給藥後,後段的高濃度維持了前兩個月,到第三個月時達到與玻璃體內注射相當的水平。
Mackensen等人的試驗中,干擾素β(44 mg皮下注射,每週3次)組黃斑厚度平均減少206 μm,而甲氨蝶呤(20 mg皮下注射,每週1次)組增加47 μm(p<0.0001)1)。干擾素α2a對包括貝西氏症在內的難治性UME有效率超過80%。
Taylor等人對15例患者的前瞻性研究中,玻璃體內注射甲氨蝶呤400 μg使平均黃斑厚度從425 μm降至275 μm1)。三分之一的患者在中位4個月時復發,但再次注射顯示與初次治療相似的療效。
奧曲肽(100 μg皮下注射,每日3次,或長效20 mg肌肉注射,每月1次)據報導可使9隻常規治療抵抗的慢性UME眼中的7隻眼水腫消退6)。局部眼內製劑的開發也在進行中。
玻璃體內西羅莫司(mTOR抑制劑)在SAVE-2試驗中未達到減輕UME的統計學顯著性,但在部分患者中觀察到顯著改善1)。適當的患者選擇是未來的挑戰。
法瑞西單抗(抗VEGF-A/Ang-2雙重抑制劑)同時靶向VEGF和血管生成素-2,預期在視網膜血管穩定化和通透性抑制方面具有協同效應。在糖尿病黃斑水腫和滲出性AMD獲批後,其應用於葡萄膜炎性黃斑水腫正處於研究階段。作為利用抗VEGF藥物多面作用的新治療方向而受到關注。
SCS-TA(Xipere)於2021年在美國獲批,但截至2026年3月,在日本尚未獲批。關於國內的使用可能性,需要確認未來的監管動態。