อาการบวมน้ำที่จุดรับภาพจากม่านตาอักเสบ (UME) เป็นสาเหตุหลักของความบกพร่องทางการมองเห็น ในผู้ป่วยม่านตาอักเสบ โดยเกิดขึ้นประมาณ 8-40% ของผู้ป่วย
อาการบวมน้ำที่จุดรับภาพอาจคงอยู่แม้การอักเสบจะทุเลาลง จึงจำเป็นต้องจัดการทั้งการอักเสบและอาการบวมน้ำ
การแตกของสิ่งกีดขวางเลือด-จอประสาทตา และการเกี่ยวข้องของไซโตไคน์ที่ก่อการอักเสบเป็นศูนย์กลางของพยาธิสภาพ
การรักษาทางเลือกแรกคือการให้สเตียรอยด์ โดยเส้นทางการให้มีตั้งแต่ยาหยอดตาเฉพาะที่ไปจนถึงการฉีดใต้เยื่อหุ้มเทนอนและการฉีดเข้าแก้วตา
การปลูกถ่ายเดกซาเมทาโซนเข้าแก้วตา (Ozurdex ) มีประสิทธิภาพใน UME เรื้อรังและดื้อต่อการรักษา
ไตรแอมซิโนโลน อะซีโทไนด์ เหนือคอรอยด์ (Xipere) เป็นยาตัวแรกที่ได้รับการอนุมัติเฉพาะสำหรับ UMEต้องระวังความดันลูกตา สูงและต้อกระจก ที่เกิดจากการรักษา และจำเป็นต้องมีการติดตามอย่างสม่ำเสมอ
อาการบวมน้ำที่จุดรับภาพจากม่านตาอักเสบ (uveitic macular edema; UME) คือภาวะที่มีของเหลวสะสมในจุดรับภาพร่วมกับม่านตาอักเสบ ม่านตาอักเสบ เป็นสาเหตุของตาบอดทั้งหมดมากถึง 15% ในประเทศที่พัฒนาแล้ว 2) ภาวะแทรกซ้อนที่พบบ่อยที่สุดคือ UME ซึ่งทำให้เกิดความบกพร่องทางการมองเห็น ในประมาณหนึ่งในสามของผู้ป่วยม่านตาอักเสบ 2)
ประมาณ 8.3% ของผู้ป่วยม่านตาอักเสบที่ไม่ติดเชื้อ คาดว่าจะเกิด UME 1) อาการบวมน้ำที่จุดรับภาพแบบถุงน้ำ (CMO) พบใน 10-70% ของผู้ป่วยม่านตาอักเสบ โดยรายงาน 5.1% ในม่านตาอักเสบ ส่วนหน้า และ 40.7% ในม่านตาอักเสบส่วนกลาง 5) ซาร์คอยโดซิส ม่านตาอักเสบส่วนกลาง และโรคเบห์เซ็ตเป็นชนิดโรคที่มักเกิดร่วมกับ UME มากที่สุด
อาการบวมน้ำที่จุดรับภาพแบบถุงน้ำคือภาวะที่ของเหลวในเนื้อเยื่อสะสมในช่องว่างระหว่างเซลล์ประสาทจอประสาทตา บริเวณจุดรับภาพ ทำให้เกิดอาการบวมน้ำแบบถุงน้ำที่จุดรับภาพ ในม่านตาอักเสบ อาการบวมน้ำที่จุดรับภาพแบบถุงน้ำเกิดขึ้นผ่านการแตกของสิ่งกีดขวางเลือด-จอประสาทตา (BRB) โดยมีการเปลี่ยนแปลงแบบถุงน้ำที่มีลักษณะเฉพาะในชั้นพลีซิฟอร์มนอกและชั้นนิวเคลียร์ใน ผนังของถุงน้ำเกิดจากเซลล์มุลเลอร์และเส้นใยประสาท อาการบวมน้ำที่จุดรับภาพแบบถุงน้ำหลังการผ่าตัดต้อกระจก หรือการตัดแก้วตาเรียกว่า Irvine-Gass syndrome และแตกต่างจาก UME 7)
อาการบวมน้ำอาจคงอยู่แม้ควบคุมการอักเสบได้แล้ว ดังนั้นจึงจำเป็นต้องแทรกแซงทั้งการอักเสบและอาการบวมน้ำ 2) หากมีม่านตาอักเสบติดเชื้อ ต้องให้ความสำคัญกับการรักษาเชื้อก่อโรคก่อน แนวทางการรักษาม่านตาอักเสบ ถือว่าอาการบวมน้ำที่จุดรับภาพแบบถุงน้ำเป็นภาวะแทรกซ้อนร้ายแรงของม่านตาอักเสบ ที่ยังดำเนินอยู่ และแนะนำให้แทรกแซงตั้งแต่เนิ่นๆ 7)
Q
อาการบวมน้ำที่จุดรับภาพยังคงอยู่หลังจากม่านตาอักเสบหายหรือไม่?
A
อาการบวมน้ำที่จุดรับภาพอาจคงอยู่หลังการอักเสบทุเลาลง ดังนั้นอาจจำเป็นต้องรักษาเพิ่มเติมสำหรับอาการบวมน้ำนั้นเอง ดูรายละเอียดในหัวข้อ “วิธีการรักษามาตรฐาน”
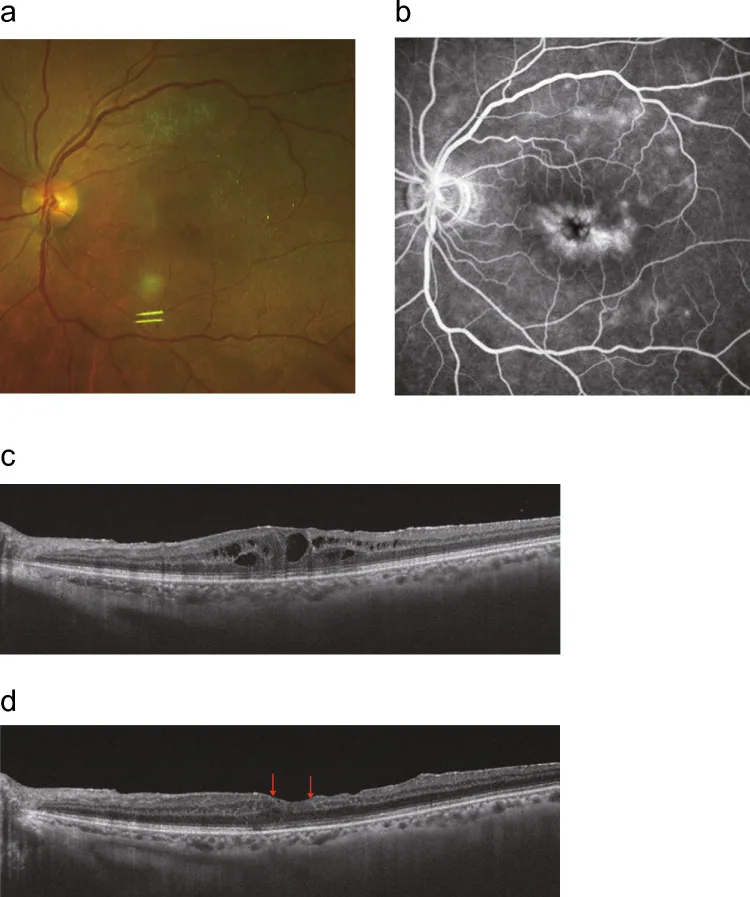
ภาพถ่ายจอตา, การถ่ายภาพหลอดเลือดด้วยฟลูออเรสซีน และ OCT ของจอตาบวมน้ำจากม่านตาอักเสบ Takeda A, et al. Recent advances in the diagnosis and treatment of refractory ocular inflammatory diseases: focus on uveitic macular edema, acute retinal necrosis, and vitreoretinal lymphoma. Jpn J Ophthalmol. 2026. Figure 1. PM
CI D: PMC12948802. License: CC BY.
ภาพหลายแผงแสดงจอตาบวมน้ำจากม่านตาอักเสบ ในภาพถ่ายจอตา, การถ่ายภาพหลอดเลือดด้วยฟลูออเรสซีน และ OCT การรั่วของฟลูออเรสซีน ที่จุดภาพชัด ใน FA และช่องว่างคล้ายถุงน้ำใน OCT แสดงผลการตรวจทางคลินิกและการวินิจฉัยหลักอย่างชัดเจน
อาการหลักที่ผู้ป่วยรับรู้ของ UME คือการมองเห็น ส่วนกลางลดลง
การมองเห็น ลดลงจุดภาพชัด ทำให้การมองเห็น ส่วนกลางบกพร่อง มักดำเนินไปอย่างช้าๆตามัว : การเปลี่ยนแปลงโครงสร้างจอตาจากจอตาบวมน้ำทำให้ภาพรวมเบลอภาพบิดเบี้ยว จุดภาพชัด ผิดรูป เส้นตรงจะมองเห็นเป็นเส้นโค้งจุดบอดกลาง
ในม่านตาอักเสบ การมองเห็น ลดลงอาจเกิดจากการแทรกซึมของเซลล์ในช่องหน้าหรือวุ้นตา , กระจกตา ขุ่น, หรือต้อกระจก แทรกซ้อน หากการมองเห็น ลดลงมากกว่าที่คาดจากผลการตรวจเหล่านี้ ให้สงสัยจอตาบวมน้ำชนิดถุงน้ำ การมองเห็น ลดลงมักอยู่ในระดับปานกลางถึงรุนแรง ดังนั้นการประเมินจุดภาพชัด อย่างละเอียดจึงจำเป็น
ผลการตรวจทางคลินิกของ UME แตกต่างกันไปตามชนิดของม่านตาอักเสบ ที่เป็นสาเหตุและกิจกรรมการอักเสบ
จอตาบวมน้ำชนิดถุงน้ำ : การถ่ายภาพหลอดเลือดด้วยฟลูออเรสซีน (FA ) แสดงการรั่วของฟลูออเรสซีน เป็นรูปกลีบดอกไม้ การตรวจด้วยแสงร่วมประสาน (OCT ) แสดงช่องว่างคล้ายถุงน้ำในจอตาและจอตาหนาตัว ในม่านตาอักเสบ มักพบแบบถุงน้ำจอตาบวมน้ำแบบกระจาย : OCT แสดงการหนาตัวกระจายทั่วทุกชั้นจอตาจอตาลอกชนิดมีน้ำใต้จอตา : พบลักษณะเฉพาะในระยะเริ่มต้นของโรคโวกท์-โคยานางิ-ฮาราดา และอาจแสดงการลอกแบบตุ่มพองในส่วนล่างหลอดเลือดจอประสาทตาอักเสบ ฟลูออเรสซีน ใน FA มีประโยชน์ในการยืนยันอาการอักเสบในช่องหน้าตา : มีเซลล์ในช่องหน้า, flare, และความขุ่นในวุ้นตา
สาเหตุพื้นฐานของ UME คือการอักเสบภายในลูกตา และสาเหตุมีความหลากหลาย
ไม่ติดเชื้อ
โรคเบห์เซ็ต : UME เกิดขึ้นได้ง่ายร่วมกับอาการตาอักเสบ
โรคโวกท์-โคยานางิ-ฮาราดะ : ร่วมกับจอประสาทตา หลุดลอกชนิดเซรุ่มในระยะเริ่มแรก
ซาร์คอยโดซิส จอประสาทตา อักเสบและแกรนูโลมาคอรอยด์
ข้ออักเสบไม่ทราบสาเหตุในเด็ก : นำไปสู่ UME ผ่านการอักเสบของม่านตา และซิลิอารีบอดี เรื้อรัง
ติดเชื้อ
ไวรัสเฮอร์ปีส์ : UME ร่วมกับจอประสาทตาตายเฉียบพลัน
วัณโรค : ทำให้เกิดอาการบวมน้ำผ่านตุ่มวัณโรคคอรอยด์ หรือหลอดเลือดอักเสบ
ทอกโซพลาสมา : การแพร่กระจายของจอประสาทตา อักเสบและคอรอยด์ อักเสบไปยังจุดรับภาพ
ซิฟิลิส : ร่วมกับยูเวียอักเสบส่วนหลังและทำให้เกิด UME
ปัจจัยเสี่ยงของ UME ได้แก่:
ม่านตาอักเสบส่วนกลาง ส่วนหลัง และทั้งหมดม่านตาอักเสบ ส่วนหน้า5) การอักเสบเรื้อรังหรือต่อเนื่อง : การอักเสบเป็นเวลานานเพิ่มความเสี่ยงในการเกิด UMEการใช้สเตียรอยด์ เป็นเวลานาน : ยังเพิ่มความเสี่ยงของภาวะแทรกซ้อน เช่น ต้อกระจก จากสเตียรอยด์ และต้อหินจากสเตียรอยด์ การดึงรั้งของวุ้นตา : การดึงรั้งของเยื่อวุ้นตา ส่วนหลังบนจอประสาทตา ก็เป็นสาเหตุหนึ่งของ UME
การตรวจที่สำคัญที่สุดในการวินิจฉัย UME คือ Optical Coherence Tomography (OCT ) การวินิจฉัยทำได้โดยการตรวจอวัยวะภายในตาอย่างละเอียดด้วยเลนส์นูนและกล้องจุลทรรศน์ชนิดกรีดแสง ร่วมกับ OCT และการถ่ายภาพหลอดเลือดด้วยฟลูออเรสซีน
OCT จอประสาทตา โดยไม่ต้องผ่าตัด สามารถตรวจพบความหนาของจอประสาทตา การเกิดถุงน้ำ และจอประสาทตาลอก แบบมีน้ำใต้จอประสาทตา มักวินิจฉัย UME เมื่อความหนาจอประสาทตา บริเวณรอยบุ๋ม (CST) ≥300 ไมโครเมตร2) นอกจากนี้ยังจำเป็นสำหรับการประเมินประสิทธิภาพของการรักษา ใช้ติดตามการเปลี่ยนแปลงความหนาเมื่อเวลาผ่านไปการถ่ายภาพหลอดเลือดด้วยฟลูออเรสซีน (FA ) : มีประโยชน์ในการตรวจหาการซึมผ่านของหลอดเลือดจอประสาทตา ที่เพิ่มขึ้นและเส้นเลือดใหม่ ในจอประสาทตา บวมชนิดถุงน้ำ จะแสดงรูปแบบการรั่วของฟลูออเรสซีน เป็นกลีบดอกไม้รอบรอยบุ๋มในระยะท้ายการถ่ายภาพหลอดเลือดด้วยอินโดไซยานีนกรีน (ICG) : ใช้เพื่อประเมินการไหลเวียนของคอรอยด์ มีประโยชน์ในการประเมินรอยโรคคอรอยด์ ในโรคซาร์คอยโดซิส และโรคโวกท์-โคยานางิ-ฮาราดะOCTA (OCT Angiography )จอประสาทตา และเส้นเลือดใหม่คอรอยด์ โดยไม่ต้องใช้สารทึบรังสี มีประโยชน์ในการแสดงภาพเส้นเลือดใหม่ที่เกิดร่วมการตรวจด้วยกล้องจุลทรรศน์ชนิดกรีดแสง ความขุ่นของวุ้นตา การตรวจอวัยวะภายในลูกตา : ตรวจสอบว่ามีอาการบวมน้ำที่จอตา, หลอดเลือดจอตาอักเสบ, และความขุ่นของวุ้นตา
โรคที่ต้องแยกออก ได้แก่ จอตาบวมน้ำจากเบาหวาน, จอตาบวมน้ำจากหลอดเลือดดำจอตาอุดตัน, จอตาเสื่อมตามอายุ, และจอตาบวมน้ำจากการดึงรั้งของเยื่อเหนือจอตา จอตาบวมน้ำหลังผ่าตัดต้อกระจก (Irvine-Gass syndrome ) ก็อยู่ในกลุ่มที่ต้องแยก
Q
ในการตรวจตามปกติ ควรตรวจ OCT บ่อยแค่ไหน?
A
ระหว่างการติดตาม UME การประเมินจอตาด้วย OCT เป็นสิ่งจำเป็น แพทย์ผู้รักษาจะกำหนดความถี่ตามกิจกรรมการอักเสบและระยะการรักษา แต่โดยทั่วไประหว่างการรักษาจะตรวจทุก 1-3 เดือน
การรักษา UME มีความซับซ้อน และวิธีการที่เหมาะสมที่สุดแตกต่างกันไปในผู้ป่วยแต่ละราย1) ในม่านตาอักเสบติดเชื้อ ให้ความสำคัญกับการรักษาสาเหตุ ส่วนม่านตาอักเสบ ไม่ติดเชื้อ การรักษาหลักคือสเตียรอยด์ แนวทางการรักษาม่านตาอักเสบ แนะนำให้ฉีดสเตียรอยด์ ใต้เยื่อหุ้มเทนอนสำหรับจอตาบวมน้ำแบบถุงน้ำที่เรื้อรัง และการผ่าตัดวุ้นตา เป็นทางเลือกสำหรับกรณีที่ดื้อต่อสเตียรอยด์ 7)
ยาหยอดตาสเตียรอยด์ : ใช้สำหรับ UME เล็กน้อยร่วมกับม่านตาอักเสบ ส่วนหน้า หยอด betamethasone หรือ dexamethasone 3-6 ครั้งต่อวัน ปรับตามระดับการอักเสบ ผลต่อรอยโรคส่วนหลังมีจำกัด1) ยาหยอดตาขยายม่านตา : ใช้ tropicamide และ phenylephrine ร่วมกันเพื่อป้องกันการยึดติดของม่านตา ด้านหลังยาหยอดตา NSAID : มีประโยชน์สำหรับจอตาบวมน้ำในตาที่ใส่เลนส์แก้วตาเทียม แต่ประสิทธิภาพใน UME ยังไม่ได้รับการพิสูจน์อย่างชัดเจน1)
นี่เป็นหัตถการเฉพาะที่แรกในการควบคุมการอักเสบเรื้อรังของส่วนหลัง และมีข้อบ่งชี้ที่ดีสำหรับจอตาบวมน้ำ, หลอดเลือดจอตาอักเสบ, และความขุ่นของวุ้นตา
การฉีด triamcinolone acetonide ใต้เยื่อหุ้มเทนอนส่วนหลัง : มีประสิทธิภาพในม่านตาอักเสบ เรื้อรังที่เกี่ยวข้องกับส่วนหลัง เช่น จอตาบวมน้ำแบบถุงน้ำ ใช้เมื่อการเปลี่ยนแปลงการอักเสบที่ขั้วหลังของอวัยวะภายในลูกตารุนแรง7) ขั้นตอน: เจาะเยื่อบุตา บริเวณ fornix ใน quadrant ด้านล่างขมับ ฉีด triamcinolone acetonide 20 มก./0.5 มล. เข้าไปในช่องใต้เยื่อหุ้มเทนอนส่วนหลังด้วยเข็มทื่อหรือแหลมเบอร์ 24-25G แนะนำให้ฉีดจากด้านล่างขมับเพื่อหลีกเลี่ยงความเสี่ยงหนังตาตก ยาจะคงอยู่ใต้เยื่อหุ้มเทนอนประมาณ 3 เดือน จุดสูงสุดของฤทธิ์ประมาณ 1 เดือน
สำหรับจอตาบวมน้ำแบบถุงน้ำร่วมกับ sarcoidosis และโรค Behçet ให้ฉีด Kenacort-A 40 มก./มล. (triamcinolone acetonide) 0.5 มล. ใต้เยื่อหุ้มเทนอนส่วนหลัง (นอกข้อบ่งใช้)
ต้องระวังความดันลูกตา สูง (เกิดในผู้ป่วย 15-20%) และการฉีดไปทางด้านหลังอาจลดความเสี่ยงของความดันลูกตา สูง1)
Q
การฉีดใต้เยื่อหุ้มเทนอนซ้ำๆ ปลอดภัยหรือไม่?
A
จอประสาทตา บวมจากม่านตาอักเสบ อาจกลับมาเป็นซ้ำได้ จึงอาจต้องฉีดหลายครั้ง สำหรับการให้ซ้ำ แนะนำให้เว้นระยะอย่างน้อย 2 เดือน อย่างไรก็ตาม ต้องวัดความดันลูกตา ทุกครั้งและตรวจสอบว่ามีความดันลูกตา สูงหรือต้อกระจก ก่อนทำ หากความดันลูกตา สูงเป็นปัญหา ให้พิจารณาเปลี่ยนไปใช้การรักษาอื่น เช่น การฉีดเข้าแก้วตา
การฉีดเข้าแก้วตาให้ความเข้มข้นของยาได้สูง แต่มีความเสี่ยงต่อการติดเชื้อในลูกตา และความดันลูกตา สูง
ยา ระยะเวลาออกฤทธิ์ ลักษณะเฉพาะ Triamcinolone (4 มก.) ประมาณ 3 เดือน ใช้กันอย่างแพร่หลาย ต้องฉีดซ้ำ Ozurdex (DEX implant 0.7 มก.)ประมาณ 4-6 เดือน ปลดปล่อยช้า ยืนยันประสิทธิภาพในจอประสาทตา บวมจากม่านตาอักเสบ Iluvien (fluocinolone 0.19 มก.)ประมาณ 36 เดือน ออกฤทธิ์นาน เสี่ยงต้อกระจก และต้อหิน สูง Retisert (ฟลูโอซิโนโลน 0.59 มก.) ประมาณ 30 เดือน ออกฤทธิ์นาน อัตราการผ่าตัดต้อหิน 40%
การฉีดไตรแอมซิโนโลน อะซีโทไนด์เข้าแก้วตา : ขนาด 4 มก. ช่วยให้การมองเห็น ดีขึ้นในผู้ป่วยประมาณ 50% 1) การดำเนินของต้อกระจก สัมพันธ์กับจำนวนครั้งที่ฉีด โดยจะเกิดขึ้นเกือบแน่นอนหลังฉีด 4-5 ครั้ง ความดันลูกตา สูงขึ้นพบได้ 20-45% แต่ส่วนใหญ่สามารถควบคุมได้ด้วยยาหยอดตา 1)
การปลูกถ่ายเดกซาเมทาโซนเข้าแก้วตา (Ozurdex ) : เป็นการปลูกถ่ายโพลิเมอร์ที่ปล่อยเดกซาเมทาโซน 0.7 มก. แบบช้าๆ ในการทดลอง HURON (ระยะที่ 3) กลุ่ม Ozurdex 0.7 มก. 42% มีคะแนนความขุ่นของวุ้นตา เป็นศูนย์ที่สัปดาห์ที่ 26 (กลุ่มยาหลอก 12%, p<0.001) 9) ที่สัปดาห์ที่ 8 พบว่าความหนาของจอประสาทตา ส่วนโฟเวียลดลงอย่างมีนัยสำคัญและความขุ่นของวุ้นตา ดีขึ้น 9)
ในการทบทวนวรรณกรรมอย่างเป็นระบบและการวิเคราะห์อภิมานของ Fan และคณะ (2023) หลังการปลูกถ่าย DEX ครั้งเดียว ค่า BCVA ดีขึ้น -0.15 logMAR ที่ 1 เดือน, -0.22 logMAR ที่ 3 เดือน และ -0.24 logMAR ที่ 6 เดือน 3) ความหนาจุดรับภาพส่วนกลาง (CMT) ลดลง -179.77 μm ที่ 1 เดือน, -179.13 μm ที่ 3 เดือน และ -140.25 μm ที่ 6 เดือน
อุบัติการณ์ของความดันลูกตา สูง (IOP >21 mmHg) หลังปลูกถ่าย DEX คือ 13.6% และการเกิดต้อกระจก 5.4% ซึ่งทั้งสองอย่างสามารถควบคุมได้ด้วยยาหยอดตา 3)
ในการทดลอง POINT ได้เปรียบเทียบโดยตรงระหว่างไตรแอมซิโนโลน รอบลูกตา (PTA), ไตรแอมซิโนโลน ในแก้วตา (ITA) และการปลูกถ่าย DEX ในแก้วตา (IDI) โดยอัตราการลดความหนาจอประสาทตา ส่วนโฟเวียคือ 23%, 39% และ 46% ตามลำดับ 1) การให้ยาในแก้วตาดีกว่าการให้รอบลูกตา แต่ความเสี่ยงต่อความดันลูกตา สูงก็สูงกว่าในกลุ่มที่ให้ยาในแก้วตาเช่นกัน
การปลูกถ่ายฟลูโอซิโนโลน อะซีโทไนด์ เข้าแก้วตา : รวมถึง Iluvien (0.19 มก., อยู่นาน 36 เดือน) และ Retisert (0.59 มก., อยู่นาน 30 เดือน) ให้ผลระยะยาว แต่จำเป็นต้องผ่าตัดต้อกระจก ใน 73.8% (Iluvien ) ถึงมากกว่า 90% (Retisert) ของตาที่ยังมีเลนส์ และจำเป็นต้องผ่าตัดต้อหิน ใน 11.9% และ 40% ตามลำดับ 1)
สารแขวนลอยฉีดไตรแอมซิโนโลน อะซีโทไนด์เหนือคอรอยด์ (Xipere; SCS-TA) เป็นยาตัวแรกที่ได้รับการอนุมัติสำหรับรักษาภาวะจอประสาทตา บวมน้ำจากยูเวียอักเสบ (UME) และยังเป็นสูตรยาตัวแรกที่ได้รับการอนุมัติสำหรับการให้ยาเหนือคอรอยด์ 2)
ช่องเหนือคอรอยด์ (SCS) เป็นช่องว่างที่อาจเกิดขึ้นได้ระหว่างคอรอยด์ และตาขาว ซึ่งยาจะกระจายตัวแบบเลือกสรรไปยังส่วนหลังของดวงตา 2) ในการศึกษาในสัตว์ การให้ยาทางเหนือคอรอยด์ ส่งผลให้การได้รับยาที่ส่วนหลังสูงกว่าการฉีดเข้าน้ำวุ้นตา 12 เท่า ในขณะที่การได้รับยาที่ส่วนหน้าลดลง 96% 2) คุณสมบัตินี้ช่วยลดความเสี่ยงของต้อกระจก และความดันลูกตา สูง
ในการทดลอง PEA CHTREE (ระยะที่ 3) ผู้ป่วยในกลุ่ม SCS-TA 4 มก. ร้อยละ 46.9 มีการมองเห็น ดีขึ้น ≥15 ตัวอักษรที่สัปดาห์ที่ 24 (กลุ่มหลอก ร้อยละ 15.6, p<0.001) 2) ความหนาจอประสาทตา ส่วนโฟเวียลดลงเฉลี่ย 152.6 ไมครอน เทียบกับ 17.9 ไมครอน (p<0.001) โดยพบความแตกต่างที่มีนัยสำคัญตั้งแต่สัปดาห์ที่ 4
ในการทดลองต่อเนื่อง MAGNOLIA ผู้ป่วยในกลุ่ม SCS-TA ร้อยละ 50 ไม่จำเป็นต้องได้รับการรักษาช่วยเหลือนานถึง 9 เดือนหลังจากให้ยาครั้งที่สอง 2) ค่ามัธยฐานของเวลาจนถึงการรักษาช่วยเหลือตลอด 48 สัปดาห์คือ 257 วันในกลุ่ม SCS-TA เทียบกับ 55.5 วันในกลุ่มหลอก
SCS-TA แสดงประสิทธิภาพโดยไม่ขึ้นกับการใช้สเตียรอยด์ ทั่วร่างกาย ตำแหน่งทางกายวิภาคของม่านตาอักเสบ หรือระยะเวลาของโรค 2) อุบัติการณ์ของความดันลูกตา สูงที่เกี่ยวข้องกับสเตียรอยด์ ในผู้ป่วยที่ไม่ได้รับการรักษาช่วยเหลือคือร้อยละ 10.8 ซึ่งต่ำกว่าร้อยละ 21.7 ในผู้ป่วยกลุ่มหลอกที่ได้รับการรักษาช่วยเหลือ 2)
สเตียรอยด์ ทั่วร่างกาย1) ในโรคโวกท์-โคยานางิ-ฮาราดะ ให้ทำการรักษาแบบสเตียรอยด์ พัลส์ เนื่องจากมีผลข้างเคียงมาก การลดขนาดยาต้องทำอย่างช้าๆ เป็นเวลา 6 เดือนหรือมากกว่ายากดภูมิคุ้มกัน : ไซโคลสปอริน (นีออรัล 3–5 มก./กก./วัน) ใช้เมื่อการลดสเตียรอยด์ ทำได้ยาก จำเป็นต้องติดตามระดับยาในเลือด (ระดับ trough 50–200 นาโนกรัม/มล.) และจัดการการทำงานของไต ในโรคเบห์เซ็ต โคลชิซิน (0.5–1.5 มก./วัน) เป็นทางเลือกแรกในการระงับการอักเสบแอนติบอดีต่อต้าน TNF -α (อินฟลิซิแมบ ) : ใช้ในโรคเบห์เซ็ตชนิดรุนแรงที่ยังคงกำเริบแม้ใช้โคลชิซินและไซโคลสปอริน ขนาดปกติคือ 5 มก./กก. ให้โดยการหยดทางหลอดเลือดดำทุก 2 เดือนม่านตาอักเสบที่เกี่ยวข้องกับข้ออักเสบไม่ทราบสาเหตุในเด็ก (JIA)จอประสาทตา บวมจากม่านตาอักเสบ (UME) ที่เกิดร่วมกับม่านตาอักเสบ เรื้อรัง แนะนำให้รักษาแบบเป็นขั้นตอนรวมถึง methotrexate และยาชีวภาพ (adalimumab) 4) รายงาน IOIS แนะนำ methotrexate, azathioprine และ mycophenolate mofetil เป็นทางเลือกแรกในการเริ่มยากดภูมิคุ้มกันสำหรับม่านตาอักเสบ ที่มี UME 8) Adalimumab มีรายงานอัตราการควบคุมจอประสาทตา บวมแบบถุงน้ำ (CME ) ถึง 97.7% ใน CME ที่เกี่ยวข้องกับม่านตาอักเสบ จาก JIA ที่ไม่ตอบสนองต่อ methotrexate 8)
ยาที่ยับยั้ง VEGF ใช้นอกเหนือข้อบ่งชี้สำหรับ UME 1) ยานี้เป็นทางเลือกแรกหากมีเส้นเลือดใหม่ในคอรอยด์ เป็นทางเลือกสำคัญในผู้ป่วยที่ไม่ทนต่อสเตียรอยด์ หรือตอบสนองต่อสเตียรอยด์ (มีแนวโน้มความดันลูกตา สูง) อย่างไรก็ตาม ยังไม่มีการกำหนดสูตรยาที่ชัดเจนสำหรับ UME 1)
การตัดแก้วตา (vitrectomy) มีข้อบ่งชี้ในจอประสาทตา บวมแบบถุงน้ำที่ดื้อต่อยาหรือสเตียรอยด์ 7) การตัดแก้วตาร่วมกับการลอกเยื่อหุ้มขอบใน หรือการตัดแก้วตาร่วมกับการเปิดถุงน้ำ ทำในจอประสาทตา บวมแบบถุงน้ำที่เรื้อรัง เยื่อเหนือจอตา, รูที่จอตา และเลือดออกในแก้วตา ก็เป็นข้อบ่งชี้ในการผ่าตัด ควรผ่าตัดเมื่อการอักเสบสงบ และพิจารณาเสริมสเตียรอยด์ ก่อนและหลังผ่าตัด
การอักเสบอาจแย่ลงหลังผ่าตัด ดังนั้นต้องประเมินความเสี่ยงและประโยชน์อย่างรอบคอบ 1) หลังตัดแก้วตา ครึ่งชีวิตของ triamcinolone ลดลงจาก 18.6 วันเหลือ 3.2 วัน ดังนั้นแนะนำให้ใช้ยาที่ออกฤทธิ์นาน 1)
Q
จะทำอย่างไรถ้าความดันลูกตาสูงจากการรักษาด้วยสเตียรอยด์?
A
ขั้นแรก พยายามควบคุมด้วยยาหยอดตาลดความดัน ในหลายกรณีสามารถควบคุมได้ด้วยยาหยอด หากยาหยอดและยากินไม่เพียงพอ ให้พิจารณาผ่าตัดต้อหิน เช่น trabeculectomy Trabeculectomy มีประสิทธิภาพโดยเฉพาะสำหรับต้อหินจากสเตียรอยด์
การสลายของสิ่งกีดขวางเลือด-จอตาทั้งภายในและภายนอกมีบทบาทสำคัญในการเกิด UME
โดยปกติ สิ่งกีดขวางเลือด-จอตา (BRB) จะถูกคงไว้โดยรอยต่อแน่นของเซลล์บุผนังหลอดเลือดจอตา (ด้านใน) และเซลล์เยื่อบุผิวรงควัตถุจอตา (ด้านนอก) ในม่านตาอักเสบ (uveitis) ไซโตไคน์ที่ก่อการอักเสบ (TNF -α, IL-1β, IL-6) จะลดการแสดงออกของโปรตีนรอยต่อแน่น (ZO-1, occludin, claudin) ทำให้การซึมผ่านของหลอดเลือดเพิ่มขึ้น 5) VEGF ยังเพิ่มการซึมผ่านของหลอดเลือดและส่งเสริมการสร้างเส้นเลือดใหม่ 2) การสะสมของของเหลวเกิดขึ้นส่วนใหญ่ในชั้นนิวเคลียสชั้นในและชั้นเส้นใยเฮนเล และสังเกตได้จากการเปลี่ยนแปลงแบบถุงน้ำในชั้นเพล็กซิฟอร์มชั้นนอกและชั้นแกรนูลชั้นใน
ในการอักเสบจากม่านตาอักเสบ เกิดลำดับเหตุการณ์ดังนี้:
การแทรกซึมของเซลล์ภูมิคุ้มกัน : เซลล์ทีและมาโครฟาจเคลื่อนที่เข้าสู่ลูกตาและปล่อยสารสื่อกลางการอักเสบการผลิตพรอสตาแกลนดิน : การผลิตเพิ่มขึ้นโดยการกระตุ้นไซโคลออกซีจีเนส ทำให้การซึมผ่านของหลอดเลือดเพิ่มขึ้น 1) การเพิ่มขึ้นของ VEGF : ทำให้เกิดการซึมผ่านของหลอดเลือดเพิ่มขึ้นและการเกิดอาการบวมน้ำโดยตรงการกระตุ้นคอมพลีเมนต์ : ส่งเสริมความเสียหายของหลอดเลือดส่วนปลายและการบาดเจ็บโดยตรงต่อเซลล์บุผนังหลอดเลือดจอตา
การดึงรั้งของเยื่อวุ้นตา ส่วนหลังต่อจุดภาพชัด (macula) อาจมีส่วนทำให้เกิดอาการบวมน้ำที่จุดภาพชัด (UME) ได้เช่นกัน ในเยื่อเหนือจอตา (epiretinal membrane) และกลุ่มอาการดึงรั้งวุ้นตา -จอตา (vitreomacular traction syndrome) การดึงรั้งของวุ้นตา อาจทำให้เกิดอาการบวมน้ำที่จุดภาพชัด ความขุ่นและการเกิดพังผืดของวุ้นตา ที่เกี่ยวข้องกับม่านตาอักเสบ มีแนวโน้มที่จะทำให้เกิดการดึงรั้งที่จุดภาพชัด
Triamcinolone acetonide จับกับตัวรับกลูโคคอร์ติคอยด์ภายในเซลล์ ส่งเสริมการผลิต lipocortin และยับยั้งการปล่อยกรดอะราคิโดนิกที่ต้านการอักเสบ 2) ยับยั้งการแทรกซึมและการกระตุ้นเซลล์ภูมิคุ้มกัน ลดการแสดงออกของ VEGF ทำให้การซึมผ่านของหลอดเลือดดีขึ้นและลดอาการบวมน้ำ 2) หากการรักษาได้ผลและอาการบวมน้ำทุเลา สามารถคาดหวังการมองเห็น ที่ดีขึ้น แต่ในม่านตาอักเสบ เรื้อรัง การกลับเป็นซ้ำหรือการคงอยู่ของอาการบวมน้ำอาจทำให้การพยากรณ์โรคทางสายตาแย่ลง
เนื้อหาต่อไปนี้อยู่ในขั้นตอนการวิจัยหรือการทดลองทางคลินิกในปัจจุบัน และไม่ใช่การรักษามาตรฐานที่สามารถรับได้ในโรงพยาบาลทั่วไป เป็นข้อมูลอ้างอิงสำหรับผู้เชี่ยวชาญเกี่ยวกับความก้าวหน้าทางการแพทย์ในอนาคต
ในการศึกษาของ Muya และคณะในกระต่าย SCS-TA แสดงแรงเลื่อนที่ต่ำกว่าและความแปรปรวนน้อยกว่าระหว่างการฉีดเมื่อเทียบกับสูตร triamcinolone สำหรับฉีดเข้าแก้วตา 2) ซึ่งช่วยให้การนำส่งยาไปยังช่องเหนือคอรอยด์ ปลอดภัยยิ่งขึ้น หลังการให้ยาเหนือคอรอยด์ ความเข้มข้นสูงในส่วนหลังของลูกตาจะคงอยู่นาน 2 เดือนแรก และในเดือนที่ 3 จะเทียบเท่ากับระดับการฉีดเข้าแก้วตา
ในการทดลองของ Mackensen และคณะ กลุ่มที่ได้รับอินเตอร์เฟอรอนเบตา (44 มก. ฉีดใต้ผิวหนัง 3 ครั้ง/สัปดาห์) มีความหนาจุดรับภาพลดลงเฉลี่ย 206 ไมโครเมตร ในขณะที่กลุ่ม methotrexate (20 มก. ฉีดใต้ผิวหนัง 1 ครั้ง/สัปดาห์) เพิ่มขึ้น 47 ไมโครเมตร (p<0.0001) 1) อินเตอร์เฟอรอนอัลฟา 2a มีรายงานอัตราประสิทธิภาพมากกว่า 80% สำหรับอาการบวมน้ำที่จุดรับภาพจากยูเวียอักเสบที่ดื้อต่อการรักษา รวมถึงโรคเบห์เซ็ต
ในการศึกษาไปข้างหน้าของ Taylor และคณะในผู้ป่วย 15 ราย การฉีด methotrexate 400 ไมโครกรัมเข้าแก้วตาทำให้ความหนาจุดรับภาพลดลงจากเฉลี่ย 425 ไมโครเมตรเหลือ 275 ไมโครเมตร 1) หนึ่งในสามของผู้ป่วยกลับเป็นซ้ำที่ค่ามัธยฐาน 4 เดือน แต่การฉีดซ้ำมีประสิทธิภาพเท่ากับการฉีดครั้งแรก
Octreotide (100 ไมโครกรัม ฉีดใต้ผิวหนัง 3 ครั้ง/วัน หรือ 20 มก. ชนิดออกฤทธิ์นาน ฉีดเข้ากล้าม 1 ครั้ง/เดือน) มีรายงานว่าทำให้อาการบวมน้ำลดลงใน 7 ใน 9 ตาที่มีอาการบวมน้ำที่จุดรับภาพจากยูเวียอักเสบเรื้อรังที่ดื้อต่อการรักษาแบบดั้งเดิม 6) การพัฒนาสูตรยาสำหรับฉีดเข้าตาเฉพาะที่ก็กำลังดำเนินการอยู่เช่นกัน
Sirolimus เข้าแก้วตา (ยายับยั้ง mTOR) ไม่บรรลุนัยสำคัญทางสถิติในการลดอาการบวมน้ำที่จุดรับภาพจากยูเวียอักเสบในการทดลอง SAVE-2 แต่ผู้ป่วยบางรายมีการปรับปรุงอย่างชัดเจน 1) การเลือกผู้ป่วยที่เหมาะสมเป็นความท้าทายในอนาคต
Faricimab (ยายับยั้งคู่ anti-VEGF-A/Ang-2) มุ่งเป้าไปที่ทั้ง VEGF และ angiopoietin-2 ให้ผลเสริมฤทธิ์ที่คาดหวังในการทำให้หลอดเลือดจอประสาทตา คงตัวและยับยั้งการซึมผ่าน หลังจากได้รับการอนุมัติสำหรับอาการบวมน้ำที่จุดรับภาพจากเบาหวานและจอประสาทตา เสื่อมชนิดเปียก การประยุกต์ใช้ในอาการบวมน้ำที่จุดรับภาพจากยูเวียอักเสบอยู่ในขั้นตอนการวิจัย ถือเป็นการพัฒนาการรักษาแบบใหม่ที่ใช้ประโยชน์จากฤทธิ์หลายด้านของยาต้าน VEGF
Q
การฉีดยาเหนือคอรอยด์สามารถทำได้ในญี่ปุ่นหรือไม่?
A
SCS-TA (Xipere) ได้รับการอนุมัติในสหรัฐอเมริกาในปี 2021 แต่ ณ เดือนมีนาคม 2026 ยังไม่ได้รับการอนุมัติในญี่ปุ่น ความเป็นไปได้ในการใช้ในประเทศจำเป็นต้องติดตามแนวโน้มด้านกฎระเบียบในอนาคต
Teper SJ. Update on the management of uveitic macular edema. J Clin Med. 2021;10(18):4133.
Fung S, Syed YY. Suprachoroidal space triamcinolone acetonide: a review in uveitic macular edema. Drugs. 2022;82(13):1403-1410.
Fan S, Shi XY, Zhao CF , et al. Efficacy and safety of single-dose intravitreal dexamethasone implant in non-infectious uveitic macular edema: a systematic review and meta-analysis. Front Med. 2023;10:1126724.
Angeles-Han ST, Lo MS , Henderson LA, et al. Childhood arthritis and rheumatology research alliance consensus treatment plans for juvenile idiopathic arthritis-associated and idiopathic chronic anterior uveitis. Arthritis Care Res. 2019;71(4):482-491.
Haydinger CD, Ferreira LB, Williams KA, Smith JR. Mechanisms of macular edema. Front Med. 2023;10:1128983.
Kafkala C, Choi JY, Engelbrecht NE, et al. Octreotide treatment for chronic uveitic cystoid macular edema. Graefes Arch Clin Exp Ophthalmol. 2006;244(5):563-569.
日本眼科学会ぶどう膜炎診療ガイドライン作成委員会. ぶどう膜炎診療ガイドライン. 日眼会誌. 2019;123(6):635-696.
Branford JA, Pavesio C, Goldstein DA, et al. IOIS report on immunomodulatory treatment of non-infectious uveitis. Br J Ophthalmol. 2025;109(4):482-489.
Lowder C, Belfort R Jr, Lightman S, et al. Dexamethasone intravitreal implant for noninfectious intermediate or posterior uveitis (HURON). Arch Ophthalmol. 2011;129(5):545-553.