非感染性

葡萄膜炎性黄斑水肿
一目了然的要点
Section titled “一目了然的要点”1. 什么是葡萄膜炎性黄斑水肿?
Section titled “1. 什么是葡萄膜炎性黄斑水肿?”葡萄膜炎性黄斑水肿(uveitic macular edema; UME)是指葡萄膜炎导致黄斑部液体蓄积的状态。葡萄膜炎在发达国家占全盲原因的15% 2)。其最常见的并发症是UME,约三分之一的葡萄膜炎患者因此出现视力障碍 2)。
约8.3%的非感染性葡萄膜炎患者发生UME 1)。囊样黄斑水肿(CMO)见于10%–70%的葡萄膜炎患者,前葡萄膜炎为5.1%,中间葡萄膜炎为40.7% 5)。结节病、中间葡萄膜炎和白塞病是UME合并率特别高的类型。
囊样黄斑水肿是指黄斑部视网膜神经元间隙中组织液蓄积,导致黄斑部出现囊样水肿的状态。葡萄膜炎通过血-视网膜屏障(BRB)破坏导致囊样黄斑水肿,特征为外丛状层和内颗粒层的囊样改变。囊壁由Müller细胞和轴索纤维形成。白内障手术或玻璃体手术后发生的术后囊样黄斑水肿称为Irvine-Gass综合征,需与葡萄膜炎性黄斑水肿区分 7)。
炎症控制后水肿仍可能持续,因此需要对炎症和水肿两方面进行干预 2)。如果存在感染性葡萄膜炎,应优先治疗病原体。葡萄膜炎诊疗指南将囊样黄斑水肿列为活动性葡萄膜炎的严重并发症,推荐早期治疗干预 7)。
炎症消退后黄斑水肿可能迁延。因此可能需要针对水肿本身的额外治疗。详见“标准治疗方法”一节。
2. 主要症状和临床所见
Section titled “2. 主要症状和临床所见”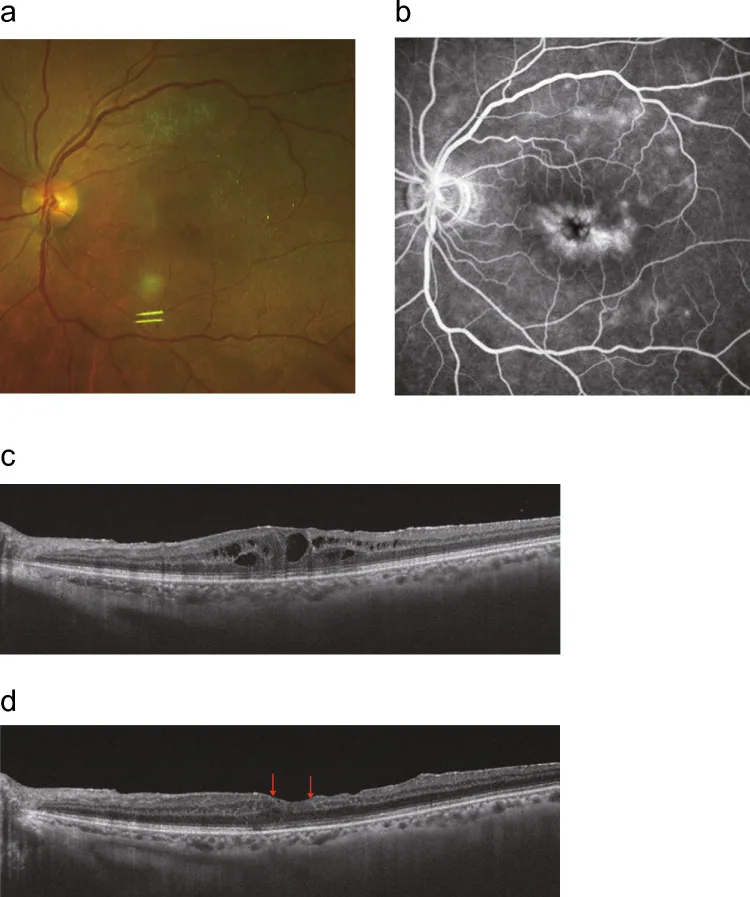
UME的主要自觉症状是中心视力下降。
- 视力下降:黄斑部液体蓄积导致中心视力受损。通常缓慢进展。
- 视物模糊:黄斑水肿引起的视网膜结构变化导致整个视野模糊。
- 视物变形:黄斑变形导致直线看起来弯曲。
- 中心暗点:严重病例在视野中心感觉到暗区。
在葡萄膜炎中,前房或玻璃体细胞浸润、角膜混浊、并发性白内障等也可导致视力下降。如果视力下降程度超过这些所见,应怀疑囊样黄斑水肿。视力下降通常为中度至重度,黄斑部的详细评估必不可少。
UME的临床所见因葡萄膜炎的类型和炎症活动性而异。
- 囊样黄斑水肿:荧光眼底造影(FA)显示花瓣状荧光渗漏。光学相干断层扫描(OCT)显示视网膜内囊泡和视网膜增厚。葡萄膜炎中囊样模式常见。
- 弥漫性黄斑水肿:OCT显示视网膜全层弥漫性增厚。
- 浆液性视网膜脱离:Vogt-小柳-原田病发病初期特征性表现,有时下方呈泡状脱离。
- 视网膜血管炎:伴有血管扩张迂曲、白鞘形成。FA检查确认荧光素渗漏是有用的。
- 前房炎症表现:伴有前房细胞、闪辉、玻璃体混浊。
3. 原因与风险因素
Section titled “3. 原因与风险因素”UME的根本原因是眼内炎症,其病因多种多样。
感染性
UME的风险因素包括以下内容:
- 中间部、后部和全葡萄膜炎:比前葡萄膜炎更常见 5)
- 慢性或持续性炎症:长期炎症增加发生UME的风险
- 长期使用类固醇:也增加类固醇性白内障和类固醇性青光眼的风险
- 玻璃体牵拉:后玻璃体膜对黄斑的牵拉也导致UME
4. 诊断与检查方法
Section titled “4. 诊断与检查方法”光学相干断层扫描(OCT)是诊断UME最重要的检查。结合前置镜和裂隙灯显微镜进行详细的眼底检查、OCT和荧光素眼底血管造影进行诊断。
- OCT:无创显示黄斑部横断面。可检测视网膜增厚、囊样形成和浆液性视网膜脱离。中心凹视网膜厚度(CST)≥300 μm常诊断为UME 2)。对评估治疗效果和追踪厚度变化也至关重要。
- 荧光素眼底血管造影(FA):用于检测视网膜血管通透性增加和新生血管。囊样黄斑水肿晚期表现为以中心凹为中心的花瓣状荧光渗漏和积存。
- 吲哚青绿血管造影(ICG):用于评估脉络膜循环。对结节病和Vogt-小柳-原田病的脉络膜病变评估有用。
- OCTA(OCT血管成像):无需造影剂即可评估视网膜血管和脉络膜新生血管,有助于检测相关新生血管。
- 裂隙灯显微镜检查:通过评估前房细胞、闪辉和玻璃体混浊判断炎症活动性。
- 眼底检查:确认黄斑部水肿、视网膜血管炎、玻璃体混浊的有无。
需要鉴别的疾病包括糖尿病黄斑水肿、视网膜静脉阻塞伴黄斑水肿、年龄相关性黄斑变性、以及由视网膜前膜引起的牵拉性黄斑水肿。白内障术后黄斑水肿(Irvine-Gass综合征)也需鉴别。
在UME的随访中,OCT对黄斑部的评估不可或缺。主治医生会根据炎症活动性和治疗阶段判断频率,但治疗期间通常每1~3个月检查一次。
5. 标准治疗方法
Section titled “5. 标准治疗方法”UME的治疗复杂,每位患者的最佳方法不同1)。感染性葡萄膜炎优先治疗病因,非感染性UME则以类固醇为中心进行治疗。葡萄膜炎诊疗指南推荐对持续性囊样黄斑水肿进行Tenon囊下类固醇注射,对于类固醇抵抗的难治病例,将玻璃体手术作为选项之一7)。
局部治疗(滴眼液)
Section titled “局部治疗(滴眼液)”- 类固醇滴眼液:用于前葡萄膜炎伴轻度UME。每日使用倍他米松或地塞米松滴眼液3~6次,根据炎症程度调整。对后段病变的效果有限1)。
- 散瞳药:联合使用托吡卡胺/去氧肾上腺素滴眼液预防虹膜后粘连。
- NSAIDs滴眼液:对人工晶状体眼的黄斑水肿有效,但对UME的疗效尚未明确证实1)。
Tenon囊下及眼周注射
Section titled “Tenon囊下及眼周注射”这是控制后段慢性炎症的首选局部操作,适用于黄斑水肿、视网膜血管炎及玻璃体混浊等。
- 曲安奈德后Tenon囊下注射:对累及后段的持续性葡萄膜炎如囊样黄斑水肿有效。用于眼底后极部炎症变化严重时7)。
- 操作:在颞下方结膜穹窿部穿刺,用24~25G钝针或锐针将曲安奈德20 mg/0.5 mL注入后Tenon囊下。上方注射有眼睑下垂风险,因此推荐颞下方穿刺。药物注入后约停留于Tenon囊下3个月,效果高峰约在1个月左右。
- 对于结节病和贝赫切特病伴发的囊样黄斑水肿,实施Kenacort-A 40 mg/mL(曲安奈德)0.5 mL后Tenon囊下注射(超说明书使用)。
- 需注意眼压升高(发生于15-20%的患者),后方注射可能降低眼压升高风险1)。
葡萄膜炎性黄斑水肿可能反复发作,因此可能需要多次注射。重复给药时建议间隔至少2个月。但每次注射前应测量眼压,并检查有无眼压升高或白内障。如果眼压升高成为问题,考虑改用其他治疗方法,如玻璃体内注射。
玻璃体内类固醇给药
Section titled “玻璃体内类固醇给药”玻璃体内给药可获得高药物浓度,但存在眼内感染和眼压升高的风险。
| 药物 | 作用持续时间 | 特点 |
|---|---|---|
| 曲安奈德(4 mg) | 约3个月 | 广泛使用。需要重复给药。 |
| Ozurdex(地塞米松植入剂 0.7 mg) | 约4-6个月 | 缓释型。已证实对UME有效。 |
| Iluvien(氟轻松 0.19 mg) | 约36个月 | 长效。白内障和青光眼风险高。 |
| Retisert(氟轻松 0.59 mg) | 约30个月 | 长效作用。青光眼手术率40% |
玻璃体内注射曲安奈德:给予4 mg可使约50%的患者视力改善1)。白内障进展与注射次数相关,注射4-5次后几乎必然发生。眼压升高见于20-45%的患者,但多数可通过滴眼液控制1)。
地塞米松玻璃体内植入剂(Ozurdex):这是一种缓释0.7 mg地塞米松的聚合物植入物。HURON试验(III期)中,Ozurdex 0.7 mg组在26周时42%的患者玻璃体混浊评分为零(安慰剂组12%,p<0.001)9)。在8周时确认了中心凹视网膜厚度显著降低和玻璃体混浊改善9)。
Fan等人(2023)的系统评价和荟萃分析显示,单次DEX植入后,BCVA在1个月时改善-0.15 logMAR,3个月时改善-0.22 logMAR,6个月时改善-0.24 logMAR3)。中心黄斑厚度(CMT)在1个月时减少-179.77 μm,3个月时减少-179.13 μm,6个月时减少-140.25 μm。
DEX植入后眼压升高(IOP>21 mmHg)的发生率为13.6%,白内障形成为5.4%,均可用滴眼液控制3)。
POINT试验直接比较了眼周曲安奈德(PTA)、玻璃体内曲安奈德(ITA)和玻璃体内DEX植入剂(IDI),中心凹视网膜厚度减少率分别为23%、39%和46%1)。玻璃体内给药优于眼周给药,但玻璃体内给药组的眼压升高风险也更高。
氟轻松玻璃体内植入剂:有Iluvien(0.19 mg,持续36个月)和Retisert(0.59 mg,持续30个月)。可获得长期效果,但有晶状体眼中73.8%(Iluvien)至90%以上(Retisert)需要白内障手术,青光眼手术分别需要11.9%和40%1)。
脉络膜上腔注射曲安奈德(Xipere)
Section titled “脉络膜上腔注射曲安奈德(Xipere)”曲安奈德脉络膜上腔注射混悬液(Xipere; SCS-TA)是首个获批用于治疗UME的药物,也是首个获批用于脉络膜上腔给药的制剂2)。
上脉络膜腔(SCS)是位于脉络膜和巩膜之间的潜在空间,药物可选择性分布到眼后段2)。动物实验表明,与玻璃体内注射相比,上脉络膜给药使眼后段药物暴露量高出12倍,而眼前段暴露量降低96%2)。这一特性降低了白内障和眼压升高的风险。
在PEACHTREE试验(III期)中,SCS-TA 4 mg组在24周时达到BCVA改善≥15个字母的患者比例为46.9%(假手术组15.6%,p<0.001)2)。中心凹视网膜厚度平均减少152.6 μm对比17.9 μm(p<0.001),从第4周起即观察到显著差异。
在MAGNOLIA扩展研究中,SCS-TA组50%的患者在第二次注射后长达9个月内无需挽救治疗2)。48周内至挽救的中位时间,SCS-TA组为257天,假手术组为55.5天。
SCS-TA的疗效不受是否合并全身性类固醇使用、葡萄膜炎的解剖位置或病程长短的影响2)。非挽救患者中类固醇相关眼压升高的发生率为10.8%,低于假手术组接受挽救治疗患者的21.7%2)。
- 全身性皮质类固醇:对于双眼或重度UME,起始泼尼松龙0.5–1 mg/kg1)。Vogt-小柳-原田病采用类固醇冲击疗法。由于副作用多,应在至少6个月内缓慢减量。
- 免疫抑制剂:环孢素(新山地明3–5 mg/kg/日)在类固醇减量困难时联合使用。需监测血药浓度(谷值50–200 ng/mL)和肾功能。Behçet病中,秋水仙碱(0.5–1.5 mg/日)是抑制炎症发作的一线药物。
- 抗TNF-α抗体(英夫利西单抗):用于秋水仙碱和环孢素治疗后仍反复发作的重症Behçet病。通常每2个月静脉输注5 mg/kg。
- 幼年特发性关节炎(JIA)相关葡萄膜炎:对于伴有慢性虹膜睫状体炎的UME,推荐包括甲氨蝶呤和生物制剂(阿达木单抗)在内的阶梯治疗4)。IOIS报告推荐甲氨蝶呤、硫唑嘌呤、吗替麦考酚酯作为伴有UME的葡萄膜炎的一线免疫抑制剂8)。阿达木单抗在甲氨蝶呤治疗无效的JIA相关葡萄膜炎伴囊样黄斑水肿中,报告了97.7%的CME控制率8)。
VEGF抑制剂
Section titled “VEGF抑制剂”VEGF抑制剂在UME中为超说明书使用1)。合并脉络膜新生血管时作为一线选择。对于类固醇不耐受或类固醇反应者(易出现眼压升高者)是强有力的选择。然而,针对UME的明确给药方案尚未确立1)。
玻璃体切除术适用于药物治疗抵抗或类固醇抵抗的囊样黄斑水肿7)。联合内界膜剥离的玻璃体切除术、联合囊切开术的玻璃体切除术用于持续性囊样黄斑水肿。视网膜前膜、黄斑裂孔、玻璃体积血也是手术适应证。最好在炎症稳定期进行,并考虑术前术后补充类固醇。
术后炎症可能加重,因此需仔细评估风险获益比1)。玻璃体切除术后,曲安奈德的半衰期从18.6天缩短至3.2天,因此推荐使用长效药物1)。
首先尝试用降压滴眼液控制。多数情况下滴眼液可以控制。如果滴眼液和口服药物不足,则考虑青光眼手术如小梁切开术。小梁切开术对类固醇性青光眼特别有效。
6. 病理生理学与详细发病机制
Section titled “6. 病理生理学与详细发病机制”内层和外层血-视网膜屏障(BRB)的破坏在UME的发生中起核心作用。
血-视网膜屏障的破坏
Section titled “血-视网膜屏障的破坏”正常情况下,BRB由视网膜血管内皮细胞(内侧)和视网膜色素上皮细胞(外侧)的紧密连接维持。在葡萄膜炎中,炎症细胞因子(TNF-α、IL-1β、IL-6)降低紧密连接蛋白(ZO-1、occludin、claudin)的表达,导致血管通透性增加5)。VEGF也促进血管通透性增加和新生血管形成2)。液体积聚主要发生在内核层和Henle纤维层,表现为外丛状层和内颗粒层的囊样改变。
炎症级联反应
Section titled “炎症级联反应”葡萄膜炎引起的炎症触发以下连锁反应:
- 免疫细胞浸润:T细胞和巨噬细胞迁移至眼内并释放炎症介质
- 前列腺素产生:通过环氧化酶激活增强产生,增加血管通透性1)
- VEGF升高:直接导致血管通透性增加和水肿形成
- 补体激活:促进外周血管损伤和视网膜内皮细胞的直接损伤
玻璃体的参与
Section titled “玻璃体的参与”后玻璃体膜对黄斑的牵引也可能导致UME的发生。在视网膜前膜和玻璃体黄斑牵引综合征中,玻璃体牵引可引起黄斑水肿。与葡萄膜炎相关的玻璃体混浊和玻璃体纤维化容易对黄斑产生牵引。
糖皮质激素的作用机制
Section titled “糖皮质激素的作用机制”曲安奈德与细胞内糖皮质激素受体结合,促进脂皮质素产生,抑制促炎性花生四烯酸的释放2)。它抑制免疫细胞浸润和活化,降低VEGF表达,从而改善血管通透性并减轻水肿2)。如果治疗有效且水肿消退,可预期视力改善;但在慢性葡萄膜炎中,水肿的复发或持续存在可能恶化视力预后。
7. 最新研究与未来展望
Section titled “7. 最新研究与未来展望”上脉络膜腔给药的药代动力学
Section titled “上脉络膜腔给药的药代动力学”Muya等人使用兔子的研究表明,与玻璃体内注射曲安奈德制剂相比,SCS-TA在注射时的滑动力更低且变异性更小2)。这有助于安全地将药物递送到上脉络膜腔。上脉络膜给药后,后段的高浓度维持了前两个月,到第三个月时达到与玻璃体内注射相当的水平。
Mackensen等人的试验中,干扰素β(44 mg皮下注射,每周3次)组黄斑厚度平均减少206 μm,而甲氨蝶呤(20 mg皮下注射,每周1次)组增加47 μm(p<0.0001)1)。干扰素α2a对包括白塞病在内的难治性UME有效率超过80%。
玻璃体内甲氨蝶呤
Section titled “玻璃体内甲氨蝶呤”Taylor等人对15例患者的前瞻性研究中,玻璃体内注射甲氨蝶呤400 μg使平均黄斑厚度从425 μm降至275 μm1)。三分之一的患者在中位4个月时复发,但再次注射显示出与初次治疗相似的疗效。
奥曲肽(100 μg皮下注射,每日3次,或长效20 mg肌肉注射,每月1次)据报道可使9只常规治疗抵抗的慢性UME眼中的7只眼水肿消退6)。局部眼内制剂的开发也在进行中。
玻璃体内西罗莫司
Section titled “玻璃体内西罗莫司”玻璃体内西罗莫司(mTOR抑制剂)在SAVE-2试验中未达到减轻UME的统计学显著性,但在部分患者中观察到显著改善1)。适当的患者选择是未来的挑战。
法瑞西单抗(抗VEGF-A/Ang-2双重抑制剂)同时靶向VEGF和血管生成素-2,预期在视网膜血管稳定化和通透性抑制方面具有协同效应。在糖尿病黄斑水肿和渗出性AMD获批后,其应用于葡萄膜炎性黄斑水肿正处于研究阶段。作为利用抗VEGF药物多面作用的新治疗方向而受到关注。
SCS-TA(Xipere)于2021年在美国获批,但截至2026年3月,在日本尚未获批。关于国内的使用可能性,需要确认未来的监管动态。
8. 参考文献
Section titled “8. 参考文献”- Teper SJ. Update on the management of uveitic macular edema. J Clin Med. 2021;10(18):4133.
- Fung S, Syed YY. Suprachoroidal space triamcinolone acetonide: a review in uveitic macular edema. Drugs. 2022;82(13):1403-1410.
- Fan S, Shi XY, Zhao CF, et al. Efficacy and safety of single-dose intravitreal dexamethasone implant in non-infectious uveitic macular edema: a systematic review and meta-analysis. Front Med. 2023;10:1126724.
- Angeles-Han ST, Lo MS, Henderson LA, et al. Childhood arthritis and rheumatology research alliance consensus treatment plans for juvenile idiopathic arthritis-associated and idiopathic chronic anterior uveitis. Arthritis Care Res. 2019;71(4):482-491.
- Haydinger CD, Ferreira LB, Williams KA, Smith JR. Mechanisms of macular edema. Front Med. 2023;10:1128983.
- Kafkala C, Choi JY, Engelbrecht NE, et al. Octreotide treatment for chronic uveitic cystoid macular edema. Graefes Arch Clin Exp Ophthalmol. 2006;244(5):563-569.
- 日本眼科学会ぶどう膜炎診療ガイドライン作成委員会. ぶどう膜炎診療ガイドライン. 日眼会誌. 2019;123(6):635-696.
- Branford JA, Pavesio C, Goldstein DA, et al. IOIS report on immunomodulatory treatment of non-infectious uveitis. Br J Ophthalmol. 2025;109(4):482-489.
- Lowder C, Belfort R Jr, Lightman S, et al. Dexamethasone intravitreal implant for noninfectious intermediate or posterior uveitis (HURON). Arch Ophthalmol. 2011;129(5):545-553.
