非增殖性RR

放射性视网膜病变(Radiation Retinopathy)
一目了然的要点
Section titled “一目了然的要点”1. 什么是放射性视网膜病变?
Section titled “1. 什么是放射性视网膜病变?”放射性视网膜病变(Radiation Retinopathy; RR)是一种慢性进行性闭塞性视网膜微血管病变,发生于眼内肿瘤、眼眶或鼻窦肿瘤、颅内疾病等放射治疗时视网膜被照射的情况。常见于脉络膜恶性黑色素瘤等眼内肿瘤、眼眶肿瘤、头颈部肿瘤、脑肿瘤的放射治疗后。1933年由Stallard首次报道。
此外,事故性大量照射可在数周内导致视网膜和视神经坏死。
由于增殖能力强的视网膜血管内皮细胞对放射线具有选择性敏感性,从而形成毛细血管闭塞、缺血、新生血管等一系列病理过程1)。脉络膜血管内皮也会受损。发病多在照射后半年以上,尤其是2~3年后。总体发病率因照射野而异。
以下按部位显示发病率。
| 照射部位 | 发病率 |
|---|---|
| 眼眶 | 85.7% |
| 鼻窦 | 45.4% |
| 鼻咽 | 36.4% |
| 脑 | 3.1% |
一项荟萃分析显示,脑头颈部肿瘤放疗后RR患病率约为6%,视神经病变(ON)约为2% 3)。包括迟发性病例在内的总体发病率约为17% 4)。
发病率因照射部位、剂量、分割方法和合并症而异。总体发病率据报道为17%,并非所有患者都会发病 4)。定期眼底检查对于早期发现很重要。
2. 主要症状和临床所见
Section titled “2. 主要症状和临床所见”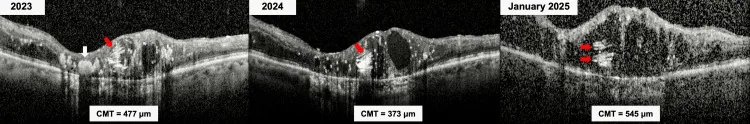
早期常无症状,有时在体检中偶然发现。当病变累及黄斑部或视神经时,会出现以下症状。
眼底所见类似糖尿病视网膜病变,从微动脉瘤、视网膜出血、硬性渗出开始,随后出现棉絮斑。进展时发生视网膜新生血管,导致玻璃体出血。黄斑水肿和中心凹周围毛细血管闭塞导致视力下降。一旦发病,进展比糖尿病视网膜病变更快。
临床经过分为以下阶段:
- 初期:出现微动脉瘤、视网膜出血、硬性渗出。
- 进展期:出现棉絮状白斑。提示缺血范围扩大。
- 重症期:发生视网膜新生血管,导致玻璃体出血。
- 并发症期:黄斑水肿和中心凹周围毛细血管闭塞进展,视力显著下降。
放射性视网膜病变大致分为非增殖性和增殖性两类。
增殖性RR
作为迟发性特殊表现,一例17年后发病的病例中,OCT显示囊腔内胆固醇结晶形成的洋葱环征,被认为是慢性期治疗抵抗的标志 6)。
此外,一例全脑照射30 Gy后16个月出现上方视网膜局限性RR的病例中,病变分布与照射野的30 Gy等剂量线一致,证实即使在低剂量区域,发病模式也与照射野相对应 7)。
照射后半年以上,特别是2~3年后发病较多。诊断时的中位时间据报道为照射后39个月3),但也有17年后迟发的病例4)。照射后需要长期定期进行眼底检查。
3. 原因与风险因素
Section titled “3. 原因与风险因素”剂量阈值通常被认为是35 Gy4)。超过45 Gy的照射容易发病,超过50 Gy时发病风险特别高3)。但也有在20 Gy时发生的报告,并且在30 Gy的全脑照射后也有发病报道7),因此即使低于阈值剂量也需要注意。增殖能力强的视网膜血管内皮细胞最容易受损,脉络膜血管内皮也会受损。
照射后的潜伏期为半年以上,特别是2~3年后多见。这被认为是由于放射线引起的内皮细胞损伤累积,需要时间才能超过临床阈值。
以下列出风险因素。
| 风险因素 | 内容 |
|---|---|
| 总剂量 | >35 Gy(阈值)4),超过45 Gy为高风险 |
| 分割剂量 | 高分割照射 |
| 照射部位 | 眼眶或视交叉附近3) |
| 糖尿病 | 加重微血管脆弱性 |
| 联合化疗 | 敏感性增加 |
靠近视交叉的照射与RR发病有显著相关性(p=0.009)3)。
增殖性RR的风险因素
Section titled “增殖性RR的风险因素”增殖性RR约占所有RR的3%至25%5)。在 plaque 近距离放射治疗后,部分病例在照射后32个月进展为增殖性RR。
糖尿病是放射性视网膜病变的重要危险因素。糖尿病引起的微血管脆弱性与放射线导致的内皮损伤协同作用,可能在较低剂量下即可发病。在维持血糖控制的同时,建议放射治疗后进行更频繁的眼底检查。
4. 诊断与检查方法
Section titled “4. 诊断与检查方法”荧光眼底血管造影(FA)与分期
Section titled “荧光眼底血管造影(FA)与分期”FA是RR诊断和分期的基础检查。早期可见视网膜毛细血管通透性增加,随着病情进展,毛细血管闭塞。小动脉也闭塞,导致视网膜无灌注区广泛扩大,并出现视网膜新生血管。Amoaku FA分级(1~4级)被广泛使用1)。
| 分级 | 主要表现 |
|---|---|
| 1 | 微动脉瘤和局限性毛细血管扩张 |
| 2 | 毛细血管闭塞和广泛血管异常 |
| 3 | 视盘或视网膜新生血管 |
| 4 | 玻璃体出血/牵拉性视网膜脱离 |
吲哚青绿(ICG)荧光造影也可观察到脉络膜血管闭塞。
OCT·OCTA
Section titled “OCT·OCTA”OCT用于根据Horgan分级(1~5级)对ME进行定量评估,在 plaque 近距离放射治疗后4个月即可通过OCT检测到1)。OCTA可无创地可视化毛细血管脱落、无灌注区域及FAZ的变化,对早期检测有用1)。
发病时机与监测计划
Section titled “发病时机与监测计划”RR通常在照射后半年以上发病,尤其是2~3年后。发病中位时间为照射后39个月,>50Gy的照射需要特别密切观察3)。照射后建议定期(至少每6~12个月)进行眼底检查和OCT检查。
诊断时,询问放射治疗史(眼内肿瘤、眼眶肿瘤、颅内肿瘤、鼻窦肿瘤)非常重要。
由于眼底表现与糖尿病视网膜病变相似,需要进行鉴别。通过确认有无放射照射史,通常可以轻松鉴别。
- 糖尿病视网膜病变:眼底表现(微动脉瘤、出血、渗出、新生血管)与放射性视网膜病变极为相似。有无糖尿病和放射照射史是鉴别的关键。放射性视网膜病变一旦发病,进展速度比糖尿病视网膜病变更快,这是其特征。
- 视网膜静脉阻塞:以沿阻塞静脉的出血和水肿为主,呈扇形分布,这在放射性视网膜病变中看不到。如果没有放射照射史,鉴别很容易。
眼底表现(微动脉瘤、出血、白斑、新生血管)两者非常相似。最重要的鉴别点是有无放射线照射史。此外,放射性视网膜病变一旦发生,进展比糖尿病视网膜病变更快,其时间特征为照射后半年至数年。两病合并时管理尤其困难。
5. 标准治疗方法
Section titled “5. 标准治疗方法”抗VEGF治疗(一线选择)
Section titled “抗VEGF治疗(一线选择)”抗VEGF药物是目前RR治疗的一线选择。使用的药物包括贝伐珠单抗(IVB)、雷珠单抗和阿柏西普1)。也有使用高剂量雷珠单抗2mg的报道1)。
预防性抗VEGF给药旨在抑制放疗后RR的发生。一项纳入4项研究共2109例患者的荟萃分析显示以下结果2)。
- 黄斑水肿(ME)减少50%(OR 0.50)
- 放射性视神经病变(RON)减少38%(OR 0.62)
- 不良视力(视力<20/200等效)减少50%(OR 0.50)
推荐方案为IVB 1.25–1.5 mg,每4个月一次,持续24个月2)。预防性抗VEGF治疗48个月后,最佳矫正视力显著改善:预防组0.54 logMAR vs. 对照组2.00 logMAR5)。
Sahoo等人(2021)的综述中,Schefler和Murray的RCT验证了抗VEGF疗法的有效性,并建议对黄斑水肿进行早期干预(照射后90天内)1)。
Victor等人(2023)对4项研究共2109例患者的荟萃分析证实,预防性IVB可显著减少斑块近距离放疗后的ME(50%)和RON(38%)2)。
对视网膜无血管区进行激光光凝,以预防视网膜新生血管和新生血管性青光眼的发生。全视网膜光凝(PRP)用于增殖性RR,报道的消退率为66% 5)。斑块治疗后病例中也有64.4%观察到消退 5)。局灶激光作为ME的辅助治疗。
局部类固醇给药
Section titled “局部类固醇给药”曲安奈德(TA)、地塞米松玻璃体内植入剂(DEX)和氟轻松(FA)用于抗VEGF治疗抵抗时的辅助治疗 5)。
增殖性RR的处理
Section titled “增殖性RR的处理”玻璃体积血需行玻璃体切除术。牵拉性视网膜脱离也适用玻璃体切除术。NVG可能需要滤过手术或睫状体光凝术。COMS数据显示,照射后3年43%的患者矫正视力低于20/200 2)。
- 根据放射治疗史和眼底表现确诊放射性视网膜病变
- 通过荧光血管造影评估视网膜无灌注区的范围和程度
- 如果存在视网膜无灌注区 → 激光光凝(预防新生血管和新生血管性青光眼)
- 如果发生玻璃体积血 → 保守观察或玻璃体切除术
- 如果存在黄斑水肿 → 抗VEGF药物(一线)和类固醇(辅助)
目前没有有效的方法阻止其进展,预后通常不良。
预防性给药推荐每4个月一次,持续24个月的方案2)。治疗性给药的持续时间根据疾病活动性而变化。在治疗抵抗的慢性病例中,可能需要超过72次注射6)。
6. 病理生理学与详细发病机制
Section titled “6. 病理生理学与详细发病机制”放射性视网膜损伤的核心机制是视网膜血管内皮细胞的选择性消失。增殖能力高的视网膜血管内皮细胞最易受损,脉络膜血管内皮也会受损。内皮细胞对放射线特别敏感,DNA损伤和凋亡导致毛细血管壁崩解。
病理进展遵循以下阶段:
- 内皮细胞损伤期:照射后立即进展。内皮细胞发生DNA双链断裂和凋亡,血管壁完整性丧失。
- 毛细血管闭塞与缺血期:内皮细胞消失导致毛细血管闭塞,视网膜缺血区扩大。荧光素血管造影早期显示通透性增加,但随着进展,闭塞占主导。小动脉也闭塞,导致视网膜无血管区广泛扩大。
- VEGF产生与血管新生期:缺血视网膜中VEGF过度产生,诱导脆弱的新生血管增殖。
- 终末期(增殖性改变):进展为玻璃体出血、牵拉性视网膜脱离和新生血管性青光眼。
晚期糖基化终末产物(AGE)的积累、周细胞丢失和基底膜增厚也被认为会导致内皮损伤。这一机制与糖尿病视网膜病变相似,解释了糖尿病患者RR风险增加的原因之一。
从照射到临床发病存在半年以上,尤其是2-3年的潜伏期。这反映了内皮细胞损伤积累和毛细血管闭塞临床显现所需的时间。
7. 最新研究与未来展望(研究阶段报告)
Section titled “7. 最新研究与未来展望(研究阶段报告)”预防性抗VEGF的证据强化
Section titled “预防性抗VEGF的证据强化”Victor等人(2023)的荟萃分析是目前显示预防性抗VEGF给药有效性的最大规模证据,但大多数研究对象为观察性研究,需要通过随机对照试验(RCT)进一步验证2)。最佳给药间隔、药物和疗程的标准化也是未来的课题。
OCTA(光学相干断层扫描血管成像)早期检测
Section titled “OCTA(光学相干断层扫描血管成像)早期检测”OCTA无需造影剂即可定量评估毛细血管脱落、FAZ扩大和毛细血管密度降低。它可以在放疗后早期阶段检测无灌注区域,并正在应用于RR的筛查和监测1)。
治疗抵抗性放射性视网膜病变的慢性化标志物
Section titled “治疗抵抗性放射性视网膜病变的慢性化标志物”Kayabai等人(2025)报告了一例53岁男性病例,他在眼内肿瘤放疗后19年出现放射性视网膜病变6)。OCT上观察到的洋葱环征(囊腔内胆固醇结晶的多层沉积)被认为是慢性、治疗抵抗性放射性视网膜病变的影像标志物,该患者需要超过72次玻璃体内注射的长期治疗过程。
brolucizumab和faricimab(血管生成素/VEGF双靶点)等下一代抗VEGF药物正在研究用于放射性视网膜病变5)。它们被期待作为现有药物抵抗病例的替代选择。
质子线和重粒子线治疗后的风险评估
Section titled “质子线和重粒子线治疗后的风险评估”除了传统的X线和伽马射线外,质子线和重粒子线(碳离子线)治疗后放射性视网膜病变的风险评估正在进行中。即使采用剂量高度集中的粒子线治疗,如果视网膜包含在照射野内,仍可能发生视网膜病变,因此治疗计划中的视网膜剂量评估和术后监测是重要课题。
与放射性视神经病变(RON)的合并管理
Section titled “与放射性视神经病变(RON)的合并管理”RR和放射性视神经病变(RON)可能在同一照射野同时发生。EBRT后RON的发生率约为2% 3)。当RR和RON合并时,视功能损害更为严重,因此除眼底检查外,定期进行视野检查和OCT视神经评估已成为重要的研究课题。
8. 参考文献
Section titled “8. 参考文献”- Sahoo NK, Lim JW, Laude A, et al. Radiation retinopathy—the complex interplay of radiation, vasculature, and clinical outcomes. Clin Ophthalmol. 2021;15:3797-3809.
- Victor AA, Mauldin WM, Houston SK, et al. Prophylactic intravitreal bevacizumab and radiation retinopathy after plaque brachytherapy for uveal melanoma: a meta-analysis. Clin Ophthalmol. 2023;17:2997-3009.
- Kinaci-Tas B, Wilschut JA, Kilic E, et al. The incidence of radiation-induced optic neuropathy and retinopathy in patients treated with external beam radiation therapy: a systematic review and meta-analysis. Cancers. 2023;15:1999.
- Chakraborty K, Jain S, Tripathy K, et al. Delayed onset radiation retinopathy following skull base tumor treatment. Indian J Ophthalmol. 2023;71:303-305.
- Mularska W, Nowak-Gospodarowicz I, Golik B, et al. Radiation retinopathy after plaque brachytherapy for uveal melanoma—pathogenesis, diagnosis, and management. J Contemp Brachytherapy. 2023;15:372-382.
- Kayabai M, Ilhan S, Celik E, et al. Onion ring sign as a biomarker of chronic treatment-resistant radiation retinopathy. Cureus. 2025;17(11):e97758.
- Chan L, Eftekari SC, Nguyen QT, et al. Radiation retinopathy after whole-brain radiotherapy: a case report and literature review. Adv Radiat Oncol. 2021;6:100706.
