จอประสาทตาเสื่อมจากรังสีเป็นโรคหลอดเลือดฝอยจอตาที่เรื้อรังและลุกลาม เกิดขึ้นหลังการฉายรังสีรักษาเนื้องอกในลูกตา เบ้าตา โพรงอากาศ หรือในกะโหลกศีรษะ
ลักษณะของจอประสาทตา คล้ายกับจอประสาทตาเสื่อมจากเบาหวาน แต่เมื่อเกิดขึ้นแล้วจะดำเนินโรคเร็วกว่าจอประสาทตาเสื่อมจากเบาหวาน
เกณฑ์ปริมาณรังสีโดยทั่วไปคือ 35 เกรย์ แต่ความเสี่ยงจะเพิ่มขึ้นโดยเฉพาะเมื่อเกิน 45 เกรย์ และมีรายงานการเกิดโรคที่ 20 เกรย์
การเกิดโรคหลังการฉายรังสี 6 เดือน โดยเฉพาะอย่างยิ่ง 2-3 ปีต่อมา ค่ามัธยฐานของการวินิจฉัยคือ 39 เดือนหลังการฉายรังสี แต่มีกรณีที่เกิดช้าถึง 17 ปี
การรักษาด้วยยาต้าน VEGF เป็นทางเลือกแรกในปัจจุบัน และผลการวิเคราะห์อภิมานแสดงว่าการให้ยาเพื่อป้องกันช่วยลดอุบัติการณ์ของจอประสาทตา บวมน้ำได้ประมาณ 50%เมื่อดำเนินไปสู่จอประสาทตาเสื่อมจากรังสีชนิดมีเส้นเลือดงอกใหม่ อาจจำเป็นต้องตัดลูกตาออกเนื่องจากเลือดออกในน้ำวุ้นตา หรือต้อหิน ชนิดเส้นเลือดงอกใหม่
ไม่มีวิธีที่มีประสิทธิภาพในการหยุดการดำเนินโรค และการพยากรณ์โรคมักไม่ดี
จอประสาทตาเสื่อมจากรังสี (Radiation Retinopathy; RR) เป็นโรคหลอดเลือดฝอยจอประสาทตา อุดตันเรื้อรังที่ดำเนินไปอย่างช้าๆ ซึ่งเกิดขึ้นเมื่อจอประสาทตา อยู่ในบริเวณที่ได้รับรังสีระหว่างการฉายรังสีรักษาเนื้องอกในลูกตา เนื้องอกในเบ้าตา หรือไซนัส หรือโรคในกะโหลกศีรษะ เกิดขึ้นหลังการฉายรังสีรักษาเนื้องอกในลูกตา เช่น มะเร็งเมลาโนมาชนิดร้ายของคอรอยด์ เนื้องอกในเบ้าตา เนื้องอกบริเวณศีรษะและคอ และเนื้องอกในสมอง รายงานครั้งแรกโดยสตอลลาร์ดในปี ค.ศ. 1933
ทั้งนี้ การได้รับรังสีปริมาณมากจากอุบัติเหตุอาจทำให้จอประสาทตา และเส้นประสาทตา ตายภายในไม่กี่สัปดาห์
เนื่องจากเซลล์บุผนังหลอดเลือดจอประสาทตา ที่มีความสามารถในการเพิ่มจำนวนสูงแสดงความไวต่อรังสีแบบเลือกสรร จึงเกิดเป็นชุดของภาวะทางพยาธิวิทยาที่นำไปสู่การอุดตันของเส้นเลือดฝอย ภาวะขาดเลือด และการสร้างเส้นเลือดใหม่ 1) เซลล์บุผนังหลอดเลือดคอรอยด์ ก็ได้รับความเสียหายเช่นกัน การเกิดโรคมักเกิดขึ้นหลังจากหกเดือนหรือมากกว่าหลังการฉายรังสี โดยเฉพาะอย่างยิ่งหลังจาก 2-3 ปี อัตราการเกิดโรคโดยรวมแตกต่างกันไปตามขอบเขตการฉายรังสี
ด้านล่างนี้คืออัตราการเกิดโรคตามตำแหน่งต่างๆ
ตำแหน่งที่ฉายรังสี อัตราการเกิดโรค เบ้าตา 85.7% โพรงจมูกข้าง 45.4% ช่องคอส่วนจมูก 36.4% สมอง 3.1%
มีการวิเคราะห์อภิมานรายงานความชุกของ RR หลังการฉายรังสีรักษาเนื้องอกในสมอง ศีรษะ และคอประมาณ 6% และโรคเส้นประสาทตา (ON) ประมาณ 2% 3) อุบัติการณ์โดยรวมรวมถึงกรณีที่เกิดอาการช้ารายงานประมาณ 17% 4)
Q
ผู้ที่ได้รับการฉายรังสีรักษาทุกคนจะเป็นโรคนี้หรือไม่?
A
อุบัติการณ์แตกต่างกันอย่างมากตามตำแหน่งที่ฉายรังสี ปริมาณรังสี วิธีการแบ่งขนาดรังสี และโรคร่วม มีรายงานอุบัติการณ์โดยรวม 17% และไม่ใช่ผู้ป่วยทุกรายจะเป็นโรคนี้ 4) การตรวจอวัยวะตาเป็นประจำมีความสำคัญต่อการตรวจพบตั้งแต่เนิ่นๆ
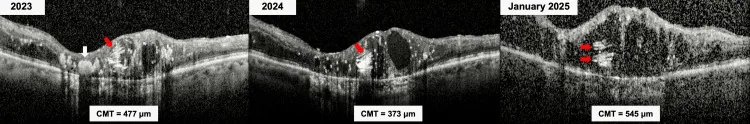
จอประสาทตาบวมจากรังสีรักษาใน OCT Kayabaşı M, et al. Evolution of the Onion Ring Sign in Radiation Retinopathy. Cureus. 2025. Figure 3. PM
CI D: PMC12740121. License: CC BY.
ใน OCT เดือนมกราคม 2023, 2024 และ 2025 ค่า CMT คือ 477 μm, 373 μm และ 545 μm ตามลำดับ ซึ่งสอดคล้องกับจอประสาทตา บวมที่กล่าวถึงในหัวข้อ “2. อาการหลักและอาการแสดงทางคลินิก”
ระยะแรกมักไม่มีอาการ และอาจพบโดยบังเอิญจากการตรวจสุขภาพ เมื่อรอยโรคลุกลามถึงจอประสาทตา หรือประสาทตา จะเกิดอาการดังต่อไปนี้
สายตาลดลง : เกิดจากจอประสาทตา บวมหรือขาดเลือด มักค่อยเป็นค่อยไปภาพบิดเบี้ยว เซลล์รับแสง เนื่องจากจอประสาทตา บวมอาการเห็นจุดลอยและตามัว : เกิดขึ้นเมื่อมีเลือดออกในน้ำวุ้นตา ข้อบกพร่องของลานสายตา : พบในกรณีที่มีภาวะขาดเลือดของจอประสาทตา อย่างกว้างขวางหรือโรคเส้นประสาทตา
ลักษณะที่พบในจอประสาทตา คล้ายกับจอประสาทตาเสื่อมจากเบาหวาน โดยเริ่มจาก microaneurysm, จอประสาทตา ตกเลือด, และ hard exudate ต่อมาจึงเกิด cotton-wool spot เมื่อดำเนินไปจะเกิดเส้นเลือดใหม่ที่จอประสาทตา ซึ่งนำไปสู่เลือดออกในน้ำวุ้นตา การมองเห็น ลดลงเนื่องจากจอประสาทตา บวมน้ำและการอุดตันของเส้นเลือดฝอยรอบรอยบุ๋มจอประสาทตา เมื่อเกิดขึ้นแล้วจะดำเนินโรคเร็วกว่าจอประสาทตาเสื่อมจากเบาหวาน
การดำเนินโรคทางคลินิกเป็นไปตามระยะต่อไปนี้
ระยะเริ่มแรก : เกิด microaneurysm, จอประสาทตา ตกเลือด, และ hard exudateระยะลุกลาม : เกิดจุดขาวคล้ายสำลี บ่งชี้ถึงการขยายตัวของบริเวณขาดเลือดระยะรุนแรง : เกิดเส้นเลือดใหม่ในจอตาและเลือดออกในน้ำวุ้นตา ระยะแทรกซ้อน : ภาวะจอตาบวมน้ำและการอุดตันของเส้นเลือดฝอยรอบรอยบุ๋มจอตา ดำเนินไป ทำให้การมองเห็น ลดลงอย่างมาก
จอตาถูกทำลายจากรังสีแบ่งเป็นชนิดไม่เจริญงอกงามและชนิดเจริญงอกงาม
RR ชนิดไม่เจริญงอกงาม
หลอดเลือดโป่งพองขนาดเล็ก
Telangiectasia : การขยายและคดเคี้ยวของหลอดเลือดผิดปกติ เห็นชัดเจนในการตรวจฟลูออเรสซีน แองจิโอกราฟี (FA )
เลือดออกในจอตา : เลือดออกแบบจุดหรือแบบเปลวไฟกระจาย
สารคัดหลั่งแข็ง : การแทรกซึมสีเหลืองขาวจากการสะสมของไขมัน
จอตาบวมที่จุดรับภาพ (ME) : สิ่งตรวจพบที่ส่งผลต่อพยากรณ์การมองเห็น มากที่สุด ปรากฏเป็นจอตาบวมแบบถุงน้ำหรือแบบกระจายใน OCT
RR ชนิดงอกขยาย
เส้นเลือดใหม่ในจอตา (NV) : หลอดเลือดผิดปกติที่ถูกกระตุ้นจากบริเวณขาดเลือด ทำให้เกิดเลือดออกในวุ้นตา
เลือดออกในน้ำวุ้นตา : การมองเห็น ลดลงอย่างเฉียบพลันจากการแตกของเส้นเลือดใหม่ที่ผิดปกติ
จอประสาทตาลอก ชนิด tractional
โรคต้อหินจากเส้นเลือดใหม่ (NVG ) : โรคต้อหิน ที่ดื้อต่อการรักษาเนื่องจากการงอกของเส้นเลือดใหม่เข้าไปในม่านตา และมุมตา อัตราการตัดลูกตาออกจากเบ้าตา จาก NVG รายงานอยู่ที่ 1-12% 5) .
ในฐานะที่เป็นลักษณะพิเศษที่พบได้ช้า ในกรณีที่เกิดอาการหลังจาก 17 ปี พบ สัญญาณวงแหวนหัวหอม (onion ring sign) ซึ่งเกิดจากผลึกคอเลสเตอรอลภายในโพรงถุงน้ำ ได้รับการยืนยันด้วย OCT และถูกจับตามองว่าเป็นเครื่องหมายของการดื้อต่อการรักษาในระยะเรื้อรัง 6) .
นอกจากนี้ ในกรณีของ RR ที่จำกัดอยู่ที่จอประสาทตา ส่วนบนซึ่งเกิดขึ้น 16 เดือนหลังจากการฉายรังสีสมองทั้งหมด 30 Gy การกระจายของรอยโรคสอดคล้องกับเส้นไอโซโดส 30 Gy ของสนามฉายรังสี และได้รับการยืนยันว่ารูปแบบการเกิดโรคสอดคล้องกับสนามฉายรังสีแม้ในบริเวณที่ได้รับปริมาณรังสีต่ำ 7) .
Q
อาการมักเกิดขึ้นเมื่อใด?
A
มักเกิดขึ้นหลังจากได้รับรังสีไปแล้ว 6 เดือน โดยเฉพาะอย่างยิ่งหลังจาก 2-3 ปี ค่ามัธยฐานของเวลาที่วินิจฉัยรายงานว่าอยู่ที่ 39 เดือนหลังการฉายรังสี3) แต่ก็มีกรณีที่เกิดช้าถึง 17 ปี4) หลังการฉายรังสี จำเป็นต้องตรวจอวัยวะตาเป็นประจำในระยะยาว
โดยทั่วไปถือว่าเกณฑ์ปริมาณรังสีอยู่ที่ 35 Gy4) การฉายรังสีที่มากกว่า 45 Gy ทำให้เกิดโรคได้ง่าย และที่มากกว่า 50 Gy ความเสี่ยงจะสูงเป็นพิเศษ3) อย่างไรก็ตาม มีรายงานการเกิดโรคที่ 20 Gy และหลังการฉายรังสีทั้งสมอง 30 Gy7) ดังนั้นจึงต้องระวังแม้ในปริมาณที่ต่ำกว่าเกณฑ์ เซลล์บุผนังหลอดเลือดจอประสาทตา ที่มีความสามารถในการแบ่งตัวสูงจะเสียหายได้ง่ายที่สุด และเซลล์บุผนังหลอดเลือดคอรอยด์ ก็เสียหายด้วย
ระยะแฝงหลังการฉายรังสีคือ 6 เดือนขึ้นไป โดยเฉพาะอย่างยิ่งมักเกิดหลังจาก 2-3 ปี เชื่อว่าเป็นเพราะความเสียหายของเซลล์บุผนังหลอดเลือดจากรังสีสะสมและต้องใช้เวลาเพื่อเกินเกณฑ์ทางคลินิก
ปัจจัยเสี่ยงมีดังนี้:
ปัจจัยเสี่ยง เนื้อหา ปริมาณรังสีรวม >35 Gy (เกณฑ์) 4) เสี่ยงสูงเมื่อเกิน 45 Gy ปริมาณรังสีแบบแบ่งส่วน การฉายรังสีแบบแบ่งส่วนสูง ตำแหน่งที่ฉายรังสี เบ้าตา /ใกล้จุดไขว้ประสาทตา 3) เบาหวาน ทำให้หลอดเลือดขนาดเล็กเปราะบางมากขึ้น การใช้เคมีบำบัดร่วม เพิ่มความไวต่อการตอบสนอง
มีการรายงานความสัมพันธ์ที่มีนัยสำคัญ (p=0.009) ระหว่างการฉายรังสีใกล้จุดไขว้ประสาทตาและการเกิด RR 3)
RR ชนิดเพิ่มจำนวนเกิดขึ้นใน 3–25% ของผู้ป่วย RR ทั้งหมด 5) ในกรณีหลังการรักษาด้วยการฝังแร่แบบแผ่น พบว่ามีการดำเนินไปเป็น RR ชนิดเพิ่มจำนวนที่ 32 เดือนหลังการฉายรังสี
หลังการรักษาด้วยรังสี คุณควรตรวจอวัยวะตาเป็นประจำ แม้ในระยะแรกจะไม่มีอาการ การตรวจพบแต่เนิ่นๆ จะช่วยเพิ่มทางเลือกในการรักษา ผู้ป่วยเบาหวานมีความเสี่ยงสูง ดังนั้นควรควบคุมระดับน้ำตาลในเลือดด้วย
Q
โรคเบาหวานเพิ่มความเสี่ยงของจอประสาทตาจากรังสีหรือไม่?
A
โรคเบาหวานเป็นปัจจัยเสี่ยงสำคัญของจอประสาทตาเสื่อมจากรังสี ความเปราะบางของหลอดเลือดขนาดเล็กจากโรคเบาหวานออกฤทธิ์ร่วมกับความเสียหายของเยื่อบุผนังหลอดเลือดจากรังสี ทำให้เกิดโรคได้แม้ในปริมาณรังสีที่ต่ำกว่า แนะนำให้ควบคุมระดับน้ำตาลในเลือดและตรวจอวัยวะภายในตาบ่อยขึ้นหลังการฉายรังสี
FA คือการตรวจพื้นฐานสำหรับการวินิจฉัยและแบ่งระยะของ RR ในระยะเริ่มแรกจะพบการซึมผ่านของหลอดเลือดฝอยจอประสาทตา เพิ่มขึ้น และเมื่อดำเนินไป หลอดเลือดฝอยจะอุดตัน หลอดเลือดแดงเล็กก็อุดตัน ทำให้บริเวณจอประสาทตา ที่ไม่มีหลอดเลือดขยายกว้าง และเกิดเส้นเลือดใหม่ในจอประสาทตา การจำแนก Amoaku FA (เกรด 1–4) ถูกใช้อย่างแพร่หลาย 1)
เกรด ผลการตรวจหลัก 1 Microaneurysm และการขยายตัวของเส้นเลือดฝอยเฉพาะที่ 2 การอุดตันของเส้นเลือดฝอยและความผิดปกติของหลอดเลือดอย่างกว้างขวาง 3 เส้นเลือดใหม่ที่จานประสาทตา หรือจอประสาทตา 4 เลือดออกในน้ำวุ้นตา และจอประสาทตาลอก แบบดึงรั้ง
ในการตรวจหลอดเลือดด้วยสีอินโดไซยานีนกรีน (ICG) จะสังเกตเห็นการอุดตันของหลอดเลือดคอรอยด์ ด้วย
OCT ใช้สำหรับการประเมินปริมาณของจอประสาทตา บวมน้ำ (ME) ตามการจำแนกของ Horgan (ระดับ 1–5) และสามารถตรวจพบด้วย OCT ได้หลังจาก 4 เดือนของการรักษาด้วยการฝังแร่ plaque 1) OCTA มีประโยชน์สำหรับการตรวจพบตั้งแต่ระยะแรกโดยการสร้างภาพแบบไม่รุกล้ำของการสูญเสียเส้นเลือดฝอย บริเวณที่ไม่มีการไหลเวียนเลือด และการเปลี่ยนแปลงของบริเวณไร้หลอดเลือดที่โฟเวีย (FA Z) 1)
RR มักเกิดขึ้นหลังการฉายรังสี 6 เดือนขึ้นไป โดยเฉพาะอย่างยิ่งหลังจาก 2-3 ปี ค่ามัธยฐานของการเกิดคือ 39 เดือนหลังการฉายรังสี และจำเป็นต้องสังเกตอย่างระมัดระวังเป็นพิเศษสำหรับการฉายรังสี >50 Gy 3) หลังการฉายรังสี แนะนำให้ตรวจอวัยวะและ OCT เป็นประจำ (อย่างน้อยทุก 6-12 เดือน)
ในการวินิจฉัย การซักประวัติการรักษาด้วยรังสี (เนื้องอกในลูกตา เนื้องอกในเบ้าตา เนื้องอกในกะโหลกศีรษะ เนื้องอกในโพรงอากาศข้างจมูก) มีความสำคัญ
เนื่องจากผลการตรวจอวัยวะคล้ายกับจอประสาทตาเสื่อมจากเบาหวาน จึงจำเป็นต้องวินิจฉัยแยกโรค การตรวจสอบประวัติการฉายรังสีทำให้การแยกโรคโดยทั่วไปทำได้ง่าย
จอประสาทตาเสื่อมจากเบาหวาน จอประสาทตาเสื่อมจากเบาหวาน หลอดเลือดดำจอประสาทตาอุดตัน
Q
อะไรคือความแตกต่างจากจอประสาทตาเสื่อมจากเบาหวาน?
A
ผลการตรวจอวัยวะภายในลูกตา (หลอดเลือดฝอยโป่งพอง เลือดออก จุดขาว หลอดเลือดใหม่) มีความคล้ายคลึงกันมากในทั้งสองภาวะ จุดที่แตกต่างที่สำคัญที่สุดคือประวัติการได้รับรังสี นอกจากนี้ จอประสาทตาเสื่อมจากรังสีเมื่อเกิดขึ้นแล้วจะดำเนินโรคเร็วกว่าจอประสาทตาเสื่อมจากเบาหวาน โดยมีระยะเวลาที่เป็นลักษณะเฉพาะคือครึ่งปีถึงหลายปีหลังการฉายรังสี ในกรณีที่มีโรคร่วมทั้งสอง การจัดการจะยากเป็นพิเศษ
ยาต้าน VEGF เป็นทางเลือกแรกในการรักษา RR ในปัจจุบัน ยาที่ใช้ ได้แก่ เบวาซิซูแมบ (IVB), รานิบิซูแมบ และอะฟลิเบอร์เซปต์ 1) มีรายงานการใช้รานิบิซูแมบ ขนาดสูง 2 มก. ด้วย 1)
การให้ยาต้าน VEGF เพื่อป้องกัน มีวัตถุประสงค์เพื่อยับยั้งการเกิด RR หลังการฉายรังสี การวิเคราะห์อภิมานจาก 4 การศึกษาในผู้ป่วย 2109 รายแสดงผลดังนี้ 2)
ลดอาการบวมน้ำที่จอตา (ME) 50% (OR 0.50)
ลดโรคเส้นประสาทตาจากรังสี (RON) 38% (OR 0.62)
ลดการมองเห็น ไม่ดี (สายตา <20/200) 50% (OR 0.50)
โปรโตคอลที่แนะนำคือ IVB 1.25–1.5 มก. ทุก 4 เดือนเป็นเวลา 24 เดือน2) การให้ anti-VEGF แบบป้องกันเป็นเวลา 48 เดือนแสดงให้เห็นการปรับปรุงอย่างมีนัยสำคัญของค่าสายตาที่ดีที่สุดที่แก้ไขแล้ว (0.54 logMAR ในกลุ่มป้องกัน เทียบกับ 2.00 logMAR ในกลุ่มควบคุม)5) .
ในการทบทวนของ Sahoo และคณะ (2021) การทดลองแบบสุ่มของ Schefler และ Murray ยืนยันประสิทธิภาพของการรักษาด้วย anti-VEGF โดยแนะนำให้แทรกแซงตั้งแต่เนิ่นๆ สำหรับอาการบวมน้ำที่จอตา (ภายใน 90 วันหลังการฉายรังสี)1) .
การวิเคราะห์อภิมานโดย Victor และคณะ (2023) จาก 4 การศึกษาในผู้ป่วย 2109 รายยืนยันว่า IVB แบบป้องกันช่วยลด ME 50% และ RON 38% อย่างมีนัยสำคัญหลังการรักษาด้วยแผ่นกัมมันตรังสี2) .
การจี้ด้วยเลเซอร์ทำในบริเวณจอประสาทตา ที่ไม่มีหลอดเลือดเพื่อป้องกันการเกิดเส้นเลือดใหม่ที่จอประสาทตา และต้อหินจากเส้นเลือดใหม่ การจี้จอประสาทตา ทั่วทั้งแผ่น (PRP ) ทำใน RR ชนิด proliferative โดยมีรายงานอัตราการยุบตัว 66% 5) ในกรณีหลังการรักษาด้วยแผ่นรังสี พบการยุบตัว 64.4% 5) เลเซอร์แบบโฟกัสใช้เป็น adjunctive สำหรับจอประสาทตา บวมน้ำ
Triamcinolone (TA), การปลูกถ่าย dexamethasone เข้าแก้วตา (DEX) และ fluocinolone acetonide (FA ) ใช้เป็น adjunctive therapy เมื่อการรักษาด้วย anti-VEGF ดื้อ 5)
การตัดแก้วตา (vitrectomy) ทำในกรณีเลือดออกในแก้วตา การตัดแก้วตายังมีข้อบ่งชี้ในจอประสาทตาลอก ชนิด tractional NVG อาจต้องผ่าตัดกรองหรือ cyclophotocoagulation ข้อมูล COMS รายงานว่า 43% ของกรณีมีสายตาที่แก้ไขแล้ว 20/200 หรือแย่ลงหลังการฉายรังสี 3 ปี 2)
วินิจฉัยจอประสาทตา อักเสบจากรังสีโดยอาศัยประวัติการฉายรังสีและผลตรวจอวัยวะภายในตา
ประเมินขอบเขตและระดับของบริเวณจอประสาทตา ที่ไม่มีหลอดเลือดด้วย FA
หากพบบริเวณจอประสาทตา ที่ไม่มีหลอดเลือด → การจี้ด้วยเลเซอร์ (ป้องกันการสร้างเส้นเลือดใหม่และ NVG )
หากเกิดเลือดออกในน้ำวุ้นตา → สังเกตอาการแบบประคับประคองหรือผ่าตัดน้ำวุ้นตา
หากพบจอประสาทตา บวมน้ำ → ยาต้าน VEGF (ทางเลือกแรก) และสเตียรอยด์ (เสริม)
ทั้งนี้ ไม่มีวิธีที่มีประสิทธิภาพในการหยุดการดำเนินโรค และการพยากรณ์โรคมักไม่ดี
การรักษาด้วย anti-VEGF จำเป็นต้องฉีดเข้าแก้วตาเป็นประจำในระยะยาว ในกรณีเรื้อรังที่ดื้อต่อการรักษา มีรายงานผู้ป่วยที่ต้องฉีดมากกว่า 72 ครั้ง6)
เพื่อป้องกันการลุกลามไปเป็น RR ชนิด proliferative ควรพิจารณาเลเซอร์ป้องกันในบริเวณจอประสาทตา ที่ไม่มีเลือดไปเลี้ยง
ระยะเวลาและจำนวนครั้งของการให้ anti-VEGF ป้องกันระหว่างการฉายรังสีอาจแตกต่างกันไปในแต่ละสถานพยาบาล
Q
การฉีด anti-VEGF ต้องทำต่อเนื่องนานเท่าใด?
A
สำหรับการให้ยาเพื่อป้องกัน แนะนำให้ใช้สูตรการรักษา 24 เดือน โดยให้ทุก 4 เดือน 2) สำหรับการให้ยาเพื่อรักษา ระยะเวลาจะแตกต่างกันไปตามกิจกรรมของโรค ในกรณีเรื้อรังที่ดื้อต่อการรักษา อาจต้องฉีดมากกว่า 72 ครั้ง 6) .
กลไกหลักของการทำลายจอประสาทตา จากรังสีคือ การสูญเสียเซลล์บุผนังหลอดเลือดจอประสาทตา แบบเลือกสรร เซลล์บุผนังหลอดเลือดจอประสาทตา ที่มีความสามารถในการแบ่งตัวสูงจะเสียหายได้ง่ายที่สุด และบุผนังหลอดเลือดคอรอยด์ ก็ได้รับผลกระทบเช่นกัน เซลล์บุผนังหลอดเลือดมีความไวต่อรังสีเป็นพิเศษ ทำให้เกิดความเสียหายต่อดีเอ็นเอและอะพอพโทซิส ส่งผลให้ผนังเส้นเลือดฝอยพังทลาย
การดำเนินของโรคเป็นไปตามขั้นตอนต่อไปนี้:
ระยะเซลล์บุผนังหลอดเลือดเสียหาย : เกิดขึ้นทันทีหลังการได้รับรังสี เกิดการแตกของสายดีเอ็นเอคู่และอะพอพโทซิส ของเซลล์บุผนังหลอดเลือด ทำให้สูญเสียความสมบูรณ์ของผนังหลอดเลือดระยะเส้นเลือดฝอยอุดตันและขาดเลือด : การสูญเสียเซลล์บุผนังหลอดเลือดทำให้เส้นเลือดฝอยอุดตันและบริเวณจอประสาทตา ขาดเลือดขยายตัว ในการตรวจฟลูออเรสซีน แองจิโอกราฟี จะมีการซึมผ่านเพิ่มขึ้นในระยะแรก จากนั้นการอุดตันจะเด่นชัดขึ้นเมื่อดำเนินโรค หลอดเลือดแดงเล็กก็อุดตันเช่นกัน ทำให้บริเวณจอประสาทตา ไร้หลอดเลือดขยายกว้างระยะการสร้าง VEGF และการสร้างเส้นเลือดใหม่ : VEGF ถูกผลิตมากเกินไปในจอประสาทตา ขาดเลือด ทำให้เกิดการเพิ่มจำนวนของเส้นเลือดใหม่ที่เปราะบางระยะสุดท้าย (การเปลี่ยนแปลงแบบเพิ่มจำนวน) : ดำเนินไปสู่เลือดออกในวุ้นตา จอประสาทตาลอก แบบดึงรั้ง และ NVG
การสะสมของผลิตภัณฑ์ปลายทางของไกลเคชัน (AGE) การสูญเสียเพอริไซต์ และการหนาตัวของเยื่อฐานยังมีส่วนทำให้เกิดความเสียหายต่อเซลล์บุผนังหลอดเลือด กลไกนี้คล้ายคลึงกับจอประสาทตาเสื่อมจากเบาหวาน ซึ่งอธิบายสาเหตุหนึ่งที่ทำให้ความเสี่ยงของ RR เพิ่มขึ้นในผู้ป่วยเบาหวาน
มีระยะแฝงตั้งแต่หกเดือนถึงสองถึงสามปีหลังการฉายรังสีจนถึงการเริ่มมีอาการทางคลินิก ซึ่งสะท้อนถึงเวลาที่จำเป็นสำหรับการสะสมความเสียหายของเซลล์บุผนังหลอดเลือดและการปรากฏทางคลินิกของการอุดตันของเส้นเลือดฝอย
การวิเคราะห์อภิมานโดย Victor และคณะ (2023) เป็นหลักฐานที่ใหญ่ที่สุดในปัจจุบันเกี่ยวกับประสิทธิผลของการให้ anti-VEGF เชิงป้องกัน แต่การศึกษาส่วนใหญ่ที่รวมอยู่เป็นการศึกษาเชิงสังเกต จึงจำเป็นต้องมีการตรวจสอบเพิ่มเติมผ่านการทดลองแบบสุ่มและมีกลุ่มควบคุม (RCT)2) การกำหนดมาตรฐานของช่วงเวลา ยา และระยะเวลาการให้ที่เหมาะสมก็เป็นความท้าทายในอนาคต
OCTA สามารถประเมินการสูญเสียเส้นเลือดฝอย การขยายตัวของ FA Z และความหนาแน่นของเส้นเลือดฝอยที่ลดลงในเชิงปริมาณโดยไม่ต้องใช้สารทึบรังสี สามารถตรวจพบบริเวณที่ไม่มีการไหลเวียนเลือด ได้ตั้งแต่ระยะแรกหลังการฉายรังสี และการประยุกต์ใช้ในการคัดกรองและติดตาม RR กำลังก้าวหน้า1) .
Kayabai และคณะ (2025) รายงานกรณีผู้ป่วยชายอายุ 53 ปี หลังการฉายรังสีรักษาเนื้องอกในลูกตาเป็นเวลา 19 ปี 6) สัญญาณวงแหวนหัวหอม (การสะสมของผลึกคอเลสเตอรอลหลายชั้นภายในโพรงถุงน้ำ) ที่พบใน OCT ถือเป็นเครื่องหมายภาพของจอประสาทตา อักเสบจากรังสีเรื้อรังและดื้อต่อการรักษา และมีการบันทึกประวัติระยะยาวที่ต้องฉีดยาเข้าแก้วตา 72 ครั้งขึ้นไป
ยาต้าน VEGF รุ่นต่อไป เช่น brolucizumab และ faricimab (เป้าหมายคู่ angiopoietin/VEGF) กำลังถูกพิจารณานำมาใช้กับ RR5) คาดว่าจะเป็นทางเลือกในกรณีที่ดื้อต่อยาที่มีอยู่เดิม
นอกเหนือจากรังสีเอกซ์และรังสีแกมมาแบบดั้งเดิมแล้ว การประเมินความเสี่ยงของการเกิดจอประสาทตา อักเสบจากรังสีหลังการรักษาด้วยโปรตอนและลำอนุภาคหนัก (คาร์บอนไอออน) กำลังดำเนินการอยู่ แม้แต่การรักษาด้วยอนุภาคที่มีการกระจายปริมาณรังสีสูง จอประสาทตา อาจเกิดโรคได้หากจอประสาทตา อยู่ในขอบเขตการฉายรังสี ดังนั้นการประเมินปริมาณรังสีที่จอประสาทตา ในระหว่างการวางแผนการรักษาและการติดตามผลหลังการผ่าตัดจึงเป็นความท้าทาย
จอประสาทตา จากรังสี (RR) และโรคเส้นประสาทตาจากรังสี (RON) อาจเกิดขึ้นพร้อมกันจากบริเวณที่ได้รับรังสีเดียวกัน อุบัติการณ์ของ RON หลังการฉายรังสีภายนอก (EB RT) รายงานว่าประมาณ 2% 3) ในกรณีที่มี RR และ RON ร่วมกัน ความบกพร่องทางการมองเห็น จะรุนแรงมากขึ้น ดังนั้นการตรวจอวัยวะภายในตาอย่างสม่ำเสมอร่วมกับการตรวจลานสายตา และการประเมินเส้นประสาทตา ด้วย OCT จึงเป็นหัวข้อวิจัยที่สำคัญ
Sahoo NK , Lim JW, Laude A, et al. Radiation retinopathy—the complex interplay of radiation, vasculature, and clinical outcomes. Clin Ophthalmol. 2021;15:3797-3809.
Victor AA, Mauldin WM, Houston SK, et al. Prophylactic intravitreal bevacizumab and radiation retinopathy after plaque brachytherapy for uveal melanoma: a meta-analysis. Clin Ophthalmol. 2023;17:2997-3009.
Kinaci-Tas B, Wilschut JA, Kilic E, et al. The incidence of radiation-induced optic neuropathy and retinopathy in patients treated with external beam radiation therapy: a systematic review and meta-analysis. Cancers. 2023;15:1999.
Chakraborty K, Jain S, Tripathy K, et al. Delayed onset radiation retinopathy following skull base tumor treatment. Indian J Ophthalmol. 2023;71:303-305.
Mularska W, Nowak-Gospodarowicz I, Golik B, et al. Radiation retinopathy after plaque brachytherapy for uveal melanoma—pathogenesis, diagnosis, and management. J Contemp Brachytherapy. 2023;15:372-382.
Kayabai M, Ilhan S, Celik E, et al. Onion ring sign as a biomarker of chronic treatment-resistant radiation retinopathy. Cureus. 2025;17(11):e97758.
Chan L, Eftekari SC, Nguyen QT, et al. Radiation retinopathy after whole-brain radiotherapy: a case report and literature review. Adv Radiat Oncol. 2021;6:100706.