비증식성 RR

방사선 망막병증 (Radiation Retinopathy)
한눈에 보는 포인트
섹션 제목: “한눈에 보는 포인트”1. 방사선 망막병증이란?
섹션 제목: “1. 방사선 망막병증이란?”방사선 망막병증(Radiation Retinopathy; RR)은 안내 종양, 안와 또는 부비동 종양, 두개내 질환 등에 대한 방사선 치료 시 망막이 조사야에 포함될 경우 발생하는 만성 진행성 폐쇄성 망막 미세혈관 장애입니다. 맥락막 악성 흑색종 등의 안내 종양, 안와 종양, 두경부 종양, 뇌종양에 대한 방사선 치료 후에 발생합니다. 1933년 Stallard가 처음 보고했습니다.
참고로 사고로 인한 대량 피폭은 수주 내에 망막과 시신경의 괴사를 초래할 수 있습니다.
증식 능력이 높은 망막 혈관 내피 세포가 방사선에 선택적 감수성을 나타내므로 모세혈관 폐쇄, 허혈, 신생혈관 형성에 이르는 일련의 병태를 형성합니다1). 맥락막 혈관 내피도 손상됩니다. 발병은 조사 후 6개월 이후에 많으며, 특히 2~3년 후에 많습니다. 전체 발병률은 조사야에 따라 다릅니다.
아래에 부위별 발병률을 나타냅니다.
| 조사 부위 | 발병률 |
|---|---|
| 안와 | 85.7% |
| 부비동 | 45.4% |
| 비인두 | 36.4% |
| 뇌 | 3.1% |
뇌두경부 종양에 대한 방사선 치료 후 RR 유병률은 약 6%, 시신경병증(ON)은 약 2%라는 메타분석이 있습니다 3). 지연 발병 사례를 포함한 전체 발병률은 약 17%로 보고되었습니다 4).
발병률은 조사 부위, 선량, 분할법, 동반 질환에 따라 크게 다릅니다. 전체 발병률은 17%로 보고되어 있으며, 모든 환자에게 발생하는 것은 아닙니다 4). 정기적인 안저 검사를 통한 조기 발견이 중요합니다.
2. 주요 증상 및 임상 소견
섹션 제목: “2. 주요 증상 및 임상 소견”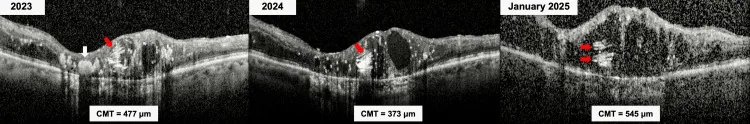
자각 증상
섹션 제목: “자각 증상”초기에는 무증상인 경우가 많으며, 검진에서 우연히 발견되기도 합니다. 병변이 황반부나 시신경에 미치면 다음과 같은 증상이 나타납니다.
- 시력 저하: 황반부종이나 황반허혈이 원인입니다. 서서히 진행되는 경우가 많습니다.
- 변시증(왜곡): 황반부종으로 인한 시세포 배열의 혼란에서 발생합니다.
- 비문증 및 시야 흐림: 유리체 출혈이 발생할 때 나타납니다.
- 시야 결손: 광범위한 망막 허혈 또는 시신경병증이 동반될 때 관찰됩니다.
임상 소견
섹션 제목: “임상 소견”안저 소견은 당뇨망막병증과 유사하며, 미세동맥류, 망막출혈, 경성백반으로 시작하여 점차 솜털모양 반점이 나타납니다. 진행되면 망막신생혈관이 발생하여 유리체출혈을 초래합니다. 황반부종과 중심와 주변 모세혈관 폐쇄로 시력이 저하됩니다. 일단 발병하면 당뇨망막병증보다 진행이 빠릅니다.
임상 경과는 다음과 같은 단계를 따릅니다.
- 초기: 미세동맥류, 망막출혈, 경성백반이 나타납니다.
- 진행기: 솜털모양 백반이 나타난다. 허혈 범위 확대를 나타낸다.
- 중증기: 망막 신생혈관이 발생하여 유리체 출혈을 일으킨다.
- 합병증기: 황반 부종 및 중심와 주변 모세혈관 폐쇄가 진행되어 시력이 현저히 저하된다.
방사선 망막병증은 비증식성과 증식성으로 크게 나뉜다.
증식성 RR
지연성 특수 소견으로, 17년 후 발병한 증례에서 낭종 내 콜레스테롤 결정으로 인한 **양파 고리 징후(onion ring sign)**가 OCT에서 확인되었으며, 만성기의 치료 저항성 지표로 주목받고 있음 6).
또한, 30Gy 전뇌 조사 후 16개월에 상부 망막에 국한된 RR이 발생한 증례에서는 병변 분포가 조사야의 30Gy 등선량 곡선과 일치하여, 저선량 영역에서도 조사야에 대응한 발병 패턴을 보이는 것이 확인됨 7).
조사 후 6개월 이후, 특히 2~3년 후에 발병이 많습니다. 진단 시 중앙값은 조사 후 39개월로 보고되었지만3), 17년 후 지연 발병 사례도 존재합니다4). 조사 후에는 장기적인 정기 안저 검사가 필요합니다.
3. 원인 및 위험 요인
섹션 제목: “3. 원인 및 위험 요인”방사선량
섹션 제목: “방사선량”선량 역치는 일반적으로 35 Gy로 간주됩니다4). 45 Gy 초과 조사 시 발병하기 쉽고, 50 Gy 초과 시 발병 위험이 특히 높아집니다3). 한편, 20 Gy에서 발생한 보고도 있으며, 30 Gy의 전뇌 조사 후에도 발병이 보고되어7), 역치 이하의 선량에서도 주의가 필요합니다. 증식 능력이 높은 망막 혈관 내피 세포가 가장 손상되기 쉽고, 맥락막 혈관 내피도 손상됩니다.
조사 후 잠복기는 6개월 이후, 특히 2~3년 후에 많습니다. 이는 방사선에 의한 내피 세포 손상이 축적되어 임상적 역치를 초과하는 데 시간이 필요하기 때문으로 생각됩니다.
아래에 위험 요인을 제시합니다.
| 위험 인자 | 내용 |
|---|---|
| 총 선량 | >35 Gy (역치) 4), 45 Gy 초과 시 고위험 |
| 분할 선량 | 고분할 조사 |
| 조사 부위 | 안와 또는 시교차 근처3) |
| 당뇨병 | 미세혈관 취약성 악화 |
| 병용 화학요법 | 감수성 증가 |
시교차에 가까운 조사는 RR 발생과 유의한 상관관계(p=0.009)가 보고되었습니다3).
증식성 RR의 위험 인자
섹션 제목: “증식성 RR의 위험 인자”증식성 RR은 전체 RR의 3~25%에서 발생하는 것으로 알려져 있습니다5). 플라크 근접방사선치료 후 증례에서는 조사 후 32개월에 증식성 RR로 진행하는 예가 관찰됩니다.
당뇨병은 방사선 망막병증의 중요한 위험 인자입니다. 당뇨병으로 인한 미세혈관 취약성이 방사선에 의한 내피 손상과 상승 작용을 하여 더 낮은 선량에서도 발병할 수 있습니다. 혈당 조절을 유지함과 동시에 방사선 치료 후에는 더 빈번한 안저 검사가 권장됩니다.
4. 진단 및 검사 방법
섹션 제목: “4. 진단 및 검사 방법”형광 안저 조영술(FA) 및 병기 분류
섹션 제목: “형광 안저 조영술(FA) 및 병기 분류”FA는 RR의 진단 및 병기 분류의 기본 검사입니다. 초기에는 망막 모세혈관의 투과성 항진이 관찰되며, 진행되면 모세혈관이 폐쇄됩니다. 세동맥도 폐쇄되어 망막 무혈관 영역이 광범위하게 확장되고 망막 신생혈관이 발생합니다. Amoaku FA 분류(Grade 1~4)가 널리 사용됩니다1).
| 등급 | 주요 소견 |
|---|---|
| 1 | 미세동맥류 및 국소 모세혈관 확장 |
| 2 | 모세혈관 폐쇄 및 광범위 혈관 이상 |
| 3 | 시신경 유두 또는 망막 신생혈관 |
| 4 | 유리체 출혈 / 견인성 망막박리 |
인도시아닌 그린(ICG) 형광조영술에서는 맥락막 혈관의 폐쇄도 관찰됩니다.
OCT·OCTA
섹션 제목: “OCT·OCTA”OCT는 Horgan 분류(1~5등급)에 따른 ME의 정량적 평가에 사용되며, 플라크 근접방사선치료 후 4개월 시점에 OCT 검출이 가능합니다1). OCTA는 비침습적으로 모세혈관 소실, 무관류 영역, FAZ의 변화를 가시화할 수 있어 조기 발견에 유용합니다1).
발병 시기와 모니터링 계획
섹션 제목: “발병 시기와 모니터링 계획”RR은 조사 후 6개월 이후에 많이 발생하며, 특히 23년 후에 많습니다. 발병 중앙값은 조사 후 39개월이며, >50Gy 조사 시 특히 주의 깊은 관찰이 필요합니다3). 조사 후 정기적(적어도 612개월마다) 안저 검사 및 OCT 촬영이 권장됩니다.
진단을 위해서는 방사선 치료 병력(안내 종양, 안와 종양, 두개내 종양, 부비동 종양) 청취가 중요합니다.
감별 진단
섹션 제목: “감별 진단”안저 소견이 당뇨망막병증과 유사하므로 감별이 필요합니다. 방사선 조사 병력 유무를 확인하면 감별이 대체로 용이합니다.
- 당뇨망막병증: 안저 소견(모세혈관류, 출혈, 백반, 신생혈관)이 방사선 망막병증과 매우 유사합니다. 당뇨 유무와 방사선 조사 병력 확인이 감별의 핵심입니다. 방사선 망막병증은 일단 발병하면 당뇨망막병증보다 진행이 빠른 것이 특징입니다.
- 망막정맥폐쇄증: 폐쇄된 정맥을 따라 출혈과 부종이 주로 나타나며, 방사선 망막병증에서는 보이지 않는 부채꼴 분포를 보입니다. 방사선 조사 병력이 없으면 감별이 용이합니다.
5. 표준 치료법
섹션 제목: “5. 표준 치료법”항VEGF 요법(1차 선택)
섹션 제목: “항VEGF 요법(1차 선택)”항VEGF 약물은 현재 RR 치료의 1차 선택입니다. 사용되는 약제는 베바시주맙(IVB), 라니비주맙, 애플리버셉트입니다1). 고용량 라니비주맙 2mg 사용도 보고되었습니다1).
예방적 항VEGF 투여는 방사선 치료 후 RR 발생 억제를 목적으로 시행됩니다. 4개 연구, 2109명의 환자를 대상으로 한 메타분석에서 다음과 같은 결과가 나타났습니다2).
- 황반부종(ME) 50% 감소(OR 0.50)
- 방사선시신경병증(RON) 38% 감소(OR 0.62)
- 불량 시력(시력 <20/200 상당) 50% 감소(OR 0.50)
권장 프로토콜은 IVB 1.25~1.5mg을 4개월마다 24개월간 투여하는 것입니다2). 48개월간의 예방적 항VEGF 투여는 최대교정시력이 0.54 logMAR(예방군) 대 2.00 logMAR(대조군)으로 유의한 개선을 보였습니다5).
Sahoo 등(2021)의 리뷰에서 Schefler와 Murray의 RCT는 항VEGF 요법의 유효성을 검증했으며, 황반부종에 대한 조기 중재(조사 후 90일 이내)를 권장합니다1).
Victor 등(2023)의 4개 연구 2109명 환자 메타분석에서는 예방적 IVB 투여가 플라크 소선원 치료 후 ME를 50%, RON을 38% 각각 유의하게 감소시키는 것을 확인했습니다2).
레이저 광응고
섹션 제목: “레이저 광응고”망막 무혈관 영역에 레이저 광응고를 시행하여 망막 신생혈관 및 신생혈관 녹내장의 발생을 예방합니다. 범망막 광응고(PRP)는 증식성 RR에 대해 시행되며, 66%의 퇴축률이 보고되었습니다 5). 플라크 치료 후 사례에서도 64.4%에서 퇴축이 확인되었습니다 5). 포컬 레이저는 ME에 보조적으로 사용됩니다.
스테로이드 국소 투여
섹션 제목: “스테로이드 국소 투여”트리암시놀론(TA), 덱사메타손 유리체강내 임플란트(DEX), 플루오시놀론 아세토나이드(FA)는 항VEGF 요법에 저항하는 경우 보조 요법으로 사용됩니다 5).
증식성 RR의 대응
섹션 제목: “증식성 RR의 대응”유리체 출혈에는 유리체 절제술을 시행합니다. 견인 망막 박리에도 유리체 절제술이 적응됩니다. NVG에는 여과 수술 또는 사이클로포토응고술이 필요한 경우가 있습니다. COMS 데이터에 따르면 조사 후 3년에 43%가 교정 시력 20/200 이하가 된다고 보고되었습니다 2).
치료 흐름
섹션 제목: “치료 흐름”- 방사선 조사 병력과 안저 소견을 바탕으로 방사선 망막병증 진단을 확립합니다
- FA를 통해 망막 무혈관 영역의 범위와 정도를 평가합니다
- 망막 무혈관 영역이 확인되는 경우 → 레이저 광응고술 (신생혈관 및 NVG 예방)
- 유리체 출혈이 발생한 경우 → 보존적 경과 관찰 또는 유리체 절제술
- 황반 부종이 확인되는 경우 → 항VEGF 약물 (1차 선택) 및 스테로이드 (보조)
진행을 막는 효과적인 방법은 없으며, 예후가 좋지 않은 경우가 많습니다.
예방적 투여에서는 4개월마다 24개월간의 프로토콜이 권장됩니다2). 치료적 투여에서는 병태의 활동성에 따라 지속 기간이 달라집니다. 치료 저항성 만성 사례에서는 72회 이상의 주사가 필요할 수도 있습니다6).
6. 병태생리학 및 상세한 발병 기전
섹션 제목: “6. 병태생리학 및 상세한 발병 기전”방사선에 의한 망막 손상의 중심 기전은 망막 혈관 내피 세포의 선택적 소실입니다. 증식 능력이 높은 망막 혈관 내피 세포가 가장 손상되기 쉽고, 맥락막 혈관 내피도 손상됩니다. 내피 세포는 방사선에 특히 민감하며, DNA 손상과 세포자멸사로 인해 모세혈관벽이 붕괴됩니다.
병태의 진행은 다음 단계를 따릅니다.
- 내피 세포 손상기: 조사 직후부터 진행됩니다. 내피 세포의 DNA 이중 가닥 절단과 세포자멸사가 발생하여 혈관벽의 완전성이 상실됩니다.
- 모세혈관 폐쇄 및 허혈기: 내피 세포 소실로 인해 모세혈관이 폐쇄되고 망막 허혈 영역이 확대됩니다. 형광 혈관 조영술에서 초기에는 투과성 항진이 나타나지만, 진행됨에 따라 폐쇄가 우세해집니다. 세동맥도 폐쇄되어 망막 무혈관 영역이 광범위하게 확대됩니다.
- VEGF 생성 및 혈관신생기: 허혈 망막에서 VEGF가 과도하게 생성되어 취약한 신생 혈관 증식이 유도됩니다.
- 말기(증식성 변화): 유리체 출혈, 견인성 망막박리, 신생혈관녹내장으로 진행됩니다.
최종당화산물(AGE) 축적, 주세포 소실, 기저막 비후도 내피 손상에 기여하는 것으로 알려져 있습니다. 이 기전은 당뇨망막병증과 유사하며, 당뇨병 환자에서 RR 위험이 증가하는 이유 중 하나로 설명됩니다.
조사 후 임상 발현까지 6개월 이상, 특히 2~3년의 잠복기가 있습니다. 이는 내피세포 손상이 축적되고 모세혈관 폐쇄가 임상적으로 나타나기까지의 시간을 반영합니다.
7. 최신 연구 및 향후 전망(연구 단계 보고)
섹션 제목: “7. 최신 연구 및 향후 전망(연구 단계 보고)”예방적 항-VEGF의 근거 강화
섹션 제목: “예방적 항-VEGF의 근거 강화”Victor 등(2023)의 메타분석은 예방적 항-VEGF 투여의 유효성을 보여주는 현재 최대 규모의 근거이지만, 대상 연구의 대부분이 관찰 연구이며 무작위 대조 시험(RCT)을 통한 추가 검증이 필요합니다2). 최적 투여 간격, 투여 약제, 투여 기간에 대한 표준화도 향후 과제입니다.
OCTA(광간섭단층혈관조영술)를 통한 조기 발견
섹션 제목: “OCTA(광간섭단층혈관조영술)를 통한 조기 발견”OCTA는 조영제를 사용하지 않고 모세혈관 소실, FAZ 확대, 모세혈관 밀도 감소를 정량적으로 평가할 수 있습니다. 방사선 치료 후 초기 단계부터 무관류 영역을 검출할 수 있으며, RR의 선별 및 모니터링에 응용이 진행되고 있습니다1).
치료 저항성 방사선 망막병증의 만성화 표지자
섹션 제목: “치료 저항성 방사선 망막병증의 만성화 표지자”Kayabai 등(2025)은 안내 종양 방사선 치료 후 19년이 지난 53세 남성의 증례를 보고했습니다6). OCT에서 관찰된 양파 고리 징후(낭포 내 콜레스테롤 결정의 다층 침착)는 만성적이고 치료 저항성인 방사선 망막병증의 영상 표지자로 주목받고 있으며, 환자는 72회 이상의 유리체내 주사를 필요로 하는 장기 경과가 기록되었습니다.
차세대 약물
섹션 제목: “차세대 약물”brolucizumab 및 faricimab(안지오포이에틴/VEGF 이중 표적)과 같은 차세대 항VEGF 약물이 방사선 망막병증에 적용되는 것이 검토되고 있습니다5). 기존 약물에 대한 치료 저항성 사례에서 대체 옵션으로 기대됩니다.
양성자선 및 중입자선 치료 후 위험 평가
섹션 제목: “양성자선 및 중입자선 치료 후 위험 평가”기존의 X선 및 감마선에 더하여 양성자선 및 중입자선(탄소 이온선) 치료 후 방사선 망막병증 발병 위험 평가가 진행되고 있습니다. 선량 집중도가 높은 입자선 치료에서도 망막이 조사야에 포함되면 발병할 수 있으므로, 치료 계획 시 망막 선량 평가와 수술 후 모니터링이 과제입니다.
방사선 시신경병증(RON)과의 병합 관리
섹션 제목: “방사선 시신경병증(RON)과의 병합 관리”RR과 방사선 시신경병증(RON)은 동일한 조사야에서 동시에 발생할 수 있습니다. EBRT 후 RON 발생률은 약 2%로 보고되었으며 3), RR과 RON이 병합된 경우 시기능 장애가 더 심각해지므로 안저 검사에 더해 시야 검사 및 OCT를 통한 시신경 평가를 정기적으로 시행하는 것이 중요한 연구 과제입니다.
8. 참고문헌
섹션 제목: “8. 참고문헌”- Sahoo NK, Lim JW, Laude A, et al. Radiation retinopathy—the complex interplay of radiation, vasculature, and clinical outcomes. Clin Ophthalmol. 2021;15:3797-3809.
- Victor AA, Mauldin WM, Houston SK, et al. Prophylactic intravitreal bevacizumab and radiation retinopathy after plaque brachytherapy for uveal melanoma: a meta-analysis. Clin Ophthalmol. 2023;17:2997-3009.
- Kinaci-Tas B, Wilschut JA, Kilic E, et al. The incidence of radiation-induced optic neuropathy and retinopathy in patients treated with external beam radiation therapy: a systematic review and meta-analysis. Cancers. 2023;15:1999.
- Chakraborty K, Jain S, Tripathy K, et al. Delayed onset radiation retinopathy following skull base tumor treatment. Indian J Ophthalmol. 2023;71:303-305.
- Mularska W, Nowak-Gospodarowicz I, Golik B, et al. Radiation retinopathy after plaque brachytherapy for uveal melanoma—pathogenesis, diagnosis, and management. J Contemp Brachytherapy. 2023;15:372-382.
- Kayabai M, Ilhan S, Celik E, et al. Onion ring sign as a biomarker of chronic treatment-resistant radiation retinopathy. Cureus. 2025;17(11):e97758.
- Chan L, Eftekari SC, Nguyen QT, et al. Radiation retinopathy after whole-brain radiotherapy: a case report and literature review. Adv Radiat Oncol. 2021;6:100706.
