다발성 경화증/시신경염

신경안과에서의 OCT 혈관조영술
한눈에 보는 포인트
섹션 제목: “한눈에 보는 포인트”1. 신경안과에서의 OCT 혈관조영술
섹션 제목: “1. 신경안과에서의 OCT 혈관조영술”OCT 혈관조영술(OCTA)은 OCT(광간섭단층촬영)의 원리를 응용하여 혈관을 가시화하는 비침습적 영상 진단 기술입니다. OCT는 1990년대에 발명되었으며, 저간섭 간섭법에 기반한 고해상도 단층 영상을 생성합니다. 안과에서 가장 중요한 영상 진단법 중 하나가 되었습니다.
기존 OCT는 모세혈관과 망막 조직 간의 대비가 낮아 혈관 변화 모니터링에 한계가 있었습니다. 형광안저혈관조영(FA)과 인도시아닌그린혈관조영(ICGA)은 조영제 정맥 주사가 필요하며 아나필락시스 쇼크의 위험이 있습니다. 또한 2차원 영상만 제공하여 병변의 깊이 정보를 얻을 수 없습니다.
OCTA는 이러한 한계를 극복하고 조영제 없이 다양한 깊이의 혈관을 3차원으로 가시화합니다. 망막 순환 이상을 일으키는 질환(당뇨망막병증, 망막정맥폐쇄 등), 시신경 순환 이상을 일으키는 질환(녹내장, 허혈시신경병증 등), 맥락막 신생혈관을 발생시키는 질환에 유용합니다.
신경안과 영역에서는 특히 시신경 유두 주변의 방사상 유두주위 모세혈관(RPC) 평가가 중요합니다. 혈관 밀도 감소는 안저 검사에서 망막신경섬유층결손(NFLD)이 관찰되는 부위와 일치하여 나타납니다.
2. OCTA 소견과 신경안과에서의 임상적 적응
섹션 제목: “2. OCTA 소견과 신경안과에서의 임상적 적응”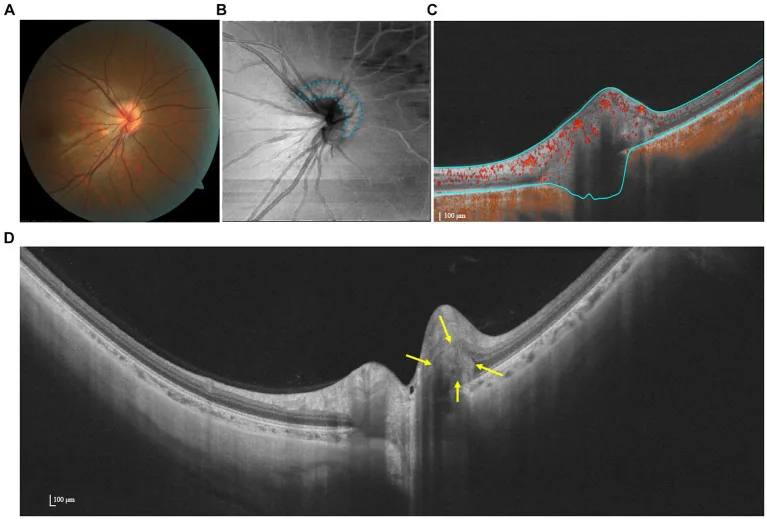
OCTA에서 관찰되는 주요 소견
섹션 제목: “OCTA에서 관찰되는 주요 소견”신경안과 질환에서 OCTA로 관찰되는 주요 혈관 변화는 다음과 같습니다.
- 혈관 밀도 감소 (모세혈관 소실): 시신경 위축, 녹내장, 시신경염 후에 나타납니다. NFLD 영역에 일치하여 분포합니다.
- 혈관 확장 및 구불거림: 유두부종의 급성기 및 일부 시신경염에서 관찰됩니다.
- 혈류 공백 (신호 소실): 맥락막모세혈관판(CC) 수준에서 검출되는 혈류 소실 영역입니다. VKH병 및 다발혈관염성 육아종증과 같은 전신 염증 질환에서 맥락막 병변 평가에 유용합니다.
- 엉킨 혈관 덩어리 (실타래 모양 혈관 형성): 유두부종에서 시신경 유두 표면의 모세혈관이 확장 및 구불거리며 형성하는 특징적인 패턴입니다.
주요 적응 질환 및 특징적 OCTA 소견
섹션 제목: “주요 적응 질환 및 특징적 OCTA 소견”허혈성 시신경병증
비동맥염성 전방 허혈성 시신경병증(비동맥염성): 유두 주변 모세혈관의 혈류 장애가 급성기와 만성기 모두에서 확인됩니다. 이측 섹터가 혈류 밀도가 가장 높으며, 비동맥염성 전방 허혈성 시신경병증 눈에서 가장 손상됩니다. 만성기의 ONH 및 유두 주변 혈관 밀도는 RNFL 손상 및 시야 결손과 직접 관련됩니다.
AAION(동맥염성): 표층 유두 주변 모세혈관의 확장과 표층 및 심층 망막 모세혈관의 국소적 비관류가 특징입니다.
유전성 및 퇴행성 질환
LHON(레베르 유전성 시신경병증): 가성부종기에는 모세혈관 확장이 확인됩니다. 병기별 맥락막모세혈관판 소실 패턴이 기술되어 있으며, 초기 아급성기에는 이측에서 감소하고 만성기에는 모든 구역에서 감소합니다.
시신경 위축: 유두주위 미세혈관 감소. 대사 활동 저하에 따라 자가조절 기전을 통해 혈류가 감소합니다.
녹내장
POAG(원발개방각녹내장): 유두내, 황반, 유두주위 혈관밀도 및 혈류지수가 감소합니다.
NTG(정상안압녹내장): 유두주위 모세혈관밀도 감소가 원발개방각녹내장과 유사하게 나타나지만 경미합니다. 녹내장 의심 예에서는 시력 저하 전에도 혈류속지수의 감소를 검출할 가능성이 있습니다.
유두부종과 가성유두부종의 감별
섹션 제목: “유두부종과 가성유두부종의 감별”OCTA는 유두부종과 가성유두부종의 감별에 유용합니다.
- 유두부종: 시신경유두 표면의 모세혈관이 확장되고 구불구불해져 ‘혈관 엉킴 덩어리’를 형성합니다. 유두주위 모세혈관 밀도는 대조안과 동등하게 유지됩니다. 혈관 소실은 동반되지 않습니다.
- 가성유두부종: 유두주위 모세혈관 밀도가 감소합니다.
유두부종에서는 부종이 하부 모세혈관을 가리지만 부종 위에 모세혈관이 보이며, 유두주위 혈관 밀도는 대조안과 동등하게 유지됩니다. 반면 가성유두부종(예: 시신경유두 드루젠)에서는 혈관 밀도 감소가 관찰되므로, 이 차이가 감별의 근거가 됩니다.
급성기 소견과 황반부 평가
섹션 제목: “급성기 소견과 황반부 평가”유두부종을 동반한 시신경염이나 AION에서는 축삭 수송 장애로 인한 cpRNFL 두께 증가로 급성기 축삭 손상 검출이 어렵습니다. 신경절세포복합체(GCC) 등의 황반부 망막내층 분석은 cpRNFL 분석보다 조기에 얇아짐을 검출할 수 있습니다.
중심암점이나 맹점중심암점을 유발하는 시신경 질환에서는 유두황반다발(PMB) 손상을 반영한 얇아짐 패턴을 보입니다. OCTA에서는 PMB 얇아짐 영역에 일치하는 RPC 밀도 감소가 관찰됩니다.
3. OCTA의 원리, 기술적 특징 및 한계
섹션 제목: “3. OCTA의 원리, 기술적 특징 및 한계”OCTA는 안저의 동일한 위치를 반복적으로 촬영하여 움직이는 부분(적혈구)만을 무작위 신호 변화로 검출합니다. 흐르는 적혈구는 정지 조직보다 스캔 간에 더 큰 신호 변동을 일으키는 원리를 이용합니다.
검출 방법에는 주로 두 가지가 있습니다.
- 진폭 디코릴레이션(Decorrelation)법: 두 B-스캔 간의 진폭 차이를 검출합니다.
- 위상 분산법: 광파의 위상 변화를 검출합니다.
대표적인 알고리즘으로 **SSADA(분할 스펙트럼 진폭 디코릴레이션 혈관조영술)**가 있습니다. OCT 스펙트럼을 더 좁은 대역으로 분할하고 각 대역의 강도 디코릴레이션을 평균화하여 신호 대 잡음비(SNR)를 크게 향상시킵니다.
자동 분할 및 평가 층
섹션 제목: “자동 분할 및 평가 층”OCTA는 4개 층의 앙파스(en face) 이미지를 자동 생성합니다.
| 층 | 명칭 | 주요 평가 대상 |
|---|---|---|
| 표층 | 표층 망막 혈관망 (SCP) | 망막 신경섬유층 ~ 신경절세포층 |
| 심층 | 심층 망막 모세혈관망 (DCP) | 내과립층 주변 |
| 외망막 | 외망막층 | 정상적으로 무혈관 |
| 심부 | 맥락막모세혈관판(CC) | Bruch막 외측 10~30μm |
기종별로 분할 설정이 다릅니다. RPC와 SCP를 합쳐서 SCP로 표시하는 경우가 많습니다. 맥락막모세혈관판의 묘사는 SD-OCT보다 SS-OCT가 더 우수하다는 의견도 있습니다.
OCTA의 장점과 한계
섹션 제목: “OCTA의 장점과 한계”OCTA의 장점은 다음과 같습니다.
- 조영제 불필요: 아나필락시스 위험이 없으며 반복 시행 가능.
- 짧은 촬영 시간: 환자 부담이 적음.
- 3차원 평가: 혈관망의 층별·입체적 관찰 가능.
- 정량적 분석: 혈관 밀도, 혈류 지수 등의 정량 파라미터 출력 가능.
한편, 다음과 같은 한계와 인공물에 주의해야 한다.
- 화질 저하: 백내장이나 유리체 혼탁이 있는 눈에서는 모세혈관망이 잘 보이지 않음. 무관류 영역으로 오인하지 않도록 주의.
- 안구 및 얼굴 움직임 인공물: 촬영 중 움직임으로 인해 흰 선이나 왜곡이 발생합니다.
- 투영 인공물: 얕은 층의 신호가 깊은 층에 투영됩니다.
- 형광 누출 비검출: 형광 누출을 식별할 수 없어 조영 검사를 완전히 대체할 수 없습니다.
- 촬영 범위 제한: 3mm×3mm에서 12mm×12mm까지 선택 가능하지만, 촬영 범위와 화질은 반비례합니다.
4. 진단 및 검사 방법
섹션 제목: “4. 진단 및 검사 방법”OCTA의 구체적인 시술
섹션 제목: “OCTA의 구체적인 시술”OCTA 시행 절차와 평가 시 주요 사항은 다음과 같습니다.
- 촬영 범위 설정: 평가 목적에 맞게 조정합니다. 모세혈관 수준의 정밀 평가에는 3×3mm와 같은 좁은 화각이 바람직합니다. 광각 평가가 필요한 경우 12×12mm를 선택합니다.
- 자동 분할 확인: SCP, DCP, 외망막, CC의 4층 앤페이스 이미지를 자동 생성하지만, 기종별 설정이 다르므로 B-스캔과의 대응을 반드시 확인합니다.
- 정량적 매개변수 평가: 유두주위 혈관 밀도, RPC 밀도, ONH 혈류 지수(ONH-FI) 등을 측정합니다.
FA/ICGA와의 비교
섹션 제목: “FA/ICGA와의 비교”각 검사법의 특성을 아래에 요약합니다.
| 특성 | OCTA | FA | ICGA |
|---|---|---|---|
| 조영제 | 불필요 | 필요 | 필요 |
| 깊이 정보 | 3차원 (층별) | 2차원 | 2차원 |
| 형광 누출 | 검출 불가 | 검출 가능 | 검출 가능 |
| 정량성 | 높음 | 낮음 | 낮음 |
| 반복 시행 | 용이 | 어려움 | 어려움 |
신경안과에서의 주요 평가 파라미터
섹션 제목: “신경안과에서의 주요 평가 파라미터”신경안과에서 OCTA를 사용할 때의 대표적인 평가 지표는 다음과 같습니다.
- 유두주위 혈관 밀도: 비동맥염성 전방허혈시신경병증 및 녹내장의 중증도 및 시야결손과의 상관관계가 보고되었습니다.
- RPC 밀도(방사상 유두주위 모세혈관 밀도): 구역별로 평가 가능하며, 병변 부위와의 대응을 확인할 수 있습니다1).
- ONH 혈류 지수(ONH-FI): ONH 전체 혈류를 정량화하는 지표입니다. 다발성 경화증 및 녹내장에서 감소가 보고되었습니다.
- 맥락막모세혈관판의 flow void(신호 결손): CC의 비관류 영역을 정량화하여 포도막염 및 전신 혈관염에서 맥락막 병변 평가에 사용됩니다2).
LSFG와의 보완적 관계
섹션 제목: “LSFG와의 보완적 관계”OCTA는 레이저 스펙클 플로우그래피(LSFG)와 보완적인 역할을 합니다. OCTA는 혈관 구조(밀도 및 형태)를 평가하는 반면, LSFG는 혈류 속도를 정량화합니다. 두 가지를 병용하면 보다 포괄적인 순환 평가가 가능합니다4).
6. OCTA 원리의 상세와 시신경의 혈관 지배
섹션 제목: “6. OCTA 원리의 상세와 시신경의 혈관 지배”신호 검출의 상세 메커니즘
섹션 제목: “신호 검출의 상세 메커니즘”동일 부위의 반복 스캔을 통해 움직이는 성분(적혈구)과 정적 성분(조직)을 분리합니다. SSADA 알고리즘은 미세한 안구 운동으로 인한 배경 잡음을 평균화 방법(볼륨 평균화)으로 감소시킵니다.
맥락막 모세혈관판(CC)의 영상화는 브루크막 외측 10–30μm 깊이에서 수행됩니다. 앤페이스 이미지의 외관은 그물망 구조가 아니라 과립상입니다. 이는 횡방향 해상도의 한계, 배경 잡음 및 혈관의 불연속성에 기인합니다.
시신경 유두의 혈관 지배
섹션 제목: “시신경 유두의 혈관 지배”시신경 유두(ONH)는 안동맥의 말단 가지인 후단모양체동맥(SPC 동맥)에 의해 혈액 공급을 받습니다. SPC 동맥은 안동맥에서 분지하여 10–20개로 나뉩니다.
각 부위의 혈관 지배는 다음과 같습니다.
- 사상판 전부(prelaminar): SPC 동맥과 망막 순환 유래 모세혈관이 혼합되어 지배합니다.
- 사상판: SPC 동맥(직접 또는 Zinn-Haller 동맥환 경유)이 지배합니다.
- 사상판 후부(retrolaminar): 연막 혈관이 지배합니다.
자가 조절 기전
섹션 제목: “자가 조절 기전”ONH 혈류는 안구 관류압(OPP = 평균 동맥압 − 안압)에 의존합니다. 혈관 내피에서 분비되는 엔도텔린-1과 일산화질소에 의한 조절이 관여하며, 동물 실험에서 OPP ≥ 30 mmHg 범위에서 자가 조절이 유효한 것으로 알려져 있습니다.
시신경 위축에서는 유두주위 신경섬유 수의 감소에 따라 대사 활동이 저하되고, 자가조절을 통해 혈류 감소가 발생합니다. 이는 혈관 밀도 감소로 관찰됩니다.
7. 최신 연구와 향후 전망 (연구 단계 보고)
섹션 제목: “7. 최신 연구와 향후 전망 (연구 단계 보고)”선천성 시신경 유두 저형성증 (NOH)
섹션 제목: “선천성 시신경 유두 저형성증 (NOH)”Yoshimura 등(2024)은 20대 여성의 선천성 비측 시신경 유두 형성부전(NOH) 1예를 보고했습니다1). OCTA(Nidek RS-3000 Advance 2, 4.5mm×4.5mm)로 RPC 밀도를 정량 평가한 결과, 환안 비측의 RPC 밀도는 19%로 현저히 감소했습니다(상측 51%, 이측 58%, 하측 38%). 이는 cpRNFL 얇아짐 영역 및 Humphrey 시야의 쐐기 모양 결손 부위와 일치하여, OCTA가 NOH의 임상적 특징과 병태 해명에 유용함을 보여주었습니다.
Vogt-고야나기-하라다병(VKH)
섹션 제목: “Vogt-고야나기-하라다병(VKH)”Erba 등(2021)은 24세 남성의 급성 VKH 1예를 보고했습니다2). OCTA(Topcon DRI OCT Triton Plus)로 맥락막 모세혈관판의 flow void spots을 검출했으며, 이는 ICGA의 저형광 부위와 상관관계가 있음을 보여주었습니다. 프레드니솔론 60mg/일 점감 + 사이클로스포린 A 100mg 1일 2회 치료 후, 최대교정시력은 양안 20/20으로 회복되었고, 맥락막 두께는 초진 시 우안 712μm, 좌안 750μm에서 3개월 후 우안 538μm, 좌안 548μm로 감소했습니다. 치료 후 flow void도 현저히 감소하여, OCTA가 질환 활동성 모니터링에 유용함이 입증되었습니다.
다발혈관염성 육아종증(GPA)
섹션 제목: “다발혈관염성 육아종증(GPA)”Mehta 등(2022)은 61세 남성의 다발혈관염성 육아종증 증례를 보고했습니다3). 우안의 표층 모세혈관 탈락과 좌안의 AION을 보였으며, OCTA로 표층 모세혈관총의 모세혈관 탈락과 맥락막 모세혈관판의 flow void를 비침습적으로 검출했습니다. 메틸프레드니솔론 500mg×3일 + 사이클로포스파미드 500mg 단회 투여의 면역억제 요법 후, 치료 1개월에 OCTA 소견이 현저히 개선되었습니다. 임상적으로 보이지 않는 맥락막 병변도 OCTA로 검출할 수 있음이 입증되었습니다.
시신경 유두 멜라닌세포종
섹션 제목: “시신경 유두 멜라닌세포종”Tsai 등(2023)은 50세 여성의 시신경유두 멜라닌세포종 1예에서 OCTA와 LSFG를 이용한 순환 평가를 시행했습니다4). OCTA로 종양 내 심층 망막 혈관 네트워크를 검출했고, 환안의 유두·황반부 LSFG MBR(평균 혈관 밀도 비율)이 건안에 비해 감소했습니다(유두 MBR: 환안 23.0±0.8 vs 건안 26.5±1.9). FA에서는 색소에 의한 차단 효과로만 평가가 가능했지만, OCTA가 이 한계를 극복했습니다. LSFG와 병용하여 더 포괄적인 순환 평가가 가능함을 보여주었습니다.
MOG 항체 관련 시신경염(MOG-ON)
섹션 제목: “MOG 항체 관련 시신경염(MOG-ON)”MOG-ON에서 유두주위 및 중심와주위 혈관 밀도 감소가 건강 대조군에 비해 확인되었습니다. 혈관 밀도 감소는 ON 에피소드 횟수, pRNFL 두께, 시력과 상관관계가 있었으며, 망막 혈관 감소는 망막 변성에 따른 대사 요구 감소로 인한 것일 가능성이 시사됩니다.
향후 전망
섹션 제목: “향후 전망”OCTA는 비침습적이고 반복 시행이 가능한 특성을 활용하여 다음과 같은 방향으로 임상 응용이 기대됩니다.
- 녹내장의 조기 발견: 시력 저하 전 단계에서도 혈류 변화를 검출할 가능성이 있습니다.
- 시신경 질환의 진행 모니터링: 혈관 밀도의 시간적 변화를 정량적으로 추적할 수 있습니다.
- 치료 효과 판정: 면역억제 요법 후 flow void 개선 등 치료 반응의 객관적 평가에 활용할 수 있습니다.
- 신경퇴행성 질환(예: 알츠하이머병): 망막 신경 구조와 미세혈관 평가에 대한 응용이 연구되고 있습니다.
유망한 분야로는 녹내장의 조기 발견(시력 저하 전 혈류 변화 감지), 시신경 질환의 진행 모니터링(혈관 밀도의 시간적 정량 평가), 전신 혈관염에서 망막 및 맥락막 병변의 비침습적 평가가 있습니다. 치료 후 flow void 변화를 지표로 한 면역억제 요법의 효과 판정에 대한 응용도 진행 중입니다.
8. 참고문헌
섹션 제목: “8. 참고문헌”- Yoshimura M, Hashimoto Y, Hatanaka A, Yoshitomi T. Findings of optical coherence tomography angiography of nasal optic disc hypoplasia. Am J Ophthalmol Case Rep. 2024;36:102198.
- Erba S, Govetto A, Scialdone A, Casalino G. Role of optical coherence tomography angiography in Vogt-Koyanagi-Harada disease. GMS Ophthalmol Cases. 2021;11:Doc06.
- Mehta S, Chitnis N, Medhekar A. Utility of Optical Coherence Tomography Angiography (OCTA) in Granulomatosis With Polyangiitis. Cureus. 2022;14(2):e22612.
- Tsai TY, Tsai YJ, Chu YC, Hwang YS, Liao YL. Ocular circulation change in optic disc melanocytoma — a case report and a review of the literature. BMC Ophthalmol. 2023;23:33.
