OCT angiography (optical coherence tomography angiography; OCTA ) เป็นเทคนิคการถ่ายภาพวินิจฉัยแบบไม่รุกรานที่ใช้หลักการของ OCT (optical coherence tomography) เพื่อแสดงภาพหลอดเลือด OCT ถูกคิดค้นขึ้นในทศวรรษ 1990 และสร้างภาพตัดขวางความละเอียดสูงโดยอาศัยอินเทอร์เฟอโรเมทรีแบบ low-coherence OCT ได้กลายเป็นหนึ่งในวิธีการถ่ายภาพวินิจฉัยที่สำคัญที่สุดในจักษุวิทยา
OCT แบบดั้งเดิมมีความคมชัดต่ำระหว่างเส้นเลือดฝอยและเนื้อเยื่อจอประสาทตา ทำให้การติดตามการเปลี่ยนแปลงของหลอดเลือดมีข้อจำกัด การถ่ายภาพหลอดเลือดด้วยฟลูออเรสซีน (FA ) และอินโดไซยานีนกรีน (ICGA ) ต้องฉีดสารทึบรังสีทางหลอดเลือดดำ ซึ่งมีความเสี่ยงต่อภาวะช็อกจากภูมิแพ้ นอกจากนี้ยังให้ภาพสองมิติเท่านั้นโดยไม่มีข้อมูลความลึกของรอยโรค
OCTA สามารถเอาชนะข้อจำกัดเหล่านี้ โดยแสดงภาพหลอดเลือดในระดับความลึกต่างๆ แบบสามมิติโดยไม่ต้องใช้สารทึบรังสี OCTA มีประโยชน์สำหรับโรคที่ทำให้เกิดความผิดปกติของการไหลเวียนเลือดจอประสาทตา (เช่น เบาหวานขึ้นจอตาและหลอดเลือดดำจอประสาทตาอุดตัน ) โรคที่ทำให้เกิดความผิดปกติของการไหลเวียนเลือดประสาทตา (เช่น ต้อหิน และโรคเส้นประสาทตา ขาดเลือด) และโรคที่ทำให้เกิดเส้นเลือดใหม่ในคอรอยด์
ในสาขาประสาทจักษุวิทยา การประเมินหลอดเลือดฝอยรอบหัวประสาทตาแบบรัศมี (radial peripapillary capillaries; RPC ) รอบจานประสาทตา มีความสำคัญเป็นพิเศษ การลดลงของความหนาแน่นของหลอดเลือดจะสังเกตได้สอดคล้องกับบริเวณที่มีข้อบกพร่องของชั้นใยประสาทจอตา (NF LD) ในจอตา
Q
ความแตกต่างหลักระหว่าง OCTA และการตรวจหลอดเลือดด้วยฟลูออเรสซีนแบบดั้งเดิม (FA/ICGA) คืออะไร?
A
OCTA ไม่ต้องใช้สารทึบรังสีและไม่รุกราน สามารถประเมินโครงข่ายหลอดเลือดแบบสามมิติและแยกชั้นได้ FA /ICGA สามารถตรวจหาการรั่วของฟลูออเรสซีน และข้อบกพร่องในการเติมเต็ม แต่มีความเสี่ยงต่อภาวะแพ้รุนแรงจากการให้สารทึบรังสี และภาพที่ได้เป็นเพียงสองมิติ ทั้งสองมีความสัมพันธ์แบบเสริมกัน และ OCTA ไม่สามารถประเมินการรั่วของฟลูออเรสซีน ได้
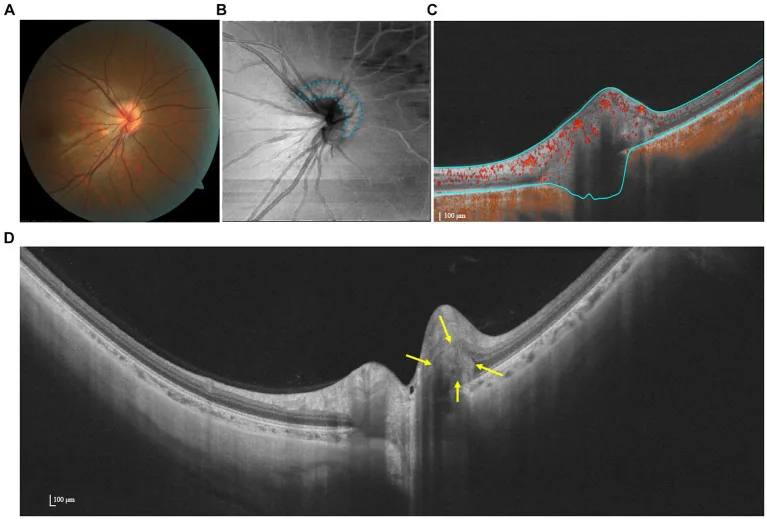
OCTA และ OCT ของ PHOMS Ruihan Hu, Qiuyan Wu, Zuohuizi Yi et al. Multimodal imaging of optic nerve head abnormalities in high myopia. Frontiers in Neurology. 2024 Apr 23; 15:1366593. Figure 3. PM
CI D: PMC11075756. License: CC BY.
ภาพ en face
OCTA และ SS-
OCT แสดง
PHOMS ภาพสร้างขึ้นโดยใช้
OCT -Angiography
ในโรคทางประสาทจักษุวิทยา การเปลี่ยนแปลงของหลอดเลือดหลักที่สังเกตได้จาก OCTA มีดังนี้
ความหนาแน่นของหลอดเลือดลดลง (capillary dropout) : พบในภาวะฝ่อของเส้นประสาทตา โรคต้อหิน และหลังโรคประสาทตาอักเสบ มีการกระจายตัวสอดคล้องกับบริเวณ NF LDการขยายและคดเคี้ยวของหลอดเลือด : สังเกตได้ในระยะเฉียบพลันของภาวะปุ่มประสาทตาบวม และในบางกรณีของโรคประสาทตาอักเสบ Flow void (การหายไปของสัญญาณ) : บริเวณที่สูญเสียการไหลเวียนของเลือดที่ตรวจพบในระดับชั้นเส้นเลือดฝอยคอรอยด์ (CC) มีประโยชน์ในการประเมินรอยโรคคอรอยด์ ในโรคอักเสบทั่วร่างกาย เช่น VKH และ granulomatosis with polyangiitisTangled ball of vessels (การสร้างหลอดเลือดแบบเป็นก้อนเส้นด้าย) : รูปแบบลักษณะเฉพาะที่เกิดจากการขยายและคดเคี้ยวของเส้นเลือดฝอยบนผิวของจานประสาทตา ในภาวะปุ่มประสาทตาบวม
MS และ Optic Neuritis
Multiple Sclerosis (MS ) : พบการลดลงของ RNFL โดยไม่ขึ้นกับการมีหรือไม่มีประวัติ optic neuritis ดัชนีการไหลเวียนเลือดของ ONH (ONH-FI) ลดลงอย่างมีนัยสำคัญในกรณีที่มีประวัติ optic neuritis ความแม่นยำในการตรวจจับเพิ่มขึ้นเมื่อใช้ร่วมกับพารามิเตอร์ OCT เชิงโครงสร้าง
Papillitis : ในภาวะบวมของจานประสาทตา จากการอักเสบ จะไม่พบการสูญเสียหลอดเลือด การกระจายแบบรัศมีของเส้นเลือดฝอยรอบจานประสาทตา ยังคงอยู่
Ischemic Optic Neuropathy
Non-Arteritic Anterior Ischemic Optic Neuropathy (Non-Arteritic) : พบความผิดปกติของการไหลเวียนเลือดในเส้นเลือดฝอยรอบจานประสาทตา ทั้งในระยะเฉียบพลันและเรื้อรัง ส่วนขมับมีความหนาแน่นของการไหลเวียนเลือดสูงสุดและได้รับผลกระทบมากที่สุดในตา NAION ความหนาแน่นของหลอดเลือด ONH และรอบจานประสาทตา ในระยะเรื้อรังสัมพันธ์โดยตรงกับความเสียหายของ RNFL และข้อบกพร่องของลานสายตา
AAION (Arteritic) : มีลักษณะเฉพาะคือการขยายตัวของเส้นเลือดฝอยรอบจานประสาทตา ชั้นผิวและการขาดเลือดเฉพาะที่ของเส้นเลือดฝอยจอประสาทตา ชั้นผิวและชั้นลึก
โรคทางพันธุกรรมและโรคเสื่อม
LHON (โรคเส้นประสาทตา ฝ่อจากพันธุกรรมแบบลีเบอร์)คอรอยด์ ตามระยะโรค ในระยะกึ่งเฉียบพลันระยะแรกจะลดลงจากด้านขมับ และในระยะเรื้อรังจะลดลงในทุกส่วน
ฝ่อของเส้นประสาทตา
ต้อหิน
POAG (ต้อหินมุมเปิด ปฐมภูมิ)
NTG (ต้อหิน ความดันปกติ)ต้อหินมุมเปิด ปฐมภูมิแต่รุนแรงน้อยกว่า ในกรณีที่สงสัยต้อหิน อาจตรวจพบการลดลงของดัชนีการไหลเวียนเลือดก่อนที่การมองเห็น จะลดลง
OCTA มีประโยชน์ในการแยกภาวะ papilledema และ pseudopapilledema
Papilledema : เส้นเลือดฝอยบนผิวของจานประสาทตา ขยายและคดเคี้ยว เกิดเป็น “tangled ball of vessels” ความหนาแน่นของเส้นเลือดฝอยรอบจานประสาทตา ยังคงเท่ากับตาข้างควบคุม ไม่มีการสูญเสียหลอดเลือดPseudopapilledema : ความหนาแน่นของเส้นเลือดฝอยรอบจานประสาทตา ลดลง
Q
เหตุใด OCTA จึงสามารถแยก papilledema และ pseudopapilledema ได้?
A
ใน papilledema อาการบวมน้ำจะบดบังเส้นเลือดฝอยในชั้นล่าง แต่สามารถมองเห็นเส้นเลือดฝอยเหนือชั้นบวมน้ำ และความหนาแน่นของหลอดเลือดรอบจานประสาทตา ยังคงเท่ากับตาข้างควบคุม ในขณะที่ pseudopapilledema (เช่น drusen ของจานประสาทตา ) จะพบความหนาแน่นของหลอดเลือดลดลง ดังนั้นความแตกต่างนี้จึงเป็นพื้นฐานในการวินิจฉัยแยกโรค
ในโรคประสาทตาอักเสบ หรือ AION ที่มีภาวะบวมของหัวประสาทตา การตรวจพบความเสียหายของแอกซอนระยะเฉียบพลันทำได้ยากเนื่องจากความหนาของ cpRNFL ที่เพิ่มขึ้นจากการขัดขวางการขนส่งตามแอกซอน การวิเคราะห์ชั้นในของจอประสาทตา บริเวณจอประสาทตา ส่วนกลาง เช่น ก้อนเซลล์ปมประสาท (GCC) สามารถตรวจพบการบางลงได้เร็วกว่าการวิเคราะห์ cpRNFL
ในโรคของเส้นประสาทตา ที่ทำให้เกิดจุดบอดกลาง หรือจุดบอดกลาง แบบ centrocecal รูปแบบการบางลงสะท้อนถึงความเสียหายของมัดเส้นใยประสาท papilomacular (PMB) ในการตรวจ OCT A จะพบความหนาแน่นของ RPC ลดลงสอดคล้องกับบริเวณที่ PMB บางลง
OCTA ถ่ายภาพซ้ำบริเวณเดียวกันของจอประสาทตา และตรวจจับเฉพาะส่วนที่เคลื่อนไหว (เม็ดเลือดแดง) เป็นการเปลี่ยนแปลงสัญญาณแบบสุ่ม เม็ดเลือดแดงที่ไหลเวียนทำให้เกิดความแปรผันของสัญญาณระหว่างการสแกนมากกว่าเนื้อเยื่อที่อยู่นิ่ง
มีวิธีการตรวจจับหลักสองประเภท
วิธีแอมพลิจูดดีคอร์รีเลชัน : ตรวจจับความแตกต่างของแอมพลิจูดระหว่างการสแกน B สองครั้งวิธีเฟสแวเรียนซ์ : ตรวจจับการเปลี่ยนแปลงเฟสของคลื่นแสง
อัลกอริทึมที่เป็นตัวแทนคือ SSADA (Split-Spectrum Amplitude Decorrelation Angiography) สเปกตรัม OCT ถูกแบ่งออกเป็นแถบแคบลง และอัตราส่วนสัญญาณต่อสัญญาณรบกวน (S/N) ได้รับการปรับปรุงอย่างมีนัยสำคัญโดยการเฉลี่ยดีคอร์รีเลชันความเข้มของแต่ละแถบ
OCTA สร้างภาพ en face ของสี่ชั้นโดยอัตโนมัติ
ชั้น ชื่อ เป้าหมายการประเมินหลัก ชั้นผิว โครงข่ายหลอดเลือดจอประสาทตา ชั้นผิว (SCP) ชั้นเส้นใยประสาทจอประสาทตา ถึงชั้นเซลล์ปมประสาทชั้นลึก โครงข่ายหลอดเลือดจอประสาทตา ชั้นลึก (DCP) รอบชั้นนิวเคลียสชั้นใน จอประสาทตา ชั้นนอกชั้นจอประสาทตา ชั้นนอก ปกติไม่มีหลอดเลือด ลึก ชั้นเส้นเลือดฝอยคอรอยด์ (CC) 10-30 ไมโครเมตรด้านนอกเยื่อบรูค
การตั้งค่าการแบ่งส่วนแตกต่างกันไปตามเครื่อง RPC และ SCP มักจะแสดงร่วมกันเป็น SCP มีความเห็นว่าการแสดงภาพของแผ่นเส้นเลือดฝอยคอรอยด์ ด้วย SS-OCT ดีกว่า SD-OCT
ข้อดีของ OCTA มีดังนี้:
ไม่ต้องใช้สารทึบรังสี : ไม่มีความเสี่ยงต่อภาวะแพ้รุนแรง และสามารถทำซ้ำได้ระยะเวลาถ่ายภาพสั้น : ลดภาระของผู้ป่วยการประเมินสามมิติ : สามารถสังเกตชั้นและโครงสร้างสามมิติของโครงข่ายหลอดเลือดได้การวิเคราะห์เชิงปริมาณ : สามารถแสดงค่าพารามิเตอร์เชิงปริมาณ เช่น ความหนาแน่นของหลอดเลือดและดัชนีการไหลเวียนเลือด
ในทางกลับกัน ต้องระวังข้อจำกัดและสิ่งรบกวนดังต่อไปนี้
คุณภาพภาพลดลง : ในตาที่มีต้อกระจก หรือขุ่นมัวในวุ้นตา จะเห็นโครงข่ายเส้นเลือดฝอยได้ยาก ระวังอย่าสับสนกับบริเวณที่ไม่มีการไหลเวียนเลือด สิ่งรบกวนจากการเคลื่อนไหวของลูกตา/ใบหน้า : การเคลื่อนไหวระหว่างการถ่ายภาพทำให้เกิดเส้นสีขาวหรือความผิดเพี้ยนสิ่งรบกวนจากการฉายภาพ : สัญญาณจากชั้นตื้นถูกฉายไปยังชั้นลึกการไม่ตรวจพบการรั่วของฟลูออเรสเซนต์ : ไม่สามารถแยกแยะการรั่วของฟลูออเรสเซนต์ได้ จึงไม่สามารถแทนที่การตรวจหลอดเลือดได้อย่างสมบูรณ์ข้อจำกัดของพื้นที่ถ่ายภาพ : สามารถเลือกได้ตั้งแต่ 3 มม. × 3 มม. ถึง 12 มม. × 12 มม. แต่พื้นที่ถ่ายภาพและคุณภาพของภาพเป็นสัดส่วนผกผัน
Q
มีสิ่งแปลกปลอมใดที่ควรระวังในการตรวจ OCTA?
A
สิ่งแปลกปลอมหลักมีสามประเภท ได้แก่ การลดลงของความเข้มสัญญาณเนื่องจากต้อกระจก หรือความขุ่นของวุ้นตา (ระวังการสับสนกับบริเวณที่ไม่มีการไหลเวียนเลือด ) เส้นสีขาวหรือการบิดเบือนจากการเคลื่อนไหวของตาหรือใบหน้า และการฉายสัญญาณชั้นผิวลงสู่ชั้นลึก (projection artifact) ในการอ่านผล ควรตรวจสอบความสอดคล้องกับ B-scan
ขั้นตอนการทำ OCTA และประเด็นสำคัญในการประเมินมีดังนี้
การกำหนดขอบเขตการถ่ายภาพ : ปรับตามวัตถุประสงค์การประเมิน สำหรับการประเมินระดับเส้นเลือดฝอยอย่างละเอียด ควรใช้มุมมองแคบ เช่น 3×3 มม. หากต้องการประเมินมุมกว้าง ให้เลือก 12×12 มม.การยืนยันการแบ่งส่วนอัตโนมัติ : ภาพ en face 4 ชั้น (SCP, DCP, จอประสาทตา ชั้นนอก, CC) ถูกสร้างขึ้นโดยอัตโนมัติ แต่เนื่องจากการตั้งค่าแตกต่างกันไปตามเครื่อง ควรตรวจสอบความสอดคล้องกับ B-scan เสมอการประเมินพารามิเตอร์เชิงปริมาณ : ความหนาแน่นของหลอดเลือดรอบหัวประสาทตา ความหนาแน่น RPC ดัชนีการไหลเวียนเลือด ONH (ONH-FI) ฯลฯ ถูกวัด
ลักษณะของแต่ละวิธีการตรวจสอบสรุปไว้ด้านล่าง
ลักษณะ OCTA FA ICGA สารทึบรังสี ไม่จำเป็น จำเป็น จำเป็น ข้อมูลความลึก สามมิติ (แยกชั้น) สองมิติ สองมิติ การรั่วของฟลูออเรสซีน ตรวจไม่พบ ตรวจพบ ตรวจพบ การวัดเชิงปริมาณ สูง ต่ำ ต่ำ การทำซ้ำ ง่าย ยาก ยาก
ด้านล่างนี้คือตัวชี้วัดการประเมินที่เป็นตัวแทนเมื่อใช้ OCTA ในจักษุวิทยาประสาท
ความหนาแน่นของหลอดเลือดรอบหัวประสาทตา (peripapillary vessel density) : มีรายงานความสัมพันธ์กับความรุนแรงของภาวะเส้นประสาทตา ขาดเลือดส่วนหน้าชนิดไม่ใช่หลอดเลือดแดงอักเสบและโรคต้อหิน รวมถึงความบกพร่องของลานสายตา ความหนาแน่น RPC (ความหนาแน่นของเส้นเลือดฝอยรอบหัวประสาทตาแบบรัศมี) : สามารถประเมินแยกตามส่วน และสามารถยืนยันความสอดคล้องกับตำแหน่งรอยโรคได้1) ดัชนีการไหลเวียนเลือดของ ONH (ONH-FI) : ดัชนีที่ใช้หาปริมาณการไหลเวียนเลือดของ ONH ทั้งหมด มีรายงานว่าลดลงในโรคปลอกประสาทเสื่อมแข็งและโรคต้อหิน Flow void (การไม่มีสัญญาณ) ในแผ่นเส้นเลือดฝอยคอรอยด์ : ใช้หาปริมาณบริเวณที่ไม่มีการไหลเวียนเลือด ของคอรอยด์ ใช้ประเมินรอยโรคคอรอยด์ ในม่านตาอักเสบ และหลอดเลือดอักเสบทั่วร่างกาย2)
OCTA มีบทบาทเสริมกับ Laser Speckle Flowgraphy (LSFG) ในขณะที่ OCTA ประเมินโครงสร้างหลอดเลือด (ความหนาแน่นและสัณฐานวิทยา) LSFG จะหาปริมาณความเร็วการไหลเวียนเลือด การใช้ทั้งสองร่วมกันช่วยให้ประเมินการไหลเวียนได้ครอบคลุมมากขึ้น4)
ส่วนประกอบที่เคลื่อนที่ (เม็ดเลือดแดง) และส่วนประกอบที่อยู่นิ่ง (เนื้อเยื่อ) จะถูกแยกออกโดยการสแกนซ้ำบริเวณเดียวกัน ในอัลกอริทึม SSADA สัญญาณรบกวนพื้นหลังจากการเคลื่อนไหวของดวงตาในระดับจุลภาคจะลดลงโดยวิธีการเฉลี่ย (volume averaging)
การแสดงภาพชั้นเส้นเลือดฝอยคอรอยด์ (CC) ทำที่ความลึก 10-30 ไมโครเมตรนอกเยื่อบรูค ลักษณะของภาพเอนเฟซเป็นแบบเม็ด ไม่ใช่โครงสร้างแบบตาข่าย สาเหตุมาจากข้อจำกัดของความละเอียดตามขวาง สัญญาณรบกวนพื้นหลัง และความไม่ต่อเนื่องของหลอดเลือด
หัวประสาทตา (ONH) ได้รับเลือดจากหลอดเลือดแดงซิลิอารีส่วนหลังสั้น (หลอดเลือดแดง SPC) ซึ่งเป็นแขนงปลายของหลอดเลือดแดงจักษุ หลอดเลือดแดง SPC แยกจากหลอดเลือดแดงจักษุและแบ่งออกเป็น 10-20 แขนง
การกระจายของหลอดเลือดในแต่ละส่วนมีดังนี้
บริเวณก่อนแผ่นคริบรอซา (prelaminar) : เลือดมาเลี้ยงจากหลอดเลือดแดงซิลิอารีส่วนหลังสั้นและเส้นเลือดฝอยจากการไหลเวียนของจอประสาทตา แผ่นคริบรอซา : เลือดมาเลี้ยงจากหลอดเลือดแดงซิลิอารีส่วนหลังสั้น (โดยตรงหรือผ่านวงแหวนซินน์-ฮาลเลอร์)บริเวณหลังแผ่นคริบรอซา (retrolaminar) : เลือดมาเลี้ยงจากหลอดเลือดของเยื่อเพีย
การไหลเวียนเลือดของ ONH ขึ้นอยู่กับความดันเลือดไปเลี้ยงลูกตา (OPP = ความดันหลอดเลือดแดงเฉลี่ย − ความดันลูกตา ) การควบคุมโดยเอนโดทีลิน-1 และไนตริกออกไซด์จากเยื่อบุผนังหลอดเลือดมีส่วนเกี่ยวข้อง และในการทดลองในสัตว์ การควบคุมตนเองมีประสิทธิภาพในช่วง OPP ≥ 30 มิลลิเมตรปรอท
ในภาวะฝ่อของเส้นประสาทตา กิจกรรมการเผาผลาญจะลดลงตามจำนวนเส้นใยประสาทรอบหัวประสาทตาที่ลดลง ส่งผลให้การไหลเวียนเลือดลดลงผ่านกลไกการควบคุมตนเอง ซึ่งสังเกตได้จากความหนาแน่นของหลอดเลือดที่ลดลง
เนื้อหาต่อไปนี้อยู่ในขั้นตอนการวิจัยหรือการทดลองทางคลินิกในปัจจุบัน และรวมถึงรายงานที่อยู่นอกขอบเขตการประยุกต์ใช้ทางคลินิกมาตรฐานที่มีในโรงพยาบาลทั่วไป เป็นข้อมูลอ้างอิงสำหรับผู้เชี่ยวชาญเกี่ยวกับการพัฒนาทางการแพทย์ในอนาคต
Yoshimura และคณะ (2024) รายงานผู้ป่วยหญิงอายุ 20 ปีที่มีภาวะ hypoplasia ของเส้นประสาทตา ชนิด congenital nasal (NOH) จำนวน 1 ราย 1) การประเมินความหนาแน่นของ RPC เชิงปริมาณด้วย OCTA (Nidek RS-3000 Advance 2, 4.5mm×4.5mm) พบว่าความหนาแน่นของ RPC ด้าน nasal ของตาข้างที่ได้รับผลกระทบลดลงอย่างมีนัยสำคัญเหลือ 19% (ด้านบน 51% ด้านขมับ 58% ด้านล่าง 38%) ซึ่งสอดคล้องกับบริเวณที่ cpRNFL บางลงและตำหนิรูปลิ่มในลานสายตา Humphrey แสดงให้เห็นว่า OCTA มีประโยชน์ในการอธิบายลักษณะทางคลินิกและพยาธิสรีรวิทยาของ NOH
Erba และคณะ (2021) รายงานผู้ป่วยชายอายุ 24 ปีที่มี VKH ระยะเฉียบพลัน 1 ราย 2) OCTA (Topcon DRI OCT Triton Plus) ตรวจพบจุด flow void ใน choroidal capillary lamina ซึ่งสัมพันธ์กับบริเวณ hypofluorescence ในการตรวจ ICGA หลังการรักษาด้วย prednisolone 60 มก./วัน แบบลดขนาดและ cyclosporine A 100 มก. วันละ 2 ครั้ง ค่าความคมชัดของสายตาที่ดีที่สุดที่แก้ไขแล้วฟื้นคืนเป็น 20/20 ในทั้งสองข้าง และความหนาของคอรอยด์ ลดลงจาก RE 712 μm และ LE 750 μm ในการตรวจครั้งแรกเป็น RE 538 μm และ LE 548 μm หลังจาก 3 เดือน flow void ก็ลดลงอย่างมีนัยสำคัญหลังการรักษา แสดงให้เห็นว่า OCTA มีประโยชน์ในการติดตามกิจกรรมของโรค
Mehta และคณะ (2022) รายงานผู้ป่วยชายอายุ 61 ปีที่เป็น granulomatosis with polyangiitis 1 ราย 3) ตาขวาแสดงการสูญเสียหลอดเลือดฝอยชั้นผิว และตาซ้ายแสดง AION และ OCTA ตรวจพบการสูญเสียหลอดเลือดฝอยใน superficial capillary plexus และ flow void ใน choroidal capillary lamina โดยไม่ต้องผ่าตัด หลังการรักษาด้วย immunosuppressive therapy ด้วย methylprednisolone 500 มก. นาน 3 วัน และ cyclophosphamide 500 มก. ครั้งเดียว ผล OCTA ดีขึ้นอย่างมีนัยสำคัญหลังการรักษา 1 เดือน การศึกษาแสดงให้เห็นว่า OCTA สามารถตรวจพบรอยโรคคอรอยด์ ที่มองไม่เห็นทางคลินิก
Tsai และคณะ (2023) รายงานการประเมินการไหลเวียนโลหิตโดยใช้ OCTA และ LSFG ในผู้ป่วยหญิงอายุ 50 ปีที่มีเมลาโนไซโตมาของจานประสาทตา 1 ราย 4) OCTA ตรวจพบเครือข่ายหลอดเลือดจอประสาทตา ชั้นลึกภายในเนื้องอก และ MBR (อัตราส่วนความหนาแน่นของหลอดเลือดเฉลี่ย) ของจานประสาทตา และจุดรับภาพในตาข้างที่ได้รับผลกระทบลดลงเมื่อเทียบกับตาข้างปกติ (MBR จานประสาทตา : ตาข้างที่ได้รับผลกระทบ 23.0±0.8 เทียบกับตาข้างปกติ 26.5±1.9) FA สามารถประเมินได้เฉพาะผ่านผลการบดบังของสีเท่านั้น แต่ OCTA สามารถเอาชนะข้อจำกัดนี้ได้ การใช้ร่วมกับ LSFG แสดงให้เห็นถึงความเป็นไปได้ในการประเมินการไหลเวียนโลหิตที่ครอบคลุมมากขึ้น
ใน MOG-ON พบว่าความหนาแน่นของหลอดเลือดรอบจานประสาทตา และรอบรอยบุ๋มจอประสาทตา ลดลงเมื่อเทียบกับกลุ่มควบคุมที่มีสุขภาพดี การลดลงของความหนาแน่นของหลอดเลือดมีความสัมพันธ์กับจำนวนครั้งของ ON ความหนาของ pRNFL และความคมชัดของภาพ และการลดลงของหลอดเลือดจอประสาทตา อาจเกิดจากความต้องการเมแทบอลิซึมที่ลดลงตามการเสื่อมของจอประสาทตา
OCTA ซึ่งมีคุณสมบัติไม่รุกรานและสามารถทำซ้ำได้ คาดว่าจะมีการประยุกต์ใช้ทางคลินิกในทิศทางต่อไปนี้
การตรวจพบต้อหิน ในระยะเริ่มต้น : ความเป็นไปได้ในการตรวจพบการเปลี่ยนแปลงของการไหลเวียนเลือดแม้ก่อนระยะที่การมองเห็น ลดลงการติดตามความก้าวหน้าของโรคเส้นประสาทตา : สามารถติดตามการเปลี่ยนแปลงความหนาแน่นของหลอดเลือดเมื่อเวลาผ่านไปในเชิงปริมาณการประเมินประสิทธิภาพการรักษา : การปรับปรุงของ flow void หลังการรักษาด้วยยากดภูมิคุ้มกันสามารถใช้เป็นเกณฑ์ประเมินการตอบสนองต่อการรักษาได้อย่างเป็นกลางโรคทางระบบประสาทเสื่อม (เช่น อัลไซเมอร์) : กำลังมีการวิจัยเพื่อประยุกต์ใช้ในการประเมินโครงสร้างประสาทจอตาและหลอดเลือดขนาดเล็ก
Q
OCTA คาดว่าจะนำไปใช้ทางคลินิกกับโรคใดในอนาคต?
A
การตรวจพบต้อหิน ระยะแรก (ตรวจจับการเปลี่ยนแปลงการไหลเวียนเลือดก่อนการมองเห็น ลดลง) การติดตามความก้าวหน้าของโรคเส้นประสาทตา (การประเมินความหนาแน่นของหลอดเลือดเชิงปริมาณตามเวลา) และการประเมินรอยโรคจอตาและคอรอยด์ ในหลอดเลือดอักเสบทั่วร่างกายแบบไม่รุกล้ำเป็นสาขาที่มีแนวโน้มดี การประยุกต์ใช้ในการประเมินประสิทธิภาพการรักษาด้วยยากดภูมิคุ้มกันโดยใช้การเปลี่ยนแปลงของ flow void หลังการรักษาเป็นตัวบ่งชี้ก็กำลังก้าวหน้าเช่นกัน
Yoshimura M, Hashimoto Y, Hatanaka A, Yoshitomi T. Findings of optical coherence tomography angiography of nasal optic disc hypoplasia. Am J Ophthalmol Case Rep. 2024;36:102198.
Erba S, Govetto A, Scialdone A, Casalino G. Role of optical coherence tomography angiography in Vogt-Koyanagi-Harada disease. GMS Ophthalmol Cases. 2021;11:Doc06.
Mehta S, Chitnis N, Medhekar A. Utility of Optical Coherence Tomography Angiography (OCTA ) in Granulomatosis With Polyangiitis. Cureus. 2022;14(2):e22612.
Tsai TY, Tsai YJ, Chu YC, Hwang YS, Liao YL. Ocular circulation change in optic disc melanocytoma — a case report and a review of the literature. BMC Ophthalmol. 2023;23:33.
ถาม AI เกี่ยวกับบทความนี้
คัดลอกข้อความบทความแล้ววางในผู้ช่วย AI ที่คุณต้องการใช้
เปิดผู้ช่วย AI ด้านล่าง แล้ววางข้อความที่คัดลอกลงในช่องแชต