外观
色调:白色至黄白色。边界不清晰,呈蓬松的棉絮状质感。
大小:通常小于视盘面积的1/3

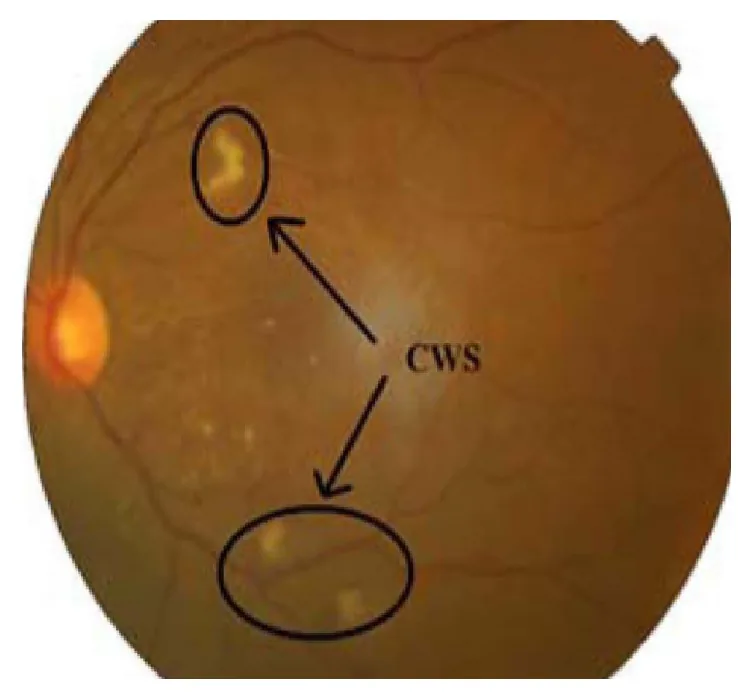
棉絮斑(cotton wool spots)是出现在视网膜表层的小型黄白色(灰白色)轻微隆起的病变。也称为“软性渗出”。
健康患者出现棉絮状白斑是不正常的。即使单眼只有一个,也很可能是糖尿病视网膜病变或高血压视网膜病变的最早期眼底表现。无既往史的棉絮状白斑患者中,50%舒张压≥90 mmHg,20%血糖升高。
病变好发于视乳头周围及上下颞侧血管弓沿线。表现为边界不清的白色至黄色斑状病变。
病变随时间推移而消退。通常在6至12周内消失,但在糖尿病视网膜病变患者中可能持续更长时间。
外观
色调:白色至黄白色。边界不清晰,呈蓬松的棉絮状质感。
大小:通常小于视盘面积的1/3
好发部位
视乳头周围:可能在视乳头周围多发
沿血管弓:出现在上下颞侧血管弓沿线
病程
自然消退:通常在6-12周内消失
持续病例:在糖尿病视网膜病变中可能持续更长时间
临床意义
非正常:健康眼中不出现的异常表现
全身疾病的征兆:高血压、糖尿病等全身疾病的眼底体征
一般来说,棉絮斑本身不会引起视觉症状。如果中心凹受累,可能会出现视力下降。也可能伴有基础疾病引起的全身症状。
各病因相关症状的示例如下。
散瞳眼底检查时,在后极部视网膜表层可见白色、边界不清、轻微隆起的病变。病变边缘呈丛状,具有棉絮样柔软质感。易与有髓神经纤维混淆,但形状和质地均不同。
以下为主要白色病变的鉴别诊断。
| 病变名称 | 颜色/质地 | 所在层次 |
|---|---|---|
| 软性渗出(棉絮状白斑) | 白色、柔软、边界不清 | 神经纤维层 |
| 硬性渗出 | 黄色、硬质、边界清晰 | 外丛状层 |
| 玻璃膜疣 | 黄白色、颗粒状 | 色素上皮下 |
以下展示代表性病例的所见。
棉絮状白斑本身没有直接的治疗方法。病变通常在6至12周内自然消退。最优先的是识别和治疗基础疾病;对于疑似GCA的患者,需要紧急处理以防止视力丧失。详情请参阅“标准治疗方法”一节。
棉絮状白斑并非特定疾病,而是多种全身性和局部性疾病的眼底征象。原因大致分为四类。
缺血性
免疫/炎症性
感染性
其他
栓塞性:Purtscher样视网膜病变(颈动脉栓塞、心源性栓塞、药物诱发)
肿瘤性:白血病(静脉扩张、迂曲、出血、棉絮状白斑、Roth斑)、淋巴瘤、转移
COVID-19:27名肺炎恢复期患者中6名(22%)出现棉絮状白斑2)
化疗药物(吉西他滨、顺铂)可引起Purtscher样视网膜病变,表现为棉絮状白斑。糖尿病和高血压会增加吉西他滨诱导的Purtscher样视网膜病变的风险。1)
在COVID-19中,高凝状态和病毒直接感染血管内皮引起的血管炎被认为是其机制。2)
视网膜静脉阻塞(RVO)的早期临床表现可能包括棉絮状白斑。4)
高血压和糖尿病是最常见的原因。即使没有既往病史的患者,出现棉絮状白斑时,50%有舒张压≥90 mmHg的升高,20%有血糖升高。
诊断通常通过散瞳眼底检查进行。确认病变后,必须详细检查基础疾病。
以下是主要影像学检查及其所见。
| 检查方法 | 主要所见 |
|---|---|
| 眼底检查 | 白色、边界不清的隆起性病变(神经纤维层水平) |
| OCT | 神经纤维层高反射伴局灶性增厚(急性期)→ 内层变薄(消退期) |
| FA | 邻近毛细血管无灌注区 |
各项检查的详细所见如下所示。
在视网膜动脉阻塞的鉴别诊断中,也需要评估棉絮斑。5)
初始检查包括以下项目:
根据需要可追加的检查如下:
需要与有髓神经纤维、硬性渗出、视网膜浸润、视网膜炎、玻璃膜疣、脉络膜视网膜萎缩进行鉴别。
初始检查推荐测量血压、HbA1c、血常规和HIV检测。必要时可加做心脏超声、颈动脉超声、ESR、CRP和凝血检查。疑似GCA时,颞动脉超声有助于鉴别诊断,可能需要紧急处理。
棉絮状白斑本身没有直接的治疗方法。识别并治疗基础疾病是关键。病变通常在6至12周内自然消退。
在CD4计数低于200的HIV感染患者中,新出现的棉絮状白斑可能是病毒性视网膜炎的早期征兆,需引起注意。
以下按基础疾病总结治疗和转归。
| 基础疾病 | 治疗 | 转归 |
|---|---|---|
| GCA | 大剂量类固醇治疗 | 数月内消退3) |
| 高血压 | 降压治疗 | 数月内消退 |
| 贫血 | 病因治疗 | 血液改善后消退 |
多数情况下可无后遗症消退。但如果累及中心凹或GCA导致视神经病变,则可能残留视力障碍。GCA中高达20%的患者会发生永久性视力丧失。3)
棉絮斑发生于视网膜小动脉闭塞导致的缺血之后。它与局部轴浆运输碎屑的积聚有关,是视网膜缺血的表现。3)
过程如下:视网膜小动脉微梗死→毛细血管前小动脉闭塞→神经纤维层梗死。
局部缺血阻断轴浆运输。线粒体和细胞内物质在受阻的轴突内积聚,导致神经纤维肿胀。这种肿胀的组织在眼底表现为白色至黄白色病变。
组织学上,细胞样小体是特征性表现。细胞样小体是肿胀的神经节细胞轴突的嗜酸性碎片,充满积聚的线粒体和细胞内物质。
特定原因引起的棉絮状白斑遵循Purtscher样视网膜病变的机制。
COVID-19患者视网膜微血管病变的报告正在增加。有报告称,27名COVID-19肺炎康复患者中有6名(22%)出现棉絮状白斑,SARS-CoV-2对血管内皮的影响受到关注。2) OCT-A对血流空区的可视化有助于病情评估。
托珠单抗已被证明对预防GCA复发有效。预计可延长复发时间并减少类固醇累积剂量。3) 颞动脉超声作为一种非侵入性GCA诊断方法正在普及。双侧晕征特异性100%的报道有助于提高诊断准确性。3)
对吉西他滨等化疗药物引起的视网膜毒性的认识正在提高。合并糖尿病或高血压的患者风险尤其高,强调化疗期间定期眼科监测的重要性。1)
Brummer SR, Joffe JA, Liggett PE. Chemotherapy-induced retinopathy in a diabetic and hypertensive patient with stage 4 metastatic pancreatic adenocarcinoma. J Vitreoret Dis. 2023;7(3):242-244.
Bottini AR, Steinmetz S, Blinder KJ, Shah GK. Purtscher-like retinopathy in a patient with COVID-19. Case Rep Ophthalmol Med. 2021;2021:6661541.
Fu L, O’Sullivan EP. Giant cell arteritis presenting as bilateral cotton wool spots. Cureus. 2022;14(10):e29804.
Retinal Vein Occlusions Preferred Practice Pattern. American Academy of Ophthalmology. 2024.
Retinal and Ophthalmic Artery Occlusions Preferred Practice Pattern. American Academy of Ophthalmology. 2024.