自觉症状

糖尿病性黄斑缺血
一目了然的要点
Section titled “一目了然的要点”1. 什么是糖尿病黄斑缺血?
Section titled “1. 什么是糖尿病黄斑缺血?”糖尿病黄斑缺血(DMI)是指糖尿病患者黄斑部视网膜毛细血管闭塞、萎缩、消失,并出现毛细血管前小动脉狭窄和闭塞的状态。在荧光素眼底血管造影(FA)或光学相干断层扫描血管成像(OCTA)上表现为中心凹无血管区(FAZ)扩大、不规则以及黄斑部不连续无血管区的扩大。
历史上,Norman Ashton通过死后眼球的周边虹膜前粘连染色和墨汁灌注研究,首次详细描述了糖尿病视网膜病变中动脉和毛细血管的参与。病理上,过程为终末小动脉和毛细血管前血管的玻璃样变性→管腔闭塞→动脉和毛细血管床消失→静脉侧新生血管形成。
糖尿病黄斑病变分为三型:黄斑水肿、缺血性黄斑病变和视网膜色素上皮病变;DMI相当于缺血性黄斑病变。
患病率与糖尿病视网膜病变的严重程度密切相关。
| DMI严重程度 | 发生率 |
|---|---|
| 无 | 39.7% |
| 疑似 | 18.4% |
| 轻度 | 25.2% |
| 中度 | 11.0% |
| 重度 | 5.6% |
CSME(临床有意义的黄斑水肿)病例中29.4%合并DMI,其中19.4%为中重度。此外,增殖性糖尿病视网膜病变(PDR)的77.2%和重度非增殖性糖尿病视网膜病变(NPDR)的59.7%存在DMI。
2. 主要症状与临床所见
Section titled “2. 主要症状与临床所见”- 视力下降:无中心凹浸润型DME但视力不良时,应怀疑DMI。
- 视物模糊:整个视野不清晰。
- 中心暗点:中心视野缺损
- 视野缺损:与缺血区域对应的局部视野缺失
- 进行性或稳定性视力下降:常见于有晚期DR病史的患者
DMI的表现有时被描述为“无特征视网膜”。中心凹反射变差,出血、微动脉瘤、渗出物、软性白斑和新生血管消失或仅轻度存在。
临床所见
无特征视网膜:中心凹反射差,出血、渗出物消失或减轻。
鬼影血管:失去灌注的毛细血管的残影。
小动脉狭窄:中重度DMI患者平均小动脉直径变窄。
功能检查
微视野计:在DCP无灌注区域,视网膜敏感性显著降低。1)
AO-OCT:在DCP无灌注区域,光感受器信号密度(IS/OS、COST)降低约40%。1)
关于DMI严重程度与视力的相关性,中重度DMI可见显著视力下降。VA-FAZ相关性报告为R²=0.41~0.51,视乳头黄斑间缺血与视力下降独立相关。
Datlinger等人(2021)使用AO-OCT和微视野计的研究表明,在DCP无灌注区域,光感受器信号密度(IS/OS和COST)降低约40%,且该区域的视网膜敏感度也显著下降。1)
轻度DMI可能不会对视力产生显著影响。中重度时与视力下降存在显著相关性(VA-FAZ相关性R²=0.41~0.51),视乳头黄斑间缺血也与视力下降独立相关。如果无DME但视力不佳,则需通过“诊断与检查方法”一节中的检查进行DMI评估。
3. 原因与风险因素
Section titled “3. 原因与风险因素”DMI的风险因素反映了糖尿病视网膜病变的总体风险因素。
- 糖尿病病程:病程越长,DMI风险越高
- HbA1c(血糖控制):持续高血糖促进毛细血管损伤
- 高血压:导致视网膜血流调节障碍
- 血脂异常:促进视网膜血管动脉硬化
- 年龄与种族:老年人和特定种族(如亚洲人、非洲裔)风险较高
- 贫血、肾脏疾病等全身因素可能促进周边缺血
DMI的存在与DME和DR严重程度增加相关。内科治疗(控制血糖、血压和血脂)可有效延缓视网膜病变进展。
此外,有报告显示,通过良好的血糖控制(HbA1c从6.1%改善至5.6%),毛细血管无灌注区(NPA)出现了自然再灌注。2)
4. 诊断与检查方法
Section titled “4. 诊断与检查方法”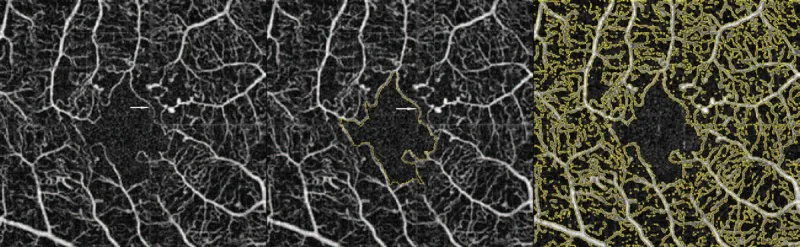
荧光素眼底血管造影(FA)
Section titled “荧光素眼底血管造影(FA)”FA是诊断DMI的金标准。
- FA表现:FAZ扩大(大的低荧光斑块)、毛细血管扩张、毛细血管间隙增宽。
- 正常FAZ直径:平均0.53–0.73 mm。糖尿病眼平均0.79 mm(范围0.66–0.91 mm)。
- 诊断参考:临床上FAZ直径超过0.5 mm怀疑DMI。
FA的缺点包括有创性(静脉注射造影剂)、并发症风险(死亡风险约1/20万)、所需时间20分钟以上。
OCTA(光学相干断层扫描血管成像)
Section titled “OCTA(光学相干断层扫描血管成像)”OCTA是一种无创、高分辨率的检查,可分层分析SCP(浅层毛细血管网)、DCP(深层毛细血管网)和CC(脉络膜毛细血管层)。
- 优点:无需染料渗漏即可显示FAZ边界。可检测到比FA更广泛的非灌注区(NPA)2)
- 缺点:伪影,低血流速度下的检测限制
- NPA分类:存在两种NPA:(1)伴有视网膜变薄的NPA(FFA可检测),(2)不伴视网膜变薄的NPA(仅OCTA可检测)2)
- OCTA黄斑非灌注定量与DR严重程度相关,并可检测临床前微血管变化3)
OCT和AO-OCT
Section titled “OCT和AO-OCT”- OCT:中心凹内层视网膜变薄或消失与视力下降相关3)
- AO-OCT(自适应光学OCT):可实现单个视锥细胞的三维可视化,在光感受器水平进行DMI评估1)
FA和OCTA的特性比较如下所示。
| 特征 | FA | OCTA |
|---|---|---|
| 侵入性 | 有 | 无 |
| 分层分析 | 不可 | 可 |
| NPA检测范围 | 有限 | 广泛 |
FA
金标准:显示FAZ扩大和毛细血管消失。
有创性:需要静脉注射造影剂。死亡风险约1/20万。
所需时间:需要20分钟以上。
OCTA
无创、高分辨率:可进行SCP/DCP/CC的分层分析。
NPA量化:与DR严重程度相关。也可检测临床前变化。3)
两种NPA检测:根据有无变薄,与FA的检测范围不同。2)
FA是金标准但有创。OCTA无创,且能检测出比FA更广泛的NPA。2) 特别是无视网膜变薄的早期NPA(无变薄NPA)仅能通过OCTA检测。两者特性互补,应根据临床情况酌情使用。
5. 标准治疗方法
Section titled “5. 标准治疗方法”DMI的直接治疗
Section titled “DMI的直接治疗”目前,尚无针对DMI的既定特异性治疗方法。对于不伴有DME的黄斑缺血,没有直接的治疗方法,全身管理是基础。
有报道称良好的血糖控制可能有助于NPA的自然再灌注,2) 内科治疗(血糖、血压、血脂)是抑制视网膜病变进展的基本策略。
在重度NPDR之后的阶段,建议考虑PRP(全视网膜光凝)或抗VEGF治疗。3)
合并DME时的治疗
Section titled “合并DME时的治疗”当DMI合并DME时,进行以下治疗。
- 抗VEGF药物(一线选择):雷珠单抗(Lucentis)每次0.5mg/0.05mL,阿柏西普(Eylea)每次2mg/0.05mL。效果是暂时的,可能需要频繁给药。
- 玻璃体内注射曲安奈德:MacuAid每次4mg/0.1mL。可能存在白内障进展和眼压升高的风险。
- 局部/格栅样光凝:DME的辅助治疗。
目前尚无针对DMI的既定特异性治疗方法。全身管理(血糖、血压、血脂)是基础,有病例报告显示良好的血糖控制可使NPA自然再灌注。2) 合并DME时,使用抗VEGF药物等治疗水肿,但不能直接改善缺血本身。
6. 病理生理学与详细发病机制
Section titled “6. 病理生理学与详细发病机制”初期变化:周细胞和内皮细胞损伤
Section titled “初期变化:周细胞和内皮细胞损伤”周细胞丢失和内皮细胞损伤是DR血管变化的最早期征兆。
- 周细胞:调节血管张力,产生基底膜和细胞外基质成分
- 内皮细胞:通过紧密连接形成血-视网膜屏障
III型和IV型胶原沉积导致毛细血管基底膜增厚,进而管腔狭窄。还会发生白细胞停滞(leukostasis),异常内皮细胞加剧血管闭塞。
毛细血管网的渐进性闭塞
Section titled “毛细血管网的渐进性闭塞”氧气和微量营养素供应减少刺激VEGF表达,导致毛细血管渐进性萎缩→毛细血管间隙扩大→长期缺氧→感光细胞损伤。随着DR进展,出现静脉异常、IRMA、严重出血和渗出。3)
黄斑部血管层和感光细胞的影响
Section titled “黄斑部血管层和感光细胞的影响”黄斑部有三层视网膜血管层(SCP、ICP/MCP、DCP)。DCP为感光细胞提供10-15%的氧气供应,1) 其闭塞直接导致感光细胞损伤。
Müller细胞(MC)在灌注障碍下通过向感光细胞提供乳酸作为能量来源。1) 当MC受损时,除了视锥细胞、视杆细胞和MC功能下降外,还观察到感光细胞外节片状消失和毛细血管脱失的共定位。1)
缺血模式的分类
Section titled “缺血模式的分类”缺血模式分为以下四种类型(Takashi等人的分类)。
| 缺血类型 | 频率 |
|---|---|
| 周边型 | 2.6% |
| 中间周边部型 | 61.2% |
| 中心部型 | 26.3% |
| 广泛型 | 9.9% |
深层毛细血管丛(DCP)的无灌注导致视细胞的氧气供应减少(DCP对视细胞氧气供应的贡献为10-15%)。1) 米勒细胞损伤也会阻碍视细胞的能量供应。使用AO-OCT的研究证实,在DCP无灌注区域,视细胞信号密度(IS/OS和COST)下降约40%。1)
7. 最新研究与未来展望(研究阶段报告)
Section titled “7. 最新研究与未来展望(研究阶段报告)”先进影像学评估
Section titled “先进影像学评估”Datlinger等人(2021)表明,AO-OCT与OCTA的结合能够在单个视锥细胞水平评估DMI。他们指出,将微视野计与OCTA相结合的研究方法有助于理解DMI的时间进程,并认为这些先进的影像学参数可能成为未来治疗研究的生物标志物。1)
毛细血管闭塞的可逆性与自然再灌注
Section titled “毛细血管闭塞的可逆性与自然再灌注”传统上认为毛细血管闭塞是不可逆的,但已有自然再灌注的病例报道。
Hou等人(2022)观察到,在HbA1c从6.1%改善至5.6%的糖尿病患者中,NPA发生了自然再灌注。他们通过OCTA记录了IRMA侵入NPA并形成新毛细血管网的过程。2)
该报告提示NPA可能具有两种不同的性质。2)
- 伴有变薄的NPA(晚期改变):再灌注较慢
- 无变薄的NPA(早期改变):2个月内易再灌注,可能是治疗干预的“窗口”
定量生物标志物与预后预测
Section titled “定量生物标志物与预后预测”在一项为期1年的OCTA随访研究中,基线非灌注与DR进展的比值比(OR)=8.73,深层非灌注与治疗干预的OR=3.39,表明OCTA非灌注指标可能成为预后预测的生物标志物。已知DMI眼的基线FAZ面积每年扩大5%~10%。AI在OCTA图像分析中的应用也在研究中。3)
尽管罕见,但有自然再灌注的报道。Hou等人(2022)报道了IRMA侵入NPA区域并形成新毛细血管网的过程。2) 特别是无变薄的NPA(早期改变)在2个月内易再灌注。良好的血糖控制也可能促进再灌注。
8. 参考文献
Section titled “8. 参考文献”-
Datlinger F, Georgi T, Stegmann H, et al. Assessment of detailed photoreceptor structure and retinal sensitivity in diabetic macular ischemia using adaptive optics-OCT and microperimetry. Invest Ophthalmol Vis Sci. 2021;62(13):1.
-
Hou S, Chen L, Shan K, et al. Spontaneous retinal reperfusion of capillary nonperfusion areas in diabetic retinopathy. Case Rep Ophthalmol. 2022;13:818-824.
-
American Academy of Ophthalmology Retina/Vitreous Panel. Diabetic Retinopathy Preferred Practice Pattern. Ophthalmology. 2024.
