自覺症狀

糖尿病黃斑缺血
一目瞭然的要點
Section titled “一目瞭然的要點”1. 什麼是糖尿病黃斑缺血?
Section titled “1. 什麼是糖尿病黃斑缺血?”糖尿病黃斑缺血(DMI)是糖尿病患者黃斑部視網膜微血管阻塞、萎縮、消失,並出現微血管前小動脈狹窄和阻塞的狀態。在螢光眼底血管攝影(FA)或光學同調斷層掃描血管成像(OCTA)上表現為中心凹無血管區(FAZ)擴大、不規則以及黃斑部不連續無血管區的擴大。
歷史上,Norman Ashton透過死後眼球的周邊虹膜前粘連染色和墨汁灌注研究,首次詳細描述了糖尿病視網膜病變中動脈和微血管的參與。病理上,過程為終末小動脈和微血管前血管的玻璃樣變性→管腔阻塞→動脈和微血管床消失→靜脈側新生血管形成。
糖尿病黃斑病變分為三型:黃斑水腫、缺血性黃斑病變和視網膜色素上皮病變;DMI相當於缺血性黃斑病變。
盛行率與糖尿病視網膜病變的嚴重程度密切相關。
| DMI嚴重程度 | 發生率 |
|---|---|
| 無 | 39.7% |
| 疑似 | 18.4% |
| 輕度 | 25.2% |
| 中度 | 11.0% |
| 重度 | 5.6% |
CSME(臨床上有意義的黃斑水腫)病例中29.4%合併DMI,其中19.4%為中重度。此外,增殖性糖尿病視網膜病變(PDR)的77.2%和重度非增殖性糖尿病視網膜病變(NPDR)的59.7%存在DMI。
2. 主要症狀與臨床所見
Section titled “2. 主要症狀與臨床所見”- 視力下降:無中心凹浸潤型DME但視力不良時,應懷疑DMI。
- 視物模糊:整個視野不清晰。
- 中心暗點:中心視野缺損
- 視野缺損:對應缺血區域的局部視野缺損
- 進行性或穩定性視力下降:常見於有晚期DR病史的患者
DMI的表現有時被描述為「無特徵視網膜」。中心凹反射變差,出血、微血管瘤、滲出物、軟性白斑和新生血管消失或僅輕度存在。
臨床所見
功能檢查
微視野計:在DCP無灌流區域,視網膜敏感性顯著降低。1)
AO-OCT:在DCP無灌流區域,感光細胞訊號密度(IS/OS、COST)降低約40%。1)
關於DMI嚴重度與視力的相關性,中重度DMI可見顯著視力下降。VA-FAZ相關性報告為R²=0.41~0.51,視神經盤黃斑間缺血與視力下降獨立相關。
Datlinger等人(2021)使用AO-OCT和微視野計的研究顯示,在DCP無灌流區域,感光細胞訊號密度(IS/OS和COST)降低約40%,且該區域的視網膜敏感度也顯著下降。1)
輕度DMI可能不會對視力產生顯著影響。中重度時與視力下降存在顯著相關性(VA-FAZ相關性R²=0.41~0.51),視神經盤黃斑間缺血也與視力下降獨立相關。如果無DME但視力不佳,則需透過「診斷與檢查方法」一節中的檢查進行DMI評估。
3. 原因與風險因素
Section titled “3. 原因與風險因素”- 糖尿病病程:病程越長,DMI風險越高
- HbA1c(血糖控制):持續高血糖促進微血管損傷
- 高血壓:導致視網膜血流調節障礙
- 血脂異常:促進視網膜血管動脈硬化
- 年齡與種族:老年人和特定種族(如亞洲人、非洲裔)風險較高
- 貧血、腎臟疾病等全身因素可能促進周邊缺血
DMI的存在與DME和DR嚴重程度增加相關。內科治療(控制血糖、血壓和血脂)可有效延緩視網膜病變進展。
此外,有報告顯示,透過良好的血糖控制(HbA1c從6.1%改善至5.6%),微血管無灌流區(NPA)出現了自然再灌流。2)
4. 診斷與檢查方法
Section titled “4. 診斷與檢查方法”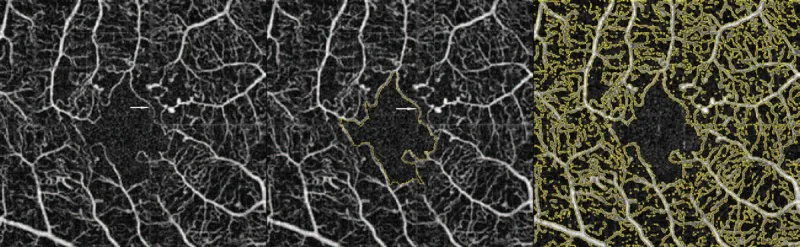
螢光眼底血管攝影(FA)
Section titled “螢光眼底血管攝影(FA)”FA是診斷DMI的黃金標準。
- FA所見:FAZ擴大(大的低螢光斑塊)、毛細血管擴張、毛細血管間隙增寬。
- 正常FAZ直徑:平均0.53–0.73 mm。糖尿病眼平均0.79 mm(範圍0.66–0.91 mm)。
- 診斷參考:臨床上FAZ直徑超過0.5 mm懷疑DMI。
FA的缺點包括侵入性(靜脈注射顯影劑)、併發症風險(死亡風險約1/20萬)、所需時間20分鐘以上。
OCTA(光學同調斷層掃描血管成像)
Section titled “OCTA(光學同調斷層掃描血管成像)”OCTA是一種非侵入性、高解析度的檢查,可分層分析SCP(表層毛細血管網)、DCP(深層毛細血管網)和CC(脈絡膜毛細血管層)。
- 優點:無需染料滲漏即可顯示FAZ邊界。可檢測到比FA更廣泛的非灌注區(NPA)2)
- 缺點:偽影,低血流速度下的檢測限制
- NPA分類:存在兩種NPA:(1)伴有視網膜變薄的NPA(FFA可檢測),(2)不伴視網膜變薄的NPA(僅OCTA可檢測)2)
- OCTA黃斑非灌注定量與DR嚴重程度相關,並可檢測臨床前微血管變化3)
OCT和AO-OCT
Section titled “OCT和AO-OCT”- OCT:中心凹內層視網膜變薄或消失與視力下降相關3)
- AO-OCT(自適應光學OCT):可實現單個視錐細胞的三維可視化,在光感受器水平進行DMI評估1)
FA和OCTA的特性比較如下所示。
| 特徵 | FA | OCTA |
|---|---|---|
| 侵入性 | 有 | 無 |
| 分層分析 | 不可 | 可 |
| NPA檢測範圍 | 有限 | 廣泛 |
FA
黃金標準:顯示FAZ擴大和微血管消失。
侵入性:需要靜脈注射顯影劑。死亡風險約1/20萬。
所需時間:需要20分鐘以上。
OCTA
非侵入性、高解析度:可進行SCP/DCP/CC的分層分析。
NPA量化:與DR嚴重程度相關。也可檢測臨床前變化。3)
兩種NPA檢測:根據有無變薄,與FA的檢測範圍不同。2)
FA是黃金標準但有侵入性。OCTA非侵入性,且能檢測出比FA更廣泛的NPA。2) 特別是無視網膜變薄的早期NPA(無變薄NPA)僅能透過OCTA檢測。兩者特性互補,應根據臨床情況酌情使用。
5. 標準治療方法
Section titled “5. 標準治療方法”DMI的直接治療
Section titled “DMI的直接治療”目前,尚無針對DMI的既定特異性治療方法。對於不伴有DME的黃斑缺血,沒有直接的治療方法,全身管理是基礎。
有報告指出良好的血糖控制可能有助於NPA的自然再灌注,2) 內科治療(血糖、血壓、血脂)是抑制視網膜病變進展的基本策略。
在重度NPDR之後的階段,建議考慮PRP(全視網膜光凝)或抗VEGF治療。3)
合併DME時的治療
Section titled “合併DME時的治療”當DMI合併DME時,進行以下治療。
- 抗VEGF藥物(第一線選擇):雷珠單抗(Lucentis)每次0.5mg/0.05mL,阿柏西普(Eylea)每次2mg/0.05mL。效果是暫時的,可能需要頻繁給藥。
- 玻璃體內注射曲安奈德:MacuAid每次4mg/0.1mL。可能存在白內障進展和眼壓升高的風險。
- 局部/格柵樣光凝:DME的輔助治療。
目前尚無針對DMI的既定特異性治療方法。全身管理(血糖、血壓、血脂)是基礎,有病例報告顯示良好的血糖控制可使NPA自然再灌注。2) 合併DME時,使用抗VEGF藥物等治療水腫,但不能直接改善缺血本身。
6. 病理生理學與詳細發病機制
Section titled “6. 病理生理學與詳細發病機制”初期變化:周細胞和內皮細胞損傷
Section titled “初期變化:周細胞和內皮細胞損傷”周細胞消失和內皮細胞損傷是DR血管變化的最早徵兆。
- 周細胞:調節血管張力,產生基底膜和細胞外基質成分
- 內皮細胞:通過緊密連接形成血-視網膜屏障
III型和IV型膠原沉積導致毛細血管基底膜增厚,進而管腔狹窄。還會發生白血球停滯(leukostasis),異常內皮細胞加劇血管閉塞。
毛細血管網的漸進性閉塞
Section titled “毛細血管網的漸進性閉塞”氧氣和微量營養素供應減少刺激VEGF表現,導致毛細血管漸進性萎縮→毛細血管間隙擴大→長期缺氧→感光細胞損傷。隨著DR進展,出現靜脈異常、IRMA、嚴重出血和滲出。3)
黃斑部血管層和感光細胞的影響
Section titled “黃斑部血管層和感光細胞的影響”黃斑部有三層視網膜血管層(SCP、ICP/MCP、DCP)。DCP為感光細胞提供10-15%的氧氣供應,1) 其閉塞直接導致感光細胞損傷。
Müller細胞(MC)在灌流障礙下通過向感光細胞提供乳酸作為能量來源。1) 當MC受損時,除了視錐細胞、視桿細胞和MC功能下降外,還觀察到感光細胞外節片狀消失和毛細血管脫失的共定位。1)
缺血模式的分類
Section titled “缺血模式的分類”缺血模式分為以下四種類型(Takashi等人的分類)。
| 缺血類型 | 頻率 |
|---|---|
| 周邊型 | 2.6% |
| 中間周邊部型 | 61.2% |
| 中心部型 | 26.3% |
| 廣泛型 | 9.9% |
深層微血管叢(DCP)的無灌流導致視細胞的氧氣供應減少(DCP對視細胞氧氣供應的貢獻為10-15%)。1) 穆勒細胞損傷也會阻礙視細胞的能量供應。使用AO-OCT的研究證實,在DCP無灌流區域,視細胞訊號密度(IS/OS和COST)下降約40%。1)
7. 最新研究與未來展望(研究階段報告)
Section titled “7. 最新研究與未來展望(研究階段報告)”先進影像學評估
Section titled “先進影像學評估”Datlinger等人(2021)表明,AO-OCT與OCTA的結合能夠在單一視錐細胞層級評估DMI。他們指出,將微視野計與OCTA相結合的研究方法有助於理解DMI的時間進程,並認為這些先進的影像學參數可能成為未來治療研究的生物標記。1)
微血管阻塞的可逆性與自然再灌流
Section titled “微血管阻塞的可逆性與自然再灌流”傳統上認為微血管阻塞是不可逆的,但已有自然再灌流的病例報告。
Hou等人(2022)觀察到,在HbA1c從6.1%改善至5.6%的糖尿病患者中,NPA發生了自然再灌流。他們透過OCTA記錄了IRMA侵入NPA並形成新微血管網的過程。2)
該報告提示NPA可能具有兩種不同的性質。2)
- 伴有變薄的NPA(晚期變化):再灌流較慢
- 無變薄的NPA(早期變化):2個月內易再灌流,可能是治療介入的「窗口」
定量生物標誌物與預後預測
Section titled “定量生物標誌物與預後預測”在一項為期1年的OCTA追蹤研究中,基線非灌流與DR進展的勝算比(OR)=8.73,深層非灌流與治療介入的OR=3.39,顯示OCTA非灌流指標可能成為預後預測的生物標誌物。已知DMI眼的基線FAZ面積每年擴大5%~10%。AI在OCTA影像分析中的應用也在研究中。3)
儘管罕見,但有自然再灌流的報告。Hou等人(2022)報告了IRMA侵入NPA區域並形成新微血管網的過程。2) 特別是無變薄的NPA(早期變化)在2個月內易再灌流。良好的血糖控制也可能促進再灌流。
8. 參考文獻
Section titled “8. 參考文獻”-
Datlinger F, Georgi T, Stegmann H, et al. Assessment of detailed photoreceptor structure and retinal sensitivity in diabetic macular ischemia using adaptive optics-OCT and microperimetry. Invest Ophthalmol Vis Sci. 2021;62(13):1.
-
Hou S, Chen L, Shan K, et al. Spontaneous retinal reperfusion of capillary nonperfusion areas in diabetic retinopathy. Case Rep Ophthalmol. 2022;13:818-824.
-
American Academy of Ophthalmology Retina/Vitreous Panel. Diabetic Retinopathy Preferred Practice Pattern. Ophthalmology. 2024.
