자각 증상
시력 저하: DME가 없어도 시력이 나쁩니다.
시야 흐림/중심암점: 황반부 허혈에 따른 기능 저하.
시야결손: 허혈 영역에 대응하는 국소 결손.

당뇨병성 황반 허혈(DMI)은 당뇨 환자에서 황반부 망막 모세혈관이 폐쇄, 위축, 소실되고 모세혈관전 세동맥의 협착 및 폐쇄를 나타내는 상태입니다. 형광안저혈관조영술(FA) 또는 광간섭단층혈관조영술(OCTA)에서 중심와 무혈관 영역(FAZ)의 확장 및 불규칙, 황반부의 불연속적 무혈관 영역 확장으로 나타납니다.
역사적으로 Norman Ashton은 사후 안구의 주변 홍채전유착 염색 및 먹물 주입법 연구를 통해 당뇨망막병증에서 동맥 및 모세혈관의 관여를 처음으로 상세히 기술했습니다. 병리학적으로는 말단 세동맥 및 모세혈관전 혈관의 유리질 변성 → 내강 폐쇄 → 동맥 및 모세혈관상 소실 → 정맥측 신생혈관 형성의 과정을 거칩니다.
당뇨병성 황반병증은 황반부종, 허혈성 황반병증, 망막색소상피병증의 세 유형으로 분류되며, DMI는 허혈성 황반병증에 해당합니다.
유병률은 당뇨망막병증의 중증도와 밀접하게 관련됩니다.
| DMI 중증도 | 발생률 |
|---|---|
| 없음 | 39.7% |
| 의심 | 18.4% |
| 경증 | 25.2% |
| 중등도 | 11.0% |
| 중증 | 5.6% |
CSME(임상적으로 유의한 황반부종) 증례의 29.4%에서 DMI가 동반되며, 이 중 19.4%가 중등도~중증입니다. 또한 증식성 당뇨망막병증(PDR)의 77.2%, 중증 비증식성 당뇨망막병증(NPDR)의 59.7%에서 DMI가 관찰됩니다.
DMI 소견은 때때로 “특징 없는 망막(featureless retina)“으로 특징지어집니다. 중심와 반사가 불량해지고, 출혈, 미세혈관류, 삼출물, 연성 백반, 신생혈관이 소실되거나 경미하게 유지됩니다.
자각 증상
시력 저하: DME가 없어도 시력이 나쁩니다.
시야 흐림/중심암점: 황반부 허혈에 따른 기능 저하.
시야결손: 허혈 영역에 대응하는 국소 결손.
임상 소견
기능 검사
미세시야계: DCP 비관류 영역에서 망막 민감도가 현저히 감소. 1)
AO-OCT: DCP 비관류 영역에서 광수용체 신호 밀도(IS/OS, COST)가 약 40% 감소합니다. 1)
DMI 중증도와 시력의 상관관계에 대해, 중등도중증 DMI에서 유의한 시력 저하가 관찰됩니다. VA-FAZ 상관관계는 R²=0.410.51로 보고되며, 시신경유두-황반 간 허혈은 시력 저하와 독립적으로 관련됩니다.
Datlinger 등(2021)은 AO-OCT와 미세시야계를 이용한 연구에서 DCP 비관류 영역에서 광수용체 신호 밀도(IS/OS 및 COST)가 약 40% 감소하고, 해당 영역의 망막 민감도도 현저히 감소함을 보였습니다. 1)
경증 DMI에서는 시력에 유의한 영향이 없을 수 있습니다. 중등도중증이 되면 시력 저하와 유의한 상관관계가 관찰되며(VA-FAZ 상관관계 R²=0.410.51), 시신경유두-황반 간 허혈도 시력 저하와 독립적으로 관련됩니다. DME가 없음에도 시력이 불량한 경우, 「진단 및 검사 방법」 항목의 검사를 통한 DMI 평가가 중요합니다.
DMI의 위험 요인은 당뇨망막병증 전반의 위험 요인을 반영합니다.
DMI의 존재는 DME 및 DR의 중증도 증가와 관련됩니다. 내과적 치료(혈당, 혈압, 지질 관리)는 망막병증 진행 억제에 효과적입니다.
또한, 양호한 혈당 조절(HbA1c 6.1%→5.6%로 개선)을 통해 모세혈관 비관류 영역(NPA)의 자연 재관류가 발생한 증례도 보고되었습니다. 2)
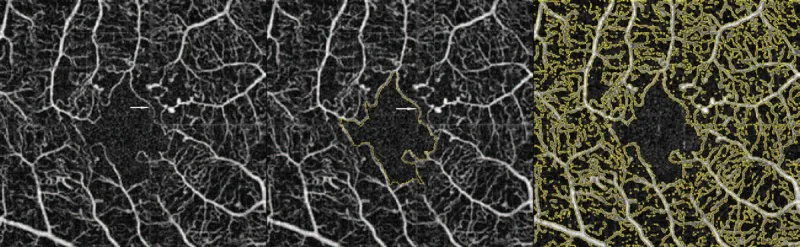
FA는 DMI 진단의 표준 검사입니다.
FA의 단점으로는 침습성(정맥 내 조영제 주입), 합병증 위험(사망 위험 약 1/20만), 소요 시간 20분 이상이 있습니다.
OCTA는 비침습적이고 고해상도의 검사로, SCP(표층 모세혈관망), DCP(심층 모세혈관망), CC(맥락막 모세혈관층)의 층별 분석이 가능합니다.
FA와 OCTA의 특성 비교는 아래와 같습니다.
| 특징 | FA | OCTA |
|---|---|---|
| 침습성 | 있음 | 없음 |
| 층별 분석 | 불가능 | 가능 |
| NPA 검출 범위 | 제한적 | 광범위 |
FA
표준 검사(Gold standard):FAZ 확대 및 모세혈관 소실을 시각화합니다.
침습적:조영제 정맥 주사 필요. 사망 위험 약 1/20만.
소요 시간:20분 이상 소요됩니다.
OCTA
비침습적, 고해상도:SCP/DCP/CC의 층별 분석이 가능합니다.
NPA 정량화:DR 중증도와 상관관계가 있습니다. 임상 전 변화도 검출합니다. 3)
두 가지 NPA 검출:얇아짐 유무에 따라 FA와 검출 범위가 다릅니다. 2)
FA는 표준 검사이지만 침습적입니다. OCTA는 비침습적이며 FA보다 더 광범위한 NPA를 검출할 수 있는 장점이 있습니다. 2) 특히 망막 얇아짐을 동반하지 않은 조기 NPA(얇아짐 없는 NPA)는 OCTA로만 검출 가능합니다. 두 검사의 특성은 상호 보완적이며, 임상 상황에 따라 적절히 사용하는 것이 바람직합니다.
현재 DMI에 대한 확립된 특이적 치료법은 존재하지 않습니다. DME를 동반하지 않은 황반허혈에 대한 직접적인 치료법은 없으며, 전신 관리가 기본입니다.
좋은 혈당 조절이 NPA 자연 재관류에 기여할 가능성이 보고되었으며, 2) 내과적 치료(혈당, 혈압, 지질)가 망막병증 진행 억제의 기본 전략입니다.
중증 NPDR 이후 단계에서는 PRP(전망막광응고술) 또는 항VEGF 치료를 고려하는 것이 권장됩니다. 3)
DMI에 DME가 동반되는 경우 다음과 같은 치료가 시행됩니다.
DMI에 대한 확립된 특이적 치료법은 현재 없습니다. 전신 관리(혈당, 혈압, 지질)가 기본이며, 좋은 혈당 조절로 NPA가 자연 재관류된 증례 보고가 있습니다. 2) DME가 동반된 경우 항VEGF 약물 등으로 부종을 치료하지만, 허혈 자체를 직접 개선할 수는 없습니다.
주세포 소실과 내피세포 손상은 DR 혈관 변화의 가장 초기 징후입니다.
III형 및 IV형 콜라겐 침착으로 인한 모세혈관 기저막 비후가 진행되면 내강이 좁아집니다. 백혈구 정체(leukostasis)도 발생하며, 비정상 내피세포가 유발되어 혈관 폐쇄를 악화시킵니다.
산소 및 미량영양소 공급 감소가 VEGF 발현을 자극하여 모세혈관망의 단계적 위축 → 모세혈관 간격 확대 → 장기 저산소증 → 시세포 손상으로 진행됩니다. DR이 진행됨에 따라 정맥 이상, IRMA, 심한 출혈 및 삼출이 나타납니다. 3)
황반부에는 3층의 망막 혈관층(SCP, ICP/MCP, DCP)이 있습니다. DCP는 시세포 산소 공급에 10~15% 기여하며, 1) 그 폐쇄는 직접적인 시세포 손상으로 이어집니다.
뮐러 세포(MC)는 관류 장애 하에서 시세포에 젖산을 공급하는 에너지원으로 기능합니다. 1) MC 손상이 발생하면 원추세포, 간상세포 및 MC 기능 저하에 더하여 시세포 외절의 패치 모양 소실과 모세혈관 탈락의 공동 위치가 관찰됩니다. 1)
허혈 패턴은 다음 4가지 유형으로 분류됩니다(Takashi 등의 분류).
| 허혈 유형 | 빈도 |
|---|---|
| 주변부형 | 2.6% |
| 중간 주변부형 | 61.2% |
| 중심부형 | 26.3% |
| 광범위형 | 9.9% |
심부 모세혈관망(DCP)의 비관류로 인해 시세포로의 산소 공급이 감소합니다(DCP는 시세포 산소 공급의 10~15%를 담당). 1) 뮐러 세포 손상도 시세포로의 에너지 공급을 저해합니다. AO-OCT를 사용한 연구에서는 DCP 비관류 영역에서 시세포 신호 밀도(IS/OS 및 COST)가 약 40% 감소하는 것이 확인되었습니다. 1)
Datlinger 등(2021)은 AO-OCT와 OCTA의 조합을 통해 단일 원추 시세포 수준에서 DMI 평가가 가능함을 보여주었습니다. 미세시야계와 OCTA를 통합한 연구 접근법이 DMI의 시간 경과 이해에 기여한다고 언급하며, 이러한 첨단 영상 매개변수가 향후 치료 연구에서 바이오마커가 될 가능성을 지적했습니다. 1)
전통적으로 모세혈관 폐쇄는 비가역적인 것으로 여겨졌으나, 자연 재관류 사례가 보고되었습니다.
Hou 등(2022)은 HbA1c가 6.1%에서 5.6%로 개선된 당뇨병 환자에서 NPA의 자연 재관류를 관찰했습니다. IRMA가 NPA 내로 침투하여 새로운 모세혈관망을 형성하는 과정을 OCTA로 시간 경과에 따라 기록했습니다. 2)
이 보고는 NPA에 두 가지 성질이 있음을 시사합니다. 2)
1년간의 OCTA 추적 연구에서 기준선 비관류와 DR 진행의 오즈비(OR)=8.73, 심층 비관류와 치료 개입의 OR=3.39가 보고되어, OCTA 비관류 지표가 예후 예측 바이오마커가 될 가능성이 제시되었습니다. FAZ의 기준선 면적은 알려진 DMI 안에서 연간 5~10% 확장되는 경향이 있습니다. AI의 OCTA 이미지 분석 적용에 대한 연구도 진행 중입니다. 3)
드물지만 자연 재관류 보고가 있습니다. Hou 등(2022)은 IRMA가 NPA 영역으로 침투하여 새로운 모세혈관망을 형성하는 과정을 보고했습니다. 2) 특히 얇아짐이 없는 NPA(초기 변화)는 2개월 이내에 재관류되기 쉬운 경향이 있습니다. 좋은 혈당 조절이 재관류를 촉진할 가능성도 제시되었습니다.
Datlinger F, Georgi T, Stegmann H, et al. Assessment of detailed photoreceptor structure and retinal sensitivity in diabetic macular ischemia using adaptive optics-OCT and microperimetry. Invest Ophthalmol Vis Sci. 2021;62(13):1.
Hou S, Chen L, Shan K, et al. Spontaneous retinal reperfusion of capillary nonperfusion areas in diabetic retinopathy. Case Rep Ophthalmol. 2022;13:818-824.
American Academy of Ophthalmology Retina/Vitreous Panel. Diabetic Retinopathy Preferred Practice Pattern. Ophthalmology. 2024.