อาการที่ผู้ป่วยรู้สึก
การมองเห็นลดลง: การมองเห็นไม่ดีอาจเกิดขึ้นได้แม้ไม่มีจอประสาทตาบวมจากเบาหวาน
ตามัวและจุดบอดกลาง: การทำงานที่ลดลงเนื่องจากการขาดเลือดที่จอประสาทตาส่วนกลาง
ความบกพร่องของลานสายตา: การสูญเสียเฉพาะที่สอดคล้องกับบริเวณที่ขาดเลือด

ภาวะขาดเลือดของจอประสาทตาจากเบาหวาน (DMI) เป็นภาวะในผู้ป่วยเบาหวานที่เส้นเลือดฝอยจอตาบริเวณจอประสาทตาอุดตัน ฝ่อ และหายไป ร่วมกับการตีบและอุดตันของหลอดเลือดแดงเล็กก่อนเส้นเลือดฝอย ในการตรวจ FA หรือ OCTA จะเห็นเป็นการขยายและไม่สม่ำเสมอของ FAZ และการขยายของบริเวณไร้หลอดเลือดที่ไม่ต่อเนื่องในจอประสาทตา
ในอดีต Norman Ashton เป็นคนแรกที่อธิบายรายละเอียดการมีส่วนร่วมของหลอดเลือดแดงและเส้นเลือดฝอยในจอประสาทตาเสื่อมจากเบาหวานผ่านการศึกษาตาหลังเสียชีวิตโดยใช้การย้อมซิเนเคียม่านตาส่วนปลายและการฉีดหมึกจีน ทางพยาธิวิทยา ดำเนินไปดังนี้: การเสื่อมแบบไฮยาลินของหลอดเลือดแดงเล็กส่วนปลายและหลอดเลือดก่อนเส้นเลือดฝอย → การอุดตันของลูเมน → การหายไปของเตียงหลอดเลือดแดงและเส้นเลือดฝอย → การสร้างเส้นเลือดใหม่ทางด้านหลอดเลือดดำ
โรคจอประสาทตาจากเบาหวานแบ่งเป็นสามประเภท: จอประสาทตาบวมน้ำ, จอประสาทตาขาดเลือด, และจอประสาทตาจาก RPE; DMI สอดคล้องกับจอประสาทตาขาดเลือด
ความชุก สัมพันธ์อย่างใกล้ชิดกับความรุนแรงของจอประสาทตาเสื่อมจากเบาหวาน
| ความรุนแรงของ DMI | อุบัติการณ์ |
|---|---|
| ไม่มี | 39.7% |
| สงสัย | 18.4% |
| เล็กน้อย | 25.2% |
| ปานกลาง | 11.0% |
| รุนแรง | 5.6% |
ใน 29.4% ของผู้ป่วยที่มีจอประสาทตาบวมที่มีนัยสำคัญทางคลินิก (CSME) จะเกิด DMI ร่วมด้วย โดย 19.4% มีระดับปานกลางถึงรุนแรง นอกจากนี้ยังพบ DMI ใน 77.2% ของผู้ป่วยเบาหวานขึ้นจอประสาทตาระยะ proliferative (PDR) และ 59.7% ของผู้ป่วยเบาหวานขึ้นจอประสาทตาระยะ nonproliferative ชนิดรุนแรง (NPDR)
อาการแสดงของ DMI อาจถูกอธิบายว่าเป็น “จอประสาทตาไร้ลักษณะเฉพาะ” (featureless retina) การสะท้อนแสงที่รอยบุ๋มจอประสาทตาจะไม่ดี เลือดออก หลอดเลือดโป่งพองขนาดเล็ก สารคัดหลั่ง จุดขาวนิ่ม และเส้นเลือดใหม่จะหายไปหรือมีเพียงเล็กน้อย
อาการที่ผู้ป่วยรู้สึก
การมองเห็นลดลง: การมองเห็นไม่ดีอาจเกิดขึ้นได้แม้ไม่มีจอประสาทตาบวมจากเบาหวาน
ตามัวและจุดบอดกลาง: การทำงานที่ลดลงเนื่องจากการขาดเลือดที่จอประสาทตาส่วนกลาง
ความบกพร่องของลานสายตา: การสูญเสียเฉพาะที่สอดคล้องกับบริเวณที่ขาดเลือด
อาการแสดงทางคลินิก
จอประสาทตาไร้ลักษณะเฉพาะ: การสะท้อนแสงที่รอยบุ๋มจอประสาทตาไม่ดี เลือดออกและสารคัดหลั่งหายไปหรือลดลง
หลอดเลือดผี (Ghost vessels): ซากของหลอดเลือดฝอยที่สูญเสียการไหลเวียน
หลอดเลือดแดงเล็กตีบ: ใน DMI ระดับปานกลางถึงรุนแรง เส้นผ่านศูนย์กลางเฉลี่ยของหลอดเลือดแดงเล็กจะแคบลง
การตรวจการทำงาน
ไมโครเพอริเมทรี (Microperimetry): ความไวของจอประสาทตาลดลงอย่างมากในบริเวณที่ไม่มีการไหลเวียนของหลอดเลือดฝอยชั้นลึก 1)
AO-OCT: ความหนาแน่นสัญญาณของเซลล์รับแสง (IS/OS · COST) ลดลงประมาณ 40% ในบริเวณที่ไม่มีการไหลเวียนเลือดของ DCP 1)
สำหรับความสัมพันธ์ระหว่างความรุนแรงของ DMI และการมองเห็น พบว่าการมองเห็นลดลงอย่างมีนัยสำคัญใน DMI ระดับปานกลางถึงรุนแรง ความสัมพันธ์ VA-FAZ รายงานว่ามีค่า R²=0.41–0.51 และภาวะขาดเลือดระหว่างหัวประสาทตาและรอยบุ๋มจอประสาทตามีความสัมพันธ์อย่างอิสระกับการมองเห็นที่ลดลง
Datlinger และคณะ (2021) ในการศึกษาโดยใช้ AO-OCT และไมโครเพอริเมทรี แสดงให้เห็นว่าความหนาแน่นสัญญาณของเซลล์รับแสง (IS/OS และ COST) ลดลงประมาณ 40% ในบริเวณที่ไม่มีการไหลเวียนเลือดของ DCP และความไวของจอประสาทตาในบริเวณนั้นก็ลดลงอย่างมีนัยสำคัญเช่นกัน 1)
ใน DMI ระดับเล็กน้อย อาจไม่มีผลกระทบอย่างมีนัยสำคัญต่อการมองเห็น ใน DMI ระดับปานกลางถึงรุนแรง พบความสัมพันธ์อย่างมีนัยสำคัญกับการมองเห็นที่ลดลง (ความสัมพันธ์ VA-FAZ R²=0.41–0.51) และภาวะขาดเลือดระหว่างหัวประสาทตาและรอยบุ๋มจอประสาทตามีความสัมพันธ์อย่างอิสระกับการมองเห็นที่ลดลง หากการมองเห็นไม่ดีแม้ไม่มี DME การประเมิน DMI ผ่านการตรวจในส่วน «การวินิจฉัยและวิธีการตรวจ» จึงมีความสำคัญ
ปัจจัยเสี่ยงของ DMI สะท้อนถึงปัจจัยเสี่ยงของจอประสาทตาเสื่อมจากเบาหวานโดยทั่วไป
การมี DMI สัมพันธ์กับความรุนแรงของ DME และ DR ที่เพิ่มขึ้น การรักษาทางอายุรกรรม (การควบคุมระดับน้ำตาล ความดันโลหิต และไขมัน) มีประสิทธิภาพในการยับยั้งการดำเนินของจอประสาทตาเสื่อม
ทั้งนี้ มีรายงานกรณีที่มีการไหลเวียนเลือดกลับมาเองในบริเวณที่ไม่มีการไหลเวียนของเส้นเลือดฝอย (NPA) หลังจากการควบคุมระดับน้ำตาลในเลือดดีขึ้น (การปรับปรุง HbA1c จาก 6.1% เป็น 5.6%) 2)
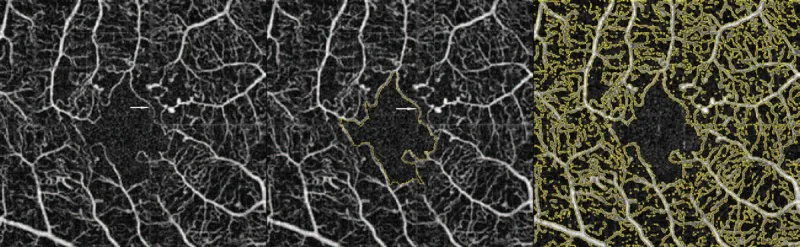
FA เป็นมาตรฐานทองคำในการวินิจฉัย DMI
ข้อเสียของ FA ได้แก่ การรุกล้ำ (ฉีดสารทึบรังสีทางหลอดเลือดดำ), ความเสี่ยงของภาวะแทรกซ้อน (ความเสี่ยงเสียชีวิตประมาณ 1/200,000), ใช้เวลาประมาณ 20 นาทีหรือมากกว่า
OCTA เป็นการตรวจที่ไม่รุกล้ำและมีความละเอียดสูง สามารถวิเคราะห์แยกชั้นของ SCP (โครงข่ายเส้นเลือดฝอยชั้นผิว), DCP (โครงข่ายเส้นเลือดฝอยชั้นลึก) และ CC (ชั้นเส้นเลือดฝอยคอรอยด์)
การเปรียบเทียบลักษณะของ FA และ OCTA แสดงไว้ด้านล่าง
| ลักษณะ | FA | OCTA |
|---|---|---|
| การรุกราน | มี | ไม่มี |
| การวิเคราะห์แยกชั้น | ไม่สามารถ | สามารถ |
| ขอบเขตการตรวจหา NPA | จำกัด | กว้าง |
FA
มาตรฐานทองคำ: แสดงการขยายของ FAZ และการหายไปของเส้นเลือดฝอย
รุกราน: ต้องฉีดสารทึบรังสีทางหลอดเลือดดำ ความเสี่ยงเสียชีวิตประมาณ 1/200,000
ระยะเวลาที่ใช้: ใช้เวลา 20 นาทีขึ้นไป
OCTA
ไม่รุกรานและความละเอียดสูง: สามารถวิเคราะห์ชั้น SCP/DCP/CC ได้
การวัดปริมาณ NPA: สัมพันธ์กับความรุนแรงของ DR ตรวจพบการเปลี่ยนแปลงก่อนทางคลินิกได้ด้วย 3)
การตรวจหา NPA สองแบบ: ขอบเขตการตรวจหาแตกต่างจาก FA ขึ้นอยู่กับการมีหรือไม่มีจอประสาทตาบาง 2)
FA เป็นมาตรฐานทองคำแต่รุกราน OCTA ไม่รุกรานและมีข้อดีคือตรวจพบ NPA ได้กว้างกว่า FA 2) โดยเฉพาะ NPA ระยะแรกที่ไม่มีจอประสาทตาบาง (NPA ไม่บาง) สามารถตรวจพบได้ด้วย OCTA เท่านั้น ลักษณะของทั้งสองเสริมกัน ควรเลือกใช้ตามสถานการณ์ทางคลินิก
ปัจจุบันยังไม่มีการรักษาเฉพาะที่ได้รับการยืนยันสำหรับ DMI ไม่มีการรักษาโดยตรงสำหรับภาวะขาดเลือดของจอประสาทตาที่ไม่มี DME และการจัดการทั่วร่างกายเป็นพื้นฐาน
มีการรายงานว่าการควบคุมระดับน้ำตาลในเลือดที่ดีอาจช่วยให้ NPA เกิดการไหลเวียนเลือดกลับมาเองได้ 2) และการรักษาทางอายุรกรรม (ระดับน้ำตาลในเลือด ความดันโลหิต ไขมัน) เป็นกลยุทธ์พื้นฐานในการยับยั้งการดำเนินของจอประสาทตาเสื่อม
ในระยะ severe NPDR ขึ้นไป แนะนำให้พิจารณา PRP (การจี้แสงทั่วจอประสาทตา) หรือการรักษาด้วยยาต้าน VEGF 3)
เมื่อ DMI มี DME ร่วม จะทำการรักษาดังต่อไปนี้
ปัจจุบันยังไม่มีการรักษาเฉพาะที่ได้รับการยืนยันสำหรับ DMI การจัดการทั่วร่างกาย (ระดับน้ำตาลในเลือด ความดันโลหิต ไขมัน) เป็นพื้นฐาน และมีรายงานผู้ป่วยที่ NPA เกิดการไหลเวียนเลือดกลับมาเองด้วยการควบคุมระดับน้ำตาลที่ดี 2) หากมี DME ร่วม จะรักษาอาการบวมน้ำด้วยยาต้าน VEGF เป็นต้น แต่ไม่สามารถทำให้ภาวะขาดเลือดดีขึ้นโดยตรงได้
การสูญเสียเพอริไซต์และความเสียหายของเซลล์บุผนังหลอดเลือดเป็นสัญญาณเริ่มต้นที่สุดของการเปลี่ยนแปลงหลอดเลือดใน DR
เมื่อเยื่อหุ้มชั้นฐานของเส้นเลือดฝอยหนาตัวขึ้นเนื่องจากการสะสมของคอลลาเจนชนิดที่ 3 และ 4 ทำให้รูหลอดเลือดแคบลง เกิดเม็ดเลือดขาวคั่ง (leukostasis) ซึ่งทำให้หลอดเลือดอุดตันรุนแรงขึ้นโดยกระตุ้นเซลล์บุผนังหลอดเลือดที่ผิดปกติ
การลดลงของออกซิเจนและสารอาหารระดับจุลภาคกระตุ้นการแสดงออกของ VEGF นำไปสู่การฝ่อแบบค่อยเป็นค่อยไปของเครือข่ายเส้นเลือดฝอย → การขยายช่องว่างระหว่างเส้นเลือดฝอย → ภาวะขาดออกซิเจนเรื้อรัง → ความเสียหายต่อเซลล์รับแสง เมื่อ DR ดำเนินไป จะเกิดความผิดปกติของหลอดเลือดดำ IRMA เลือดออกรุนแรง และสารคัดหลั่ง 3)
ที่จอประสาทตาส่วนกลางมีชั้นหลอดเลือดจอตาสามชั้น (SCP, ICP/MCP, DCP) DCP มีส่วนช่วย 10-15% ในการให้ออกซิเจนแก่เซลล์รับแสง 1) และการอุดตันของชั้นนี้นำไปสู่ความเสียหายโดยตรงต่อเซลล์รับแสง
เซลล์มุลเลอร์ (MC) ทำหน้าที่เป็นแหล่งพลังงานโดยให้แลคเตตแก่เซลล์รับแสงภายใต้สภาวะการไหลเวียนเลือดบกพร่อง 1) เมื่อเกิดความเสียหายต่อ MC นอกจากการลดลงของการทำงานของเซลล์รูปกรวย เซลล์รูปแท่ง และ MC แล้ว ยังพบการหายไปเป็นหย่อมๆ ของส่วนนอกของเซลล์รับแสงและการอยู่ร่วมกันกับการสูญเสียเส้นเลือดฝอย 1)
รูปแบบของภาวะขาดเลือดจำแนกเป็นสี่ประเภท (การจำแนกของ Takashi และคณะ)
| ประเภทของภาวะขาดเลือด | ความถี่ |
|---|---|
| ชนิดรอบนอก | 2.6% |
| ชนิดรอบนอกกลาง | 61.2% |
| ชนิดส่วนกลาง | 26.3% |
| ชนิดกว้างขวาง | 9.9% |
การไม่มีการไหลเวียนเลือดของ DCP (โครงข่ายเส้นเลือดฝอยชั้นลึก) ทำให้การส่งออกซิเจนไปยังเซลล์รับแสงลดลง (DCP มีส่วนช่วย 10-15% ในการส่งออกซิเจนไปยังเซลล์รับแสง) 1) ความเสียหายของเซลล์มุลเลอร์ยังขัดขวางการส่งพลังงานไปยังเซลล์รับแสง การศึกษาโดยใช้ AO-OCT ยืนยันว่าความหนาแน่นของสัญญาณเซลล์รับแสง IS/OS และ COST ลดลงประมาณ 40% ในบริเวณที่ไม่มีการไหลเวียนเลือดของ DCP 1)
Datlinger และคณะ (2021) แสดงให้เห็นว่าการรวมกันของ AO-OCT และ OCTA ช่วยให้สามารถประเมิน DMI ในระดับเซลล์รูปกรวยเดี่ยวได้ พวกเขากล่าวว่าแนวทางการวิจัยที่บูรณาการไมโครเพอริเมทรีและ OCTA มีส่วนช่วยในการเข้าใจระยะเวลาของ DMI และชี้ให้เห็นว่าพารามิเตอร์การถ่ายภาพขั้นสูงเหล่านี้อาจกลายเป็นตัวบ่งชี้ทางชีวภาพในการวิจัยการรักษาในอนาคต 1)
ตามธรรมเนียมแล้ว การอุดตันของเส้นเลือดฝอยถือว่าไม่สามารถฟื้นคืนได้ แต่มีรายงานกรณีที่มีการไหลเวียนเลือดกลับมาเอง
Hou และคณะ (2022) สังเกตเห็นการไหลเวียนเลือดกลับมาเองของ NPA ในผู้ป่วยเบาหวานที่ HbA1c ดีขึ้นจาก 6.1% เป็น 5.6% กระบวนการที่ IRMA บุกรุกเข้าไปใน NPA และสร้างเครือข่ายเส้นเลือดฝอยใหม่ถูกบันทึกตามลำดับเวลาด้วย OCTA 2)
รายงานนี้ชี้ให้เห็นว่า NPA มีคุณสมบัติสองประเภท 2)
ในการศึกษาติดตามผล OCTA เป็นเวลา 1 ปี มีรายงานอัตราส่วนออดส์ (OR) = 8.73 สำหรับการไม่มีการไหลเวียนเลือดพื้นฐานและการดำเนินของจอประสาทตาเสื่อมจากเบาหวาน และ OR = 3.39 สำหรับการไม่มีการไหลเวียนเลือดในชั้นลึกและการแทรกแซงการรักษา ซึ่งบ่งชี้ว่าดัชนีการไม่มีการไหลเวียนเลือดจาก OCTA อาจเป็นตัวบ่งชี้ทางชีวภาพในการพยากรณ์โรค พื้นที่ FAZ พื้นฐานมีแนวโน้มขยายตัว 5-10% ต่อปีในดวงตาที่ทราบว่าเป็น DMI การประยุกต์ใช้ AI ในการวิเคราะห์ภาพ OCTA ก็กำลังอยู่ระหว่างการวิจัย 3)
แม้จะพบได้ยาก แต่มีรายงานการไหลเวียนเลือดกลับมาเอง Hou และคณะ (2022) รายงานกระบวนการที่ IRMA บุกรุกพื้นที่ NPA และสร้างเครือข่ายเส้นเลือดฝอยใหม่ 2) โดยเฉพาะ NPA ที่ไม่มีการบางลง (การเปลี่ยนแปลงระยะแรก) มีแนวโน้มที่จะไหลเวียนเลือดกลับมาภายใน 2 เดือน การควบคุมระดับน้ำตาลในเลือดที่ดีอาจส่งเสริมการไหลเวียนเลือดกลับมาได้เช่นกัน
Datlinger F, Georgi T, Stegmann H, et al. Assessment of detailed photoreceptor structure and retinal sensitivity in diabetic macular ischemia using adaptive optics-OCT and microperimetry. Invest Ophthalmol Vis Sci. 2021;62(13):1.
Hou S, Chen L, Shan K, et al. Spontaneous retinal reperfusion of capillary nonperfusion areas in diabetic retinopathy. Case Rep Ophthalmol. 2022;13:818-824.
American Academy of Ophthalmology Retina/Vitreous Panel. Diabetic Retinopathy Preferred Practice Pattern. Ophthalmology. 2024.