Síntomas subjetivos
Pérdida de visión: Mala visión incluso sin DME.
Visión borrosa/escotoma central: Deterioro funcional debido a isquemia macular.
Defecto del campo visual: Defecto localizado correspondiente al área isquémica.

La isquemia macular diabética (DMI) es una condición en pacientes diabéticos donde los capilares retinianos en la mácula se ocluyen, atrofian y pierden, con estrechamiento y oclusión de las arteriolas precapilares. Se visualiza como agrandamiento e irregularidad de la zona avascular foveal (FAZ) y expansión de áreas avasculares discontinuas en la mácula en la angiografía con fluoresceína (FA) o la angiografía por tomografía de coherencia óptica (OCTA).
Históricamente, Norman Ashton describió por primera vez en detalle la participación de arterias y capilares en la retinopatía diabética mediante estudios post mórtem con tinción de sinequias iridianas periféricas e inyección de tinta china. Patológicamente, el proceso implica degeneración hialina de arteriolas terminales y vasos precapilares → oclusión luminal → pérdida de lechos arteriolares y capilares → formación de neovascularización venosa.
La maculopatía diabética se clasifica en tres tipos: edema macular, maculopatía isquémica y retinopatía del epitelio pigmentario; la DMI corresponde a la maculopatía isquémica.
La prevalencia está estrechamente relacionada con la gravedad de la retinopatía diabética.
| Gravedad de la DMI | Incidencia |
|---|---|
| Ninguno | 39.7% |
| Sospechoso | 18.4% |
| Leve | 25.2% |
| Moderado | 11.0% |
| Grave | 5.6% |
El 29.4% de los casos de CSME (edema macular clínicamente significativo) presentan DMI, de los cuales el 19.4% son de moderados a graves. Además, se encuentra DMI en el 77.2% de la retinopatía diabética proliferativa (RDP) y en el 59.7% de la retinopatía diabética no proliferativa grave (RDNP).
Los hallazgos de DMI a veces se caracterizan como una “retina sin rasgos distintivos”. El reflejo foveal se vuelve deficiente, y las hemorragias, microaneurismas, exudados, exudados blandos y neovascularización desaparecen o se vuelven leves.
Síntomas subjetivos
Pérdida de visión: Mala visión incluso sin DME.
Visión borrosa/escotoma central: Deterioro funcional debido a isquemia macular.
Defecto del campo visual: Defecto localizado correspondiente al área isquémica.
Hallazgos clínicos
Retina sin rasgos distintivos: Reflejo foveal deficiente, desaparición o reducción de hemorragias y exudados.
Vasos fantasma: Sombras residuales de capilares que han perdido la perfusión.
Estrechamiento arteriolar: En DMI moderada a grave, el diámetro arteriolar medio se estrecha.
Pruebas funcionales
Microperimetría: La sensibilidad retiniana se reduce notablemente en las áreas de no perfusión del DCP. 1)
AO-OCT: En áreas de no perfusión del DCP, la densidad de señal de los fotorreceptores (IS/OS, COST) se reduce aproximadamente un 40%. 1)
En cuanto a la correlación entre la gravedad de la DMI y la agudeza visual, se observa una disminución significativa de la agudeza visual en la DMI moderada a grave. La correlación VA-FAZ se ha reportado como R² = 0.41–0.51, y la isquemia papilomacular se asocia de forma independiente con la disminución de la agudeza visual.
Datlinger et al. (2021) utilizaron AO-OCT y microperimetría para demostrar que en las áreas de no perfusión del DCP, la densidad de señal de los fotorreceptores (IS/OS y COST) disminuyó aproximadamente un 40%, y la sensibilidad retiniana en la misma área también se redujo notablemente. 1)
La DMI leve puede no tener un impacto significativo en la agudeza visual. En casos moderados a graves, se observa una correlación significativa con la disminución de la agudeza visual (correlación VA-FAZ R² = 0.41–0.51), y la isquemia papilomacular también se asocia de forma independiente con la disminución de la agudeza visual. Si la agudeza visual es mala a pesar de la ausencia de DME, es importante evaluar la DMI mediante las pruebas descritas en la sección “Diagnóstico y métodos de prueba”.
Los factores de riesgo de la DMI reflejan los factores de riesgo generales de la retinopatía diabética.
La presencia de DMI se asocia con un aumento de la gravedad de la DME y la RD. El tratamiento médico (control de glucosa, presión arterial y lípidos) es eficaz para retardar la progresión de la retinopatía.
Además, se ha reportado un caso de reperfusión espontánea de áreas de no perfusión capilar (NPA) tras una mejora del control glucémico (HbA1c de 6.1% a 5.6%). 2)
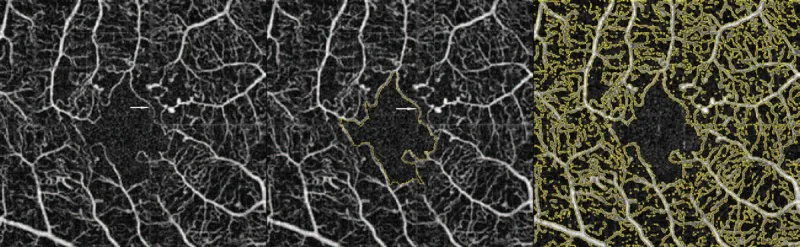
La FA es el estándar de oro para diagnosticar DMI.
Las desventajas de la FA incluyen invasividad (inyección de contraste intravenoso), riesgo de complicaciones (riesgo de muerte aproximadamente 1 en 200,000) y un tiempo de procedimiento de 20 minutos o más.
La OCTA es un examen no invasivo y de alta resolución que permite el análisis por capas del SCP (plexo capilar superficial), DCP (plexo capilar profundo) y CC (coriocapilar).
A continuación se muestra una comparación de las características de la FA y la OCTA.
| Característica | FA | OCTA |
|---|---|---|
| Invasividad | Sí | No |
| Análisis por capas | No posible | Posible |
| Rango de detección de NPA | Limitado | Extenso |
FA
Estándar de oro: Visualiza el agrandamiento de la FAZ y la pérdida capilar.
Invasivo: Requiere inyección intravenosa de contraste. Riesgo de muerte aproximadamente 1 en 200,000.
Tiempo requerido: Toma 20 minutos o más.
OCTA
No invasivo, alta resolución: Permite el análisis por capas de SCP/DCP/CC.
Cuantificación de NPA: Se correlaciona con la gravedad de la DR. También detecta cambios preclínicos. 3)
Dos tipos de detección de NPA: El rango de detección difiere de la FA según la presencia o ausencia de adelgazamiento. 2)
La FA es el estándar de oro pero es invasiva. La OCTA es no invasiva y tiene la ventaja de detectar NPA más extensos que la FA. 2) En particular, los NPA tempranos sin adelgazamiento retiniano (NPA sin adelgazamiento) solo se pueden detectar con OCTA. Las características de ambos son complementarias, y es deseable usarlos adecuadamente según la situación clínica.
Actualmente, no existe un tratamiento específico establecido para la DMI. No hay un tratamiento directo para la isquemia macular sin DME, y el manejo sistémico es fundamental.
Se ha informado que un buen control glucémico puede contribuir a la reperfusión natural de las NPA, 2) y el tratamiento médico (glucosa, presión arterial, lípidos) es la estrategia básica para suprimir la progresión de la retinopatía.
En etapas posteriores a la NPDR grave, se recomienda considerar la PRP (fotocoagulación panretiniana) o la terapia anti-VEGF. 3)
Cuando la DMI se complica con DME, se realizan los siguientes tratamientos.
Actualmente, no existe un tratamiento específico establecido para la DMI. El manejo sistémico (glucosa, presión arterial, lípidos) es fundamental, y hay informes de casos de reperfusión natural de NPA con buen control glucémico. 2) Cuando hay DME concomitante, se trata el edema con fármacos anti-VEGF, etc., pero la isquemia en sí misma no puede mejorarse directamente.
La pérdida de pericitos y el daño a las células endoteliales son los signos más tempranos de los cambios vasculares en la DR.
El engrosamiento progresivo de la membrana basal capilar debido a la deposición de colágeno tipo III y IV conduce al estrechamiento de la luz. También se produce leucostasis, y las células endoteliales anormales exacerban la oclusión vascular.
La reducción del suministro de oxígeno y micronutrientes estimula la expresión de VEGF, lo que lleva a atrofia capilar progresiva → ensanchamiento de los espacios intercapilares → hipoxia prolongada → daño fotorreceptor. A medida que la DR progresa, aparecen anomalías venosas, IRMA, hemorragia grave y exudación. 3)
La mácula tiene tres capas vasculares retinianas (SCP, ICP/MCP, DCP). La DCP contribuye entre un 10 y un 15% al suministro de oxígeno a los fotorreceptores, 1) y su oclusión conduce directamente al daño fotorreceptor.
Las células de Müller (MC) funcionan como fuente de energía al suministrar lactato a los fotorreceptores bajo alteración de la perfusión. 1) Cuando ocurre daño a las MC, además de la disfunción de conos, bastones y MC, se observa pérdida parcheada de los segmentos externos de los fotorreceptores y colocalización con la pérdida capilar. 1)
Los patrones isquémicos se clasifican en los siguientes cuatro tipos (clasificación de Takashi et al.).
| Tipo de isquemia | Frecuencia |
|---|---|
| Tipo periférico | 2.6% |
| Tipo medioperiférico | 61.2% |
| Tipo central | 26.3% |
| Tipo extenso | 9.9% |
La no perfusión del plexo capilar profundo (DCP) reduce el suministro de oxígeno a los fotorreceptores (el DCP contribuye entre un 10 y un 15% del suministro de oxígeno a los fotorreceptores). 1) El daño a las células de Müller también afecta el suministro de energía a los fotorreceptores. Estudios con AO-OCT han confirmado que la densidad de señal de los fotorreceptores (IS/OS y COST) disminuye aproximadamente un 40% en áreas de no perfusión del DCP. 1)
Datlinger y colaboradores (2021) demostraron que la combinación de AO-OCT y OCTA permite la evaluación de DMI a nivel de cono fotorreceptor único. Señalaron que un enfoque de investigación que integre microperimetría y OCTA contribuye a comprender la evolución temporal de la DMI, y sugirieron que estos parámetros de imagen avanzada podrían servir como biomarcadores en futuros estudios terapéuticos. 1)
Tradicionalmente, la oclusión capilar se consideraba irreversible, pero se han reportado casos de reperfusión espontánea.
Hou et al. (2022) observaron reperfusión espontánea de NPA en pacientes diabéticos cuya HbA1c mejoró de 6.1% a 5.6%. Registraron el proceso de IRMA invadiendo la NPA y formando nuevas redes capilares a lo largo del tiempo mediante OCTA. 2)
Este informe sugiere que las NPA pueden tener dos tipos de características. 2)
En un estudio de seguimiento de OCTA de 1 año, se reportó una odds ratio (OR) de 8.73 para la no perfusión basal y la progresión de la RD, y una OR de 3.39 para la no perfusión profunda y la intervención terapéutica, lo que sugiere que los índices de no perfusión en OCTA pueden ser biomarcadores pronósticos. El área basal de la FAZ tiende a expandirse un 5-10% anual en ojos con DMI conocida. También se está investigando la aplicación de IA al análisis de imágenes de OCTA. 3)
Aunque es raro, se ha reportado reperfusión espontánea. Hou et al. (2022) reportaron el proceso de IRMA invadiendo el área de NPA y formando nuevas redes capilares. 2) En particular, las NPA sin adelgazamiento (cambios tempranos) tienden a reperfundirse dentro de los 2 meses. Un buen control glucémico también puede promover la reperfusión.
Datlinger F, Georgi T, Stegmann H, et al. Assessment of detailed photoreceptor structure and retinal sensitivity in diabetic macular ischemia using adaptive optics-OCT and microperimetry. Invest Ophthalmol Vis Sci. 2021;62(13):1.
Hou S, Chen L, Shan K, et al. Spontaneous retinal reperfusion of capillary nonperfusion areas in diabetic retinopathy. Case Rep Ophthalmol. 2022;13:818-824.
American Academy of Ophthalmology Retina/Vitreous Panel. Diabetic Retinopathy Preferred Practice Pattern. Ophthalmology. 2024.