علائم ذهنی
کاهش بینایی: حتی بدون DME نیز بینایی ضعیف میشود.
تاری دید و اسکوتوم مرکزی: کاهش عملکرد به دلیل ایسکمی ماکولا.
نقص میدان بینایی: نقص موضعی مطابق با ناحیه ایسکمیک.

ایسکمی ماکولای دیابتی (DMI) وضعیتی است که در بیماران دیابتی، مویرگهای شبکیه در ماکولا مسدود، آتروفی و ناپدید میشوند و تنگی و انسداد شریانهای پیشمویرگی رخ میدهد. در FA (آنژیوگرافی فلورسئین) یا OCTA (آنژیوگرافی توموگرافی همدوسی نوری)، به صورت بزرگ شدن و نامنظمی FAZ (ناحیه بدون عروق فووئال) و گسترش نواحی بدون عروق غیرمتصل در ماکولا دیده میشود.
از نظر تاریخی، نورمن اشتون اولین بار با مطالعه بر روی چشمهای پس از مرگ با استفاده از رنگآمیزی PAS و تزریق جوهر هندی، نقش شریانها و مویرگها را در رتینوپاتی دیابتی به طور دقیق توصیف کرد. از نظر پاتولوژیک، این فرآیند شامل دژنراسیون هیالین شریانهای انتهایی و عروق پیشمویرگی → انسداد لومن → از بین رفتن بستر شریانی و مویرگی → تشکیل عروق جدید در سمت وریدی است.
ماکولوپاتی دیابتی به سه نوع ادم ماکولا، ماکولوپاتی ایسکمیک و ماکولوپاتی RPE تقسیم میشود که DMI معادل ماکولوپاتی ایسکمیک است.
شیوع با شدت رتینوپاتی دیابتی ارتباط نزدیک دارد.
| شدت DMI | میزان بروز |
|---|---|
| هیچ | 39.7% |
| مشکوک | 18.4% |
| خفیف | 25.2% |
| متوسط | 11.0% |
| شدید | 5.6% |
در 29.4% موارد CSME (ادم ماکولار بالینی معنادار) DMI رخ میدهد که 19.4% از آنها متوسط تا شدید هستند. همچنین DMI در 77.2% رتینوپاتی دیابتی پرولیفراتیو (PDR) و 59.7% رتینوپاتی دیابتی غیرپرولیفراتیو شدید (NPDR) مشاهده میشود.
یافتههای DMI گاهی به عنوان «شبکیه بدون ویژگی» توصیف میشود. رفلکس فووئال ضعیف میشود و خونریزیها، میکروآنوریسمها، ترشحات، لکههای نرم و عروق جدید ناپدید یا خفیف میشوند.
علائم ذهنی
کاهش بینایی: حتی بدون DME نیز بینایی ضعیف میشود.
تاری دید و اسکوتوم مرکزی: کاهش عملکرد به دلیل ایسکمی ماکولا.
نقص میدان بینایی: نقص موضعی مطابق با ناحیه ایسکمیک.
یافتههای بالینی
شبکیه بدون ویژگی: رفلکس فووئال ضعیف، ناپدید شدن یا خفیف شدن خونریزیها و ترشحات.
عروق شبحی: بقایای مویرگهایی که پرفیوژن خود را از دست دادهاند.
باریک شدن شریانچهها: در DMI متوسط تا شدید، قطر متوسط شریانچهها کاهش مییابد.
آزمایشهای عملکردی
میکروپریمتری: حساسیت شبکیه در نواحی غیرپرفیوژن DCP به طور قابل توجهی کاهش مییابد. 1)
AO-OCT: در ناحیه غیرپرفیوژن DCP، تراکم سیگنال سلولهای بینایی (IS/OS و COST) حدود 40% کاهش مییابد. 1)
در مورد همبستگی بین شدت DMI و حدت بینایی، در DMI متوسط تا شدید کاهش معنیدار حدت بینایی مشاهده میشود. همبستگی VA-FAZ با R²=0.41 تا 0.51 گزارش شده است و ایسکمی بین پاپیلای عصب بینایی و ماکولا به طور مستقل با کاهش حدت بینایی مرتبط است.
Datlinger و همکاران (2021) در مطالعهای با استفاده از AO-OCT و میکروپریمتری نشان دادند که در ناحیه غیرپرفیوژن DCP، تراکم سیگنال سلولهای بینایی (IS/OS و COST) حدود 40% کاهش یافته و حساسیت شبکیه در همان ناحیه نیز به طور قابل توجهی کاهش مییابد. 1)
در DMI خفیف ممکن است تأثیر معنیداری بر حدت بینایی ایجاد نشود. در موارد متوسط تا شدید، همبستگی معنیداری با کاهش حدت بینایی مشاهده میشود (همبستگی VA-FAZ R²=0.41 تا 0.51) و ایسکمی بین پاپیلای عصب بینایی و ماکولا نیز به طور مستقل با کاهش حدت بینایی مرتبط است. در صورت وجود حدت بینایی ضعیف بدون DME، ارزیابی DMI با استفاده از آزمایشهای ذکر شده در بخش «تشخیص و روشهای آزمایش» اهمیت دارد.
عوامل خطر DMI منعکسکننده عوامل خطر کلی رتینوپاتی دیابتی هستند.
وجود DMI با افزایش شدت DME و DR مرتبط است. درمان داخلی (کنترل قند خون، فشار خون و چربی) در مهار پیشرفت رتینوپاتی مؤثر است.
ضمناً، مواردی از بازپرفیوژن خودبهخودی ناحیه غیرپرفیوژن مویرگی (NPA) با بهبود کنترل قند خون (کاهش HbA1c از 6.1% به 5.6%) گزارش شده است. 2)
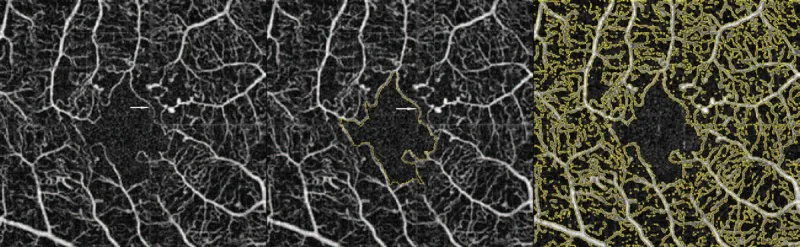
FA استاندارد طلایی تشخیص DMI است.
معایب FA شامل تهاجمی بودن (تزریق ماده حاجب داخل وریدی)، خطر عوارض (خطر مرگ حدود 1 در 200,000) و زمان لازم بیش از 20 دقیقه است.
OCTA یک آزمایش غیرتهاجمی و با وضوح بالا است که امکان تحلیل لایهای SCP (شبکه مویرگی سطحی)، DCP (شبکه مویرگی عمقی) و CC (لایه مویرگی کوروئید) را فراهم میکند.
مقایسه ویژگیهای FA و OCTA در زیر نشان داده شده است.
| ویژگی | FA | OCTA |
|---|---|---|
| تهاجمی بودن | دارد | ندارد |
| تحلیل لایهای | غیرممکن | ممکن |
| محدوده تشخیص NPA | محدود | گسترده |
FA
استاندارد طلایی: بزرگ شدن FAZ و ناپدید شدن مویرگها را نشان میدهد.
تهاجمی: نیاز به تزریق وریدی ماده حاجب دارد. خطر مرگ حدود 1 در 200,000.
زمان مورد نیاز: 20 دقیقه یا بیشتر طول میکشد.
OCTA
غیرتهاجمی و با وضوح بالا: امکان تحلیل لایهای SCP/DCP/CC را فراهم میکند.
کمیسازی NPA: با شدت DR همبستگی دارد. تغییرات پیشبالینی را نیز تشخیص میدهد. 3)
تشخیص دو نوع NPA: بسته به وجود یا عدم وجود نازکشدگی، محدوده تشخیص با FA متفاوت است. 2)
FA استاندارد طلایی است اما تهاجمی میباشد. OCTA غیرتهاجمی است و مزیت تشخیص NPA گستردهتری نسبت به FA دارد. 2) به ویژه NPA اولیه بدون نازکشدگی شبکیه (NPA بدون نازکشدگی) فقط با OCTA قابل تشخیص است. ویژگیهای این دو روش مکمل یکدیگر هستند و بسته به شرایط بالینی باید از آنها استفاده کرد.
در حال حاضر هیچ درمان اختصاصی اثبات شدهای برای DMI وجود ندارد. برای ایسکمی ماکولا بدون DME درمان مستقیمی وجود ندارد و مدیریت سیستمیک اساس درمان است.
گزارش شده است که کنترل خوب قند خون ممکن است به بازپرفیوژن خودبهخودی NPA کمک کند. 2) درمان داخلی (قند خون، فشار خون، چربی خون) استراتژی اساسی برای مهار پیشرفت رتینوپاتی است.
در مراحل بعد از severe NPDR، انجام PRP (پان رتینال فوتوکوآگولاسیون) یا درمان ضد VEGF توصیه میشود. 3)
در صورت همراهی DMI با DME، درمانهای زیر انجام میشود.
در حال حاضر هیچ درمان اختصاصی اثبات شدهای برای DMI وجود ندارد. مدیریت سیستمیک (قند خون، فشار خون، چربی خون) اساس درمان است و گزارش مواردی از بازپرفیوژن خودبهخودی NPA با کنترل خوب قند خون وجود دارد. 2) در صورت همراهی با DME، با داروهای ضد VEGF ورم درمان میشود، اما نمیتوان خود ایسکمی را مستقیماً بهبود بخشید.
از دست دادن سلولهای پریسیت و آسیب سلولهای اندوتلیال اولین نشانههای تغییرات عروقی در رتینوپاتی دیابتی هستند.
ضخیم شدن غشای پایه مویرگی به دلیل رسوب کلاژن نوع III و IV باعث تنگ شدن مجرا میشود. ایستایی لکوسیتها (leukostasis) نیز رخ میدهد و سلولهای اندوتلیال غیرطبیعی را القا کرده و انسداد عروق را تشدید میکند.
کاهش اکسیژن و مواد مغذی باعث تحریک بیان VEGF و پیشرفت به سمت آتروفی تدریجی شبکه مویرگی → افزایش فاصله بین مویرگها → هیپوکسی طولانی مدت → آسیب سلولهای بینایی میشود. با پیشرفت رتینوپاتی دیابتی، ناهنجاریهای وریدی، IRMA، خونریزی شدید و ترشحات ظاهر میشوند. 3)
ماکولا دارای سه لایه عروق شبکیه (SCP، ICP/MCP، DCP) است. DCP حدود 10-15٪ از اکسیژن سلولهای بینایی را تأمین میکند، 1) و انسداد آن مستقیماً به آسیب سلولهای بینایی منجر میشود.
سلولهای مولر (MC) در شرایط اختلال پرفیوژن به عنوان منبع انرژی با تأمین لاکتات برای سلولهای بینایی عمل میکنند. 1) آسیب MC منجر به کاهش عملکرد مخروطها، میلهها و MC، و همچنین هممحلی از دست رفتن قطعه خارجی سلولهای بینایی و ریزش مویرگها میشود. 1)
الگوهای ایسکمی به چهار نوع زیر طبقهبندی میشوند (طبقهبندی Takashi و همکاران).
| نوع ایسکمی | فراوانی |
|---|---|
| نوع محیطی | 2.6٪ |
| نوع محیطی-میانی | 61.2% |
| نوع مرکزی | 26.3% |
| نوع گسترده | 9.9% |
عدم پرفیوژن DCP (شبکه مویرگی عمقی) باعث کاهش اکسیژنرسانی به سلولهای بینایی میشود (DCP حدود 10-15٪ از اکسیژنرسانی به سلولهای بینایی را تأمین میکند). 1) آسیب سلولهای مولر نیز مانع تأمین انرژی به سلولهای بینایی میشود. مطالعات با استفاده از AO-OCT نشان داده است که در نواحی عدم پرفیوژن DCP، تراکم سیگنال سلولهای بینایی IS/OS و COST حدود 40٪ کاهش مییابد. 1)
Datlinger و همکاران (2021) نشان دادند که ترکیب AO-OCT و OCTA امکان ارزیابی DMI در سطح تک سلول مخروطی بینایی را فراهم میکند. آنها بیان کردند که رویکرد تحقیقاتی تلفیق میکروپریمتری و OCTA به درک روند زمانی DMI کمک میکند و اشاره کردند که این پارامترهای تصویربرداری پیشرفته ممکن است در آینده به عنوان نشانگرهای زیستی در تحقیقات درمانی مورد استفاده قرار گیرند. 1)
قبلاً تصور میشد که انسداد مویرگها غیرقابل برگشت است، اما مواردی از بازپرفیوژن خودبهخودی گزارش شده است.
هو و همکاران (2022) بازپرفیوژن خودبهخودی NPA را در بیماران دیابتی که HbA1c از 6.1% به 5.6% بهبود یافته بود، مشاهده کردند. فرآیند نفوذ IRMA به داخل NPA و تشکیل شبکه مویرگی جدید به صورت سری زمانی با OCTA ثبت شد. 2)
این گزارش نشان میدهد که NPA دو نوع ویژگی دارد. 2)
در یک مطالعه پیگیری یکساله OCTA، نسبت شانس (OR) برای عدم پرفیوژن پایه و پیشرفت DR برابر 8.73 و برای عدم پرفیوژن عمقی و مداخله درمانی OR=3.39 گزارش شده است که نشان میدهد شاخص عدم پرفیوژن OCTA میتواند به عنوان بیومارکر پیشبینی پیشآگهی عمل کند. مساحت پایه FAZ در چشمهای مبتلا به DMI شناخته شده تمایل به افزایش 5-10% سالانه دارد. کاربرد هوش مصنوعی در تحلیل تصاویر OCTA نیز در حال تحقیق است. 3)
به ندرت گزارشهایی از بازپرفیوژن خودبهخودی وجود دارد. هو و همکاران (2022) فرآیند نفوذ IRMA به ناحیه NPA و تشکیل شبکه مویرگی جدید را گزارش کردند. 2) به ویژه NPA بدون نازکشدگی (تغییر زودرس) تمایل به بازپرفیوژن در عرض 2 ماه دارد. کنترل خوب قند خون ممکن است بازپرفیوژن را تسهیل کند.
Datlinger F, Georgi T, Stegmann H, et al. Assessment of detailed photoreceptor structure and retinal sensitivity in diabetic macular ischemia using adaptive optics-OCT and microperimetry. Invest Ophthalmol Vis Sci. 2021;62(13):1.
Hou S, Chen L, Shan K, et al. Spontaneous retinal reperfusion of capillary nonperfusion areas in diabetic retinopathy. Case Rep Ophthalmol. 2022;13:818-824.
American Academy of Ophthalmology Retina/Vitreous Panel. Diabetic Retinopathy Preferred Practice Pattern. Ophthalmology. 2024.