妊娠相关的眼部变化大致分为生理性变化(眼压 下降、角膜 变化、屈光 波动)和病理性变化(妊娠高血压综合征、糖尿病视网膜病变 恶化、CSC )。
妊娠高血压综合征(子痫前期)发生于约3-5%的孕妇,视物模糊 、闪光、一过性视力 障碍是重症化的征兆。
已有的糖尿病视网膜病变 在妊娠期间约10-30%的患者会恶化。妊娠前的眼科管理必不可少。
抗VEGF药物 (雷珠单抗 、阿柏西普 等)在妊娠期间禁忌使用。前列腺素相关的青光眼 滴眼液(拉坦前列素等)有子宫收缩风险,原则上禁忌。使用中的患者应咨询眼科医生和产科医生。
妊娠期间的LASIK 、ICL 等屈光 矫正手术禁忌。应在产后6个月以上、屈光 稳定后再考虑。
眼底检查 的散瞳药 (托吡卡胺等)在妊娠期间也可使用,但建议通过泪囊压迫最小化全身吸收。 妊娠会导致全身广泛的生理影响,包括循环血量增加(约40-50%)、激素环境的剧烈变化(雌激素、孕激素、皮质醇升高)以及免疫状态的改变。这些变化直接或间接影响眼睛,引起从生理性变化到危及生命或视力 的病理性变化等各种眼科事件1) 。
妊娠相关的眼科变化可分为可逆的生理性变化和需要积极干预的病理性变化。
以下总结妊娠相关的主要眼科变化。
分类 主要变化/疾病 备注 生理性变化 眼压 降低(平均2-3 mmHg)孕激素促进房水 流出 生理性变化 角膜水肿 和曲率变化可能导致隐形眼镜不耐受 生理性变化 暂时性近视 和屈光 变化 多数产后恢复 生理性变化 干眼倾向 激素波动导致泪膜不稳定 病理性变化 妊娠高血压综合征(子痫前期) 约3~5%的孕妇受影响2) 。视觉症状是严重征兆。 病理性变化 糖尿病视网膜病变 (DR)加重约10~30%的已有DR患者在妊娠期恶化7) 病理性变化 中心性浆液性脉络膜视网膜病变 (CSC )好发于妊娠晚期;皮质醇升高有关12)
妊娠期眼压 下降对青光眼 管理是有利的变化,同时也提供了重新审视当前眼药水安全性的机会。屈光 手术(LASIK 、ICL 等)因妊娠期屈光 不稳定而禁忌,应在产后至少6个月、屈光 稳定后再考虑3) 。
Q
妊娠期视力会改变吗?
A
会的。激素波动可改变角膜 形态、晶状体 厚度和眼压 ,导致暂时性屈光 变化(近视 化倾向)。角膜水肿 或曲率变化也可能引起隐形眼镜不适。多数在产后恢复,但如果因妊娠期屈光 变化而更改眼镜处方,产后需重新评估。
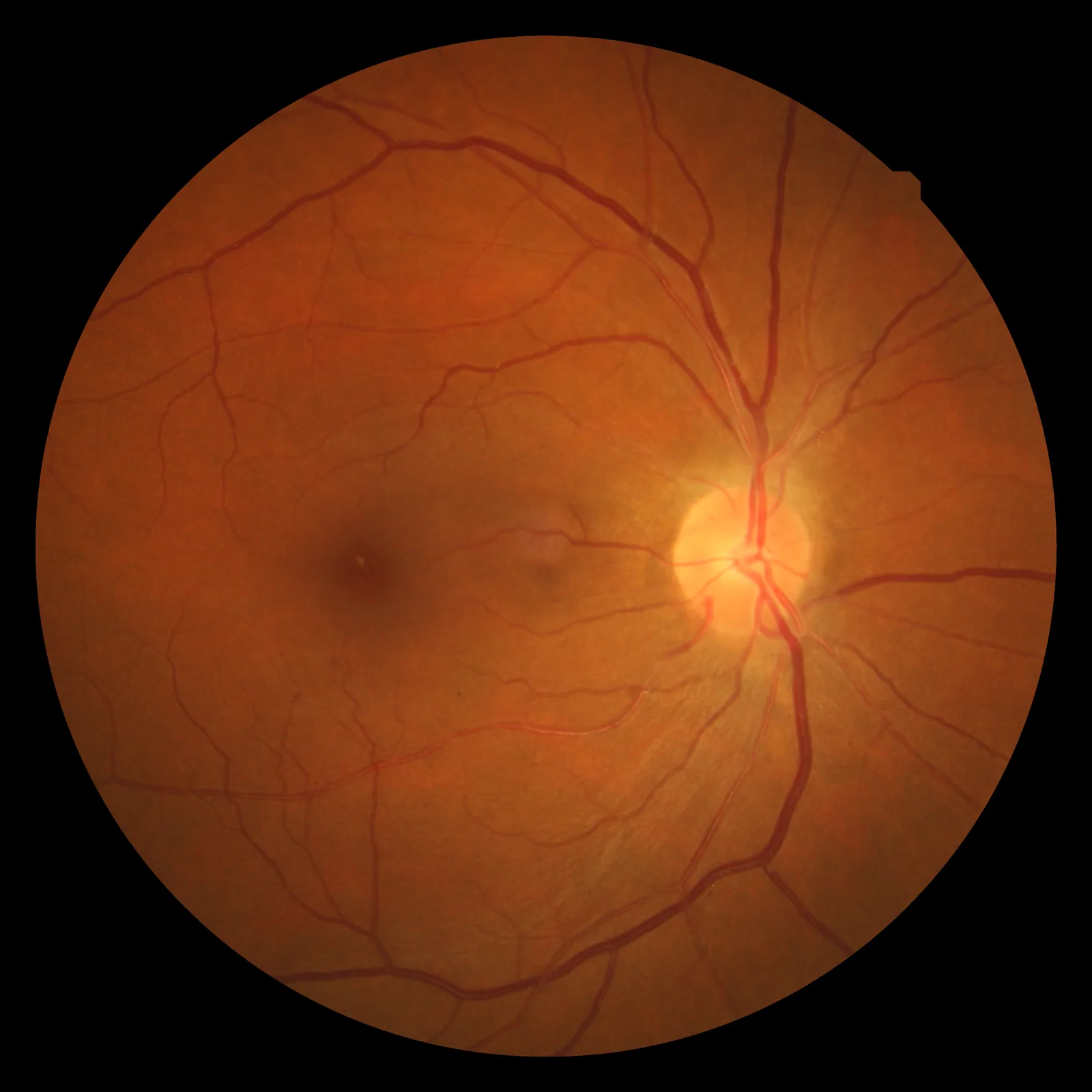
妊娠高血压综合征(子痫前期)所见的高血压性视网膜病变的眼底像 Wood F. Hypertensive retinopathy fundus photograph. Wikimedia Commons. 2009. Figure 1. Source ID: commons.wikimedia.org/wiki/File:Hypertensiveretinopathy.jpg. License: CC BY 3.0.
高血压性视网膜病变 的眼底像,可见
视网膜 动脉狭窄、银线样动脉改变、火焰状出血、棉絮状白斑(软性白斑)。对应本文“2. 主要症状和临床所见”中讨论的妊娠高血压综合征引起的
视网膜 改变。
妊娠相关的眼部症状因病因不同而异。
妊娠高血压综合征相关:
视物模糊 (雾视 )闪光感 (scintillation)、光视症暗点、视野缺损
一过性视力 障碍
伴随头痛、水肿(全身症状)
上述视觉症状是妊娠高血压综合征加重的征兆,也是子痫发作的风险信号6) 。应尽快就诊产科和眼科。
糖尿病视网膜病变 加重时:
CSC (中心性浆液性脉络膜视网膜病变 )相关
中心暗点 和视物变形 视力 下降(通常为轻度至中度)小视症
生理性变化引起的症状 :
隐形眼镜不适或贴合不良
干眼症 状(干燥感、异物感、充血 )轻度视物模糊 (因角膜水肿 )
妊娠高血压综合征
视网膜 动脉变化
出血和白斑 :火焰状出血、棉絮状白斑(软性白斑)的出现。
Elschnig斑 :由脉络膜 梗死引起的黄白色病变。预后不良的征象。
浆液性视网膜脱离 脉络膜 缺血→RPE 损伤→视网膜下液 积聚。
糖尿病视网膜病变恶化
微血管瘤增多 :原有病变恶化或新出现。
黄斑水肿 OCT 显示浆液性或囊样水肿。
新生血管 形成
玻璃体 积血视力 急剧下降。
中心性浆液性脉络膜视网膜病变(CSC)
浆液性视网膜脱离 黄斑部 的浅层浆液性视网膜脱离 。
OCT 表现视网膜下液 积聚。
荧光素眼底血管造影
皮质盲(PRES)
视力 视力 丧失(双眼)。
眼底表现 :多数正常或仅轻度异常。
影像学检查 :MRI/CT显示枕叶血管源性水肿(与神经内科、产科协作)。
病程 :适当降压及硫酸镁治疗后多可逆性恢复。
Q
怀孕期间眼睛闪烁或视物模糊是否危险?
A
闪光(眼前闪光感 )和雾视 可能是妊娠期高血压疾病加重的征兆。特别是伴有头痛、四肢水肿和血压升高时,存在从子痫前期进展为子痫(抽搐发作)的风险。出现这些症状时,应立即就诊产科,并接受眼科评估。
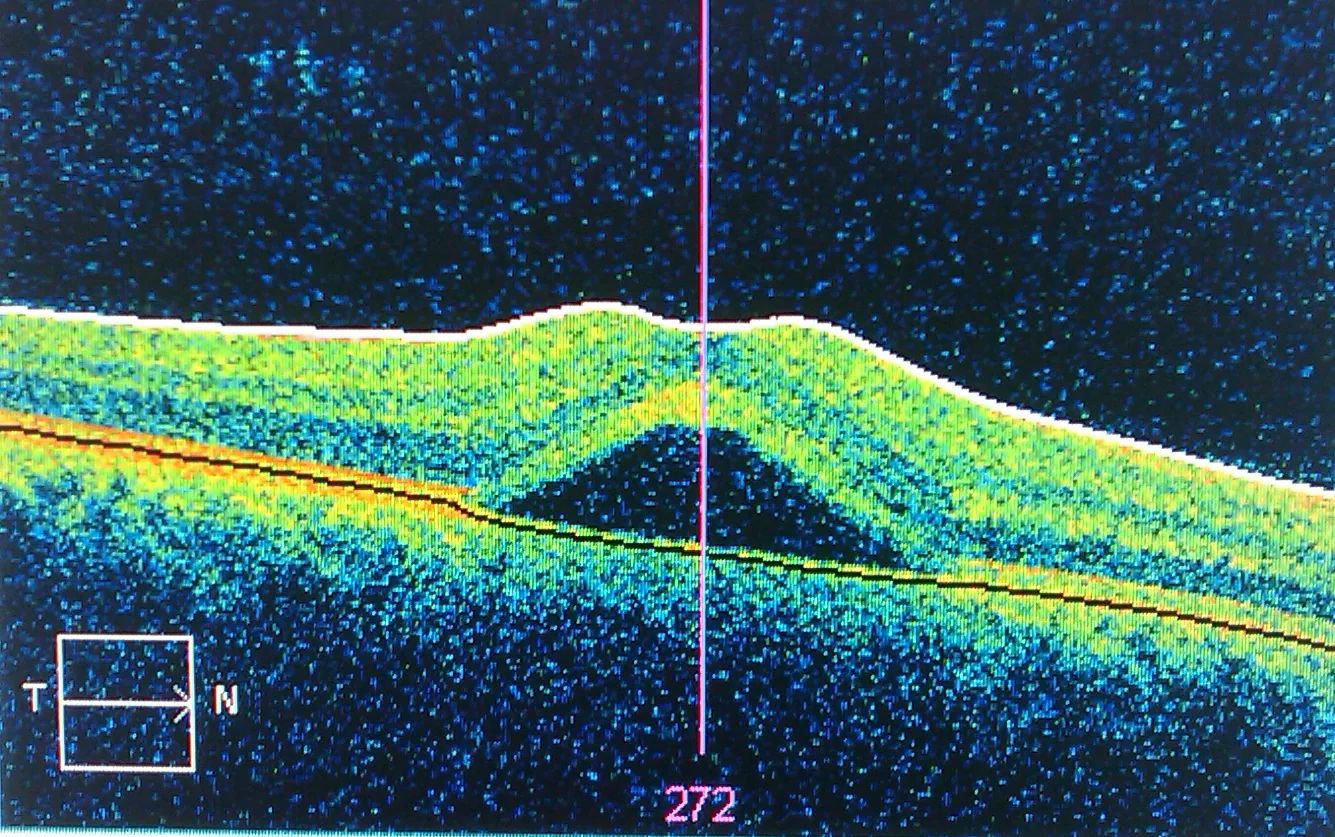
妊娠期好发的中心性浆液性脉络膜视网膜病变(CSC)的光学相干断层扫描(OCT)图像 Neches R. Central serous retinopathy OCT scan. Wikimedia Commons. 2010. Figure 1. Source ID: commons.wikimedia.org/wiki/File:Central_serous_retinopathy.jpg. License: CC BY-SA 3.0.
光学相干断层扫描 (
OCT )显示
黄斑部 浆液性视网膜脱离 (神经感觉
视网膜 隆起)和
视网膜色素上皮 (
RPE )分离。对应本文“3. 病因与危险因素”部分讨论的妊娠期
CSC (
中心性浆液性脉络膜视网膜病变 )。
妊娠期高血压疾病(子痫前期)是指妊娠20周后持续收缩压≥140 mmHg或舒张压≥90 mmHg的疾病4) 。其眼部病变的发生机制如下所述。
全身性血管内皮损伤→视网膜 动脉痉挛、缺血
抗血管生成因子(sFlt-1)过度产生→VEGF和PlGF(胎盘生长因子)活性降低
VEGF/PlGF活性降低→脉络膜 灌注减少→RPE (视网膜色素上皮 )屏障破坏
RPE 屏障破坏→视网膜下液 体积聚→浆液性视网膜脱离 枕叶血管源性水肿→PRES→皮质盲 (可逆性)6)
妊娠期高血压疾病的危险因素:
初产妇
多胎妊娠
高龄妊娠(≥35岁)
高BMI(25及以上)
既往高血压、糖尿病或肾脏疾病
既往妊娠有子痫前期病史
妊娠是糖尿病视网膜病变 (DR)的独立进展因素,尤其对于已有DR的糖尿病患者需注意7, 8) 。
加重的机制涉及以下方面:
妊娠期胰岛素抵抗增加→血糖波动加剧
循环血量增加→视网膜 血流增加→对现有微血管病变部位造成负荷
生长因子(IGF-1、生长激素、催乳素)升高→促进血管新生
HbA1c快速改善→视网膜 缺血部位氧供需不匹配→早期恶化(一过性加重)9)
妊娠期DR加重的风险因素:
妊娠前DR严重程度(越严重越易恶化)
妊娠前HbA1c高值
妊娠期间HbA1c快速改善
合并子痫前期
1型糖尿病
妊娠期间(尤其是第三孕期)内源性皮质醇升高被认为会增加脉络膜 血管通透性,诱发CSC 。妊娠相关CSC 通常在产后自然缓解,但迁延病例可能影响视力 12) 。
孕激素促进房水 流出(Schlemm管松弛)
循环血量增加导致巩膜 上静脉压降低
角膜水肿 和曲率变化:激素波动导致角膜基质 水分潴留
妊娠期眼科评估时,选择考虑胎儿安全的检查方法非常重要。
检查方法 妊娠期安全性 推荐场景 散瞳 眼底检查 (托吡卡胺/去氧肾上腺素)安全(建议泪囊压迫) 所有病例均可进行。DR:每个孕期一次 OCT (光学相干断层扫描 )安全 评估浆液性视网膜脱离 和黄斑水肿 所必需 眼压测量 安全 青光眼 随访荧光素眼底血管造影 (FA )原则上避免(FDA C类) 仅在绝对必要时进行。充分说明风险与获益 ICG眼底血管造影 视为禁忌 孕期避免(可进入母乳) 视野检查 安全 评估皮质盲 和视神经 疾病 屈光 检查/角膜地形图 安全 屈光 变化的监测(判断是否调整矫正)
合并DR的糖尿病孕妇应按以下时间表进行眼底检查 :
孕前 (计划妊娠时):进行详细的眼底检查 。如果存在DR,应提前进行激光治疗 等。孕早期(第一孕期) :确认基线值。孕中期(第二孕期) :评估DR是否进展。孕晚期(第三孕期) :分娩前的最终评估。产后 :产后3-6个月内重新评估(妊娠期间进展的DR可能在产后改善)9)
眼底检查 :根据Keith-Wagener-Barker分级评估高血压性眼底改变。OCT :检测并定量评估浆液性视网膜脱离 和视网膜 水肿。如果怀疑皮质盲 :通过MRI/CT确认枕叶水肿(与神经内科协作)。
Q
孕期进行眼底检查时使用的散瞳药对宝宝有影响吗?
A
常规剂量的散瞳药 (托吡卡胺/去氧肾上腺素滴眼液)在适当使用时被认为是安全的,可在妊娠期使用。但建议滴眼后用手指轻轻按压泪囊(内眼角),以最大程度减少全身吸收。对于患有糖尿病视网膜病变 的孕妇,散瞳 眼底检查 对于预防视力 丧失至关重要,其益处远大于风险。
妊娠期高血压疾病的根本治疗是分娩(胎儿娩出) 。大多数眼部并发症在分娩后会自然缓解11) 。
降压治疗 :
妊娠期可安全使用的降压药物包括:
甲基多巴:安全性数据最充分。一线药物之一。
拉贝洛尔:α/β受体阻滞剂 。可静脉注射或口服。
硝苯地平(缓释剂型):钙通道阻滞剂。口服给药。
禁忌的降压药物:
ACE抑制剂(卡托普利、依那普利等):有致畸性和胎儿毒性,妊娠期禁用4) 。
ARB类药物(坎地沙坦、奥美沙坦等):同样妊娠期禁用。
眼部并发症的管理 :
浆液性视网膜脱离 :分娩后多可自行吸收,通常无需额外的眼科治疗11) 。皮质盲 (PRES):通过适当的降压治疗(目标血压:收缩压140–150 mmHg)和硫酸镁(MgSO₄)给药,多数可逆。
孕前准备 (推荐计划妊娠):
尽可能降低HbA1c后再妊娠(理想:HbA1c <6.5%)
已有的DR和黄斑水肿 应在妊娠前完成眼科治疗
必要时在妊娠前进行全视网膜光凝 (PRP )
妊娠期治疗策略:
非增殖性DR(NPDR) :每三个月定期眼底检查 。恶化时考虑光凝增殖性DR(PDR)进展时 :妊娠期也可进行全视网膜光凝 (PRP )。激光光凝对胎儿的安全性已确立糖尿病黄斑水肿 (DME)抗VEGF药物 在妊娠期禁忌(动物实验有致畸性报告)。分娩后重新评估,必要时开始抗VEGF治疗 9) 血糖控制 :HbA1c快速改善存在早期恶化的风险。建议缓慢改善(每月下降约0.5–1%)8)
妊娠期以观察为主。多数病例产后自然缓解
产后3–6个月仍持续的CSC ,考虑光凝(渗漏点局部光凝)或光动力疗法 (PDT )
对于使用滴眼液(如青光眼 )的患者在妊娠或哺乳时,需要对药物进行安全性评估。以下是主要青光眼 滴眼液的安全性分类13, 14) 。
药物分类 代表药物 妊娠期评估 哺乳期评估 前列腺素相关药物 拉坦前列素、比马前列素 原则上禁忌(子宫收缩风险) 需注意 β受体阻滞剂 噻吗洛尔、卡替洛尔 需注意(胎儿心动过缓风险) 需注意 α2受体激动剂 溴莫尼定 需注意(中枢抑制风险) 哺乳期禁忌(新生儿呼吸抑制) 碳酸酐酶抑制剂 (滴眼液)多佐胺 、布林佐胺 需注意(动物实验显示致畸性) 需注意 人工泪液/透明质酸 透明质酸钠滴眼液 安全 安全 托吡卡胺(散瞳药 ) 美多丽P 安全(建议压迫泪囊) 安全(建议压迫泪囊)
如果继续使用β受体阻滞剂 滴眼液(如噻吗洛尔等),应彻底进行泪囊压迫(滴眼后立即按压内眼角1-2分钟)以最小化全身吸收。哺乳期使用溴莫尼定存在新生儿中枢神经系统抑制的风险,哺乳期间原则上不应使用。
Q
怀孕期间可以继续使用青光眼眼药水吗?
A
不同药物的安全性差异很大。前列腺素相关药物(如拉坦前列素等)可能诱发子宫收缩,怀孕期间原则上禁忌。β受体阻滞剂 (如噻吗洛尔等)需注意胎儿心动过缓,但在彻底进行泪囊压迫的情况下有时可以继续使用。一旦发现怀孕,务必咨询眼科医生和产科医生,考虑更换为安全的替代药物。忽视青光眼 的控制也会导致视野缺损 的进展,因此专科医生的个体化判断非常重要。
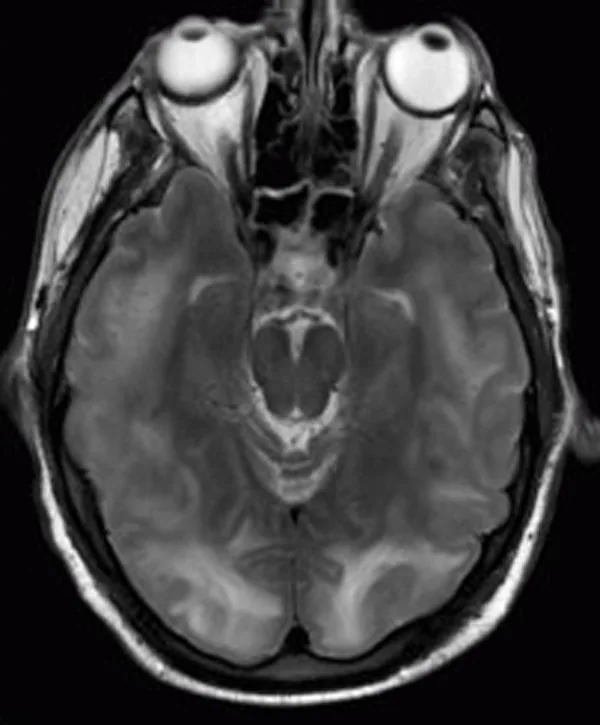
妊娠高血压综合征合并可逆性后部白质脑病(PRES)的头部MRI FLAIR像 Chawla R, Smith D, Marik PE. Near fatal posterior reversible encephalopathy syndrome complicating chronic liver failure. J Med Case Rep. 2009;3:6623. Figure 1. DOI: 10.1186/1752-1947-3-6623. License: CC BY 3.0.
脑部MRI FLAIR像显示双侧枕叶、顶叶及脑桥多发皮质下高信号区,提示可逆性后部白质脑病(PRES)引起的血管源性水肿。这与本文“6. 病理生理学·详细发病机制”中讨论的皮质盲 (PRES)相对应。
妊娠期高血压疾病的眼部病变是由全身血管内皮功能障碍为基础的复合机制引起的5, 6) 。
胎盘过度产生的抗血管生成因子sFlt-1(可溶性Flt-1)在循环血液中增加,捕获并灭活VEGF(血管内皮生长因子)和PlGF(胎盘生长因子)。这导致全身血管内皮功能障碍,引起高血压、蛋白尿和水肿。
在眼部,发生以下连锁反应:
视网膜 动脉:高血压+血管内皮功能障碍→动脉痉挛→视网膜 缺血→出血和渗出脉络膜 :灌注减少→RPE (视网膜色素上皮 )泵功能障→屏障破坏RPE 屏障破坏→视网膜下液 体积聚→浆液性视网膜脱离 脑血管:枕叶血管源性水肿→PRES(可逆性后部白质脑病)→皮质盲
PRES(可逆性后部白质脑病)引起的皮质盲 是一种一过性、可逆的病变,源于枕叶过度灌注和血脑屏障破坏,通过适当的降压和抗惊厥治疗可恢复。
妊娠期糖尿病视网膜病变 (DR)加重涉及多种机制相互作用。胰岛素抵抗增加导致血糖波动加剧,同时循环血量增加(约40-50%)使视网膜 血流量增加,对已有的微血管病变部位造成负荷7, 8) 。
生长激素、催乳素和IGF-1的升高具有促进血管生成的作用,并刺激VEGF的产生。此外,在孕前血糖控制不佳的患者中,妊娠早期HbA1c快速改善可能导致一过性视网膜 病变加重,即早期恶化现象。这被认为是由于血糖快速改善导致视网膜 缺血区域局部氧供需平衡被破坏所致8) 。
内源性皮质醇升高增加脉络膜 血管通透性。皮质醇通过脉络膜 内皮细胞的盐皮质激素受体发挥作用,导致脉络膜 过度灌注和血管通透性增加→RPE 功能障碍→浆液性视网膜脱离 12) 。
孕激素使施莱姆管 周围的小梁网 组织松弛,促进房水 流出,从而降低眼压 。此外,妊娠期循环血量增加导致的血液稀释降低了血液黏稠度,巩膜 表层静脉压的变化也有助于眼压 降低。对于正常眼压性青光眼 患者,妊娠期眼压 降低可能有利于症状稳定1) 。
妊娠期使用抗VEGF药物 :
雷珠单抗 、阿柏西普 等抗VEGF药物 在动物实验中显示出致畸性,目前妊娠期禁用。然而,有零星的病例报告在患有增殖性糖尿病视网膜病变 或眼内新生血管 的孕妇中紧急使用以防止视力 丧失。目前关于安全性的系统性数据尚不充分,需要进一步积累证据12) 。
以脉络膜 厚度作为生物标志物 进行早期预测 :
OCT 测量的脉络膜 厚度在妊娠期波动,有报道称其在子痫前期发病前发生变化。脉络膜 厚度作为子痫前期早期眼科生物标志物 的可能性正在研究中10) 。
sFlt-1/PlGF比值与眼病变的相关性 :
作为子痫前期预测标志物逐渐确立的sFlt-1/PlGF比值,正在探讨其与眼底病变严重程度的相关性。观察性研究表明,比值高的病例发生浆液性视网膜脱离 和Elschnig斑的频率较高5) 。
妊娠期青光眼 管理方案的标准化 :
妊娠期青光眼 治疗目前依赖个体化处理,需要建立基于证据的系统性方案。选择性激光小梁成形术 (SLT )可能作为药物治疗的替代方案适用于妊娠期,期待未来的研究13) 。
Dinn RB, Harris A, Marcus PS. Ocular changes in pregnancy. Obstet Gynecol Surv. 2003;58(2):137-144.
Sheth BP, Mieler WF. Ocular complications of pregnancy. Curr Opin Ophthalmol. 2001;12(6):455-463.
Schultz KL, Birnbaum AD, Goldstein DA. Ocular disease in pregnancy. Curr Opin Ophthalmol. 2005;16(5):308-314.
日本産科婦人科学会 編. 産婦人科診療ガイドライン―産科編2020. 日本産科婦人科学会; 2020.
Chawla S, Chaudhary T, Aggarwal S, et al. Ophthalmic considerations in pregnancy. Med J Armed Forces India. 2013;69(3):278-284.
Jaffe G, Schatz H. Ocular manifestations of preeclampsia. Am J Ophthalmol. 1987;103(3 Pt 1):309-315.
Klein BEK, Moss SE, Klein R. Effect of pregnancy on progression of diabetic retinopathy. Diabetes Care. 1990;13(1):34-40.
The Diabetes Control and Complications Trial Research Group. Effect of pregnancy on microvascular complications in the DCCT. Diabetes Care. 2000;23(8):1084-1091.
Morrison JL, Hodgson LA, Lim LL, et al. Diabetic retinopathy in pregnancy: a review. Clin Exp Ophthalmol. 2016;44(4):321-334.
Garg SJ, Federman J. Optociliary shunt vessels associated with central retinal vein occlusion and preeclampsia. Retina. 2007;27(9):1310-1311.
Ober RR, Grubman J, Engerman R, et al. The natural history of serous retinal detachment in preeclampsia. Ophthalmology. 1990;97(4):446-450.
Errera MH, Kohly RP , da Cruz L. Pregnancy-associated retinal diseases and their management. Surv Ophthalmol. 2013;58(2):127-142.
Mathew DJ, Pillai HJ, Demirci H. Drug safety in pregnancy and breastfeeding: ophthalmic medications. Semin Ophthalmol. 2020;35(4):237-250.
Chung CY, Kwok AKH, Chung KL. Use of ophthalmic medications during pregnancy. Hong Kong Med J. 2004;10(3):191-195.
复制全文后,可以粘贴到你常用的 AI 助手中提问。
打开下面的 AI 助手,并把复制的内容粘贴到聊天框。