妊娠に伴う眼の変化は、生理的変化(眼圧 低下・角膜 変化・屈折 変動)と病的変化(妊娠高血圧腎症・糖尿病網膜症 増悪・CSC )に大別される。
妊娠高血圧腎症(子癇前症)は妊婦の約3〜5%に発症し、霧視 ・閃光・一過性視力 障害は重症化の兆候である。
既存の糖尿病網膜症 は妊娠中に約10〜30%の患者で悪化する。妊娠前からの眼科管理が不可欠である。
抗VEGF薬 (ラニビズマブ ・アフリベルセプト 等)は妊娠中禁忌である。プロスタグランジン関連の緑内障点眼薬 (ラタノプロスト等)は子宮収縮リスクがあり原則禁忌。使用中の患者は眼科医・産科医に相談する。
妊娠中のLASIK ・ICL 等の屈折 矯正手術は禁忌。産後6ヶ月以上経過し屈折 が安定してから検討する。
眼底検査 の散瞳薬 (トロピカミド等)は妊娠中も使用可能だが、涙囊圧迫による全身吸収の最小化が推奨される。 妊娠は循環血液量の増加(約40〜50%増)、ホルモン環境の劇的な変化(エストロゲン・プロゲステロン・コルチゾールの上昇)、免疫状態の変化など、全身に広範な生理的影響をもたらす。これらの変化は眼にも直接・間接的に影響し、生理的な変化から生命・視力 に関わる病的変化まで、さまざまな眼科的事象が生じる1) 。
妊娠に伴う眼科的変化は、可逆的な生理的変化と、積極的な介入を要する病的変化に大別できる。
妊娠に関連する主な眼科的変化を以下に整理する。
分類 主な変化・疾患 特記事項 生理的変化 眼圧 低下(平均2〜3 mmHg)プロゲステロンの房水 流出促進効果 生理的変化 角膜浮腫 ・曲率変化コンタクトレンズ不適合を来たすことがある 生理的変化 一時的な近視 化・屈折 変動 多くは産後に回復 生理的変化 ドライアイ 傾向ホルモン変動による涙液層不安定化 病的変化 妊娠高血圧腎症(子癇前症) 妊婦の約3〜5%2) 。視覚症状は重篤な兆候 病的変化 糖尿病網膜症 (DR)の増悪既存DR患者の約10〜30%で妊娠中に悪化7) 病的変化 中心性漿液性網脈絡膜 症(CSC ) 第3三半期に好発。コルチゾール上昇が関与12)
妊娠中の眼圧 低下は緑内障 管理においては好ましい変化である一方、使用中の点眼薬の安全性を見直す機会にもなる。屈折 矯正手術(LASIK ・ICL 等)は妊娠中の屈折 不安定性のため禁忌であり、産後6ヶ月以上経過し屈折 が安定してから検討すべきである3) 。
Q
妊娠中に視力が変わることはあるか?
A
ある。ホルモン変動により角膜 形状・水晶体 厚・眼圧 が変化し、一時的な屈折 変動(近視 化傾向)が起こることがある。角膜 の浮腫や曲率変化によりコンタクトレンズの不快感を生じる場合もある。多くは産後に回復するが、妊娠中の屈折 変動を理由に眼鏡処方 を変更する際は、産後の再評価も必要である。
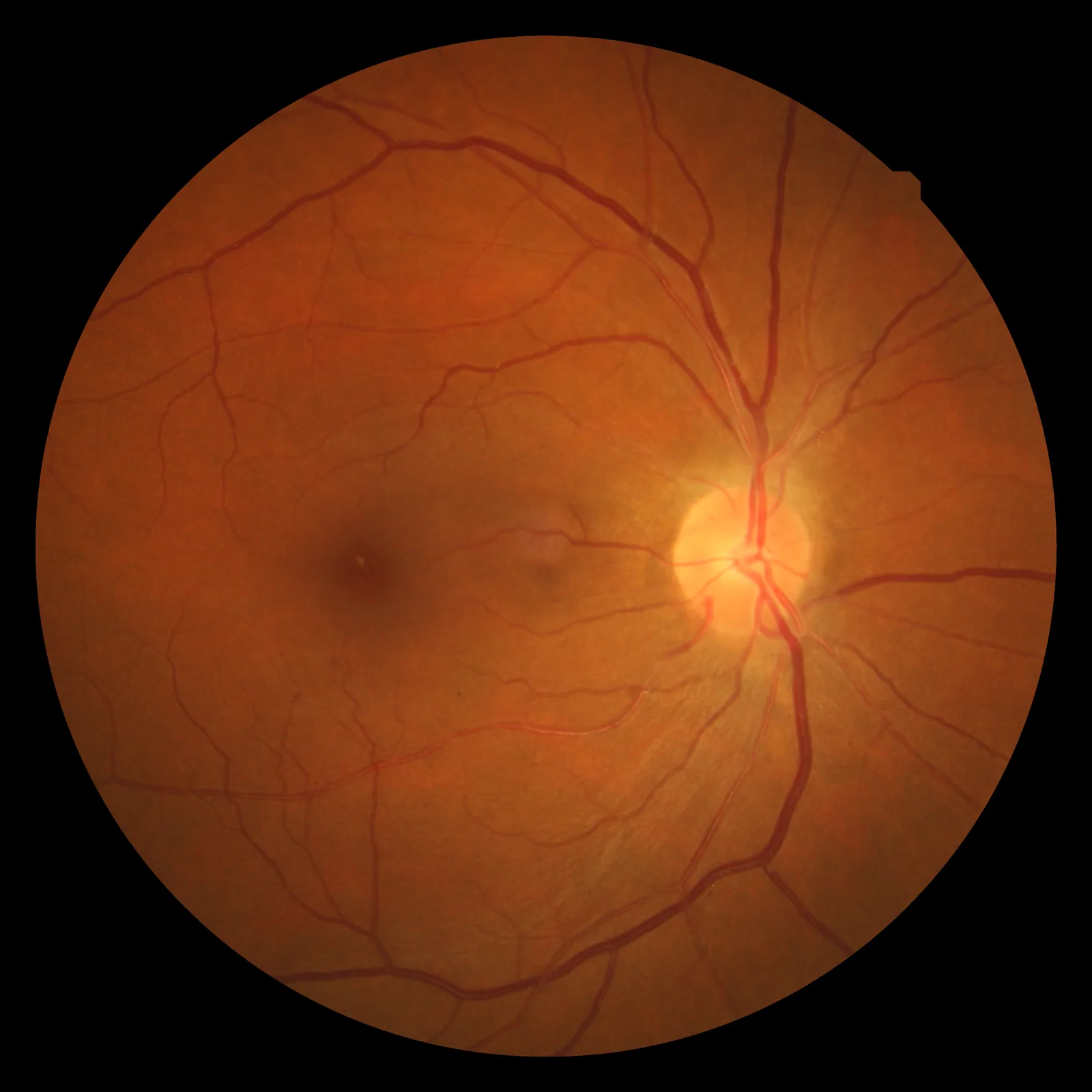
妊娠高血圧腎症(子癇前症)にみられる高血圧性網膜症の眼底像 Wood F. Hypertensive retinopathy fundus photograph. Wikimedia Commons. 2009. Figure 1. Source ID: commons.wikimedia.org/wiki/File:Hypertensiveretinopathy.jpg. License: CC BY 3.0.
高血圧性網膜 症の眼底像で、網膜 動脈の狭細化・銀線動脈変化・火炎状出血・綿花状白斑(軟性白斑)が確認できる。本文「2. 主な症状と臨床所見」の項で扱う妊娠高血圧腎症による網膜 変化に対応する。
妊娠に伴う眼症状は原因疾患により異なる。
妊娠高血圧腎症関連 :
霧視 (かすみ)閃光(scintillation)・光視症
暗点・視野欠損
一過性視力 障害
頭痛・浮腫の随伴(全身症状)
上記の視覚症状は妊娠高血圧腎症の重症化を示す兆候であり、子癇発症のリスクサインとなる6) 。速やかに産科・眼科を受診すべきである。
糖尿病網膜症 増悪時
CSC (中心性漿液性網脈絡膜 症)関連
中心暗点 ・変視症 視力 低下(通常は軽度〜中等度)小視症
生理的変化による症状 :
コンタクトレンズの不快感・フィット不良
ドライアイ 症状(乾燥感・異物感・充血 )軽度の霧視 (角膜浮腫 による)
妊娠高血圧腎症
網膜 動脈変化
出血・白斑 :火炎状出血・綿花状白斑(軟性白斑)の出現。
Elschnig斑 :脈絡膜 梗塞に由来する黄白色病変。予後不良のサイン。
漿液性網膜剥離 脈絡膜 虚血→RPE 障害→網膜下液 貯留。
糖尿病網膜症増悪
微小血管瘤の増加 :従来あった病変の増悪または新規出現。
黄斑浮腫 OCT で漿液性・嚢胞様浮腫が確認される。
新生血管 形成
硝子体出血 視力 が急激に低下しうる。
CSC
漿液性網膜剥離 黄斑部 に限局した浅い漿液性網膜剥離 。
OCT 所見網膜下液 の貯留が明確に描出される。
蛍光眼底造影
皮質盲(PRES)
視力 視力 喪失(両眼性)。
眼底所見 :多くの場合正常または軽度異常にとどまる。
画像診断 :MRI/CTで後頭葉の血管原性浮腫を確認(神経内科・産科と連携)。
経過 :適切な降圧・MgSO₄投与で多くは可逆的に回復。
Q
妊娠中に目がチカチカする・見えにくいのは危険か?
A
閃光(光がチカチカする症状)や霧視 は、妊娠高血圧腎症の重症化兆候である可能性がある。特に頭痛・手足のむくみ・血圧上昇を伴う場合は、子癇前症から子癇(けいれん発作)に移行するリスクがある。これらの症状が出現した場合は直ちに産科を受診し、眼科的評価も受けることが重要である。
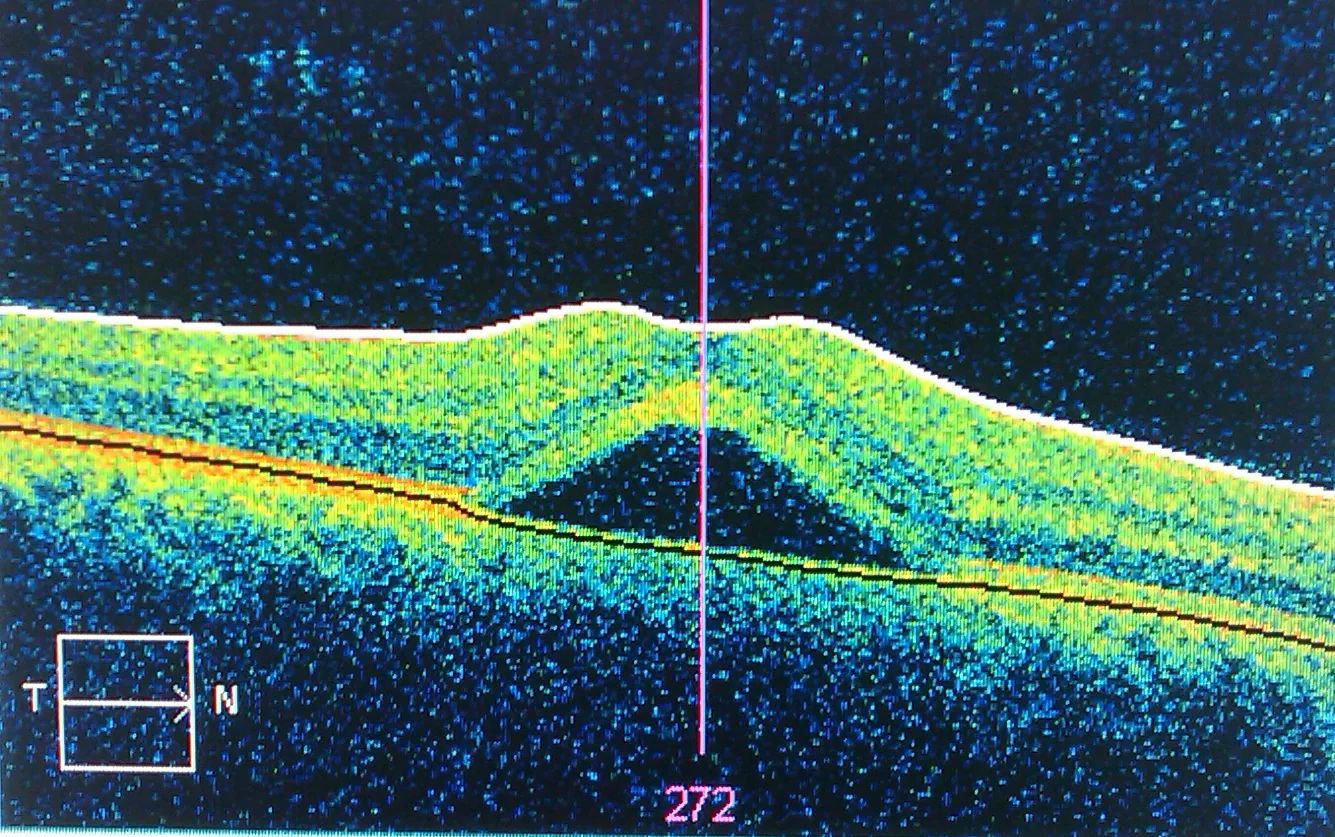
妊娠中に好発する中心性漿液性網脈絡膜症(CSC)の光干渉断層計(OCT)像 Neches R. Central serous retinopathy OCT scan. Wikimedia Commons. 2010. Figure 1. Source ID: commons.wikimedia.org/wiki/File:Central_serous_retinopathy.jpg. License: CC BY-SA 3.0.
光干渉断層計 (
OCT )で
黄斑部 に
漿液性網膜剥離 (神経感覚
網膜 の浮き上がり)と
網膜色素上皮 (
RPE )からの乖離が描出されている。本文「3. 原因とリスク要因」の項で扱う妊娠中の
CSC (中心性漿液性網
脈絡膜 症)に対応する。
妊娠高血圧腎症(子癇前症)は、妊娠20週以降に収縮期血圧≥140 mmHgまたは拡張期血圧≥90 mmHgが持続する疾患である4) 。その眼病変の発症機序として以下が重要である。
全身性の血管内皮障害→網膜 動脈のスパズム・虚血
抗血管新生因子(sFlt-1)の過剰産生→VEGF・PlGF(胎盤成長因子)の活性低下
VEGF/PlGF活性低下→脈絡膜 灌流低下→RPE (網膜色素上皮 )バリア破綻
RPE バリア破綻→網膜 下への液体貯留→漿液性網膜剥離 後頭葉の血管原性浮腫→PRES→皮質盲 (可逆的)6)
妊娠高血圧腎症のリスク因子:
初産婦
多胎妊娠
35歳以上の高齢妊娠
BMI高値(25以上)
既往の高血圧・糖尿病・腎疾患
前回妊娠時の子癇前症の既往
妊娠はDRの独立した進行因子であり、特に既存のDRを有する糖尿病患者では注意を要する7, 8) 。
増悪の機序として以下が関与する:
妊娠中のインスリン抵抗性増大→血糖変動の増幅
循環血液量増加→網膜 血流増加→既存の微小血管障害部への負荷
成長因子(IGF-1・成長ホルモン・プロラクチン)の上昇→血管新生促進
急速なHbA1c改善→網膜 虚血部位の酸素需給ミスマッチ→early worsening(一過性の悪化)9)
妊娠中のDR増悪のリスク因子:
妊娠前のDR重症度(重症なほど悪化しやすい)
妊娠前のHbA1c高値
妊娠期間中のHbA1c急速改善
妊娠高血圧腎症の合併
1型糖尿病
妊娠中(特に第3三半期)の内因性コルチゾール上昇が脈絡膜 血管の透過性を亢進させ、CSC を誘発するとされている。妊娠関連CSC は多くの場合産後に自然軽快するが、遷延例では視力 に影響する12) 。
プロゲステロンの房水 流出促進効果(シュレム管 の弛緩)
循環血液量増加に伴う上強膜 静脈圧の低下
角膜浮腫 ・曲率変化:ホルモン変動による角膜 基質への水分貯留
妊娠中の眼科的評価では、胎児への安全性を考慮した検査法の選択が重要である。
検査法 妊娠中の安全性 推奨場面 散瞳 眼底検査 (トロピカミド・フェニレフリン)安全(涙囊圧迫推奨) 全例で施行可。DRは各三半期ごとに OCT (光干渉断層計 )安全 漿液性網膜剥離 ・黄斑浮腫 の評価に必須眼圧測定 安全 緑内障 フォローアップフルオレセイン蛍光眼底造影 (FA )原則回避(FDAカテゴリC) 絶対必要な場合のみ。リスク・ベネフィットを十分説明 ICG蛍光眼底造影 禁忌に準じる 妊娠中は避ける(母乳への移行あり) 視野検査 安全 皮質盲 ・視神経 疾患の評価屈折 検査・角膜形状解析 安全 屈折 変動のモニタリング(矯正変更の判断)
DR合併の糖尿病妊婦では、以下のスケジュールで眼底検査 を行う:
妊娠前 (計画妊娠時): 精密眼底検査 。DRがある場合はレーザー治療 等を事前に施行妊娠初期(第1三半期) : 基準値の確認妊娠中期(第2三半期) : DR進行の有無を評価妊娠後期(第3三半期) : 分娩前の最終評価産後 : 産後3〜6ヶ月以内に再評価(妊娠中に進行したDRが産後に改善する場合もある)9)
眼底検査 : Keith-Wagener-Barker分類による高血圧性眼底 変化の評価OCT : 漿液性網膜剥離 ・網膜 浮腫の検出と定量評価皮質盲 が疑われる場合: MRI/CTによる後頭葉浮腫の確認(神経内科と連携)
Q
妊娠中に眼底検査の散瞳薬を使っても赤ちゃんに影響はないか?
A
通常量の散瞳薬 (トロピカミド・フェニレフリンの点眼)は、適切に使用すれば安全性が高く妊娠中も使用可能とされている。ただし、点眼後に涙囊(目頭)を指で軽く圧迫することで全身吸収を最小化することが推奨される。糖尿病網膜症 を有する妊婦では、散瞳 眼底検査 が視力 喪失防止のために不可欠であり、そのベネフィットがリスクを大幅に上回る。
妊娠高血圧腎症の根本的治療は**分娩(児の娩出)**である。眼科的合併症のほとんどは分娩後に自然軽快する11) 。
降圧療法 :
妊娠中に安全に使用できる降圧薬として以下が選択される:
メチルドパ: 最も確立した安全性データを持つ。第一選択薬の一つ
ラベタロール: α・β遮断薬 。静注・経口とも使用可
ニフェジピン(徐放製剤): カルシウム拮抗薬。経口投与
禁忌の降圧薬:
ACE阻害薬(カプトプリル・エナラプリル等): 催奇形性・胎児毒性あり、妊娠禁忌4)
ARB(カンデサルタン・オルメサルタン等): 同様に妊娠禁忌
眼合併症の管理 :
漿液性網膜剥離 : 分娩後に多くは自然吸収。追加の眼科的治療は不要なことが多い11) 皮質盲 (PRES): 適切な降圧療法(目標血圧: 収縮期140〜150 mmHg)とMgSO₄(硫酸マグネシウム)投与により多くは可逆的に回復
妊娠前の準備 (計画妊娠を推奨):
HbA1cを可能な限り低下させてから妊娠(理想: HbA1c 6.5%未満)
既存のDR・黄斑浮腫 は妊娠前に眼科的治療を完了させる
必要であれば汎網膜光凝固術 (PRP )を妊娠前に施行
妊娠中の治療方針 :
非増殖性DR(NPDR) : 各三半期での定期眼底検査 。増悪時は光凝固を検討増殖性DR(PDR)の進行時 : 汎網膜光凝固術 (PRP )は妊娠中も施行可能。レーザー光凝固 は胎児への安全性が確立している糖尿病黄斑浮腫 (DME)抗VEGF薬 は妊娠中禁忌(動物実験での催奇形性報告あり)。分娩後に再評価し、必要に応じて抗VEGF薬 を開始する9) 血糖コントロール : HbA1cの急速な改善はearly worseningリスクをはらむ。緩やかな改善(月0.5〜1%程度の低下)が望ましい8)
妊娠中は経過観察が基本方針。多くが産後自然軽快する
産後3〜6ヶ月時点で遷延するCSC には、光凝固療法(漏出点への局所光凝固)または光線力学的療法 (PDT )を検討する
緑内障 等で点眼薬を使用中の患者が妊娠・授乳する場合、薬剤の安全性評価が必要である。以下に主要な緑内障点眼薬 の安全性分類を示す13, 14) 。
薬剤分類 代表薬 妊娠中の評価 授乳中の評価 プロスタグランジン関連薬 ラタノプロスト、ビマトプロスト 原則禁忌(子宮収縮リスク) 要注意 β遮断薬 チモロール、カルテオロール 要注意(胎児徐脈リスク) 要注意 α2作動薬 ブリモニジン 要注意(中枢抑制リスク) 授乳中禁忌(新生児呼吸抑制) 炭酸脱水酵素阻害薬 (点眼)ドルゾラミド 、ブリンゾラミド 要注意(動物実験で催奇形性) 要注意 人工涙液・ヒアルロン酸 ヒアルロン酸Na点眼 安全 安全 トロピカミド(散瞳薬 ) ミドリンP 安全(涙囊圧迫推奨) 安全(涙囊圧迫推奨)
β遮断薬 点眼(チモロール等)を継続する場合は、涙囊圧迫(点眼直後に目頭を1〜2分圧迫)を徹底して全身吸収を最小化する。授乳中のブリモニジンは新生児への中枢神経系抑制のリスクがあり、授乳を行っている場合は原則使用しない。
Q
妊娠中に緑内障の目薬は使い続けてよいか?
A
薬剤によって安全性が大きく異なる。プロスタグランジン関連薬 (ラタノプロスト等)は子宮収縮を誘発する可能性があり、妊娠中は原則禁忌とされている。β遮断薬 (チモロール等)は胎児徐脈に注意が必要であるが、涙囊圧迫を徹底しながら継続可能な場合もある。妊娠が判明した時点で必ず眼科医と産科医に相談し、安全な代替薬への切り替えを検討すること。緑内障 のコントロールを放置することも視野障害の進行につながるため、専門医による個別判断が重要である。
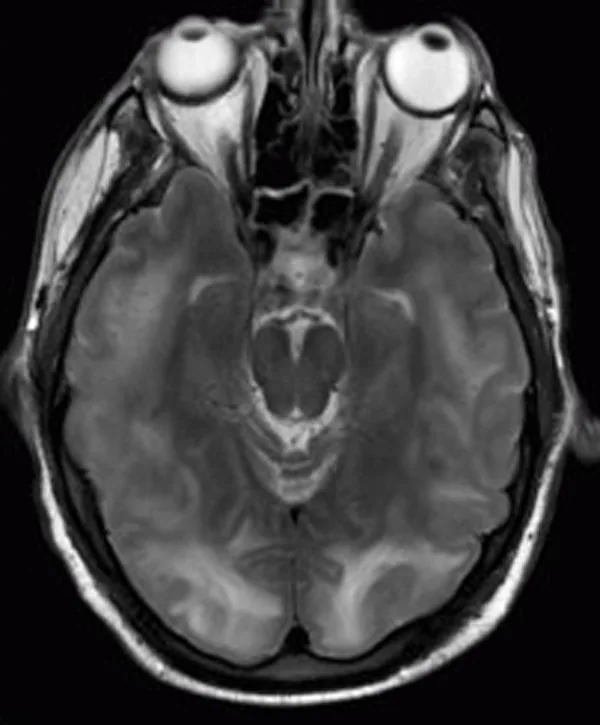
妊娠高血圧腎症に合併する可逆性後頭葉白質脳症(PRES)の頭部MRI FLAIR像 Chawla R, Smith D, Marik PE. Near fatal posterior reversible encephalopathy syndrome complicating chronic liver failure. J Med Case Rep. 2009;3:6623. Figure 1. DOI: 10.1186/1752-1947-3-6623. License: CC BY 3.0.
頭部MRI FLAIR像で両側後頭葉・頭頂葉および橋に多発する皮質下高信号域がみられ、可逆性後頭葉白質脳症(PRES)による血管原性浮腫を示している。本文「6. 病態生理学・詳細な発症機序」の項で扱う
皮質盲 (PRES)に対応する。
妊娠高血圧腎症における眼病変は、全身の血管内皮障害を共通基盤とする複合的な機序により生じる5, 6) 。
胎盤から過剰に産生される抗血管新生因子sFlt-1(可溶性Flt-1)が循環血中に増加し、VEGF(血管内皮増殖因子)とPlGF(胎盤成長因子)を捕捉して不活化する。この結果、全身の血管内皮機能が障害され、高血圧・蛋白尿・浮腫を来たす。
眼においては以下の連鎖が生じる:
網膜 動脈: 高血圧+血管内皮障害→動脈スパズム→網膜 虚血→出血・白斑脈絡膜 : 灌流低下→RPE (網膜色素上皮 )のポンプ機能障害→バリア破綻RPE バリア破綻→網膜 下への液体貯留→漿液性網膜剥離 脳血管: 後頭葉の血管原性浮腫→PRES(可逆性後頭葉白質脳症)→皮質盲
PRES(posterior reversible encephalopathy syndrome)による皮質盲 は、後頭葉の過灌流と血液脳関門破綻に由来する一過性・可逆的な病態であり、適切な降圧と抗痙攣療法で回復する。
妊娠中のDR増悪は、複数の機序が相互に作用する。インスリン抵抗性の増大により血糖変動が増幅される一方、循環血液量の増加(約40〜50%)が網膜 への血流を増加させ、既存の微小血管障害部位に負荷をかける7, 8) 。
成長ホルモン・プロラクチン・IGF-1の上昇は血管新生促進的に作用し、VEGFの産生を刺激する。また、妊娠前の血糖コントロールが不良であった患者で妊娠初期にHbA1cを急速に改善させると、一時的に網膜 症が悪化するearly worsening現象が起こりうる。これは急激な血糖改善により網膜 虚血部位の局所的な酸素需給バランスが崩れることで生じると考えられている8) 。
内因性コルチゾールの上昇は脈絡膜 血管の透過性を亢進させる。コルチゾールは脈絡膜 内皮細胞のミネラルコルチコイド受容体を介して作用し、脈絡膜 の過灌流・血管透過性亢進→RPE 機能障害→漿液性網膜剥離 の経路が想定されている12) 。
プロゲステロンはシュレム管 周囲の線維柱帯 組織を弛緩させ、房水 流出促進により眼圧 を低下させる。また、妊娠中の循環血液量増加に伴う血液希釈が血液粘稠度を低下させ、上強膜 静脈圧の変化も眼圧 低下に寄与する。正常眼圧緑内障 患者では妊娠中の眼圧 低下が症状安定に有利に働く場合がある1) 。
抗VEGF薬 の妊娠中使用ラニビズマブ ・アフリベルセプト 等の抗VEGF薬 は動物実験で催奇形性が示されており、現時点では妊娠中禁忌とされている。しかし増殖性糖尿病網膜症 や眼内血管新生を有する妊婦で視力 喪失を防ぐために緊急使用した症例報告が散見される。安全性に関する体系的なデータは現時点では不十分であり、今後のエビデンス蓄積が必要である12) 。
脈絡膜 厚をバイオマーカー とする早期予測OCT で計測した脈絡膜 厚は妊娠中に変動し、妊娠高血圧腎症の発症に先立って変化するとの報告がある。脈絡膜 厚が妊娠高血圧腎症の早期眼科的バイオマーカー となる可能性が研究されている10) 。
sFlt-1/PlGF比の眼病変との相関 :
妊娠高血圧腎症の予測マーカーとして確立しつつあるsFlt-1/PlGF比が、眼底病変の重症度とも相関する可能性が検討されている。比率が高い症例では漿液性網膜剥離 やElschnig斑の頻度が高いとの観察研究がある5) 。
妊娠中の緑内障 管理プロトコルの標準化 :
妊娠中の緑内障 治療は個別対応に依存しており、エビデンスに基づく系統的プロトコルの確立が求められている。選択的レーザー線維柱帯形成術 (SLT )は薬物療法の代替として妊娠中にも適用できる可能性があり、今後の検討が期待される13) 。
Dinn RB, Harris A, Marcus PS. Ocular changes in pregnancy. Obstet Gynecol Surv. 2003;58(2):137-144.
Sheth BP, Mieler WF. Ocular complications of pregnancy. Curr Opin Ophthalmol. 2001;12(6):455-463.
Schultz KL, Birnbaum AD, Goldstein DA. Ocular disease in pregnancy. Curr Opin Ophthalmol. 2005;16(5):308-314.
日本産科婦人科学会 編. 産婦人科診療ガイドライン―産科編2020. 日本産科婦人科学会; 2020.
Chawla S, Chaudhary T, Aggarwal S, et al. Ophthalmic considerations in pregnancy. Med J Armed Forces India. 2013;69(3):278-284.
Jaffe G, Schatz H. Ocular manifestations of preeclampsia. Am J Ophthalmol. 1987;103(3 Pt 1):309-315.
Klein BEK, Moss SE, Klein R. Effect of pregnancy on progression of diabetic retinopathy. Diabetes Care. 1990;13(1):34-40.
The Diabetes Control and Complications Trial Research Group. Effect of pregnancy on microvascular complications in the DCCT. Diabetes Care. 2000;23(8):1084-1091.
Morrison JL, Hodgson LA, Lim LL, et al. Diabetic retinopathy in pregnancy: a review. Clin Exp Ophthalmol. 2016;44(4):321-334.
Garg SJ, Federman J. Optociliary shunt vessels associated with central retinal vein occlusion and preeclampsia. Retina. 2007;27(9):1310-1311.
Ober RR, Grubman J, Engerman R, et al. The natural history of serous retinal detachment in preeclampsia. Ophthalmology. 1990;97(4):446-450.
Errera MH, Kohly RP , da Cruz L. Pregnancy-associated retinal diseases and their management. Surv Ophthalmol. 2013;58(2):127-142.
Mathew DJ, Pillai HJ, Demirci H. Drug safety in pregnancy and breastfeeding: ophthalmic medications. Semin Ophthalmol. 2020;35(4):237-250.
Chung CY, Kwok AKH, Chung KL. Use of ophthalmic medications during pregnancy. Hong Kong Med J. 2004;10(3):191-195.
記事の全文をコピーして、お好みのAIに貼り付けて質問できます
下のAIを開いて、チャット欄に貼り付け(ペースト)してください