前眼部及眼表面

免疫检查点抑制剂的眼及眼眶并发症
一目了然的要点
Section titled “一目了然的要点”1. 免疫检查点抑制剂的眼部和眼眶并发症
Section titled “1. 免疫检查点抑制剂的眼部和眼眶并发症”免疫检查点抑制剂(ICI)是阻断T细胞刹车分子(检查点分子)的单克隆抗体,从而增强对癌细胞的免疫应答1)。虽然它们给癌症治疗带来了革命性变化,但也会引起免疫相关不良事件(irAE)——在肿瘤以外的组织出现非特异性炎症1)。
ICI的分类
Section titled “ICI的分类”主要靶分子和代表性药物如下所示1)。
| 靶点分子 | 代表性药物 |
|---|---|
| CTLA-4 | 伊匹木单抗、曲美木单抗 |
| PD-1 | 帕博利珠单抗、纳武利尤单抗、西米普利单抗 |
| PD-L1 | 阿替利珠单抗、阿维鲁单抗、度伐利尤单抗 |
CTLA-4通过与T细胞表面的共刺激分子CD80/CD86相互作用抑制T细胞活化1)。PD-1是活化T细胞表面的受体,与抗原提呈细胞或肿瘤细胞上的PD-L1结合后抑制免疫应答1)。抑制这些通路可促进T细胞活化和抗肿瘤免疫,但同时也可能诱发自身免疫反应。
眼部irAE的发生频率
Section titled “眼部irAE的发生频率”眼部irAE的发生率为13%,主要表现为眼表疾病(干眼)和前葡萄膜炎1)。后段(视网膜/脉络膜)炎症占所有眼部irAE的约520%,但严重程度较高,若处理不当可能导致永久性视力损害1)。
眼部免疫相关不良事件(irAE)的发生率为13%1)。大部分为干眼或前葡萄膜炎,但后段炎症(520%)可能成为影响视力预后的严重并发症。
2. 主要症状和临床所见
Section titled “2. 主要症状和临床所见”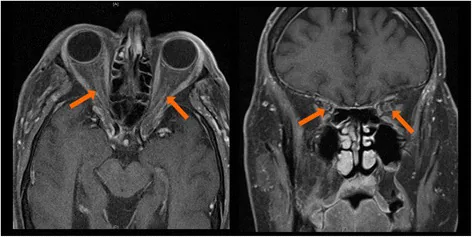
症状因部位和严重程度而异。干眼症主要表现为干燥感和异物感。葡萄膜炎引起充血、视物模糊和畏光。眼眶肌炎表现为复视、上睑下垂和眼球突出2)。后段炎症导致视力下降和飞蚊症1)。
ICI相关眼部irAE可发生于眼球的几乎所有区域。按部位的主要病态如下所示。
后眼部
眼眶
眼眶肌炎:多为双侧。MRI显示眼外肌肿大和强化2)。
眼眶脂肪炎症:可能波及眶尖和眶上裂2)。
甲状腺眼病样炎症:甲状腺功能正常患者也可出现。
神经
眼眶炎症的发病时间从首次给药后2天到2个月不等2)。可能伴有全身症状(乏力、发热、消化道症状、全身肌炎、心肌炎)2)。
3. 原因和风险因素
Section titled “3. 原因和风险因素”ICI引起的眼部irAE的根本原因是T细胞免疫检查点解除导致的自身免疫反应诱发1)。
- CTLA-4抑制:解除控制T细胞活化的刹车,不仅允许攻击癌细胞,也允许攻击正常组织1)
- PD-1/PD-L1抑制:增强肿瘤微环境中的T细胞反应,但同时破坏眼组织中PD-L1依赖的免疫特权1)
- 眼部免疫特权的脆弱性:正常眼中,血-视网膜屏障(BRB)和缺乏淋巴管阻止T细胞浸润,但糖尿病视网膜病变等已存在BRB破坏的情况会增加风险1)
- 宿主遗传易感性:遗传背景参与自身炎症事件的发生1)
- 联合治疗:抗CTLA-4与抗PD-1/PD-L1联合使用会增加irAE风险
4. 诊断与检查方法
Section titled “4. 诊断与检查方法”ICI相关眼部irAE的诊断基于ICI使用史与眼部表现的时间关联性。采用以下检查方法。
- 裂隙灯显微镜检查:评估前房炎症细胞、闪辉及角膜表现
- 眼底检查:检测视网膜血管炎、视网膜下液及脉络膜肉芽肿
- 光学相干断层扫描(OCT):评估视网膜外层信号消失、视网膜内高反射点、视网膜下液及脉络膜增厚1)
- 荧光素眼底血管造影(FA):评估血管渗漏、黄斑水肿及血管闭塞1)
- 视网膜电图(ERG):在MAR样视网膜病变中检测视杆和视锥细胞功能障碍
- MRI:在眼眶肌炎中显示眼外肌肿大、强化及眼眶脂肪的炎性改变2)
| 部位 | 主要检查方法 |
|---|---|
| 前节 | 裂隙灯检查 |
| 后眼部 | OCT、FA、视网膜电图 |
| 眼眶 | MRI |
ICI相关的眼部irAE可模仿多种已知眼病。前葡萄膜炎需与感染性和非感染性葡萄膜炎鉴别。VKH样反应在临床上与原发性VKH相似,但黑色素瘤的ICI使用史是重要线索1)。眼眶肌炎需与甲状腺眼病、IgG4相关疾病和特发性眼眶炎症鉴别2)。
5. 标准治疗方法
Section titled “5. 标准治疗方法”治疗需在肿瘤内科医生和眼科医生协商下,根据严重程度个体化进行。
轻度(眼表疾病、前葡萄膜炎)
Section titled “轻度(眼表疾病、前葡萄膜炎)”- 类固醇滴眼液局部治疗为主;大多数前葡萄膜炎可由此控制。
- 对于干眼症,使用人工泪液和泪点塞。
- 眼内类固醇植入
- 后Tenon囊下类固醇注射
重度(后眼部炎症、眼眶炎症)
Section titled “重度(后眼部炎症、眼眶炎症)”- 全身性类固醇是治疗的主要手段1)2)
- 免疫调节疗法(IMT)在少数病例中有使用报道1)
- 眼眶炎症大多通过全身性类固醇缓解,但部分病例会出现残留复视2)
6. 病理生理学与详细发病机制
Section titled “6. 病理生理学与详细发病机制”眼的免疫特权与ICI的影响
Section titled “眼的免疫特权与ICI的影响”眼是免疫特权器官,以下机制抑制T细胞介导的炎症1)。
- 血-视网膜屏障(BRB)限制外周T细胞进入眼内
- 视网膜色素上皮(RPE)细胞表达PD-L1和PD-L2,将T细胞转化为调节性T细胞(Treg)
- Müller细胞和小胶质细胞也表达PD-L1,抑制T细胞介导的炎症。
- TGF-β维持的免疫抑制微环境得以保持。
ICIs直接靶向这些PD-1/PD-L1依赖的免疫特权机制,从而产生眼内T细胞激活的风险1)。
ICI诱导的后段炎症的三种机制
Section titled “ICI诱导的后段炎症的三种机制”Haliyur等人(2025)提出将ICI诱导的后段irAE分为以下三种类型1)。
1型
T细胞交叉反应和自身反应性扩增
1a型:抗肿瘤T细胞与含黑色素细胞等眼组织发生交叉反应,引发VKH样全葡萄膜炎1)。在黑色素瘤患者中,VKH样反应占5-14%。
1b型:预先存在的眼组织驻留记忆T细胞被ICIs扩增和激活1),导致自身免疫性视网膜病变。
2型
3型
Haliyur等人(2025)提出了ICI诱导的后段irAE的三机制分类1)。1型涉及T细胞与眼组织的交叉反应(1a)和自身反应性T细胞的扩增(1b),2型涉及旁观者效应引起的视网膜血管炎,3型涉及自身抗体介导的炎症。临床表现不限于单一机制,多种机制可能重叠。
眼眶炎症的机制
Section titled “眼眶炎症的机制”抗CTLA-4抑制剂(伊匹木单抗)最常引起眼眶炎症2)。抗PD-1/PD-L1抑制剂也有类似的临床报道2)。MRI显示眼外肌肿大和强化,以及眼眶脂肪的炎症性改变,倾向于双侧出现2)。
7. 最新研究与未来展望(研究阶段报告)
Section titled “7. 最新研究与未来展望(研究阶段报告)”随着ICI适应症的迅速扩大,预计未来几十年ICI相关眼部irAE的病例数将增加1)。
目前,对后段irAE病理生理学的理解主要基于病例报告和病例系列,关于机制的实验研究很少1)。ICI相关的VKH样反应的诊断标准和治疗指南尚未建立。虽然有些病例治疗反应良好,但持续性渗出性视网膜脱离或ICI诱导的闭塞性视网膜血管炎可能导致永久性视力损害1)。
未来的挑战包括:根据后段irAE的机制类型建立治疗策略,标准化ICI给药前的基线眼科检查,以及制定肿瘤科和眼科之间的协作方案。
8. 参考文献
Section titled “8. 参考文献”-
Haliyur R, Elner SG, Sassalos T, Kodati S, Johnson MW. Pathogenic Mechanisms of Immune Checkpoint Inhibitor (ICI)-Associated Retinal and Choroidal Adverse Reactions. Am J Ophthalmol. 2025;272:8-18.
-
Ang T, Chaggar V, Tong JY, Selva D. Medication-associated orbital inflammation: A systematic review. Surv Ophthalmol. 2024;69(4):622-631. doi:10.1016/j.survophthal.2024.03.003. PMID:38490453.
