前眼部及眼表面

免疫檢查點抑制劑的眼及眼眶併發症
一目瞭然的要點
Section titled “一目瞭然的要點”1. 免疫檢查點抑制劑的眼部與眼窩併發症
Section titled “1. 免疫檢查點抑制劑的眼部與眼窩併發症”免疫檢查點抑制劑(ICI)是阻斷T細胞煞車分子(檢查點分子)的單株抗體,從而增強對癌細胞的免疫反應1)。雖然它們為癌症治療帶來革命性變化,但也會引起免疫相關不良事件(irAE)——在腫瘤以外的組織出現非特異性炎症1)。
ICI的分類
Section titled “ICI的分類”主要標靶分子和代表性藥物如下所示1)。
| 標靶分子 | 代表性藥物 |
|---|---|
| CTLA-4 | 伊匹木單抗、曲美木單抗 |
| PD-1 | 帕博利珠單抗、納武利尤單抗、西米普利單抗 |
| PD-L1 | 阿替利珠單抗、阿維魯單抗、度伐利尤單抗 |
CTLA-4透過與T細胞表面的共刺激分子CD80/CD86相互作用抑制T細胞活化1)。PD-1是活化T細胞表面的受體,與抗原呈現細胞或腫瘤細胞上的PD-L1結合後抑制免疫反應1)。抑制這些路徑可促進T細胞活化和抗腫瘤免疫,但同時也可能誘發自體免疫反應。
眼部irAE的發生頻率
Section titled “眼部irAE的發生頻率”眼部irAE的發生率為13%,主要表現為眼表疾病(乾眼)和前葡萄膜炎1)。後段(視網膜/脈絡膜)發炎約佔所有眼部irAE的520%,但嚴重度較高,若處理不當可能導致永久性視力損害1)。
眼部免疫相關不良事件(irAE)的發生率為13%1)。大部分為乾眼或前葡萄膜炎,但後段發炎(520%)可能成為影響視力預後的嚴重併發症。
2. 主要症狀與臨床所見
Section titled “2. 主要症狀與臨床所見”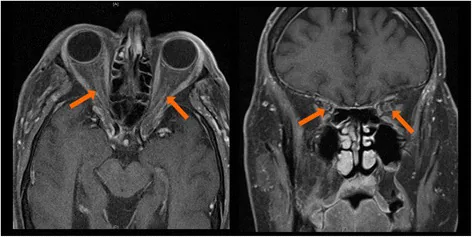
症狀因部位和嚴重程度而異。乾眼症主要表現為乾燥感和異物感。葡萄膜炎引起充血、視力模糊和畏光。眼眶肌炎表現為複視、眼瞼下垂和眼球突出2)。後段炎症導致視力下降和飛蚊症1)。
ICI相關眼部irAE可發生於眼球的幾乎所有區域。按部位的主要病態如下所示。
後眼部
眼眶
眼眶肌炎:多為雙側。MRI顯示眼外肌腫大和顯影2)。
眼眶脂肪發炎:可能波及眼眶尖端及眶上裂2)。
甲狀腺眼症樣發炎:甲狀腺功能正常患者也可能出現。
神經
眼眶發炎的發生時間從首次給藥後2天到2個月不等2)。可能伴隨全身症狀(疲倦、發燒、消化道症狀、全身肌炎、心肌炎)2)。
3. 原因與風險因素
Section titled “3. 原因與風險因素”ICI引起的眼部irAE的根本原因是T細胞免疫檢查點解除導致的自體免疫反應誘發1)。
- CTLA-4抑制:解除控制T細胞活化的煞車,不僅允許攻擊癌細胞,也允許攻擊正常組織1)
- PD-1/PD-L1抑制:增強腫瘤微環境中的T細胞反應,但同時破壞眼組織中PD-L1依賴的免疫特權1)
- 眼部免疫特權的脆弱性:正常眼中,血-視網膜屏障(BRB)和缺乏淋巴管阻止T細胞浸潤,但糖尿病視網膜病變等已存在BRB破壞的情況會增加風險1)
- 宿主遺傳易感性:遺傳背景參與自體發炎事件的發生1)
- 聯合治療:抗CTLA-4與抗PD-1/PD-L1聯合使用會增加irAE風險
4. 診斷與檢查方法
Section titled “4. 診斷與檢查方法”ICI相關眼部irAE的診斷基於ICI使用史與眼部表現的時間關聯性。採用以下檢查方法。
- 裂隙燈顯微鏡檢查:評估前房發炎細胞、閃輝及角膜表現
- 眼底檢查:檢測視網膜血管炎、視網膜下液及脈絡膜肉芽腫
- 光學同調斷層掃描(OCT):評估視網膜外層訊號消失、視網膜內高反射點、視網膜下液及脈絡膜增厚1)
- 螢光素眼底血管攝影(FA):評估血管滲漏、黃斑部水腫及血管阻塞1)
- 視網膜電圖(ERG):在MAR樣視網膜病變中檢測桿狀和錐狀細胞功能障礙
- MRI:在眼眶肌炎中顯示眼外肌腫大、顯影增強及眼眶脂肪的發炎性變化2)
| 部位 | 主要檢查方法 |
|---|---|
| 前節 | 裂隙燈檢查 |
| 後眼部 | OCT、FA、視網膜電圖 |
| 眼窩 | MRI |
ICI相關眼部irAE可模仿多種已知眼疾。前葡萄膜炎需與感染性及非感染性葡萄膜炎鑑別。VKH樣反應在臨床上與原發性VKH相似,但黑色素瘤的ICI使用史是重要線索1)。眼窩肌炎需與甲狀腺眼病、IgG4相關疾病及特發性眼窩炎症鑑別2)。
5. 標準治療方法
Section titled “5. 標準治療方法”治療需在腫瘤內科醫師與眼科醫師協商下,根據嚴重度個別化進行。
輕度(眼表疾病、前葡萄膜炎)
Section titled “輕度(眼表疾病、前葡萄膜炎)”- 類固醇眼藥水局部治療為主;大多數前葡萄膜炎可由此控制。
- 對於乾眼症,使用人工淚液及淚點塞。
- 眼內類固醇植入
- 後Tenon囊下類固醇注射
重度(後眼部炎症、眼窩炎症)
Section titled “重度(後眼部炎症、眼窩炎症)”- 全身性類固醇是治療的主軸1)2)
- 免疫調節療法(IMT)在少數病例中有使用報告1)
- 眼眶炎症大多經全身性類固醇緩解,但部分病例會出現殘留複視2)
6. 病理生理學與詳細發病機制
Section titled “6. 病理生理學與詳細發病機制”眼的免疫特權與ICI的影響
Section titled “眼的免疫特權與ICI的影響”眼是免疫特權器官,以下機制抑制T細胞介導的炎症1)。
- 血-視網膜屏障(BRB)限制外周T細胞進入眼內
- 視網膜色素上皮(RPE)細胞表現PD-L1和PD-L2,將T細胞轉化為調節性T細胞(Treg)
- Müller細胞和小膠質細胞也表現PD-L1,抑制T細胞介導的發炎。
- TGF-β維持的免疫抑制微環境得以保持。
ICIs直接靶向這些PD-1/PD-L1依賴的免疫特權機制,從而產生眼內T細胞激活的風險1)。
ICI誘導的後段發炎的三種機制
Section titled “ICI誘導的後段發炎的三種機制”Haliyur等人(2025)提出將ICI誘導的後段irAE分為以下三種類型1)。
第1型
T細胞交叉反應和自體反應性擴增
第1a型:抗腫瘤T細胞與含黑色素細胞等眼組織發生交叉反應,引發VKH樣全葡萄膜炎1)。在黑色素瘤患者中,VKH樣反應佔5-14%。
第1b型:預先存在的眼組織駐留記憶T細胞被ICIs擴增和激活1),導致自體免疫性視網膜病變。
第2型
第3型
Haliyur等人(2025)提出了ICI誘導的後段irAE的三機制分類1)。第1型涉及T細胞與眼組織的交叉反應(1a)和自體反應性T細胞的擴增(1b),第2型涉及旁觀者效應引起的視網膜血管炎,第3型涉及自體抗體介導的炎症。臨床表現不限於單一機制,多種機制可能重疊。
眼眶炎症的機制
Section titled “眼眶炎症的機制”抗CTLA-4抑制劑(伊匹木單抗)最常引起眼眶炎症2)。抗PD-1/PD-L1抑制劑也有類似的臨床報告2)。MRI顯示眼外肌腫大和增強,以及眼眶脂肪的炎症性變化,傾向於雙側出現2)。
7. 最新研究與未來展望(研究階段報告)
Section titled “7. 最新研究與未來展望(研究階段報告)”隨著ICI適應症的迅速擴大,預計未來幾十年ICI相關眼部irAE的病例數將增加1)。
目前,對後段irAE病理生理學的理解主要基於病例報告和病例系列,關於機制的實驗研究很少1)。ICI相關的VKH樣反應的診斷標準和治療指南尚未建立。雖然有些病例治療反應良好,但持續性滲出性視網膜剝離或ICI誘導的閉塞性視網膜血管炎可能導致永久性視力損害1)。
未來的挑戰包括:根據後段irAE的機制類型建立治療策略,標準化ICI給藥前的基線眼科檢查,以及制定腫瘤科和眼科之間的協作方案。
8. 參考文獻
Section titled “8. 參考文獻”-
Haliyur R, Elner SG, Sassalos T, Kodati S, Johnson MW. Pathogenic Mechanisms of Immune Checkpoint Inhibitor (ICI)-Associated Retinal and Choroidal Adverse Reactions. Am J Ophthalmol. 2025;272:8-18.
-
Ang T, Chaggar V, Tong JY, Selva D. Medication-associated orbital inflammation: A systematic review. Surv Ophthalmol. 2024;69(4):622-631. doi:10.1016/j.survophthal.2024.03.003. PMID:38490453.
