前段/眼表

免疫檢查點抑制劑引起的葡萄膜炎(Immune Checkpoint Inhibitor Uveitis)
一目瞭然的要點
Section titled “一目瞭然的要點”1. 免疫檢查點抑制劑引起的葡萄膜炎
Section titled “1. 免疫檢查點抑制劑引起的葡萄膜炎”免疫檢查點抑制劑(ICI)是阻斷T細胞煞車分子(檢查點分子)的單株抗體,從而增強對癌細胞的免疫反應1)。雖然它們為癌症治療帶來了革命性變化,但也會引起腫瘤以外部位的非特異性發炎,即免疫相關不良事件(irAE)1)。
ICI的分類
Section titled “ICI的分類”主要靶點分子和代表性藥物如下所示1)。
| 靶點分子 | 代表性藥物 |
|---|---|
| CTLA-4 | 伊匹木單抗(Yervoy®)、曲美木單抗 |
| PD-1 | 納武利尤單抗(Opdivo®)、帕博利珠單抗(Keytruda®)、西米普利單抗 |
| PD-L1 | 阿特珠單抗(Tecentriq®)、阿維魯單抗、德瓦魯單抗 |
CTLA-4 在淋巴結中調控 T 細胞活化,而 PD-1 抑制周邊組織中的 T 細胞反應1)。抑制這些路徑可促進抗腫瘤免疫,但同時也可能誘發自體免疫反應。2019 年葡萄膜炎診療指南也將 ICI 列為藥物性葡萄膜炎的重要致病藥物3)。
眼部 irAE 的發生頻率
Section titled “眼部 irAE 的發生頻率”眼部 irAE 的發生率為 1–3%1)。後段發炎(視網膜/脈絡膜)約占所有眼部 irAE 的 5–20%,但嚴重度較高,若處理不當可能導致永久性視力損害1)。隨著 ICI 適應症的擴大,眼科和腫瘤內科雙方的認識變得更加重要。
眼部 irAE 總體發生頻率為 1–3%1)。不同藥物存在差異:CTLA-4 單藥約 1%,PD-1 單藥 0.3–0.6%,兩藥合併使用時風險增加 2–3 倍4)。大部分為乾眼症或前葡萄膜炎,但後段發炎(占所有眼部 irAE 的 5–20%)可能成為影響視力預後的嚴重併發症。
2. 主要症狀與臨床所見
Section titled “2. 主要症狀與臨床所見”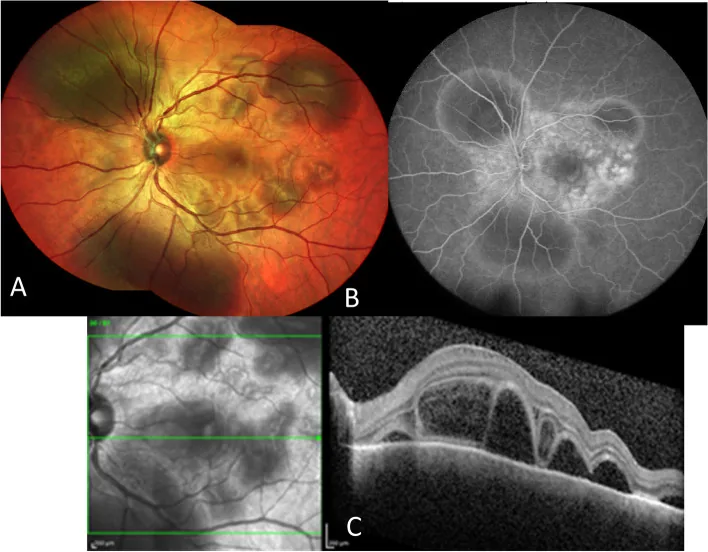
葡萄膜炎主要表現為充血、視力模糊、畏光和眼痛。後段發炎出現視力下降、飛蚊症和視物變形1)。眼眶肌炎表現為複視、眼瞼下垂和眼球突出2)。乾眼症主要表現為乾燥感和異物感。
ICI 相關眼部 irAE 可發生於眼球的幾乎所有區域。
後節
眼眶
眼眶肌炎(抗CTLA-4最常見):傾向於雙側發生。MRI顯示眼外肌腫大和顯影增強2)。
眼眶脂肪發炎:可能波及眶尖和眶上裂2)。
甲狀腺眼病變樣發炎:即使甲狀腺功能正常也可出現。
神經
眼眶發炎的發病時間從首次給藥後2天到2個月不等2)。與全身性irAE(肌炎、心肌炎、結腸炎)合併的病例需注意重症化。
3. 原因與風險因素
Section titled “3. 原因與風險因素”ICI引起眼部irAE的根本原因是T細胞免疫檢查點解除導致的自體免疫反應誘發1)。
- CTLA-4抑制:解除控制T細胞活化的煞車,允許對正常組織的攻擊1)
- PD-1/PD-L1抑制:直接破壞眼組織的PD-L1依賴性免疫特權1)
- CTLA-4+PD-1聯合:眼部irAE風險比單藥增加2~3倍4)
- 黑色素瘤患者:含黑色素的眼組織(脈絡膜、RPE)與腫瘤抗原的交叉反應導致VKH樣全葡萄膜炎風險高1, 10)
- 已有BRB破壞:糖尿病視網膜病變等血-視網膜屏障已破壞的狀態下風險增加1)
- 宿主遺傳易感性:提示HLA-DR15等HLA類型的參與7)
4. 診斷與檢查方法
Section titled “4. 診斷與檢查方法”ICI相關眼部irAE的診斷基於ICI使用史與眼部表現的時間關聯性。應實施葡萄膜炎診療指南(2019)的基本篩查3)。診斷原則是確認可疑藥物使用與症狀出現的時間關係,並排除其他原因。
| 部位 | 主要檢查方法 | 目的 |
|---|---|---|
| 前眼部 | 裂隙燈顯微鏡 | 前房發炎細胞/閃輝、角膜所見 |
| 後眼部 | OCT/FA | 視網膜外層訊號消失、血管滲漏、囊樣黃斑水腫1) |
| 後眼部 | 視網膜電圖(ERG) | 評估MAR樣視網膜病變的桿體與錐體功能 |
| 眼眶 | MRI | 眼外肌腫大/顯影增強、眼眶脂肪發炎2) |
發病時間參考
Section titled “發病時間參考”- 葡萄膜炎:首次給藥後2週至6個月(中位數3-4個月)
- 眼眶炎症:首次給藥後2天至2個月
- VKH樣全葡萄膜炎:吲哚青綠血管造影(ICGA)早期顯示脈絡膜高螢光(與原田病相似)1, 10)
前葡萄膜炎需與感染性和非感染性葡萄膜炎鑑別。VKH樣反應在臨床上與原發性VKH相似,但黑色素瘤ICI使用史是重要線索1, 10)。眼肌炎需與甲狀腺眼病、IgG4相關疾病和特發性眼眶炎症鑑別2)。MAR(黑色素瘤相關視網膜病變)樣視網膜病變需與副腫瘤症候群鑑別1)。感染性葡萄膜炎和轉移性眼內腫瘤(偽裝症候群)也應排除。
5. 標準治療方法
Section titled “5. 標準治療方法”治療需在腫瘤內科醫師和眼科醫師協商下,根據CTCAE分級個別化進行。停藥是治療原則,但由於ICI的抗腫瘤效果直接關係到生命,停藥決定應由多學科團隊慎重做出。
按CTCAE分級的管理演算法5)
Section titled “按CTCAE分級的管理演算法5)”| 分級 | 嚴重程度 | 眼科管理 | ICI是否繼續 |
|---|---|---|---|
| 1 | 輕度(無症狀,僅裂隙燈檢查發現) | 局部類固醇:Rinderon® 0.1% 每日4-6次 | 可繼續 |
| 2 | 中度(視力下降1級、前房發炎) | Tenon囊下注射:曲安奈德20 mg + 強化類固醇眼藥水 | 謹慎繼續 |
| 3 | 重度(視力下降≥2級、全葡萄膜炎) | 全身PSL 1~2 mg/kg/日,逐漸減量(眼部症狀改善後) | ICI中斷 |
| 4 | 失明風險 | 類固醇脈衝:甲潑尼龍1 g/日×3天 + 免疫抑制劑 | 中斷;恢復困難 |
VKH樣全葡萄膜炎的治療
Section titled “VKH樣全葡萄膜炎的治療”- 高劑量類固醇:潑尼松龍(PSL)1 mg/kg/日,早期導入
- 重症病例:類固醇脈衝(甲潑尼龍1 g/日×3天)
- 難治性病例:加用環孢素 3~5 mg/kg/日
- ICI 重啟需在與腫瘤內科充分協商後決定5)
眼科局部治療的詳細說明
Section titled “眼科局部治療的詳細說明”前葡萄膜炎(1~2級)
- 類固醇眼藥水:倍他米松 0.1% 或地塞米松 0.1% 頻繁點眼
- 散瞳藥:預防虹膜後粘連(阿托品 1% 或托吡卡胺 0.5%)
中度至重度後段炎症
- Tenon囊下注射:曲安奈德 20 mg
- 眼內植入物(限於適應症病例)
特殊病理狀態
- 合併重症肌無力:考慮血漿置換療法9)
- 眼眶炎症:大部分病例透過全身類固醇治療緩解,但部分患者可能出現殘留複視2)
在發炎充分控制後(第1級以下),可與腫瘤內科醫師協商考慮恢復治療。但VKH樣全葡萄膜炎等嚴重眼部irAE復發風險高,是否恢復需個別判斷。恢復後需要眼科密切追蹤 6)。
6. 病理生理學與詳細發病機轉
Section titled “6. 病理生理學與詳細發病機轉”眼的免疫特權與ICI的影響
Section titled “眼的免疫特權與ICI的影響”眼是免疫特權器官,以下機制抑制T細胞介導的發炎 1)。
- 血-視網膜屏障(BRB)限制周邊T細胞進入眼內。
- 視網膜色素上皮(RPE)細胞表現PD-L1和PD-L2,將T細胞轉化為調節性T細胞(Treg)。
- Müller細胞和小膠質細胞也表現PD-L1,抑制T細胞介導的發炎。
- TGF-β維持免疫抑制微環境。
ICI直接靶向這些PD-1/PD-L1依賴的免疫特權機制,因此存在眼內T細胞活化的風險 1)。
ICI誘發的後段發炎的三種機制
Section titled “ICI誘發的後段發炎的三種機制”Haliyur等人(2025)將ICI誘發的後段irAE分為三種類型 1)。
第1型:T細胞交叉反應
第1a型:抗腫瘤T細胞與含黑色素細胞等眼組織發生交叉反應,引發VKH樣全葡萄膜炎。在黑色素瘤患者中發生率為5~14% 1)。
1b型:ICI使眼特異性組織駐留記憶T細胞擴增和活化,導致自體免疫性視網膜病變1)。
2型:旁觀者血管炎
3型:自體抗體介導
PD-1也在B細胞上表現,ICI誘導B細胞譜系擴增和漿細胞產生組織特異性自體抗體1)。
它也參與副腫瘤症候群(如MAR樣視網膜病變)的加重1)。
臨床表現不限於單一機制,多種機制可能重疊。VKH樣全葡萄膜炎(1a型)表現為滲出性視網膜剝離和脈絡膜高螢光,臨床上可能難以與原田病區分1)。
眼眶發炎的機制
Section titled “眼眶發炎的機制”抗CTLA-4抑制劑(伊匹木單抗)最常引起眼眶發炎2)。抗PD-1/PD-L1抑制劑也有類似臨床特徵的報導2)。MRI顯示眼外肌增大和強化以及眼眶脂肪的發炎性改變,傾向於雙側出現2)。
7. 最新研究與未來展望
Section titled “7. 最新研究與未來展望”隨著ICI適應症的迅速擴大,預計未來幾十年ICI相關眼部irAE的病例數將增加1)。
基於生物標記的風險預測
Section titled “基於生物標記的風險預測”- 血清IL-17和IL-23升高被認為是VKH樣反應的預測因子7)
- 通過HLA-DR15和HLA-A2等HLA分型預先識別高風險患者的研究正在進行中
- 治療前基線眼科檢查與血清生物標誌物相結合的風險分層是未來的課題7)
新型治療策略
Section titled “新型治療策略”目前,對後段irAE病理生理的理解主要基於病例報告和病例系列,診斷標準和治療指南尚未建立1)。腫瘤科與眼科之間的協作方案亟待建立。
8. 參考文獻
Section titled “8. 參考文獻”- Haliyur R, Elner SG, Sassalos T, Kodati S, Johnson MW. Pathogenic Mechanisms of Immune Checkpoint Inhibitor (ICI)-Associated Retinal and Choroidal Adverse Reactions. Am J Ophthalmol. 2025;272:8-18.
- Ang T, Kherani A, Margolin E, Bhattacharya A, Beland F, Margolin J. Orbital Inflammation: A Review. Surv Ophthalmol. 2024;69(5):622-631.
- ぶどう膜炎診療ガイドライン作成委員会. ぶどう膜炎診療ガイドライン. 日本眼科学会雑誌. 2019;123(6):635-696.
- Dalvin LA, Shields CL, Orloff M, Sato T, Shields JA. Checkpoint inhibitor immune therapy: systemic indications and ophthalmic side effects. Retina. 2018;38(6):1063-1078.
- Brahmer JR, Abu-Sbeih H, Ascierto PA, et al. Society for Immunotherapy of Cancer (SITC) clinical practice guideline on immune checkpoint inhibitor-related adverse events. J Immunother Cancer. 2021;9(6):e002435.
- Fortes BH, Liou H, Dalvin LA. Ophthalmic adverse effects of immune checkpoint inhibitors: the Mayo Clinic experience. Br J Ophthalmol. 2021;105(8):1108-1113.
- Bitton K, Michot JM, Barreau E, et al. Prevalence and clinical patterns of ocular complications associated with anti-PD-1/PD-L1 anticancer immunotherapy. Am J Ophthalmol. 2019;202:109-117.
- Chen JJ, Bhatti MT. Neuro-ophthalmic complications of immune checkpoint inhibitors. Ophthalmology. 2022;129(11):1311-1321.
- Matas-García A, Milisenda JC, Selva-O’Callaghan A, et al. Ocular myasthenia gravis and myositis following immune checkpoint inhibitor therapy. Neurology. 2020;95(14):e1672-e1680.
- Schulz TU, Urner J, Seegräber M, et al. Immune checkpoint inhibitor-induced Vogt-Koyanagi-Harada-like syndrome: a case report and review of literature. Ocul Immunol Inflamm. 2022;30(3):731-741.
