免疫チェックポイント阻害薬 (ICI )はがん免疫療法の主力であるが、眼の免疫関連有害事象(irAE)を 1〜3% の頻度で生じる1) CTLA-4 単剤で眼 irAE 約 1%、PD-1 単剤で 0.3〜0.6%、CTLA-4+PD-1 併用でリスクが 2〜3 倍に増加する4)
最も多い眼 irAE はドライアイ と前部ぶどう膜炎 であり、VKH 様汎ぶどう膜炎 はメラノーマ ICI 治療の 5〜14% に生じる1)
治療は CTCAE Grade に応じたステロイド 療法(局所・全身)が主体で、ICI 中止が必要になることは稀である5)
腫瘍内科医と眼科医の連携による個別管理が不可欠である3)
免疫チェックポイント阻害薬 (ICI )は、T 細胞のブレーキ役であるチェックポイント分子を阻害し、がん細胞に対する免疫応答を増強するモノクローナル抗体である1) 。がん治療に革命をもたらした一方、腫瘍以外の部位に非特異的な炎症を引き起こす免疫関連有害事象(irAE)が問題となる1) 。
主な標的分子と代表的薬剤を以下に示す1) 。
標的分子 代表的薬剤 CTLA-4 イピリムマブ(ヤーボイ®)、トレメリムマブ PD-1 ニボルマブ(オプジーボ®)、ペムブロリズマブ(キイトルーダ®)、セミプリマブ PD-L1 アテゾリズマブ(テセントリク®)、アベルマブ、デュルバルマブ
CTLA-4 はリンパ節での T 細胞活性化を制御し、PD-1 は末梢組織における T 細胞応答を抑制する1) 。これらの阻害により抗腫瘍免疫が促進されるが、同時に自己免疫反応も惹起されうる。ぶどう膜炎 診療ガイドライン(2019)においても ICI は薬剤性ぶどう膜炎 の重要な原因薬剤として記載されている3) 。
眼 irAE の発生率は 1〜3% である1) 。後眼部炎症(網膜 ・脈絡膜 )は全眼 irAE の約 5〜20% を占めるが、重篤度が高く、適切に対処しなければ永続的な視力 障害に至る可能性がある1) 。ICI の保険適用が拡大するに伴い、眼科・腫瘍内科双方での認識が一層重要となっている。
Q
免疫チェックポイント阻害薬の眼副作用はどのくらいの頻度で起こるか
A
眼 irAE は全体で 1〜3% の頻度で生じます1) 。薬剤の種類によって差があり、CTLA-4 単剤で約 1%、PD-1 単剤で 0.3〜0.6%、両薬剤の併用では 2〜3 倍のリスク増加が報告されています4) 。大部分はドライアイ や前部ぶどう膜炎 ですが、後眼部炎症(全眼 irAE の 5〜20%)は視力 予後に影響する重篤な合併症となりうる。
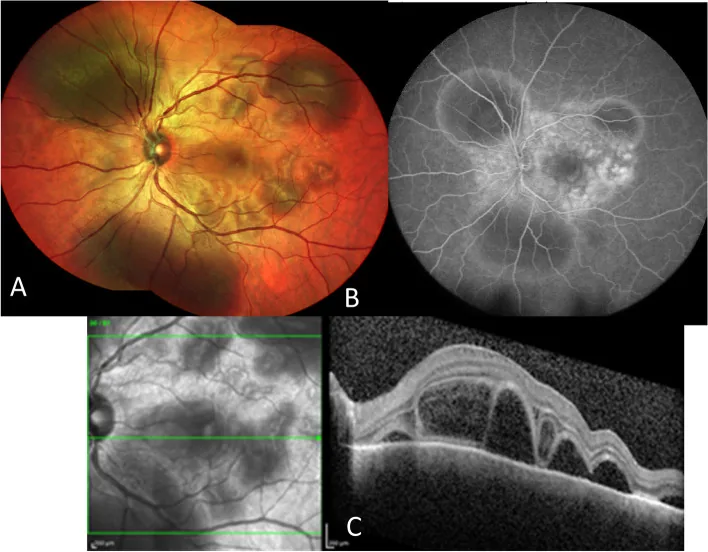
免疫チェックポイント阻害薬関連ぶどう膜炎のVKH様所見。眼底、蛍光眼底造影、OCTで漿液性網膜剥離を示す。 Paez-Escamilla M, et al. Challenges in posterior uveitis-tips and tricks for the retina specialist. J Ophthalmic Inflamm Infect. 2023. Figure 1. PM
CI D: PMC10435440. License: CC BY.
眼底写真では黄白色病変と漿液性網膜剥離 がみられる。蛍光眼底造影 の多発漏出とOCT の多房性漿液性網膜剥離 は、免疫チェックポイント阻害薬 関連ぶどう膜炎 の後部炎症所見を示す。
ぶどう膜炎 では充血 ・霧視 ・羞明 ・眼痛 が主体である。後眼部炎症では視力 低下・飛蚊症 ・変視症 が出現する1) 。眼窩 筋炎では複視 ・眼瞼下垂 ・眼球突出 がみられる2) 。ドライアイ では乾燥感・異物感が主体である。
ICI 関連眼 irAE は眼のほぼ全領域に生じうる。
前眼部・眼表面
ドライアイ シェーグレン症候群 様の涙液分泌低下を生じることがある。
前部ぶどう膜炎 :前房 炎症細胞・フレア。全眼 irAE の 30〜40% を占める。ステロイド 点眼に反応する症例が多い7) 。
角膜びらん
後眼部
VKH 様汎ぶどう膜炎 :滲出性網膜剥離 ・視神経乳頭 浮腫。メラノーマ ICI の 5〜14% に発症1) 。メラニン含有細胞への交差反応が機序。
網膜血管炎 黄斑浮腫 ・動静脈閉塞。全眼 irAE の 5〜10%4) 。
嚢胞様黄斑浮腫 OCT で確認1) 。
眼窩
眼窩 筋炎2) 。
眼窩 脂肪炎症眼窩 先端部・上眼窩 裂まで波及することがある2) 。
甲状腺眼症 様炎症
神経
眼筋型重症筋無力症 9) 。
視神経炎 ステロイド 治療で視力 維持が可能8) 。
外転神経麻痺 ステロイド で軽快することが多い8) 。
眼窩 炎症の発症時期は初回投与後 2 日〜2 ヶ月と幅広い2) 。全身 irAE(筋炎・心筋炎・大腸炎)との合併例では重症化に注意する。
ICI による眼 irAE の根本原因は、T 細胞の免疫チェックポイント解除に伴う自己免疫反応の惹起である1) 。
CTLA-4 阻害 :T 細胞の活性化を制御するブレーキを解除し、正常組織への攻撃も許容する1) PD-1/PD-L1 阻害 :眼組織の PD-L1 依存的免疫特権を直接破綻させる1) CTLA-4+PD-1 併用 :眼 irAE リスクが単剤の 2〜3 倍に増加する4) メラノーマ患者 :メラニン含有眼組織(脈絡膜 ・RPE )と腫瘍抗原の交差反応により VKH 様汎ぶどう膜炎 リスクが高い1, 10) 既存の BRB 破綻 :糖尿病網膜症 など血液網膜関門 が既存破綻した状態でリスク増大1) 宿主遺伝的素因 :HLA-DR15 など HLA 型の関与が示唆される7)
Q
なぜ免疫チェックポイント阻害薬で眼に炎症が起こるのか
A
ICI は T 細胞の免疫チェックポイントを解除してがんを攻撃させますが、眼組織の PD-L1 依存的免疫特権も同時に破綻させます1) 。病態機序は 3 型に分類され(セクション 6 参照):①抗腫瘍 T 細胞とメラニン含有眼組織の交差反応(VKH 様反応)、②バイスタンダー効果による網膜血管炎 、③自己抗体介在性炎症、が主要メカニズムです。
ICI 関連眼 irAE の診断は、ICI 使用歴と眼所見の時間的関連性に基づく。ぶどう膜炎 診療ガイドライン(2019)の基本スクリーニングを実施する3) 。被疑薬使用と症状出現の時間的関係を確認し、他の原因を除外することが診断の原則である。
部位 主な検査法 目的 前眼部 細隙灯顕微鏡 前房 炎症細胞・フレア、角膜 所見後眼部 OCT ・FA 網膜 外層信号消失、血管漏出、嚢胞様黄斑浮腫 1) 後眼部 網膜電図 (ERG )MAR 様網膜 症の杆体・錐体機能評価 眼窩 MRI 眼外筋腫大・造影増強、眼窩 脂肪炎症2)
ぶどう膜炎 眼窩 炎症VKH 様汎ぶどう膜炎 :インドシアニングリーン蛍光造影 (ICGA )で初期から脈絡膜 過蛍光(原田病 と類似の所見)1, 10)
前部ぶどう膜炎 では感染性・非感染性ぶどう膜炎 との鑑別が必要である。VKH 様反応は原発性 VKH と臨床的に類似するが、メラノーマに対する ICI 使用歴が重要な手がかりとなる1, 10) 。眼窩 筋炎では甲状腺眼症 ・IgG4 関連疾患・特発性眼窩炎症 との鑑別を要する2) 。MAR(melanoma-associated retinopathy)様網膜 症は傍腫瘍症候群との鑑別が必要である1) 。感染性ぶどう膜炎 ・転移性眼内腫瘍(仮装症候群)も除外対象に含める。
治療は腫瘍内科医と眼科医の協議のもと、CTCAE Grade に応じて個別化する。被疑薬の中止が治療の原則であるが、ICI の抗腫瘍効果は生命に直結するため、中止の判断は多職種で慎重に行う。
Grade 重症度 眼科的管理 ICI 継続可否 1 軽度(無症候・細隙灯所見のみ) ステロイド 点眼:リンデロン® 0.1% 1 日 4〜6 回継続可 2 中等度(視力 低下 1 段階・前房 炎症) テノン嚢 下注射:トリアムシノロン 20 mg+ステロイド 点眼強化慎重継続 3 重度(視力 低下 2 段階以上・汎ぶどう膜炎 ) 全身 PSL 1〜2 mg/kg/日 漸減(眼症状改善後) ICI 中断 4 失明リスク ステロイド パルス:ソル・メドロール® 1 g/日×3 日+免疫抑制薬中断・再開困難
高用量ステロイド :プレドニゾロン(PSL)1 mg/kg/日 早期導入
重症例:ステロイド パルス(メチルプレドニゾロン 1 g/日×3 日)
難治例:シクロスポリン 3〜5 mg/kg/日 追加
ICI 再開は腫瘍内科との十分な協議のもとで判断する5)
前部ぶどう膜炎 (Grade 1〜2)
ステロイド 点眼:ベタメタゾン 0.1% またはデキサメタゾン 0.1% 頻回点眼散瞳薬 :虹彩後癒着 予防(アトロピン 1% またはトロピカミド 0.5%)
中等症・後眼部炎症
テノン嚢 下注射:トリアムシノロン アセトニド 20 mg眼内インプラント(適応症例に限定)
特殊な病態
重症筋無力症 合併:血漿交換療法 を考慮9) 眼窩 炎症:全身ステロイド で大部分が軽快するが、残存複視 を呈する症例がある2)
Q
ICI ぶどう膜炎で薬を中止しなければならないか
A
ICI の中止が必要になることは稀である。Grade 1〜2 ではステロイド 点眼・局所注射により ICI を継続しながら管理できることが多い。Grade 3 以上(視力 低下 2 段階以上・汎ぶどう膜炎 )では全身ステロイド と ICI 中断が推奨される5) 。失明リスクを伴う Grade 4 では再開が困難な場合もある。中止・再開の判断は必ず腫瘍内科医との協議のもとで行う。
Q
ぶどう膜炎発症後に ICI 再開はできるか
A
炎症が十分に制御された後(Grade 1 以下)、腫瘍内科医との協議のもとで再開を検討する場合がある。ただし VKH 様汎ぶどう膜炎 などの重篤な眼 irAE では再燃リスクが高く、再開の是非は個別に判断する。再開後は眼科による密なフォローアップが必要である6) 。
眼は免疫特権臓器であり、以下の機構が T 細胞による炎症を抑制している1) 。
血液網膜関門 (BRB)が末梢 T 細胞の眼内侵入を制限する網膜色素上皮 (RPE )細胞が PD-L1・PD-L2 を発現し、T 細胞を制御性 T 細胞(Treg)へ変換するミューラー細胞・ミクログリアも PD-L1 を発現し、T 細胞介在性炎症を抑制する
TGF-β による免疫抑制的微小環境が維持される
ICI はこれらの PD-1/PD-L1 依存的な免疫特権機構を直接標的とするため、眼内 T 細胞活性化のリスクが生じる1) 。
Haliyur ら(2025)は ICI 誘発性後眼部 irAE を 3 型に分類した1) 。
Type 1: T 細胞交差反応
Type 1a :抗腫瘍 T 細胞がメラニン含有細胞など眼組織と交差反応し、VKH 様汎ぶどう膜炎 を惹起する。メラノーマ患者の 5〜14% に発症する1) 。
Type 1b :眼特異的組織常在メモリー T 細胞が ICI により拡大・活性化され、自己免疫性網膜 症を引き起こす1) 。
Type 2: バイスタンダー血管炎
ICI 使用に伴う全身的な炎症増強が非特異的に血液網膜関門 を破綻させる1) 。
CD4+ T 細胞による血管周囲リンパ形質細胞浸潤と接着分子の発現亢進が網膜血管炎 ・動静脈閉塞を引き起こす1) 。
Type 3: 自己抗体介在性
PD-1 は B 細胞にも発現しており、ICI が B 細胞系列の拡大と形質細胞からの組織特異的自己抗体産生を誘導する1) 。
傍腫瘍症候群(MAR 様網膜 症など)の増悪にも関与する1) 。
臨床所見は 1 つの機序に限定されず、複数の機序が重複することもある。VKH 様汎ぶどう膜炎 (Type 1a)は滲出性網膜剥離 と脈絡膜 過蛍光を呈し、原田病 との臨床的区別が困難な場合がある1) 。
抗 CTLA-4 阻害薬(イピリムマブ)が最も高頻度に眼窩 炎症を引き起こす2) 。抗 PD-1/PD-L1 阻害薬でも同様の臨床像が報告されている2) 。MRI では眼外筋の腫大・造影増強と眼窩 脂肪の炎症性変化を認め、両側性に出現する傾向がある2) 。
ICI 適応の急速な拡大により、今後数十年で ICI 関連眼 irAE の症例数は増加すると予測される1) 。
血清 IL-17・IL-23 の高値が VKH 様反応の予測因子として検討されている7)
HLA-DR15・HLA-A2 などの HLA タイピングによる高リスク患者の事前同定が研究されている
治療前のベースライン眼科検査と血清バイオマーカー の組み合わせによるリスク層別化が今後の課題である7)
IL-6 受容体抗体(トシリズマブ )のステロイド 抵抗性 irAE への適用が報告されている6)
ICI と抗 VEGF 薬の組み合わせによる眼内腫瘍療法への展開も注目されている
前向き多施設レジストリによる irAE 発生率・治療転帰の定量化が急務である6)
現時点では後眼部 irAE の病態理解は主に症例報告・症例集積に基づいており、診断基準や治療ガイドラインは確立されていない1) 。腫瘍内科・眼科間の連携プロトコールの整備が急務である。
Haliyur R, Elner SG, Sassalos T, Kodati S, Johnson MW. Pathogenic Mechanisms of Immune Checkpoint Inhibitor (ICI )-Associated Retinal and Choroidal Adverse Reactions. Am J Ophthalmol. 2025;272:8-18.
Ang T, Kherani A, Margolin E, Bhattacharya A, Beland F, Margolin J. Orbital Inflammation: A Review. Surv Ophthalmol. 2024;69(5):622-631.
ぶどう膜炎 診療ガイドライン作成委員会. ぶどう膜炎 診療ガイドライン. 日本眼科学会雑誌. 2019;123(6):635-696.Dalvin LA, Shields CL, Orloff M, Sato T, Shields JA. Checkpoint inhibitor immune therapy: systemic indications and ophthalmic side effects. Retina. 2018;38(6):1063-1078.
Brahmer JR, Abu-Sbeih H, Ascierto PA, et al. Society for Immunotherapy of Cancer (SITC) clinical practice guideline on immune checkpoint inhibitor-related adverse events. J Immunother Cancer. 2021;9(6):e002435.
Fortes BH, Liou H, Dalvin LA. Ophthalmic adverse effects of immune checkpoint inhibitors: the Mayo Clinic experience. Br J Ophthalmol. 2021;105(8):1108-1113.
Bitton K, Michot JM, Barreau E, et al. Prevalence and clinical patterns of ocular complications associated with anti-PD-1/PD-L1 anticancer immunotherapy. Am J Ophthalmol. 2019;202:109-117.
Chen JJ, Bhatti MT. Neuro-ophthalmic complications of immune checkpoint inhibitors. Ophthalmology. 2022;129(11):1311-1321.
Matas-García A, Milisenda JC, Selva-O’Callaghan A, et al. Ocular myasthenia gravis and myositis following immune checkpoint inhibitor therapy. Neurology. 2020;95(14):e1672-e1680.
Schulz TU, Urner J, Seegräber M, et al. Immune checkpoint inhibitor-induced Vogt-Koyanagi-Harada-like syndrome: a case report and review of literature. Ocul Immunol Inflamm. 2022;30(3):731-741.
記事の全文をコピーして、お好みのAIに貼り付けて質問できます
下のAIを開いて、チャット欄に貼り付け(ペースト)してください