전안부/안표면

면역관문억제제에 의한 포도막염 (Immune Checkpoint Inhibitor Uveitis)
한눈에 보는 포인트
섹션 제목: “한눈에 보는 포인트”1. 면역관문억제제로 인한 포도막염
섹션 제목: “1. 면역관문억제제로 인한 포도막염”면역관문억제제(ICI)는 T 세포의 브레이크 역할을 하는 관문 분자를 억제하여 암세포에 대한 면역 반응을 강화하는 단일클론항체입니다1). 암 치료에 혁명을 가져온 반면, 종양 이외의 부위에 비특이적 염증을 일으키는 면역관련 이상반응(irAE)이 문제가 됩니다1).
ICI의 분류
섹션 제목: “ICI의 분류”주요 표적 분자와 대표적인 약물은 다음과 같습니다1).
| 표적 분자 | 대표 약물 |
|---|---|
| CTLA-4 | 이필리무맙 (Yervoy®), 트레멜리무맙 |
| PD-1 | 니볼루맙 (Opdivo®), 펨브롤리주맙 (Keytruda®), 세미플리맙 |
| PD-L1 | 아테졸리주맙(Tecentriq®), 아벨루맙, 두르발루맙 |
CTLA-4는 림프절에서 T 세포 활성화를 조절하고, PD-1은 말초 조직에서 T 세포 반응을 억제합니다1). 이러한 경로의 억제는 항종양 면역을 촉진하지만 동시에 자가면역 반응을 유발할 수 있습니다. 포도막염 진료 가이드라인(2019)에서도 ICI는 약물 유발 포도막염의 중요한 원인 약물로 기재되어 있습니다3).
안구 irAE의 빈도
섹션 제목: “안구 irAE의 빈도”안구 irAE의 발생률은 13%입니다1). 후안부 염증(망막/맥락막)은 전체 안구 irAE의 약 520%를 차지하지만 중증도가 높으며 적절히 대처하지 않으면 영구적인 시력 장애로 이어질 수 있습니다1). ICI의 보험 적용 범위가 확대됨에 따라 안과와 종양내과 모두에서 인식이 더욱 중요해지고 있습니다.
안구 irAE는 전체적으로 13%의 빈도로 발생합니다1). 약제 종류에 따라 차이가 있으며, CTLA-4 단독 약 1%, PD-1 단독 0.30.6%, 두 약제 병용 시 23배의 위험 증가가 보고되었습니다4). 대부분은 안구건조증이나 전포도막염이지만, 후안부 염증(전체 안구 irAE의 520%)은 시력 예후에 영향을 미치는 중증 합병증이 될 수 있습니다.
2. 주요 증상과 임상 소견
섹션 제목: “2. 주요 증상과 임상 소견”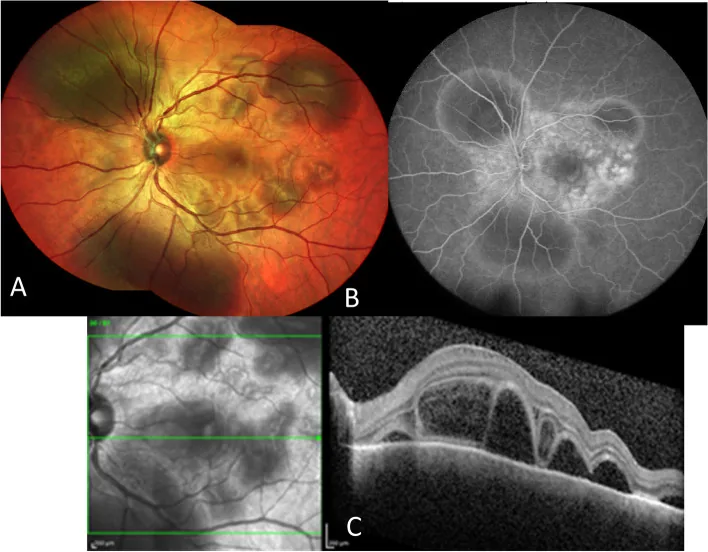
자각 증상
섹션 제목: “자각 증상”포도막염에서는 충혈, 시야 흐림, 눈부심, 안통이 주를 이룹니다. 후안부 염증에서는 시력 저하, 비문증, 변시증이 나타납니다1). 안와근염에서는 복시, 안검하수, 안구돌출이 보입니다2). 안구건조증에서는 건조감, 이물감이 주를 이룹니다.
임상 소견
섹션 제목: “임상 소견”ICI 관련 안구 irAE는 눈의 거의 모든 영역에서 발생할 수 있습니다.
후안부
안와
안와 근염(항CTLA-4에서 가장 흔함): 양측성으로 나타나기 쉽습니다. MRI에서 안외근 비대 및 조영 증강을 보입니다2).
안와 지방 염증: 안와 첨부 및 상안와열까지 파급될 수 있습니다2).
갑상선 안병증 유사 염증: 갑상선 기능이 정상인 경우에도 나타날 수 있습니다.
신경
안근형 중증 근무력증: 항AChR 항체 생산을 동반합니다. 펨브롤리주맙에서 보고됨9).
시신경염: 조기 스테로이드 치료로 시력 유지가 가능합니다8).
외전 신경 마비: 약물 중단 및 고용량 스테로이드로 호전되는 경우가 많습니다8).
안와 염증의 발병 시기는 첫 투여 후 2일에서 2개월까지 다양합니다2). 전신 irAE(근염, 심근염, 대장염)와 병발한 경우 중증화에 주의해야 합니다.
3. 원인 및 위험 요인
섹션 제목: “3. 원인 및 위험 요인”ICI에 의한 안구 irAE의 근본 원인은 T 세포의 면역관문 해제에 따른 자가면역 반응의 유발입니다1).
- CTLA-4 억제: T 세포 활성화를 조절하는 브레이크를 해제하여 정상 조직에 대한 공격도 허용합니다1)
- PD-1/PD-L1 억제: 안구 조직의 PD-L1 의존적 면역 특권을 직접 파괴합니다1)
- CTLA-4+PD-1 병용: 안구 irAE 위험이 단독 요법의 2~3배로 증가합니다4)
- 흑색종 환자: 멜라닌 함유 안구 조직(맥락막, RPE)과 종양 항원의 교차 반응으로 VKH 유사 범포도막염 위험이 높습니다1, 10)
- 기존 BRB 파괴: 당뇨망막병증 등 혈액-망막 장벽이 이미 파괴된 상태에서 위험이 증가합니다1)
- 숙주 유전적 소인: HLA-DR15 등 HLA 유형의 관여가 시사됩니다7)
ICI는 T 세포의 면역관문을 해제하여 암을 공격하게 하지만, 동시에 안구 조직의 PD-L1 의존적 면역 특권도 파괴합니다1). 병태 기전은 3가지 유형으로 분류됩니다(섹션 6 참조): ① 항종양 T 세포와 멜라닌 함유 안구 조직의 교차 반응(VKH 유사 반응), ② 방관자 효과에 의한 망막 혈관염, ③ 자가항체 매개 염증입니다.
4. 진단 및 검사 방법
섹션 제목: “4. 진단 및 검사 방법”ICI 관련 안구 irAE의 진단은 ICI 사용력과 안구 소견의 시간적 연관성에 기반합니다. 포도막염 진료 가이드라인(2019)의 기본 선별 검사를 시행합니다3). 의심 약물 사용과 증상 발현의 시간적 관계를 확인하고 다른 원인을 배제하는 것이 진단의 원칙입니다.
| 부위 | 주요 검사법 | 목적 |
|---|---|---|
| 전안부 | 세극등현미경 | 전방 염증 세포/플레어, 각막 소견 |
| 후안부 | OCT/FA | 망막 외층 신호 소실, 혈관 누출, 낭포황반부종1) |
| 후안부 | 망막전위도(ERG) | MAR 유사 망막증의 간체 및 원추체 기능 평가 |
| 안와 | MRI | 안외근 비대/조영증강, 안와 지방 염증2) |
발병 시기 참고
섹션 제목: “발병 시기 참고”- 포도막염: 첫 투여 후 2주
6개월 (중앙값 34개월) - 안와 염증: 첫 투여 후 2일~2개월
- VKH 유사 범포도막염: 인도시아닌그린 형광혈관조영술(ICGA)에서 초기 맥락막 과형광 (하라다병과 유사한 소견) 1, 10)
감별 진단
섹션 제목: “감별 진단”전방 포도막염은 감염성 및 비감염성 포도막염과의 감별이 필요합니다. VKH 유사 반응은 원발성 VKH와 임상적으로 유사하지만, 흑색종에 대한 ICI 사용력이 중요한 단서입니다1, 10). 안근염은 갑상샘 안병증, IgG4 관련 질환, 특발성 안와 염증과의 감별이 필요합니다2). MAR(흑색종 관련 망막병증) 유사 망막병증은 부종양 증후군과의 감별이 필요합니다1). 감염성 포도막염 및 전이성 안내 종양(가장 증후군)도 배제 대상에 포함됩니다.
5. 표준 치료법
섹션 제목: “5. 표준 치료법”치료는 종양내과 의사와 안과 의사의 협의 하에 CTCAE 등급에 따라 개별화합니다. 의심 약물의 중단이 치료 원칙이나, ICI의 항종양 효과는 생명에 직결되므로 중단 결정은 다학제 팀이 신중히 수행해야 합니다.
CTCAE 등급별 관리 알고리즘5)
섹션 제목: “CTCAE 등급별 관리 알고리즘5)”| 등급 | 중증도 | 안과적 관리 | ICI 지속 여부 |
|---|---|---|---|
| 1 | 경증 (무증상, 세극등 검사 소견만 있음) | 스테로이드 점안: Rinderon® 0.1% 하루 4~6회 | 지속 가능 |
| 2 | 중등도 (시력 저하 1단계, 전방 염증) | 테논낭하 주사: 트리암시놀론 20 mg + 스테로이드 점안액 강화 | 신중히 지속 |
| 3 | 중증 (시력 저하 2단계 이상, 범포도막염) | 전신 PSL 1~2 mg/kg/일, 점감 (안구 증상 호전 후) | ICI 중단 |
| 4 | 실명 위험 | 스테로이드 펄스: 솔루메드롤® 1 g/일×3일 + 면역억제제 | 중단; 재개 어려움 |
VKH 유사 범포도막염의 치료
섹션 제목: “VKH 유사 범포도막염의 치료”- 고용량 스테로이드: 프레드니솔론(PSL) 1 mg/kg/일 조기 도입
- 중증 사례: 스테로이드 펄스 (메틸프레드니솔론 1 g/일×3일)
- 난치성 증례: 사이클로스포린 3~5 mg/kg/일 추가
- ICI 재개는 종양내과와 충분한 협의 후 결정합니다5)
안과 국소 치료의 세부 사항
섹션 제목: “안과 국소 치료의 세부 사항”전포도막염(1~2등급)
중등도~중증 후안부 염증
- 테논낭하 주사: 트리암시놀론아세토나이드 20 mg
- 안내 임플란트(적응증에 한함)
특수 병태
- 중증근무력증 동반: 혈장교환술 고려9)
- 안와 염증: 대부분 전신 스테로이드로 호전되나, 잔여 복시를 보이는 증례가 있음2)
염증이 충분히 조절된 후(Grade 1 이하), 종양내과 의사와 협의하여 재개를 고려할 수 있다. 그러나 VKH 유사 범포도막염과 같은 중증 안 irAE에서는 재발 위험이 높으므로 재개 여부는 개별적으로 판단한다. 재개 후에는 안과의 밀접한 추적 관찰이 필요하다 6).
6. 병태생리학 및 상세 발병 기전
섹션 제목: “6. 병태생리학 및 상세 발병 기전”안구의 면역 특권과 ICI의 영향
섹션 제목: “안구의 면역 특권과 ICI의 영향”눈은 면역 특권 기관이며, 다음 기전이 T 세포 매개 염증을 억제한다 1).
- 혈액-망막 장벽(BRB)이 말초 T 세포의 안내 침입을 제한한다.
- 망막색소상피(RPE) 세포가 PD-L1 및 PD-L2를 발현하여 T 세포를 조절 T 세포(Treg)로 전환시킨다.
- 뮐러 세포와 미세아교세포도 PD-L1을 발현하여 T 세포 매개 염증을 억제한다.
- TGF-β에 의한 면역 억제 미세환경이 유지된다.
ICI는 이러한 PD-1/PD-L1 의존적 면역 특권 기전을 직접 표적으로 하므로, 안내 T 세포 활성화의 위험이 발생한다 1).
ICI 유발 후안부 염증의 세 가지 기전
섹션 제목: “ICI 유발 후안부 염증의 세 가지 기전”Haliyur 등(2025)은 ICI 유발 후안부 irAE를 세 가지 유형으로 분류했다 1).
Type 1: T 세포 교차 반응
Type 1a: 항종양 T 세포가 멜라닌 함유 세포 등 안구 조직과 교차 반응하여 VKH 유사 범포도막염을 유발한다. 흑색종 환자의 5~14%에서 발생한다 1).
1b형: ICI에 의해 안구 특이적 조직 상주 기억 T 세포가 확장 및 활성화되어 자가면역 망막병증을 유발합니다1).
2형: 방관자 혈관염
ICI 사용에 따른 전신 염증 증가가 비특이적으로 혈액-망막 장벽을 파괴합니다1).
CD4+ T 세포에 의한 혈관주위 림프형질세포 침윤과 부착 분자 발현 증가가 망막 혈관염 및 동정맥 폐쇄를 유발합니다1).
3형: 자가항체 매개
PD-1은 B 세포에도 발현되며, ICI가 B 세포 계열의 확장과 형질세포로부터 조직 특이적 자가항체 생성을 유도합니다1).
또한 부종양 증후군(MAR 유사 망막병증 등)의 악화에도 관여합니다1).
임상 소견은 하나의 기전에 국한되지 않으며 여러 기전이 중복될 수 있습니다. VKH 유범포도막염(1a형)은 삼출성 망막박리와 맥락막 과형광을 보이며, 하라다병과 임상적으로 구별이 어려울 수 있습니다1).
안와 염증의 기전
섹션 제목: “안와 염증의 기전”항CTLA-4 억제제(이필리무맙)가 가장 빈번하게 안와 염증을 유발합니다2). 항PD-1/PD-L1 억제제에서도 유사한 임상 양상이 보고되었습니다2). MRI에서 안외근의 비대 및 조영 증강과 안와 지방의 염증성 변화가 관찰되며, 양측성으로 나타나는 경향이 있습니다2).
7. 최신 연구 및 향후 전망
섹션 제목: “7. 최신 연구 및 향후 전망”ICI 적응증의 급속한 확대로 인해 향후 수십 년간 ICI 관련 안구 irAE 사례 수가 증가할 것으로 예상됩니다1).
바이오마커를 통한 위험 예측
섹션 제목: “바이오마커를 통한 위험 예측”- 혈청 IL-17 및 IL-23 수치 상승이 VKH 유사 반응의 예측 인자로 연구되고 있습니다7)
- HLA-DR15 및 HLA-A2와 같은 HLA 타이핑을 통한 고위험 환자의 사전 식별이 연구되고 있습니다
- 치료 전 기준 안과 검사와 혈청 바이오마커의 조합을 통한 위험 계층화는 향후 과제입니다7)
새로운 치료 전략
섹션 제목: “새로운 치료 전략”- IL-6 수용체 항체(토실리주맙)의 스테로이드 저항성 irAE에 대한 적용이 보고되었습니다6)
- ICI와 항VEGF 약물의 병용을 통한 안내 종양 치료로의 확장도 주목받고 있습니다
- 전향적 다기관 레지스트리를 통한 irAE 발생률 및 치료 결과의 정량화가 시급합니다6)
현재 후안부 irAE의 병태생리 이해는 주로 증례 보고 및 증례 집적에 기반하고 있으며, 진단 기준 및 치료 가이드라인은 확립되지 않았습니다1). 종양내과와 안과 간의 협력 프로토콜 구축이 시급합니다.
8. 참고문헌
섹션 제목: “8. 참고문헌”- Haliyur R, Elner SG, Sassalos T, Kodati S, Johnson MW. Pathogenic Mechanisms of Immune Checkpoint Inhibitor (ICI)-Associated Retinal and Choroidal Adverse Reactions. Am J Ophthalmol. 2025;272:8-18.
- Ang T, Kherani A, Margolin E, Bhattacharya A, Beland F, Margolin J. Orbital Inflammation: A Review. Surv Ophthalmol. 2024;69(5):622-631.
- ぶどう膜炎診療ガイドライン作成委員会. ぶどう膜炎診療ガイドライン. 日本眼科学会雑誌. 2019;123(6):635-696.
- Dalvin LA, Shields CL, Orloff M, Sato T, Shields JA. Checkpoint inhibitor immune therapy: systemic indications and ophthalmic side effects. Retina. 2018;38(6):1063-1078.
- Brahmer JR, Abu-Sbeih H, Ascierto PA, et al. Society for Immunotherapy of Cancer (SITC) clinical practice guideline on immune checkpoint inhibitor-related adverse events. J Immunother Cancer. 2021;9(6):e002435.
- Fortes BH, Liou H, Dalvin LA. Ophthalmic adverse effects of immune checkpoint inhibitors: the Mayo Clinic experience. Br J Ophthalmol. 2021;105(8):1108-1113.
- Bitton K, Michot JM, Barreau E, et al. Prevalence and clinical patterns of ocular complications associated with anti-PD-1/PD-L1 anticancer immunotherapy. Am J Ophthalmol. 2019;202:109-117.
- Chen JJ, Bhatti MT. Neuro-ophthalmic complications of immune checkpoint inhibitors. Ophthalmology. 2022;129(11):1311-1321.
- Matas-García A, Milisenda JC, Selva-O’Callaghan A, et al. Ocular myasthenia gravis and myositis following immune checkpoint inhibitor therapy. Neurology. 2020;95(14):e1672-e1680.
- Schulz TU, Urner J, Seegräber M, et al. Immune checkpoint inhibitor-induced Vogt-Koyanagi-Harada-like syndrome: a case report and review of literature. Ocul Immunol Inflamm. 2022;30(3):731-741.
