ยับยั้งจุดตรวจภูมิคุ้มกัน (ICI ) เป็นหลักสำคัญของการบำบัดด้วยภูมิคุ้มกันมะเร็ง แต่ก่อให้เกิดเหตุการณ์ไม่พึงประสงค์ทางภูมิคุ้มกันที่ตา (irAE) ในอัตรา 1-3% 1)
การใช้ CTLA-4 เพียงอย่างเดียวทำให้เกิด irAE ทางตาประมาณ 1% การใช้ PD-1 เพียงอย่างเดียว 0.3-0.6% และการใช้ร่วมกัน CTLA-4 + PD-1 เพิ่มความเสี่ยง 2-3 เท่า 4)
irAE ทางตาที่พบบ่อยที่สุดคือตาแห้ง และม่านตาอักเสบ ส่วนหน้า ส่วนม่านตาอักเสบ ทั่วลูกตาชนิด VKH เกิดขึ้นใน 5-14% ของการรักษามะเร็งผิวหนังเมลาโนมาด้วย ICI 1)
การรักษาหลักคือการให้สเตียรอยด์ (เฉพาะที่และทั่วร่างกาย) ตามระดับ CTCAE และไม่ค่อยจำเป็นต้องหยุด ICI 5)
การจัดการเฉพาะรายบุคคลโดยความร่วมมือระหว่างแพทย์มะเร็งวิทยาและจักษุแพทย์เป็นสิ่งจำเป็น 3)
ยับยั้งจุดตรวจภูมิคุ้มกัน (ICI ) เป็นแอนติบอดีชนิดโมโนโคลนอลที่ยับยั้งโมเลกุลจุดตรวจซึ่งทำหน้าที่เป็นเบรกของทีเซลล์ ช่วยเพิ่มการตอบสนองทางภูมิคุ้มกันต่อเซลล์มะเร็ง 1) แม้จะปฏิวัติการรักษามะเร็ง แต่ก็ก่อให้เกิดเหตุการณ์ไม่พึงประสงค์ทางภูมิคุ้มกัน (irAE) ซึ่งทำให้เกิดการอักเสบที่ไม่จำเพาะในตำแหน่งอื่นนอกเหนือจากเนื้องอก 1) .
ด้านล่างนี้คือโมเลกุลเป้าหมายหลักและยาตัวแทน 1) .
โมเลกุลเป้าหมาย ยาตัวแทน CTLA-4 อิพิลิมูแมบ (เยอร์วอย®), เทรเมลิมูแมบ PD-1 นิโวลูแมบ (ออปดิโว®), เพมโบรลิซูแมบ (คีย์ทรูดา®), เซมิพลิแมบ PD-L1 Atezolizumab (Tecentriq®), Avelumab, Durvalumab
CTLA-4 ควบคุมการกระตุ้นทีเซลล์ในต่อมน้ำเหลือง ในขณะที่ PD-1 ยับยั้งการตอบสนองของทีเซลล์ในเนื้อเยื่อรอบนอก1) การยับยั้งเหล่านี้ช่วยส่งเสริมภูมิคุ้มกันต้านเนื้องอก แต่ก็สามารถกระตุ้นปฏิกิริยาภูมิต้านตนเองได้เช่นกัน ในแนวทางการรักษาม่านตาอักเสบ (2019) มีการระบุ ICI ว่าเป็นยาสำคัญที่ทำให้เกิดม่านตาอักเสบจากยา 3)
อุบัติการณ์ของ irAE ทางตาอยู่ที่ 1–3%1) การอักเสบของส่วนหลังของตา (จอประสาทตา /คอรอยด์ ) คิดเป็นประมาณ 5–20% ของ irAE ทางตาทั้งหมด แต่มีความรุนแรงสูง และอาจนำไปสู่การสูญเสียการมองเห็น ถาวรหากไม่ได้รับการจัดการอย่างเหมาะสม1) เมื่อการครอบคลุมประกันของ ICI ขยายตัวมากขึ้น ความตระหนักรู้ทั้งในสาขาจักษุวิทยาและมะเร็งวิทยาจึงมีความสำคัญยิ่งขึ้น
Q
ผลข้างเคียงทางตาของยา checkpoint inhibitor เกิดขึ้นบ่อยแค่ไหน?
A
irAE ทางตาโดยรวมเกิดขึ้นด้วยความถี่ 1–3%1) มีความแตกต่างตามชนิดของยา: ประมาณ 1% สำหรับ CTLA-4 เพียงอย่างเดียว, 0.3–0.6% สำหรับ PD-1 เพียงอย่างเดียว และความเสี่ยงเพิ่มขึ้น 2–3 เท่าเมื่อใช้ยาทั้งสองชนิดร่วมกัน4) ส่วนใหญ่เป็นตาแห้ง หรือม่านตาอักเสบ ส่วนหน้า แต่การอักเสบส่วนหลัง (5–20% ของ irAE ทางตาทั้งหมด) อาจเป็นภาวะแทรกซ้อนรุนแรงที่ส่งผลต่อพยากรณ์การมองเห็น
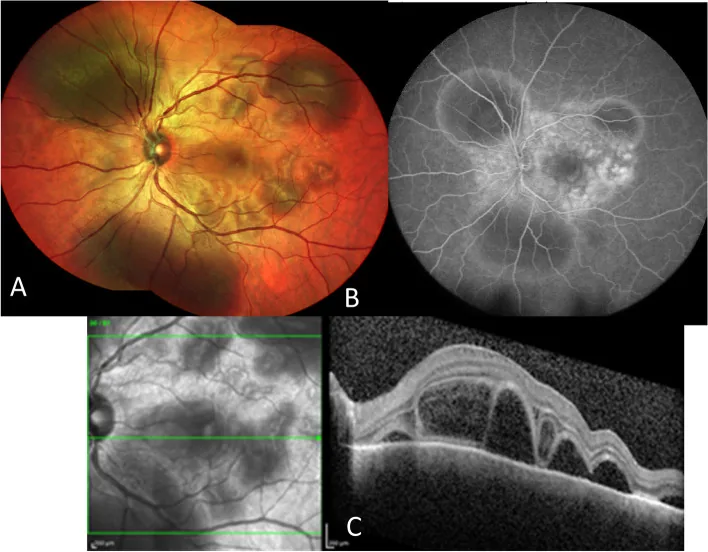
ลักษณะคล้าย VKH ในม่านตาอักเสบที่เกี่ยวข้องกับ checkpoint inhibitor จอตา, การถ่ายภาพหลอดเลือดด้วยฟลูออเรสซีน และ OCT แสดงจอตาลอกแบบมีน้ำใต้จอตา Paez-Escamilla M, et al. Challenges in posterior uveitis-tips and tricks for the retina specialist. J Ophthalmic Inflamm Infect. 2023. Figure 1. PM
CI D: PMC10435440. License: CC BY.
ภาพถ่ายจอตาแสดงรอยโรคสีขาวเหลืองและจอตาลอกแบบมีน้ำใต้จอตา การถ่ายภาพหลอดเลือดด้วยฟลูออเรสซีน แสดงการรั่วแบบหลายจุด และ OCT แสดงจอตาลอกแบบมีน้ำใต้จอตาหลายช่อง ซึ่งเป็นอาการแสดงของการอักเสบส่วนหลังในม่านตาอักเสบ ที่เกี่ยวข้องกับ checkpoint inhibitor
ในม่านตาอักเสบ อาการหลักคือ ตาแดง มองไม่ชัด กลัวแสง และปวดตา ในการอักเสบส่วนหลัง จะมีอาการตามัว เห็นจุดลอย และเห็นภาพบิดเบี้ยว 1) ในกล้ามเนื้อตาอักเสบ จะมีอาการเห็นภาพซ้อน หนังตาตก และตาโปน2) ในตาแห้ง อาการหลักคือ ความแห้งและความรู้สึกมีสิ่งแปลกปลอม
irAE ทางตาที่เกี่ยวข้องกับ ICI สามารถเกิดขึ้นได้ในเกือบทุกบริเวณของดวงตา
ส่วนหน้าและผิวตา
ตาแห้ง
ม่านตาอักเสบ ส่วนหน้าช่องหน้าลูกตา และเฟลร์ คิดเป็น 30-40% ของ irAE ทางตาทั้งหมด ผู้ป่วยส่วนใหญ่ตอบสนองต่อยาหยอดตาสเตียรอยด์ 7)
การสึกกร่อนของกระจกตา
ส่วนหลังของลูกตา
ม่านตาอักเสบทั้งลูกตา คล้าย VKHจอประสาทตาลอก แบบมีน้ำใต้จอตาและขั้วประสาทตาบวม เกิดขึ้นใน 5-14% ของผู้ป่วยที่ได้รับ ICI สำหรับมะเร็งผิวหนังเมลาโนมา1) กลไกคือปฏิกิริยาข้ามกับเซลล์ที่มีเมลานิน
หลอดเลือดจอตาอักเสบ : การรั่วของหลอดเลือด จุดรับภาพบวม หลอดเลือดแดงและดำอุดตัน คิดเป็น 5-10% ของ irAE ทางตาทั้งหมด4)
จอประสาทตา บวมชนิดซีสต์OCT 1)
เบ้าตา
กล้ามเนื้อเบ้าตา อักเสบ (พบบ่อยที่สุดกับยาต้าน CTLA-4): มักเกิดสองข้าง MRI พบกล้ามเนื้อนอกลูกตา โตและมีการเพิ่มความเข้มของสารทึบแสง2)
ไขมันเบ้าตา อักเสบ : อาจลุกลามถึงยอดเบ้าตา และรอยแยกเบ้าตา บน2)
การอักเสบคล้ายโรคตาจากต่อมไทรอยด์ : เกิดขึ้นแม้ในผู้ป่วยที่มีการทำงานของต่อมไทรอยด์ปกติ
ระบบประสาท
โรคกล้ามเนื้ออ่อนแรงชนิดตา : ร่วมกับการสร้างแอนติบอดีต่อ AChR มีรายงานกับเพมโบรลิซูแมบ9)
ประสาทตาอักเสบ : สามารถรักษาการมองเห็น ได้ด้วยการรักษาด้วยสเตียรอยด์ ตั้งแต่เนิ่นๆ8)
เส้นประสาทสมองคู่ที่ 6 เป็นอัมพาต : มักดีขึ้นเมื่อหยุดยาและให้สเตียรอยด์ ขนาดสูง8)
ระยะเวลาการเกิดการอักเสบของเบ้าตา มีความหลากหลาย ตั้งแต่ 2 วันถึง 2 เดือนหลังจากได้รับยาครั้งแรก2) ในกรณีที่มี irAE ทั่วร่างกายร่วมด้วย (กล้ามเนื้ออักเสบ กล้ามเนื้อหัวใจอักเสบ ลำไส้ใหญ่อักเสบ) ต้องระวังการลุกลามรุนแรง
สาเหตุพื้นฐานของ irAE ทางตาที่เกิดจาก ICI คือการกระตุ้นปฏิกิริยาภูมิต้านตนเองเนื่องจากการปลดล็อกจุดตรวจสอบภูมิคุ้มกันของทีเซลล์1)
การยับยั้ง CTLA-4 : ปลดเบรกที่ควบคุมการกระตุ้นทีเซลล์ ทำให้สามารถโจมตีเนื้อเยื่อปกติได้เช่นกัน1) การยับยั้ง PD-1/PD-L1 : ทำลายเอกสิทธิ์ทางภูมิคุ้มกันที่ขึ้นกับ PD-L1 ของเนื้อเยื่อตาโดยตรง1) การใช้ CTLA-4 ร่วมกับ PD-1 : ความเสี่ยงของ irAE ทางตาเพิ่มขึ้น 2-3 เท่าเมื่อเทียบกับการใช้ยาเดี่ยว4) ผู้ป่วยมะเร็งผิวหนังชนิดเมลาโนมา : เนื่องจากปฏิกิริยาข้ามระหว่างเนื้อเยื่อตาที่มีเมลานิน (คอรอยด์ , RPE ) และแอนติเจนของเนื้องอก ทำให้มีความเสี่ยงสูงต่อการเกิด panuveitis คล้าย VKH1, 10) การทำลาย BRB ที่มีอยู่ก่อน : ภาวะเช่นจอประสาทตาเสื่อมจากเบาหวาน ที่มีการทำลาย Blood-Retinal Barrier อยู่ก่อนแล้วจะเพิ่มความเสี่ยง1) ความโน้มเอียงทางพันธุกรรมของโฮสต์ : มีการเสนอว่า HLA ชนิดต่างๆ เช่น HLA-DR15 มีส่วนเกี่ยวข้อง7)
เมื่อใช้ ICI แนะนำให้ตรวจตาพื้นฐานก่อนเริ่มการรักษา หากในระหว่างการรักษามีอาการทางตา เช่น ตาแดง การมองเห็น ลดลง เห็นภาพซ้อน หรือเห็นจุดลอย ควรไปพบจักษุแพทย์ทันที
Q
ทำไมยับยั้งจุดตรวจสอบภูมิคุ้มกันจึงทำให้เกิดการอักเสบในตา?
A
ICI ปลดล็อกจุดตรวจสอบภูมิคุ้มกันของทีเซลล์เพื่อโจมตีมะเร็ง แต่ในขณะเดียวกันก็ทำลายเอกสิทธิ์ทางภูมิคุ้มกันที่ขึ้นกับ PD-L1 ของเนื้อเยื่อตา1) กลไกพยาธิวิทยาแบ่งเป็น 3 ประเภท (ดูหัวข้อ 6): ① ปฏิกิริยาข้ามระหว่างทีเซลล์ต้านเนื้องอกและเนื้อเยื่อตาที่มีเมลานิน (ปฏิกิริยาคล้าย VKH), ② หลอดเลือดจอประสาทตาอักเสบ จากผลข้างเคียง, ③ การอักเสบที่อาศัยแอนติบอดีตนเอง เป็นกลไกหลัก
การวินิจฉัย irAE ทางตาที่เกี่ยวข้องกับ ICI ขึ้นอยู่กับความสัมพันธ์ทางเวลาระหว่างประวัติการใช้ ICI และอาการทางตา ดำเนินการตรวจคัดกรองพื้นฐานตามแนวทางการรักษาม่านตาอักเสบ (2019)3) หลักการวินิจฉัยคือยืนยันความสัมพันธ์ทางเวลาระหว่างการใช้ยาที่สงสัยและการเกิดอาการ และแยกสาเหตุอื่นออก
ตำแหน่ง การตรวจหลัก วัตถุประสงค์ ส่วนหน้าของตา กล้องจุลทรรศน์หลอดกรีด เซลล์อักเสบในช่องหน้าตา, flare, ผลการตรวจกระจกตา ส่วนหลังของตา OCT และ FA การสูญเสียสัญญาณชั้นนอกของจอตา, การรั่วของหลอดเลือด, จอประสาทตา บวมแบบถุงน้ำ1) ส่วนหลังของตา การตรวจคลื่นไฟฟ้าจอตา (ERG ) การประเมินการทำงานของเซลล์รูปแท่ง และรูปกรวยในจอตาอักเสบแบบ MAR เบ้าตา MRI กล้ามเนื้อนอกตาขยายใหญ่และการเพิ่มความเข้มของสารทึบรังสี, การอักเสบของไขมันเบ้าตา 2)
ม่านตาอักเสบ (Uveitis)เบ้าตา อักเสบ (Orbital inflammation)ม่านตาอักเสบทั้งลูกตา ชนิดคล้าย VKHคอรอยด์ มากเกินไปตั้งแต่ระยะแรกในการตรวจหลอดเลือดด้วยสีอินโดไซยานีนกรีน (ICGA ) (ลักษณะคล้ายโรคฮาราดะ ) 1, 10)
ในม่านตาอักเสบ ส่วนหน้า จำเป็นต้องแยกความแตกต่างระหว่างม่านตาอักเสบ จากการติดเชื้อและไม่ใช่การติดเชื้อ ปฏิกิริยาคล้าย VKH มีลักษณะทางคลินิกคล้ายกับ VKH ปฐมภูมิ แต่ประวัติการใช้ ICI สำหรับมะเร็งผิวหนังชนิดเมลาโนมาเป็นเบาะแสสำคัญ 1, 10) ในกล้ามเนื้อเบ้าตา อักเสบ ต้องแยกจากโรคตาจากต่อมไทรอยด์ โรคที่เกี่ยวข้องกับ IgG4 และเบ้าตา อักเสบไม่ทราบสาเหตุ 2) จอประสาทตา เสื่อมชนิดคล้าย MAR (melanoma-associated retinopathy) ต้องแยกจากกลุ่มอาการพารานีโอพลาสติก 1) ต้องแยกม่านตาอักเสบ จากการติดเชื้อและเนื้องอกในลูกตาที่แพร่กระจาย (masquerade syndrome) ออกด้วย
การรักษาจะปรับให้เฉพาะบุคคลโดยปรึกษาระหว่างแพทย์มะเร็งวิทยาและจักษุแพทย์ตามระดับ CTCAE หลักการรักษาคือการหยุดยาที่สงสัย แต่เนื่องจากฤทธิ์ต้านเนื้องอกของ ICI เกี่ยวข้องโดยตรงกับชีวิต การตัดสินใจหยุดยาจึงต้องทำอย่างระมัดระวังโดยทีมสหสาขาวิชาชีพ
ระดับ ความรุนแรง การจัดการทางจักษุวิทยา การให้ ICI ต่อ 1 เล็กน้อย (ไม่มีอาการ, พบเฉพาะจากการตรวจด้วย slit lamp) ยาหยอดตาสเตียรอยด์ : Rinderon® 0.1% 4-6 ครั้งต่อวัน สามารถให้ต่อได้ 2 ปานกลาง (สายตาลดลง 1 ระดับ, อักเสบในช่องหน้าม่านตา ) ฉีดใต้เยื่อหุ้ม Tenon: triamcinolone 20 มก. + หยอดตาสเตียรอยด์ เพิ่ม ดำเนินต่อด้วยความระมัดระวัง 3 รุนแรง (สายตาลดลง ≥2 ระดับ, ม่านตาอักเสบทั้งลูกตา ) prednisolone ทั่วร่างกาย 1-2 มก./กก./วัน ลดขนาดลง (หลังจากอาการทางตาดีขึ้น) หยุด ICI 4 เสี่ยงตาบอด สเตียรอยด์ พัลส์: Solu-Medrol 1 ก./วัน × 3 วัน + ยากดภูมิคุ้มกันหยุดและยากต่อการเริ่มใหม่
สเตียรอยด์ ขนาดสูง: prednisolone 1 มก./กก./วัน เริ่มต้นเร็วกรณีรุนแรง: สเตียรอยด์ พัลส์ (methylprednisolone 1 ก./วัน × 3 วัน)
กรณีดื้อต่อการรักษา: เพิ่ม cyclosporine 3-5 มก./กก./วัน
การตัดสินใจเริ่มใช้ ICI อีกครั้งควรทำหลังจากปรึกษากับแพทย์ด้านมะเร็งวิทยาอย่างเพียงพอ5)
ม่านตาอักเสบ ส่วนหน้า (ระดับ 1-2)
ยาหยอดตาสเตียรอยด์ : betamethasone 0.1% หรือ dexamethasone 0.1% หยอดบ่อยครั้ง
ยาขยายม่านตา : เพื่อป้องกันการยึดติดของม่านตา ส่วนหลัง (atropine 1% หรือ tropicamide 0.5%)
กรณีปานกลางและการอักเสบของส่วนหลังของตา
การฉีดใต้ Tenon: triamcinolone acetonide 20 มก.
การฝังเทียมในลูกตา (เฉพาะในกรณีที่เหมาะสม)
ภาวะพิเศษ
ภาวะแทรกซ้อน myasthenia gravis: พิจารณาการแลกเปลี่ยนพลาสมา 9)
การอักเสบของเบ้าตา : ส่วนใหญ่ดีขึ้นด้วยสเตียรอยด์ ทั่วร่างกาย แต่บางรายอาจมีภาพซ้อน หลงเหลืออยู่2)
Q
จำเป็นต้องหยุดยาในม่านตาอักเสบจาก ICI หรือไม่?
A
ไม่ค่อยจำเป็นต้องหยุด ICI ในระดับ 1–2 มักสามารถจัดการได้ด้วยยาหยอดตาสเตียรอยด์ หรือการฉีดเฉพาะที่ขณะที่ยังคงใช้ ICI ต่อไป ในระดับ 3 ขึ้นไป (การมองเห็น ลดลง 2 ขั้นหรือมากกว่า, panuveitis) แนะนำให้ใช้สเตียรอยด์ ทั้งร่างกายและหยุด ICI ชั่วคราว 5) ในระดับ 4 ที่มีความเสี่ยงต่อการสูญเสียการมองเห็น อาจยากต่อการเริ่มใช้ใหม่ การตัดสินใจหยุดหรือเริ่มใช้ใหม่ต้องปรึกษากับแพทย์มะเร็งวิทยาเสมอ
Q
สามารถเริ่มใช้ ICI ใหม่หลังจากเกิด uveitis ได้หรือไม่?
A
หลังจากควบคุมการอักเสบได้ดี (ระดับ 1 หรือน้อยกว่า) อาจพิจารณาเริ่มใช้ใหม่โดยปรึกษากับแพทย์มะเร็งวิทยา อย่างไรก็ตาม ในกรณี panuveitis คล้าย VKH และ irAE ทางตาที่รุนแรงอื่นๆ ความเสี่ยงของการกลับเป็นซ้ำสูง และความเหมาะสมในการเริ่มใช้ใหม่จะพิจารณาเป็นรายบุคคล หลังจากเริ่มใช้ใหม่ จำเป็นต้องมีการติดตามอย่างใกล้ชิดโดยจักษุแพทย์ 6)
ดวงตาเป็นอวัยวะที่มีภูมิคุ้มกันพิเศษ และกลไกต่อไปนี้ยับยั้งการอักเสบที่อาศัยทีเซลล์ 1)
Blood-retinal barrier (BRB) จำกัดการเข้าสู่ดวงตาของทีเซลล์จากกระแสเลือดส่วนปลาย
เซลล์ retinal pigment epithelium (RPE ) แสดง PD-L1 และ PD-L2 และเปลี่ยนทีเซลล์ให้เป็น regulatory T cells (Treg)
เซลล์ Müller และ microglia ยังแสดง PD-L1 และยับยั้งการอักเสบที่อาศัยทีเซลล์
สภาพแวดล้อมจุลภาคที่กดภูมิคุ้มกันโดย TGF-β ถูกคงไว้
ICI มุ่งเป้าโดยตรงต่อกลไกภูมิคุ้มกันพิเศษที่ขึ้นกับ PD-1/PD-L1 ดังนั้นจึงเกิดความเสี่ยงของการกระตุ้นทีเซลล์ภายในดวงตา 1)
Haliyur และคณะ (2025) จำแนก irAE ส่วนหลังของตาที่เกิดจาก ICI ออกเป็น 3 ชนิด 1)
ชนิดที่ 1: การเกิดปฏิกิริยาข้ามของทีเซลล์
ชนิดที่ 1a : ทีเซลล์ต้านเนื้องอกเกิดปฏิกิริยาข้ามกับเนื้อเยื่อตาที่มีเมลานิน ทำให้เกิด panuveitis คล้าย VKH เกิดขึ้นในผู้ป่วยมะเร็งผิวหนังชนิดเมลาโนมา 5–14% 1)
ชนิด 1b : เซลล์ทีหน่วยความจำที่อาศัยอยู่ในเนื้อเยื่อเฉพาะของตาถูกขยายและกระตุ้นโดย ICI ทำให้เกิดจอประสาทตา อักเสบจากภูมิต้านตนเอง1)
ชนิด 2: หลอดเลือดอักเสบแบบ Bystander
การอักเสบทั่วร่างกายที่เพิ่มขึ้นจากการใช้ ICI ทำให้สิ่งกีดขวางเลือด-จอประสาทตา ถูกทำลายอย่างไม่จำเพาะ1)
การแทรกซึมของลิมโฟพลาสมาไซต์รอบหลอดเลือดโดยเซลล์ที CD4+ และการเพิ่มการแสดงออกของโมเลกุลยึดเกาะทำให้เกิดหลอดเลือดจอประสาทตาอักเสบ และการอุดตันของหลอดเลือดแดง-ดำ1)
ชนิด 3: อาศัยแอนติบอดีตนเอง
PD-1 ยังแสดงออกบนเซลล์บี และ ICI กระตุ้นการขยายสายเซลล์บีและการผลิตแอนติบอดีตนเองจำเพาะเนื้อเยื่อจากพลาสมาเซลล์1)
ยังเกี่ยวข้องกับการกำเริบของกลุ่มอาการพารานีโอพลาสติก (เช่น จอประสาทตา อักเสบคล้าย MAR)1)
ผลการตรวจทางคลินิกไม่ได้จำกัดอยู่เพียงกลไกเดียว กลไกหลายอย่างอาจซ้อนทับกันได้ ม่านตาอักเสบ ทั่วทั้งลูกตาคล้าย VKH (ชนิด 1a) แสดงจอประสาทตา หลุดลอกแบบมีน้ำใต้จอประสาทตา และคอรอยด์ เรืองแสงมากเกินไป และบางครั้งแยกจากโรคฮาราดะ ทางคลินิกได้ยาก1)
ยายับยั้ง CTLA-4 (ipilimumab) ทำให้เกิดการอักเสบของเบ้าตา บ่อยที่สุด2) มีรายงานลักษณะทางคลินิกที่คล้ายกันกับยายับยั้ง PD-1/PD-L12) MRI แสดงกล้ามเนื้อนอกลูกตา โตขึ้น การเพิ่มความเข้มของสารทึบรังสี และการเปลี่ยนแปลงการอักเสบในไขมันเบ้าตา โดยมีแนวโน้มเกิดขึ้นทั้งสองข้าง2)
เนื้อหาต่อไปนี้ยังอยู่ในขั้นตอนการวิจัยหรือการทดลองทางคลินิก และไม่ใช่การรักษามาตรฐานที่สามารถรับได้ในโรงพยาบาลทั่วไป เป็นข้อมูลอ้างอิงสำหรับผู้เชี่ยวชาญเกี่ยวกับความก้าวหน้าทางการแพทย์ในอนาคต
ด้วยการขยายตัวอย่างรวดเร็วของข้อบ่งชี้ของ ICI คาดว่าจำนวนผู้ป่วย irAE ทางตาที่เกี่ยวข้องกับ ICI จะเพิ่มขึ้นในอีกไม่กี่ทศวรรษข้างหน้า1)
ระดับ IL-17 และ IL-23 ในซีรัมที่สูงกำลังถูกศึกษาในฐานะปัจจัยทำนายปฏิกิริยาคล้าย VKH 7)
การระบุผู้ป่วยที่มีความเสี่ยงสูงล่วงหน้าด้วยการตรวจ HLA typing เช่น HLA-DR15 และ HLA-A2 กำลังอยู่ระหว่างการศึกษา
การแบ่งชั้นความเสี่ยงโดยการรวมการตรวจตาเบื้องต้นก่อนการรักษาและตัวบ่งชี้ทางชีวภาพ ในซีรัมเป็นความท้าทายในอนาคต 7)
มีการรายงานการใช้แอนติบอดีต่อตัวรับ IL-6 (tocilizumab) สำหรับ irAE ที่ดื้อต่อสเตียรอยด์ 6)
การรวม ICI และยาต้าน VEGF สำหรับการรักษาเนื้องอกในลูกตาก็กำลังได้รับความสนใจ
การจัดทำทะเบียนไปข้างหน้าแบบหลายศูนย์เพื่อวัดอุบัติการณ์ของ irAE และผลลัพธ์การรักษาเป็นเรื่องเร่งด่วน 6)
ปัจจุบัน ความเข้าใจเกี่ยวกับพยาธิสรีรวิทยาของ irAE ในส่วนหลังของตาส่วนใหญ่ขึ้นอยู่กับรายงานผู้ป่วยและชุดผู้ป่วย และยังไม่มีการกำหนดเกณฑ์การวินิจฉัยหรือแนวทางการรักษา 1) การพัฒนาโปรโตคอลความร่วมมือระหว่างอายุรศาสตร์มะเร็งและจักษุวิทยาเป็นเรื่องเร่งด่วน
Haliyur R, Elner SG, Sassalos T, Kodati S, Johnson MW. Pathogenic Mechanisms of Immune Checkpoint Inhibitor (ICI )-Associated Retinal and Choroidal Adverse Reactions. Am J Ophthalmol. 2025;272:8-18.
Ang T, Kherani A, Margolin E, Bhattacharya A, Beland F, Margolin J. Orbital Inflammation: A Review. Surv Ophthalmol. 2024;69(5):622-631.
ぶどう膜炎診療ガイドライン作成委員会. ぶどう膜炎診療ガイドライン. 日本眼科学会雑誌. 2019;123(6):635-696.
Dalvin LA, Shields CL, Orloff M, Sato T, Shields JA. Checkpoint inhibitor immune therapy: systemic indications and ophthalmic side effects. Retina. 2018;38(6):1063-1078.
Brahmer JR, Abu-Sbeih H, Ascierto PA, et al. Society for Immunotherapy of Cancer (SITC) clinical practice guideline on immune checkpoint inhibitor-related adverse events. J Immunother Cancer. 2021;9(6):e002435.
Fortes BH, Liou H, Dalvin LA. Ophthalmic adverse effects of immune checkpoint inhibitors: the Mayo Clinic experience. Br J Ophthalmol. 2021;105(8):1108-1113.
Bitton K, Michot JM, Barreau E, et al. Prevalence and clinical patterns of ocular complications associated with anti-PD-1/PD-L1 anticancer immunotherapy. Am J Ophthalmol. 2019;202:109-117.
Chen JJ, Bhatti MT. Neuro-ophthalmic complications of immune checkpoint inhibitors. Ophthalmology. 2022;129(11):1311-1321.
Matas-García A, Milisenda JC, Selva-O’Callaghan A, et al. Ocular myasthenia gravis and myositis following immune checkpoint inhibitor therapy. Neurology. 2020;95(14):e1672-e1680.
Schulz TU, Urner J, Seegräber M, et al. Immune checkpoint inhibitor-induced Vogt-Koyanagi-Harada-like syndrome: a case report and review of literature. Ocul Immunol Inflamm. 2022;30(3):731-741.
ถาม AI เกี่ยวกับบทความนี้
คัดลอกข้อความบทความแล้ววางในผู้ช่วย AI ที่คุณต้องการใช้
เปิดผู้ช่วย AI ด้านล่าง แล้ววางข้อความที่คัดลอกลงในช่องแชต