AS 단독

혈관모양줄무늬 (Angioid Streaks)
1. 망막색소선조란?
섹션 제목: “1. 망막색소선조란?”망막색소선조(Angioid Streaks; AS)는 선천적 소인으로 인해 전신의 탄력섬유 변성을 일으키는 질환입니다. Bruch막의 탄력섬유도 변성되어 파열이 발생한 결과, 시신경유두에서 방사상으로 색소 침착을 동반한 흰색 선상 변화를 특징으로 하는 안저 소견을 보입니다.
전신 탄력섬유 변성에 기인한 결합조직 질환으로, Bruch막의 취약화로 인해 파열이 생기고 색소선조가 나타납니다. 1889년 Doyne이 처음 보고하였고, 1892년 Knapp이 ‘angioid streaks’라고 명명했습니다.
역학적으로 PXE의 유병률은 1:25,0001:100,000으로 보고되며, PXE 환자의 85100%에서 AS가 나타납니다. 2) AS는 양안성으로 나타나며 남성에 많습니다.
관련 전신 질환의 암기법으로 PEPSI가 알려져 있습니다.
- P: 탄력섬유성 가성황색종(Pseudoxanthoma elasticum; PXE)
- E: 엘러스-단로스 증후군 (Ehlers-Danlos syndrome)
- P: 파제트병 (뼈 파제트병, AS 합병률 8~15%2))
- S: 겸상 적혈구병 (Sickle cell disease)
- I: 특발성 (Idiopathic)
PXE는 가장 빈번한 관련 질환이며, PXE에 망막 색소 선조가 합병된 병태는 Grönblad-Strandberg 증후군이라고 합니다. PXE는 ABCC6 유전자의 돌연변이로 인해 발생하며, 눈, 피부, 심혈관계의 세 장기에 병변을 일으키는 전신 질환입니다.3) 최근 엘러스-단로스 증후군과의 합병률은 재평가되어 실제로는 1% 미만으로 간주됩니다.2)
후생노동성 PXE 진단 기준: PXE는 2015년에 지정 난치병으로 지정되어 의료비 지원 대상이 되었습니다.
| 진단 항목 | 내용 |
|---|---|
| ① 피부 병변 | 굴곡부의 황반, 피부 이완 등 |
| ② 피부 병리 | 탄력 섬유의 석회화를 동반한 변성 |
| ③ 안저 소견 | 망막색소선조의 존재 |
| ④ 유전자 | ABCC6 유전자 돌연변이 |
- 확진:(① 또는 ②)그리고 ③
- 의심:(① 또는 ②)만, 또는 ③만
- 의증례에서 유전자 변이가 확인되면 확진으로 간주합니다.
2. 주요 증상 및 임상 소견
섹션 제목: “2. 주요 증상 및 임상 소견”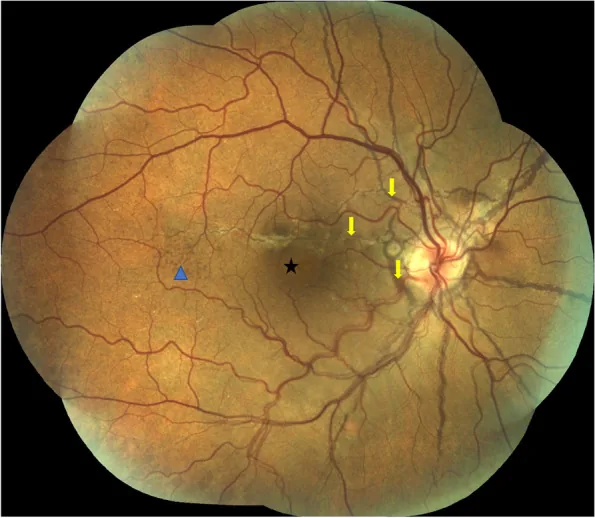
자각 증상
섹션 제목: “자각 증상”망막색소선조는 일반적으로 무증상이며 우연히 발견되는 경우가 많습니다. CNV가 발생하기 전까지는 자각 증상이 없는 경우가 많으며, 우연한 안과 또는 피부과 진료에서 발견되기도 합니다.
CNV가 합병되면 다음과 같은 증상이 나타납니다.
- 변시증(물체가 왜곡되어 보임): CNV 형성 초기부터 나타납니다.
- 중심 암점: 중심 시야에 어두운 부분이 생깁니다.
- 급격한 시력 저하: CNV가 황반부에 미치면 빠르게 진행됩니다.
CNV가 발생하면 치료에 저항성을 보이고 재발을 반복하는 경우가 많습니다.
임상 소견
섹션 제목: “임상 소견”세극등 현미경 및 안저 검사에서 다음과 같은 소견이 관찰됩니다.
혈관모양 줄무늬는 시신경 유두 주위에서 방사상(불가사리 모양)으로 뻗어 나가는 불규칙한 선상 변화입니다. 일반적으로 줄무늬는 색소 침착을 동반한 흰색을 띱니다. 형태는 화염상 또는 불가사리형을 취할 수 있습니다. 보통 양안성입니다.
오렌지 껍질 안저는 PXE의 특징적인 소견으로, 후극부에서 중간 주변부까지 거친 과립상 색소 침착과 주변부의 황백색 반점이 혼재된 안저상을 나타냅니다. 그 외에 유두 주위 맥락망막 위축 및 시신경 유두 드루젠이 동반되는 경우가 많습니다.
CNV 합병
증례 보고로, Mandura 등(2021)이 보고한 27세 여성 PXE 환자에서는 양안 시력 20/20, 정상 안압, CNV 및 망막하 출혈이 없는 소견이 확인되어, PXE 환자에서도 CNV를 동반하지 않는 경과가 존재함을 보여줍니다. 1)
3. 원인 및 위험 요인
섹션 제목: “3. 원인 및 위험 요인”혈관양 선조의 기저 병태는 브루크막의 석회화와 취약화이며, 가장 관련이 깊은 질환은 PXE입니다. PXE는 ABCC6 유전자 돌연변이에 의해 발생하며, 세 가지 유전형이 알려져 있습니다. 상염색체 열성 유전이 가장 흔합니다. 3)
PXE의 각 유전형별 임상 양상은 다음과 같습니다.
| 유전형 | 임상 양상 |
|---|---|
| AR형 (상염색체 열성) | 가장 흔한 유전형. 눈, 피부, 심혈관계의 세 장기에 병변이 나타납니다. |
| AD 1형 (상염색체 우성) | 굴곡부 발진, 협심증, 고혈압, 중증 맥락망막염 |
| AD 2형 (상염색체 우성) | 반상 발진, 경도 망막 변성 |
ABCC6 유전자의 p.R1268Q 돌연변이는 맥락막 혈관선의 조기 발병과 관련이 있는 것으로 보고되었습니다. 3)
ABCC6는 간과 신장에서 높게 발현되는 MRP6(다약제 내성 관련 단백질 6)를 코딩하며, 항석회화 인자(무기 피로인산, 페투인 A 등)의 혈중 방출에 관여합니다. 유전자 돌연변이로 인해 항석회화 인자가 결핍되어 전신 탄성 조직에 칼슘이 침착됩니다. 4)
파제트병(골 교체 증가 → 혈청 ALP 상승)에서 AS 합병률은 8~15%에 이릅니다. 2) 겸상적혈구병에서는 헤모글로빈 S → 적혈구 변형 → 브루크막 철 침착 → 약화의 기전이 관여합니다. 2) 또한 둔상이 브루크막 파열을 촉진하고 CNV 발병 위험을 높입니다. 2)
4. 진단 및 검사 방법
섹션 제목: “4. 진단 및 검사 방법”진단은 주로 안저 검사를 통한 임상 진단이며, 시신경 유두 주변에서 방사상으로 뻗어 나가는 특징적인 선조를 확인하는 것이 기본입니다.
다양한 영상 검사의 주요 소견은 아래와 같습니다.
| 검사 | 주요 소견 |
|---|---|
| FA (형광안저조영술) | 색소선조부: window defect + 조직 염색 → 뚜렷한 과형광. 색소침착부: 차단에 의한 저형광. CNV: 전형적인 CNV 소견 |
| ICGA (인도시아닌그린 조영술) | 색소선조부가 후기에 조직 염색에 의한 과형광으로 가장 뚜렷함. 감별 진단에 중요한 역할 |
| OCT | 편평한 CNV가 가로로 퍼지는 증례가 많음. 활동성이 높은 시기에는 망막하 피브린, 망막하 출혈, 망막 부종. en face OCT로 선조 병변의 층별 평가가 유용함5) |
| FAF (안저자가형광) | 다른 관찰 방법보다 광범위한 RPE 손상을 검출합니다. 병변 범위 평가에 유용합니다. |
감별 진단
섹션 제목: “감별 진단”황반부 병변에만 주의를 기울이면 연령 관련 황반변성(AMD)이나 폴립양 맥락막혈관병증(PCV)으로 오진하기 쉽습니다. 유두 주변 관찰이 감별의 핵심입니다.
- AMD/PCV: 고령자나 단안성인 경우 오진에 주의하십시오. AS-CNV는 AMD보다 젊은 나이에 발생하고 양안성인 경우가 많아 감별의 핵심입니다.
- 래커 균열(Lacquer cracks): 고도 근시와 관련된 브루크막 균열. 안축장, 굴절값, 피부 생검으로 감별.
- 맥락막 파열: 안외상 후 발생. 손상 병력으로 감별.
전신 검사
섹션 제목: “전신 검사”AS가 의심되면 피부 시진이 중요하며, PXE 합병이 의심되면 피부과에 자문하여 피부 생검을 고려합니다. PXE가 확인되면 심혈관계 이상에 대한 정밀 검사도 필수입니다.
- 피부 생검: PXE 진단의 표준 검사. 탄력섬유 석회화 확인.
- ALP, Ca/P: 파제트병 선별검사. 2)
- 헤모글로빈 전기영동: 겸상적혈구증 확인. 2)
5. 표준 치료법
섹션 제목: “5. 표준 치료법”AS 단독(CNV 비합병)에는 특정 치료가 필요하지 않으며, 정기적인 경과 관찰이 기본입니다. 환자에게 외상 회피 상담을 시행합니다. 2)
CNV 합병 시 치료
섹션 제목: “CNV 합병 시 치료”유두황반 사이에 CNV가 형성되면 비교적 단기간에 황반부로 진행하는 경향이 있습니다. 자연 경과의 예후는 매우 나쁘며 신속한 치료 시작이 필요합니다.
기존 치료(효과 제한적): 신생혈관 제거술, 레이저 광응고술, 광역학치료(PDT), 스테로이드 국소 투여가 시행되어 왔으나 치료 효과는 제한적이고 재발이 많아 어려움을 겪는 경우가 많았습니다.
현재 일차 선택: 항VEGF 약물 유리체내 주입
- 라니비주맙 0.5mg/0.05mL: 전향적 연구(12개월)에서 평균 시력 안정
개선. 평균 주사 횟수는 연 35회. 7) - 베바시주맙 1.25mg/0.05mL(적응증 외): 6~12개월에 중심와 두께 감소와 시력 안정화가 보고되었습니다. 8)
- 아플리버셉트 2mg/0.05mL: 12개월에 시력 유지~개선 및 중심와 두께의 유의한 감소. 9)
- 도입기: 매월 1회, 총 3회, 이후 PRN 방식이 일반적입니다. 7), 8)
장기 예후는 재발률이 높고, 수년간 주사를 지속해야 하는 증례가 많습니다. 황반 위축의 진행으로 장기 시력 예후가 제한적이라는 보고가 있습니다. 10)
PDT는 항VEGF 시대 이전에 중심와외 CNV에 시행되었으나, 현재는 항VEGF 단독 요법이 주류입니다. 2)
항VEGF 유리체강내 주사(라니비주맙, 베바시주맙, 아플리베르셉트)로 12개월째 시력 안정~개선이 보고되었습니다. 7), 8), 9) 그러나 재발률이 높고, 연령 관련 황반변성보다 추가 투여가 더 많이 필요한 경우가 많습니다. 장기적으로는 황반 위축이 진행되어 시력 예후가 제한적인 증례도 있습니다. 10)
6. 병태생리학 및 상세 발병 기전
섹션 제목: “6. 병태생리학 및 상세 발병 기전”Bruch막은 엘라스틴과 콜라겐이 풍부한 5층 구조로, 맥락막 모세혈관과 RPE 사이에 위치하여 대사산물과 영양소의 수송을 담당합니다. 2)
PXE에서는 ABCC6 유전자 변이로 MRP6 기능이 결손되어 간에서 무기 피로인산, 페투인 A 등의 항석회화 인자 분비가 감소합니다. 그 결과 전신 탄성 조직에 칼슘이 침착되고, Bruch 막도 석회화 및 취약화되어 파열에 이릅니다. 4)
Bruch 막 파열부와 RPE 손상부를 통해 2형 CNV가 발생합니다. Bruch 막의 비후 및 석회화는 태아 측 태반에서도 관찰되므로 대사성 변화가 의심됩니다.
망막색소선조의 병태는 단계적으로 진행됩니다.
초기
Bruch 막 비후: 석회화가 시작되어 막이 두꺼워집니다.
색소 과립 감소: RPE의 색소 과립이 감소합니다.
증상: 이 단계에서는 무증상.
진행기
색소상피박리: RPE가 부분적으로 박리됨.
색소반 형성: 유두 주위에서 방사상 선조로 망막에 나타남.
증상: 선조만 있을 경우 보통 무증상.
말기
전신 질환과의 연관성: PXE는 ABCC6 유전자 변이를 원인으로 피부, 심혈관계, 위장관, 태반 등 전신의 탄력 섬유에 진행성 손상을 일으킵니다. 심혈관계 질환(협심증, 고혈압, 말초동맥질환, 위장관 출혈)을 동반할 수 있으므로 피부과에 더하여 순환기내과 검진도 고려합니다. 2)
병리학적으로는 Bruch막의 광범위한 석회화와 비후가 관찰됩니다. 파열 부위에서는 RPE가 얇아지고 섬유혈관 조직이 침입하여 망막하 출혈, CNV, 원반 모양 반흔을 형성합니다. 2)
7. 최신 연구와 향후 전망(연구 단계의 보고)
섹션 제목: “7. 최신 연구와 향후 전망(연구 단계의 보고)”항VEGF 치료의 장기 성적과 과제
섹션 제목: “항VEGF 치료의 장기 성적과 과제”AS-CNV는 AMD-CNV에 비해 재발률이 높아 더 적극적인 투여 요법의 필요성이 논의되고 있습니다. 장기(5년 초과) 성적에서는 황반 위축 진행으로 시력 예후가 제한적인 증례가 많으며, 위축 진행을 억제하는 치료법 개발이 향후 과제입니다. 10)
OCTA를 통한 CNV 활동성 평가
섹션 제목: “OCTA를 통한 CNV 활동성 평가”OCTA의 발전으로 CNV의 미세 구조 평가가 가능해져 치료 효과 판정 및 재발 검출의 정확도 향상이 기대됩니다. 6) en face OCT를 이용한 맥락막 주름 병변의 층별 평가도 보고되었습니다. 5)
항석회화 치료(분자 표적 접근법)
섹션 제목: “항석회화 치료(분자 표적 접근법)”ABCC6 유전자 변이로 인한 PXE에 대해 무기 피로인산 보충 및 에티드로네이트 등의 항석회화 치료 임상시험이 보고되었습니다.
Kranenburg 등(2018)은 에티드로네이트(비스포스포네이트)가 PXE 환자의 이소성 석회화 진행을 억제하는 효과를 RCT로 검증했습니다. 11) 일부 석회화에서 진행 억제가 확인되었으나, 유효성 확립을 위해서는 추가 연구가 필요합니다.
마우스 모델(Abcc6-/-)을 이용한 PXE 병태 분석이 진행되고 있으며, 유전자 치료 및 분자 표적 치료의 기초 연구도 전개되고 있습니다. 4)
8. 참고문헌
섹션 제목: “8. 참고문헌”- Mandura RA, Radi RE. Angioid streaks in pseudoxanthoma elasticum. Cureus. 2021;13(6):e15720.
- Georgalas I, Papaconstantinou D, Koutsandrea C, et al. Angioid streaks, clinical course, complications, and current therapeutic management. Ther Clin Risk Manag. 2009;5(1):81-89.
- Chassaing N, Martin L, Calvas P, et al. Pseudoxanthoma elasticum: a clinical, pathophysiological and genetic update including 11 novel ABCC6 mutations. J Med Genet. 2005;42(12):881-892.
- Li Q, Jiang Q, Pfendner E, et al. Pseudoxanthoma elasticum: clinical phenotypes, molecular genetics and putative pathomechanisms. Exp Dermatol. 2009;18(1):1-11.
- Takeuchi T, Hirai H, Ogata N, et al. En-face optical coherence tomography is useful for assessing striated lesions in angioid streaks: a case report. Cureus. 2023;15(9):e45983.
- Corbelli E, Carnevali A, Marchese A, et al. Optical coherence tomography angiography features of angioid streaks. Retina. 2018;38(11):2128-2136.
- Ladas ID, Kotsolis AI, Ladas DS, et al. Intravitreal ranibizumab treatment of macular choroidal neovascularization secondary to angioid streaks: one-year results of a prospective study. Retina. 2010;30(8):1227-1233.
- Tilanus MA, Cuypers MH, Bemelmans NA, et al. Intravitreal bevacizumab in the treatment of choroidal neovascularization associated with angioid streaks. Acta Ophthalmol. 2007;85(8):918-920.
- Esen E, Sizmaz S, Demircan N. Intravitreal aflibercept for management of subfoveal choroidal neovascularization secondary to angioid streaks. Indian J Ophthalmol. 2015;63(7):616-618.
- Gliem M, Finger RP, Fimmers R, et al. Treatment of choroidal neovascularization due to angioid streaks: a comprehensive review. Retina. 2013;33(7):1300-1314.
- Kranenburg G, de Jong PA, Bartstra JW, et al. Etidronate for prevention of ectopic mineralization in patients with pseudoxanthoma elasticum. J Am Coll Cardiol. 2018;71(10):1117-1126.
