滤过泡渗漏(bleb leak)是指青光眼 滤过手术 后房水 从滤过泡壁漏出到眼外的状态,通过Seidel试验阳性进行诊断
术后早期结膜 创口的房水 渗漏发生率为3.4%~14%,使用丝裂霉素C的病例5年后渗漏风险达15%
滤过泡渗漏是滤过泡感染的最大风险因素,使感染风险增加26倍
若继发低眼压 黄斑 病变,视力 预后会显著恶化,因此持续性渗漏需要积极干预
保守治疗(加压眼罩、绷带式角膜 接触镜、自体血注射)无效时,需进行经结膜 巩膜 瓣缝合或结膜 前徙术等外科治疗
切除无血管滤过泡并前徙结膜 后,约90%的病例渗漏停止,且复发率低
滤过泡渗漏(bleb leak)是指青光眼 滤过手术 (如小梁切除术 、Express分流手术等)后形成的滤过泡(bleb)壁发生房水 渗漏至眼外的状态。通过荧光素 钠Seidel试验阳性可确认。这是滤过手术 特有的并发症,其他眼科手术通常不会出现。
根据发病时间可分为以下两类。
早期渗漏 :术后1个月内发生。主要原因为缝合部位不全或结膜 闭合不全。多数可通过巩膜 瓣缝线调整或保守管理期待自然闭合晚期渗漏(late bleb leak) :术后1个月后发生。在使用抗代谢药 物的病例中,常因滤过泡壁变薄、无血管化所致,临床上易成为问题。晚期渗漏难以自然闭合,常需手术干预
此外,根据渗漏的持续性可分为暂时性渗漏和持续性渗漏。持续性渗漏感染风险高,且可能发展为低眼压 黄斑 病变,因此需要更积极的治疗干预。
小梁切除术 后早期结膜 创口房水 渗漏的发生率为3.4%~14%1) 。联合使用丝裂霉素C(MMC)时,术后5年渗漏风险可达15%2) 。术后1个月后发生的低眼压 黄斑 病变发生率为0.9%~5%1) 。
滤过泡渗漏是滤过泡感染的最大危险因素,可使感染风险增加26倍。据报道,MMC联合小梁切除术 术后5年的累积滤过泡感染发生率为2.2%2) 。
小梁切除术 是治疗青光眼 最成熟的滤过手术 ,长期降眼压 效果优越,但通过滤过泡可能发生终身并发症。滤过泡渗漏是其典型并发症之一,早期发现和适当管理漏出对术后长期预后至关重要。
本文讨论滤过泡渗漏(漏出本身)的管理。漏出继发感染的详细信息请参见滤过泡相关感染 。
Q
滤过泡渗漏和滤过泡感染有什么区别?
A
滤过泡渗漏(bleb leak)是指房水 通过滤过泡壁漏出,通过Seidel试验阳性确认。而滤过泡感染(滤过泡相关感染 )是细菌通过漏出部位等侵入引起的感染性并发症。滤过泡渗漏是感染的最大危险因素,但仅有漏出而无感染的情况也很多。迅速封闭漏出是预防感染的关键。
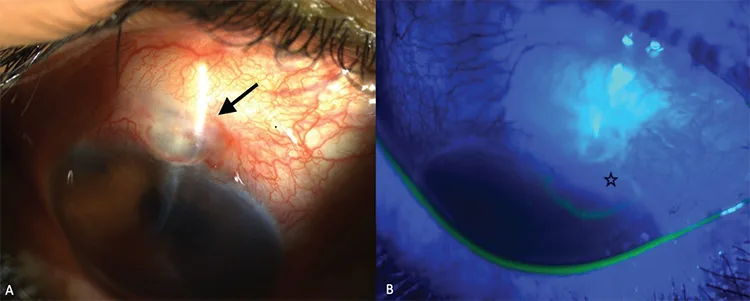
滤过泡渗漏的Seidel阳性所见 Erişti Bölük C, et al. Surgical Treatment of a Patient with Recurrent Bleb Leak and Glaucoma: Bleb Excision Combined with Gonioscopy-Assisted Transluminal Trabeculotomy. Turk J Ophthalmol. 2022. Figure 1. PM
CI D: PMC9631505. License: CC BY.
小梁切除术 后10年的滤过泡渗漏,A为右眼
裂隙灯 照片显示无血管滤过泡(黑色箭头),B显示
结膜 缺损 和Seidel试验所示的漏出(黑色星号)。对应本文“2. 主要症状与临床所见”中讨论的
房水 漏出。
滤过泡渗漏本身常无症状,但可能伴有以下症状。
晨起泪液积聚 :反映滤过泡壁薄,上眼睑抬起时房水 渗出的表现2) 眼压 降低引起的不适低眼压 ,不少情况下也无症状视力 下降低眼压 黄斑 病变时出现。由脉络膜皱襞 和黄斑部 皱襞形成所致,持续存在可导致永久性视力 障碍。常自觉视物模糊 充血 及刺激症状结膜 可能伴有轻度充血 。若出现明显充血 或疼痛,需怀疑合并感染视物变形 低眼压 黄斑 病变导致黄斑部 皱襞形成,可自觉直线扭曲等视物变形
滤过泡外观的观察以裂隙灯显微镜检查 为基础,需确认以下5个项目。
滤过泡的范围(扩散程度) :弥漫性滤过泡比局限性滤过泡降眼压 效果更好。手术时广泛剥离结膜 以确保房水 扩散面积,可促进形成低而宽的滤过泡,也有助于预防渗漏滤过泡的高度 :低平滤过泡提示滤过功能下降。反之,高而紧张的局限性滤过泡对囊壁的机械应力大,有渗漏风险滤过泡囊壁的厚度 :联合使用抗代谢药 物的小梁切除术 中,滤过泡囊壁变薄的频率较高。囊壁变薄的滤过泡降眼压 效果往往较好,但易发生房水 渗漏,需注意。用裂隙灯 显微镜的裂隙光从侧面照射滤过泡囊壁,易于评估变薄部位的透光性血管分布 :无血管滤过泡房水 渗漏风险高。缺血性滤过泡结膜 防御屏障减弱,感染风险也增加。反之,囊壁厚且有扩张血管侵入的滤过泡称为包裹性滤过泡(encapsulated bleb),是导致眼压 升高的另一种病理状态Seidel试验判断房水 渗漏的有无 :用荧光素 试纸染色后,在钴蓝光下观察整个滤过泡。如有渗漏,房水 稀释荧光素 形成流动(详见“诊断和检查方法”一节 )
持续的房水 渗漏可导致低眼压 ,并可能出现以下表现1) 。
浅前房 ·脉络膜 脱离低眼压 黄斑 病变眼轴 缩短、脉络膜 皱褶、黄斑 皱褶、视网膜 血管迂曲、视盘水肿 。多见于年轻近视 眼1)
眼前节OCT :可客观评估滤过泡壁厚度及内腔结构4) 。结合裂隙灯显微镜检查 综合判断滤过泡的滤过功能B型超声 :有助于评估脉络膜 脱离的范围
滤过泡渗漏的发生涉及多种因素。
抗代谢药 物(MMC、5-FU)的使用结膜 的物理和免疫防御屏障减弱。术后5-FU结膜 下注射明显增加房水 渗漏的频率1) 巩膜 瓣缝合不全结膜 闭合不全结膜 切口缝合不充分或组织脆弱导致房水 渗漏
滤过泡壁变薄 :变薄的滤过泡通常眼压 下降良好,但容易发生渗漏无血管滤过泡 :存在缺乏血管分布区域的滤过泡渗漏风险高下方滤过泡 :暴露于泪液积聚较多,且无上眼睑保护。机械刺激也增加渗漏风险紧张的局限性滤过泡 :小而高的滤过泡对囊壁的机械应力较大
年轻、近视 眼 :低眼压 黄斑 病变的风险较高1) 。眼球壁柔韧性高,易受低眼压 引起的眼轴 缩短影响结膜 瘢痕化倾向结膜 组织脆弱,修复能力下降合并眼睑炎 、结膜炎 :眼表慢性炎症会降低结膜 的屏障功能,增加渗漏和感染的双重风险糖尿病 :可能成为伤口愈合延迟的因素
青光眼 滤过手术 后,请定期就诊检查滤过泡的状态如果起床时出现泪液积聚、视物模糊 等新症状,请尽早就诊
请遵医嘱继续使用抗菌眼药水或眼膏。如有渗漏,预防感染尤为重要
Q
为什么使用抗代谢药物更容易发生滤过泡渗漏?
A
丝裂霉素C(MMC)和5-FU等抗代谢药 物用于抑制滤过泡周围的瘢痕形成,以长期维持降眼压 效果。但同时会促进滤过泡壁变薄、无血管化,并因杯细胞减少导致黏蛋白分泌下降。这些变化削弱了结膜 的防御屏障,增加了房水 渗漏的风险。
滤过泡渗漏的确诊采用Seidel试验。建议在小梁切除术 后每次复查时常规进行,以评估有无渗漏。操作步骤如下:
试纸准备 :将浸有表面麻醉药的荧光素 试纸轻轻涂于滤过泡表面。避免试纸过度压迫结膜 ,以免造成人为渗漏,仅轻触即可观察条件 :在钴蓝光(蓝色滤光片)下观察整个滤过泡。降低周围照明可提高微小渗漏的检出率闭眼/睁眼法 :先让患者闭眼,睁眼后立即观察滤过泡数秒,更容易判断。闭眼时眼睑压迫可暂时促进渗漏阳性判定 :若滤过泡有房水 渗漏,可见被房水 稀释的荧光素 流动(Seidel试验阳性)。特征性表现为渗漏部位流出发出绿色荧光的稀释液,而周围呈橙色染色渗漏记录 :记录渗漏位置(滤过泡顶部、边缘、结膜 缝合处等)和范围在临床上很重要。记录渗漏量大小有助于确定治疗方案
根据外观的滤过泡分类主要有Moorfields滤过泡分级系统(MBGS)和Indiana滤过泡外观分级量表(IBAGS)。这些分类对滤过泡的范围、高度、壁的血管性、壁的厚度等进行评分,用于评估滤过泡功能和分层渗漏风险。通过定期记录评分,可以客观追踪滤过泡的形态变化和变薄进展。
前段OCT 可断面评估滤过泡壁厚度、内腔状态及结膜 下组织特性4) 。对于裂隙灯显微镜检查 难以判断的细微壁变薄,以及治疗效果的纵向评估,该检查很有用。
需要与滤过泡渗漏进行鉴别的疾病如下所示。
鉴别疾病 Seidel试验 特征 滤过泡渗漏 阳性 确认房水 流出 滤泡感染 阳性~阴性 充血 、白浊(white-on-red)、疼痛过度滤过 阴性 低眼压 但结膜 无渗漏结膜松弛症 阴性 结膜 松弛导致流泪
滤过泡感染时,碎屑可能暂时堵塞渗漏部位,导致Seidel试验阴性。若发现被充血 的结膜 包围的不透明混浊滤过泡(即所谓的“白上红”),应怀疑感染,并进行包括结膜 拭子和前房 水培养在内的详细检查。过度滤过是指从巩膜 瓣过度流出房水 ,导致低眼压 和浅前房 ,但不伴有结膜 渗漏,以此与滤过泡渗漏相区别。
滤过泡渗漏的治疗根据渗漏程度、滤过泡的血管化程度以及有无并发症来选择。房水 渗漏是滤过泡感染的重大风险因素,因此需要迅速控制2) 。
发生在血管丰富的结膜 上的渗漏,通过保守治疗闭合的可能性相对较高。
非侵入性治疗
加压眼罩 :用纱布等准确压迫巩膜 瓣。对改善过度滤过也有效。
绷带式角膜 接触镜(BCL) :佩戴18mm大直径软性角膜 接触镜,促进创口闭合。
房水 生成抑制剂房水 生成量,从而减轻渗漏。
硫酸阿托品水合物滴眼液 :通过松弛睫状肌抑制房水 生成,并预期具有抗炎效果1) 。
微创治疗
自体血注射 :将患者自体血注射到滤过泡内及周围。已有报告显示可改善低眼压性黄斑病变 3) 。
氰基丙烯酸酯组织胶 :局部涂抹于小的渗漏部位以封闭渗漏。
粘弹性物质/空气前房 内注射 :形成前房 ,暂时抑制渗漏。
若保守治疗无效或继发低眼压性黄斑病变 ,则进行手术干预。
经结膜 巩膜 瓣缝合 :直接从结膜 上方用尼龙线缝合巩膜 瓣的方法,作为低眼压 黄斑 病变的治疗,长期有效性已被证实3) 。也用于抑制过度滤过直视下巩膜 瓣缝合 :当经结膜 方法无法处理时,开放结膜 在直视下缝合巩膜 瓣。伴有明显脉络膜 脱离时,联合巩膜 开窗术引流1) 无血管滤过泡切除+结膜 前徙术 :切除有房水 渗漏的无血管滤过泡,将后方正常结膜 和Tenon囊前徙。一次手术约可使90%的病例房水 渗漏停止,包括再次手术病例在内无复发3) 羊膜联合Tenon前徙术 :在结膜 前徙基础上联合羊膜的手术方式,对结膜 组织不足或复发病例有效3)
轻度、一过性渗漏且眼压 维持者 → 尝试保守治疗2~4周。血管丰富的结膜 发生的渗漏可能自行闭合
持续性渗漏导致低眼压 者 → 在保守治疗基础上考虑手术干预
继发低眼压 黄斑 病变者 → 迅速进行积极的手术闭合。在视功能损害固定前处理至关重要
感染伴随时 → 需要紧急抗菌治疗和外科处理(详见滤过泡相关感染 )
青光眼 诊疗指南(第5版)对小梁切除术 后抗菌药物的使用推荐如下1) 2) 。
术后早期 :推荐持续滴用新喹诺酮类抗菌药1~3个月(推荐强度:强烈推荐“实施”,证据强度:C)术后长期 :若存在滤过泡渗漏,应积极考虑睡前使用新喹诺酮类抗菌眼膏。长期使用可显著延缓滤过泡感染的发生(非使用组3.9年 vs 长期使用组6.4年 vs 软膏组10.5年)2)
自体血注射可改善低眼压 黄斑 病变,但可能引起眼压 急剧升高,需谨慎随访观察3)
过度的激光断线(LSL )有在血凝块溶解后导致低眼压 的风险
术后抗菌药物的长期使用需注意结膜 菌群变化和耐药菌的出现1)
低眼压 黄斑 病变多见于年轻近视 眼,若持续存在可能导致永久性视功能障碍,因此早期处理至关重要
Q
自体血注射是什么样的治疗?
A
自体血注射是采集患者自身血液,注射到滤过泡内及其周围的治疗方法3) 。通过血液的凝固作用促进渗漏部位的闭合。虽然有报道称其可改善低眼压 黄斑 病变,但可能引起眼压 急剧升高3) ,因此术后需要严密监测眼压 。
Q
滤过泡渗漏可以通过手术治愈吗?
A
保守治疗无效时需进行手术治疗。切除无血管滤过泡并前徙结膜 ,约90%的病例一次手术即可停止渗漏,且复发率低3) 。也有报道联合羊膜移植有效3) 。手术适应症根据渗漏程度、滤过泡性状及有无并发症综合判断。
小梁切除术 是在角膜缘 巩膜 开窗,建立从眼前房 到结膜 下组织的非生理性房水 流出通道的手术1) 。术后眼压 由房水 生成量与通过巩膜 瓣流入滤过泡的流出量之间的平衡决定。
术后伤口愈合过程中,结膜 下组织会形成瘢痕。这种瘢痕形成会导致滤过泡功能下降(眼压 升高),因此联合使用MMC抑制早期过度组织反应,提高长期维持滤过泡的概率已成为标准管理方法1) 。然而,MMC同时会引起以下变化。
结膜 变薄房水 容易渗透和渗漏。术中MMC涂抹浓度(通常0.2~0.4mg/mL)和涂抹时间影响变薄程度无血管化 :结膜 的血管新生受到抑制,修复能力下降。无血管滤过泡的结膜 上皮营养供应也减弱,上皮更新延迟杯状细胞减少 :黏蛋白产生减少,结膜 表面的防御功能受损。黏蛋白层具有稳定泪液和作为微生物物理屏障的作用,其丧失会增加渗漏和感染的风险成纤维细胞抑制 :伤口修复的主要承担者成纤维细胞减少,滤过泡壁的自我修复能力下降
这些变化综合作用,导致术后早期至晚期滤过泡渗漏的风险持续存在。特别是在瘢痕形成快速进展的术后数月内,巩膜 瓣的流出阻力和滤过泡形态时刻变化,需要在适当时机进行干预。
早期渗漏主要源于手术创口的机械性不全。巩膜 瓣缝合不全、结膜 切口裂开,或房水 生成与流出平衡的急剧变化导致的过度滤过是主要原因。术后追加5-FU结膜 下注射除引起角膜上皮 损伤外,还会增加房水 渗漏的频率1) 。
晚期渗漏是抗代谢药 物引起的慢性组织变性的结果。长期存在的滤过泡壁进行性变薄,在某一时刻超过临界点,导致房水 经壁渗漏显现。机械性外伤(如揉眼)也可能成为诱因。
持续性房水 渗漏导致的低眼压 可能引起以下一系列变化1) 。
眼球壁收缩与巩膜 皱缩
眼轴 缩短脉络膜皱襞 形成黄斑 皱襞和视网膜 血管迂曲视神经乳头水肿
这些因素共同导致严重的视功能下降(低眼压 黄斑 病变)。一过性术后低眼压 不影响长期眼压 ,但持续性低眼压 可能导致不可逆的黄斑 改变。
滤过泡的房水 渗漏为泪液和眼周常驻菌通过渗漏部位进入眼内提供了途径2) 。正常结膜 具有上皮紧密连接、杯细胞来源的黏蛋白、泪液中的溶菌酶和IgA等多层防御机制,但在抗代谢药 物减弱的滤过泡中,细菌容易从渗漏部位侵入。
渗漏持续时间越长,感染风险越高。感染一旦发生,可经过滤过泡炎(局限于滤过泡的感染)阶段,进而波及前房 ,甚至玻璃体 (滤过泡相关性眼内炎 )2) 。据报道,滤过泡相关性眼内炎 即使积极治疗,仍有94%的患者视力 降至0.1以下,因此在滤过泡渗漏阶段及时处理对预后至关重要。
对于出现渗漏或低眼压 的滤过泡,可通过无血管滤过泡切除或结膜 前转术等外科修复,同时实现渗漏闭合和眼压 管理3) 。
在健康结膜 不足的再次手术病例中,有时会考虑将结膜 前转与羊膜等辅助材料相结合的修复方法3) 。
近年来普及的微创青光眼手术 (MIGS )中,许多设备与传统小梁切除术 不同,不形成滤过泡。由于通过Schlemm管或脉络膜 上腔途径排出房水 ,不形成结膜 下滤过泡,从而在结构上避免了术后低眼压 和滤过泡渗漏的风险。不过,其降眼压 效果比小梁切除术 有限,适应症多限于中度以下青光眼 。也存在形成结膜 下滤过泡的MIGS 设备,但由于不使用抗代谢药 物,与传统小梁切除术 相比,渗漏风险有所降低。
Kojima等人(2015)报告了使用前段OCT 评估滤过泡内部结构的研究4) 。由于可以定量评估囊壁厚度、腔内低反射区域以及结膜 下组织的性质,该方法有望应用于Seidel试验难以检测的微小渗漏或渗漏风险的预测。未来,通过人工智能辅助OCT 图像分析,有望实现滤过泡壁变薄进展的自动检测,以及预测渗漏前预防性干预的适当时机。
除了羊膜移植外,使用胶原基质和纤维蛋白胶等生物材料修复滤过泡的方法报告正在积累。对于传统结膜 前徙术因健康结膜 不足而难以处理的病例,基于组织工程方法的结膜 替代材料开发也处于研究阶段。
日本緑内障学会. 緑内障診療ガイドライン(第5版). 日眼会誌. 2022;126(2):85-177.
Soltau JB, Rothman RF, Budenz DL, et al. Risk factors for glaucoma filtering bleb infections. Arch Ophthalmol. 2000;118(3):338-342. doi:10.1001/archopht.118.3.338. https://doi.org/10.1001/archopht.118.3.338
American Academy of Ophthalmology Preferred Practice Pattern Glaucoma Panel. Primary Open-Angle Glaucoma Preferred Practice Pattern. Ophthalmology. 2021;128(1):P71-P150. doi:10.1016/j.ophtha.2020.10.022. https://doi.org/10.1016/j.ophtha.2020.10.022
Kojima S, Inoue T, Kawaji T, Tanihara H. Risk factors for hypotony after trabeculectomy with mitomycin C: anterior segment optical coherence tomography study. JAMA Ophthalmol. 2015;133(2):148-156. doi:10.1001/jamaophthalmol.2014.4855. https://doi.org/10.1001/jamaophthalmol.2014.4855
复制全文后,可以粘贴到你常用的 AI 助手中提问。
打开下面的 AI 助手,并把复制的内容粘贴到聊天框。