ブレブリーク(bleb leak)は緑内障 濾過手術 後の濾過胞壁から房水 が眼外へ漏出する状態であり、Seidel試験陽性で診断する
術後早期の結膜 創からの房水 漏出は3.4〜14%の頻度で生じ、マイトマイシンC使用例では5年後の漏出リスクが15%に達する
濾過胞漏出は濾過胞感染の最大リスク因子であり、感染リスクを26倍に高める
低眼圧黄斑症 を続発すると視力 予後が著しく悪化するため、持続性漏出には積極的な介入が必要である保存的治療(圧迫眼帯・バンデージコンタクトレンズ・自己血注入)で改善しない場合は、経結膜 的強膜 弁縫合や結膜 前転術などの外科的治療を行う
無血管濾過胞の切除と結膜 前転により約9割の症例で漏出が停止し、再発も少ないと報告されている
ブレブリーク(bleb leak)は、緑内障 濾過手術 (線維柱帯切除術 ・エクスプレスシャント手術など)後に形成された濾過胞(ブレブ)の壁を通じて房水 が眼外へ漏出する状態である。フルオレセイン を用いたSeidel試験で陽性となることで確認される。濾過手術 特有の合併症であり、他の眼科手術では通常みられない病態である。
発症時期により以下に大別される。
早期漏出 :術後1ヶ月以内に発症する。縫合部位の不全や結膜 閉鎖不全が主な原因である。多くは強膜 弁の縫合調整や保存的管理で自然閉鎖が期待できる晩期漏出(late bleb leak) :術後1ヶ月以降に発症する。代謝拮抗薬 使用例でブレブ壁が菲薄化・無血管化した結果生じることが多く、臨床的に問題となりやすい。晩期漏出は自然閉鎖が得られにくく、外科的介入が必要となることが多い
さらに漏出の持続性から、一時的漏出と持続性漏出に分けられる。持続性漏出は感染リスクが高く、低眼圧黄斑症 への進展も懸念されるため、より積極的な治療介入が必要である。
線維柱帯切除術 後早期の結膜 創からの房水 漏出は3.4〜14%の頻度で報告されている1) 。マイトマイシンC(MMC)を併用した場合、術後5年間の漏出リスクは15%に達する2) 。術後1ヶ月以降に生じる低眼圧黄斑症 の頻度は0.9〜5%である1) 。
濾過胞漏出は濾過胞感染の最大リスク因子であり、感染リスクを26倍に高めるとされる。MMC併用線維柱帯切除術 後の5年間の累積濾過胞感染発症率は2.2%と報告されている2) 。
線維柱帯切除術 は緑内障 に対する最も確立された濾過手術 であり、長期的な眼圧 下降効果に優れる一方、濾過胞を介した合併症が生涯にわたり生じうる。ブレブリークはその代表的な合併症の一つであり、漏出の早期発見と適切な管理が術後の長期予後を左右する。
本記事ではブレブリーク(漏出そのもの)の管理を扱う。漏出に続発する感染症の詳細は濾過胞関連感染症 を参照されたい。
Q
ブレブリークとブレブ感染はどう違いますか?
A
ブレブリーク(bleb leak)は濾過胞壁を通じた房水 の漏出そのものを指し、Seidel試験陽性で確認される。一方、ブレブ感染(濾過胞関連感染症 )は漏出部位などから細菌が侵入して生じる感染性合併症である。ブレブリークは感染の最大リスク因子であるが、漏出のみで感染を伴わない状態も多い。速やかに漏出を閉鎖することが感染予防の要となる。
ブレブリークのSeidel陽性所見 Erişti Bölük C, et al. Surgical Treatment of a Patient with Recurrent Bleb Leak and Glaucoma: Bleb Excision Combined with
Gonioscopy -Assisted Transluminal Trabeculotomy. Turk J Ophthalmol. 2022. Figure 1. PM
CI D: PMC9631505. License: CC BY.
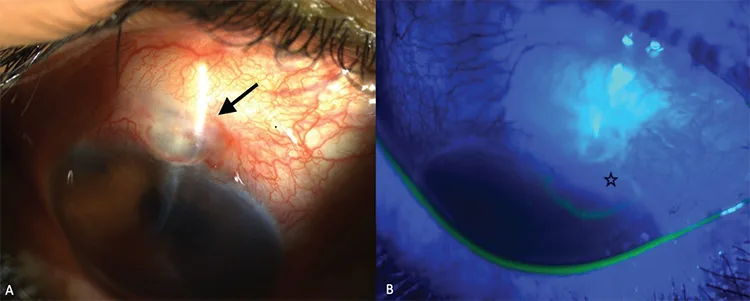
線維柱帯切除術 10年後のブレブリークで、Aは右眼の裂隙灯写真で無血管性濾過胞(黒矢印)を示し、Bは
結膜 欠損とSeidel試験で示された漏出(黒星)を示す。本文「2. 主な症状と臨床所見」の項で扱う
房水 漏出に対応する。
ブレブリーク自体は無症状のことも多いが、以下の症状を伴うことがある。
起床時の涙の貯留 :ブレブ壁が薄く、上眼瞼挙上時に房水 が染み出す所見を反映する2) 眼圧 低下に伴う不快感低眼圧 であっても無症状の場合も少なくない視力 低下低眼圧黄斑症 を続発した場合に生じる。脈絡膜皺襞 や黄斑部 皺襞の形成によるもので、持続すると恒久的な視力 障害に至りうる。霧視 (ぼやけて見える)として自覚されることが多い充血 ・刺激症状結膜 に軽度の充血 を伴うことがある。著明な充血 や疼痛がある場合は感染の合併を疑う変視症 低眼圧黄斑症 による黄斑部 の皺襞形成に伴い、直線が歪んで見えるなどの変視症 を自覚することがある
ブレブの外観の観察は細隙灯顕微鏡検査 が基本であり、以下の5項目を確認する。
ブレブの範囲(広がり) :びまん性ブレブは限局性より眼圧 下降効果が良好である。手術時に結膜 を広範囲に剥離して房水 の拡散面積を確保することで、低く広い濾過胞の形成が促され、漏出予防にも寄与するブレブの高さ :丈が低く平坦なブレブは濾過機能の低下を示唆する。逆に丈が高く緊張した限局性ブレブは壁への機械的ストレスが大きく、漏出のリスクとなるブレブ壁の厚さ :代謝拮抗薬 を併用した線維柱帯切除術 でブレブ壁が菲薄化する頻度が高い。壁が菲薄化したブレブは眼圧 下降が良好なことも多いが、房水 漏出を生じやすいため注意が必要である。細隙灯顕微鏡のスリット光でブレブ壁を横から照射すると、菲薄部の透見性を評価しやすい血管分布 :無血管ブレブは房水 漏出のリスクが高い。虚血性のブレブは結膜 の防御壁も減弱しており感染リスクも増大する。逆に壁が厚く拡張した血管侵入があるブレブは被包化ブレブ(encapsulated bleb)と呼ばれ、眼圧 上昇を来す別の病態であるSeidel試験による房水 漏出の有無 :フルオレセイン 試験紙による染色後、コバルトブルー光下でブレブ全体を観察する。漏出がある場合は房水 によりフルオレセイン が希釈されて流れるのが確認される(詳細は「診断と検査方法」の項 を参照)
持続的な房水 漏出は低眼圧 を来し、以下の所見を呈しうる1) 。
浅前房 ・脈絡膜 剥離低眼圧黄斑症 眼軸長 の短縮、脈絡膜皺襞 、黄斑部 皺襞、網膜 血管の蛇行、視神経乳頭 浮腫が生じる。若年の近視 眼に多いとされる1)
前眼部OCT 4) 。細隙灯顕微鏡検査 と併せてブレブの濾過機能を総合的に判定するBモード超音波 :脈絡膜 剥離の範囲評価に有用
ブレブリークの発症には複数の因子が関与する。
代謝拮抗薬 (MMC・5-FU)の使用結膜 の物理的・免疫学的防御壁が減弱する。術後の5-FU結膜 下注射は房水 漏出の頻度を増加させることが明らかとなっている1) 強膜 弁の縫合不全結膜 閉鎖不全結膜 切開部の不十分な縫合や組織の脆弱性により房水 が漏出する
ブレブ壁の菲薄化 :菲薄化したブレブは眼圧 下降が良好なことが多いが、漏出を生じやすい無血管ブレブ :血管分布を欠く部分が存在するブレブは漏出リスクが高い下方ブレブ :涙液溜まりへの曝露が多く、上眼瞼による保護がない。機械的刺激も加わり漏出リスクが増大する緊張した限局性ブレブ :小さく高い濾過胞は壁への機械的ストレスが大きい
若年・近視 眼 :低眼圧黄斑症 のリスクが高い1) 。眼球壁の柔軟性が高く、低眼圧 による眼軸 短縮の影響を受けやすい結膜 の瘢痕化傾向結膜 組織が脆弱で修復能力が低下している眼瞼炎 ・結膜炎 の合併結膜 のバリア機能を低下させ、漏出と感染の双方のリスクを高める糖尿病 :創傷治癒遅延の要因となりうる
緑内障 の濾過手術 後は、定期的な受診でブレブの状態を確認してもらいましょう起床時に涙が溜まる、目がぼんやりするなどの症状が新たに出た場合は早めに受診してください
担当医の指示に従い、抗菌薬の点眼や軟膏を継続してください。漏出がある場合は感染予防が特に重要です
Q
なぜ代謝拮抗薬を使うとブレブリークが起きやすくなりますか?
A
マイトマイシンC(MMC)や5-FUなどの代謝拮抗薬 は、濾過胞周囲の瘢痕形成を抑制して眼圧 下降効果を長期に維持するために使用される。しかし同時にブレブ壁の菲薄化・無血管化を促進し、杯細胞の減少によるムチン産生低下を引き起こす。これらの変化が結膜 の防御壁を減弱させ、房水 漏出のリスクを高める。
ブレブリークの確定診断にはSeidel試験を用いる。線維柱帯切除術 後の各診察時にルーチンで施行し、漏出の有無を評価することが推奨される。以下の手順で施行する。
試験紙の準備 :点眼麻酔薬を浸したフルオレセイン 試験紙をブレブ表面に丁寧に塗布する。試験紙による結膜 への過度な圧迫は人為的な漏出を招くため、軽く触れる程度とする観察条件 :コバルトブルー光(ブルーフィルター)下でブレブ全体を観察する。周囲の照明を落とすと微小漏出の検出率が向上する閉瞼・開瞼法 :いったん閉瞼させ、開瞼した直後から数秒間ブレブ全体を観察すると判定しやすい。閉瞼により眼瞼の圧迫で一時的に漏出が促される効果がある陽性判定 :ブレブからの房水 漏出がある場合、房水 により希釈されたフルオレセイン が流れるのが確認される(Seidel試験陽性)。周囲のオレンジ色の染色に対して、漏出部位から緑色の蛍光を発する希釈液が流出する所見が特徴的である漏出の記録 :漏出場所(ブレブの頂点、辺縁、結膜 縫合部など)と漏出範囲を記録することが臨床上重要である。漏出量の大小の記録は治療方針の決定に寄与する
外観によるブレブ分類にはMoorfields bleb grading system(MBGS)やIndiana bleb appearance grading scale(IBAGS)が代表的である。これらの分類はブレブの範囲、高さ、壁の血管性、壁の厚さなどをスコア化するもので、濾過胞の機能評価や漏出リスクの層別化に用いられる。経時的にスコアを記録することで、ブレブの形態変化や菲薄化の進行を客観的に追跡できる。
ブレブ壁の厚さ、内腔の状態、結膜 下組織の性状を断面像で評価できる4) 。細隙灯顕微鏡検査 では判断しにくい壁の微細な菲薄化の検出や、治療効果の経時的評価に有用である。
ブレブリークと鑑別を要する病態を以下に示す。
鑑別疾患 Seidel試験 特徴 ブレブリーク 陽性 房水 の流出を確認濾過胞感染 陽性〜陰性 充血 ・白濁(white-on-red)、疼痛過剰濾過 陰性 低眼圧 だが結膜 からの漏出なし結膜弛緩症 陰性 結膜 のたるみによる流涙
濾過胞感染ではデブリにより漏出部位が一時的に閉塞し、Seidel試験が陰性となることがある。充血 した結膜 に囲まれた不透明な白濁濾過胞(いわゆる「赤の上の白(white-on-red)」)を認めた場合は感染を疑い、結膜 スワブや前房 水の培養検査を含めた精査を行う。過剰濾過は強膜 弁からの過剰な房水 流出であり、低眼圧 と浅前房 を来すが、結膜 からの漏出を伴わない点でブレブリークと区別される。
ブレブリークの治療は漏出の程度、ブレブの血管性、合併症の有無により選択する。房水 漏出は濾過胞感染の重大なリスク因子であるため、速やかに抑制する必要がある2) 。
血管が豊富な結膜 で発生した漏出は保存的治療で閉鎖する可能性が比較的高い。
非侵襲的治療
圧迫眼帯 :ガーゼなどで強膜 弁を正確に圧迫する。過剰濾過の改善にも有効。
バンデージコンタクトレンズ(BCL) :18mmの大径ソフトコンタクトレンズを装用し、創閉鎖を促進する。
房水 産生抑制薬房水 産生量の低下で漏出を軽減する。
アトロピン硫酸塩水和物点眼 :毛様体 弛緩により房水 産生を抑制し、消炎効果も期待される1) 。
低侵襲的処置
自己血注入 :患者の自己血を濾過胞内および周囲に注射する方法。低眼圧黄斑症 の改善効果が報告されている3) 。
シアノアクリレート組織接着剤 :小さな漏出部位に局所的に塗布して閉鎖する。
粘弾性物質 ・空気の前房 内注入前房 を形成し、漏出を一時的に抑制する。
保存的治療で改善しない場合や、低眼圧黄斑症 を続発している場合には外科的介入を行う。
経結膜 的強膜 弁縫合 :結膜 の上から直接ナイロン糸で強膜 弁を縫合する方法であり、低眼圧黄斑症 の治療として長期にわたり有効性が示されている3) 。過剰濾過の抑制にも用いられる直視下強膜 弁縫合 :経結膜 的に対応できない場合、観血的に結膜 を開放して強膜 弁を直視下で縫合する。著明な脈絡膜 剥離を伴う場合は強膜 開窓術による排液を併施する1) 無血管濾過胞切除+結膜 前転術 :房水 漏出のある無血管濾過胞を切除し、後方の正常結膜 およびTenon嚢を前転する方法である。1回の手術により約9割の症例で房水 漏出が停止し、再手術症例を含め再発はないと報告されている3) 羊膜併用Tenon前転法 :結膜 前転に加え羊膜を併用する術式で、結膜 組織が不十分な症例や再発例に有効であるとの報告がある3)
軽度・一過性の漏出で眼圧 が維持されている場合 → 保存的治療を2〜4週間試みる。血管が豊富な結膜 に生じた漏出は自然閉鎖の可能性がある
持続性漏出で低眼圧 を来している場合 → 保存的治療に加え外科的介入を検討する
低眼圧黄斑症 を続発している場合 → 速やかに積極的な外科的閉鎖を行う。視機能障害が固定する前の対応が重要である感染を伴う場合 → 緊急の抗菌薬治療と外科的対応が必要(詳細は濾過胞関連感染症 を参照)
緑内障 診療ガイドライン(第5版)では、線維柱帯切除術 後の抗菌薬使用について以下のように推奨している1) 2) 。
術後早期 :1〜3ヶ月間はニューキノロン系抗菌薬の継続的な点眼を推奨する(推奨の強さ:「実施すること」を強く推奨、エビデンスの強さ:C)術後長期 :濾過胞漏出の所見がある場合は、就寝前のニューキノロン系抗菌薬眼軟膏の使用を積極的に検討する。長期使用により濾過胞感染の発症が有意に遅延する(非使用群3.9年 vs 長期使用群6.4年 vs 軟膏群10.5年)2)
自己血注入は低眼圧黄斑症 の改善効果がある一方、急激な眼圧 上昇を来すことがあるため慎重な経過観察が必要です3)
過剰なレーザー切糸(LSL )は、凝血塊溶解後に低眼圧 を招くリスクがあります
術後抗菌薬の長期使用では、結膜 細菌叢の変化と耐性菌の出現に注意してください1)
低眼圧黄斑症 は若年の近視 眼に多く、持続すると恒久的な視機能障害に至りうるため、早期の対応が重要です
Q
自己血注入とはどのような治療ですか?
A
自己血注入は、患者自身の血液を採取し、濾過胞内および周囲に注射する治療法である3) 。血液の凝固作用によって漏出部位の閉鎖を促進する。低眼圧黄斑症 の改善効果が報告されている一方、急激な眼圧 上昇を来すことがあるため3) 、術後の厳重な眼圧 モニタリングが必要である。
Q
ブレブリークは手術で治りますか?
A
保存的治療で改善しない場合は外科的治療を行う。無血管濾過胞の切除と結膜 前転術では約9割の症例で1回の手術により漏出が停止し、再発も少ないと報告されている3) 。羊膜移植 を併用する方法も有効であるとの報告がある3) 。手術の適応は漏出の程度、ブレブの性状、合併症の有無により判断される。
線維柱帯切除術 は輪部 強角膜 を開窓し、前房 から結膜 下組織へと至る非生理的な房水 流出路を作製する手術である1) 。術後の眼圧 は房水 産生量と強膜 弁を介した濾過胞への流出量のバランスによって決まる。
術後の創傷治癒過程で結膜 下組織には瘢痕が形成される。この瘢痕形成は濾過胞の機能低下(眼圧 上昇)の原因となるため、MMCの併用により早期の過剰な組織反応を抑制し、長期的に濾過胞を維持できる確率を高めることが標準的な管理となっている1) 。しかし、MMCは同時に以下の変化を引き起こす。
結膜 の菲薄化房水 の透過・漏出が生じやすくなる。術中のMMC塗布濃度(一般に0.2〜0.4mg/mL)と塗布時間が菲薄化の程度に影響する無血管化 :結膜 の血管新生が抑制され、修復能力が低下する。無血管ブレブは結膜 上皮の栄養供給も減弱し、上皮のターンオーバーが遅延する杯細胞の減少 :ムチン産生の低下により、結膜 表面の防御機能が損なわれる。ムチン層は涙液の安定化と微生物への物理的バリアとして機能しており、その喪失は漏出と感染の双方のリスクを高める線維芽細胞の抑制 :創傷修復の主要な担い手である線維芽細胞が減少し、ブレブ壁の自己修復能力が低下する
これらの変化が複合的に作用し、術後早期〜晩期にわたってブレブリークのリスクが持続する。特に瘢痕形成が急速に進行する術後数ヶ月間は、強膜 弁の流出抵抗と濾過胞形態が刻々と変化する時期であり、適切なタイミングでの介入が求められる。
早期漏出は主に手術創の機械的不全に起因する。強膜 弁の縫合不全、結膜 切開部の離開、あるいは房水 産生と流出のバランスの急激な変化による過剰濾過が主な原因である。術後の5-FU結膜 下注射の追加は、角膜上皮 障害に加えて房水 漏出の頻度を増加させることが明らかとなっている1) 。
晩期漏出は代謝拮抗薬 による慢性的な組織変性の結果として生じる。長期間にわたるブレブ壁の進行性菲薄化が、ある時点で臨界点を超え、房水 の経壁的漏出が顕在化する。機械的外傷(眼を擦るなど)が引き金となることもある。
持続的な房水 漏出による低眼圧 は、以下の一連の変化を引き起こしうる1) 。
眼球壁の収縮と強膜 の収縮
眼軸長 の短縮脈絡膜皺襞 の形成黄斑部 皺襞と網膜 血管の蛇行視神経乳頭 浮腫
これらが複合して重篤な視機能低下(低眼圧黄斑症 )に至る。一過性の術後低眼圧 は長期の眼圧 に影響しないが、持続する低眼圧 は不可逆的な黄斑 変化をもたらしうる。
濾過胞からの房水 漏出は、涙液や眼周囲の常在菌が漏出部位を通じて眼内に侵入する経路となる2) 。正常な結膜 は上皮のタイトジャンクション、杯細胞由来のムチン、涙液中のリゾチームやIgAなどの多層的な防御機構を備えているが、代謝拮抗薬 によりこれらが減弱したブレブでは、漏出部位から細菌が容易に侵入しうる。
漏出の持続時間が長いほど感染リスクは上昇する。感染が成立するとブレブ炎(濾過胞に限局した感染)の段階を経て、前房 内への波及、さらには硝子体 への波及(濾過胞関連眼内炎 )へと進展しうる2) 。濾過胞関連眼内炎 は積極的な治療にもかかわらず94%で視力 0.1以下に低下するとの報告があり、ブレブリークの段階での速やかな対処が予後を大きく左右する。
漏出または低眼圧 を呈する濾過胞では、無血管濾過胞切除や結膜 前転術などの外科的修復により漏出閉鎖と眼圧 管理の両立を目指す3) 。
健常結膜 が不足する再手術例などでは、結膜 前転に羊膜などの補助材料を組み合わせた修復法が検討されることがある3) 。
近年普及が進む低侵襲緑内障手術 (MIGS )は、従来の線維柱帯切除術 と異なりブレブを形成しないタイプのデバイスが多い。Schlemm管経由や脈絡膜 上腔経由で房水 を排出する設計であるため、結膜 下濾過胞を形成せず、術後低眼圧 やブレブリークのリスクが構造的に回避される。ただし眼圧 下降効果はトラベクレクトミー より限定的であり、適応は中等度以下の緑内障 に限られる場合が多い。結膜 下にブレブを形成するタイプのMIGS デバイスも存在するが、代謝拮抗薬 を使用しないことから従来の線維柱帯切除術 と比較して漏出リスクは低減される。
Kojimaら(2015)は、前眼部OCT を用いた濾過胞の内部構造評価を報告した4) 。壁の厚さ、内腔の低反射領域、結膜 下組織の性状を定量的に評価できるため、Seidel試験だけでは捉えにくい微小漏出や漏出リスクの予測に応用が期待される。今後は人工知能を活用したOCT 画像解析により、ブレブ壁の菲薄化進行の自動検出や、漏出前の予防的介入の適切なタイミングの予測が可能になることが期待される。
羊膜移植 に加え、コラーゲンマトリクスやフィブリン糊などの生体材料を用いたブレブ修復法の報告が蓄積されつつある。従来の結膜 前転術では健常結膜 が不足する症例に対して、組織工学的アプローチによる結膜 代替材料の開発も研究段階にある。
日本緑内障 学会. 緑内障 診療ガイドライン(第5版). 日眼会誌. 2022;126(2):85-177.
Soltau JB, Rothman RF, Budenz DL, et al. Risk factors for glaucoma filtering bleb infections. Arch Ophthalmol. 2000;118(3):338-342. doi:10.1001/archopht.118.3.338. https://doi.org/10.1001/archopht.118.3.338
American Academy of Ophthalmology Preferred Practice Pattern Glaucoma Panel. Primary Open-Angle Glaucoma Preferred Practice Pattern. Ophthalmology. 2021;128(1):P71-P150. doi:10.1016/j.ophtha.2020.10.022. https://doi.org/10.1016/j.ophtha.2020.10.022
Kojima S, Inoue T, Nakashima K, Fukushima A, Tanihara H. Filtering blebs using 3-dimensional anterior-segment optical coherence tomography: a prospective investigation. JAMA Ophthalmol. 2015;133(2):148-156. PMID: 25375392. doi:10.1001/jamaophthalmol.2014.4489. https://doi.org/10.1001/jamaophthalmol.2014.4489
記事の全文をコピーして、お好みのAIに貼り付けて質問できます
下のAIを開いて、チャット欄に貼り付け(ペースト)してください