滤过泡渗漏(bleb leak)是青光眼 滤过手术后房水 从滤过泡壁漏出至眼外的状态,通过Seidel试验阳性诊断
术后早期结膜创口房水 渗漏的发生率为3.4%~14%,使用丝裂霉素C者5年后渗漏风险达15%
滤过泡渗漏是滤过泡感染的最大风险因素,使感染风险增加26倍
继发低眼压黄斑病变会显著恶化视力预后,因此持续性渗漏需要积极干预
保守治疗(加压眼罩、绷带式隐形眼镜、自体血注射)无效时,需进行经结膜巩膜瓣缝合或结膜前徙术等手术治疗
切除无血管滤过泡并前徙结膜,约90%的病例渗漏停止,复发率低
濾過泡滲漏(bleb leak)是指青光眼 濾過手術 (如小樑切除術 、Ex-Press引流管植入術等)後形成的濾過泡(bleb)壁出現房水 滲出至眼外的情況。可通過螢光素 鈉的Seidel試驗呈陽性來確認。這是濾過手術 特有的併發症,其他眼科手術通常不會出現此病況。
根據發病時間可分為以下幾類:
早期滲漏 :術後1個月內發生,主要原因是縫合部位不全或結膜 閉合不全。多數可通過鞏膜 瓣縫合調整或保守管理期待自然閉合晚期滲漏(late bleb leak) :術後1個月後發生,常見於使用抗代謝藥物 的病例,因濾過泡壁變薄、無血管化而導致,臨床上較易成為問題。晚期滲漏難以自然閉合,常需外科介入
此外,根據滲漏的持續性可分為暫時性滲漏和持續性滲漏。持續性滲漏感染風險高,且可能進展為低眼壓黃斑病變 ,因此需要更積極的治療介入。
小樑切除術 後早期結膜 傷口房水 滲漏的發生率報告為3.4%至14%1) 。併用絲裂黴素C(MMC)時,術後5年的滲漏風險可達15%2) 。術後1個月後發生的低眼壓黃斑病變 發生率為0.9%至5%1) 。
濾過胞漏出是濾過胞感染的最大風險因子,據報導會使感染風險增加26倍。MMC合併小樑切除術 後5年的累積濾過胞感染發生率為2.2%2) 。
小樑切除術 是青光眼 最確立的濾過手術 ,長期眼壓 下降效果優異,但透過濾過胞引起的併發症可能終生發生。濾過胞漏出是其代表性併發症之一,早期發現漏出並適當管理影響術後長期預後。
本文處理濾過胞漏出(漏出本身)的管理。漏出繼發感染的詳細資訊請參閱濾過胞相關感染症 。
Q
濾過胞漏出和濾過胞感染有什麼不同?
A
濾過胞漏出(bleb leak)是指房水 經濾過胞壁漏出本身,透過Seidel試驗陽性確認。另一方面,濾過胞感染(濾過胞相關感染症)是細菌經漏出部位等侵入引起的感染性併發症。濾過胞漏出是感染的最大風險因子,但僅有漏出而無感染的狀況也很多。迅速關閉漏出是預防感染的關鍵。
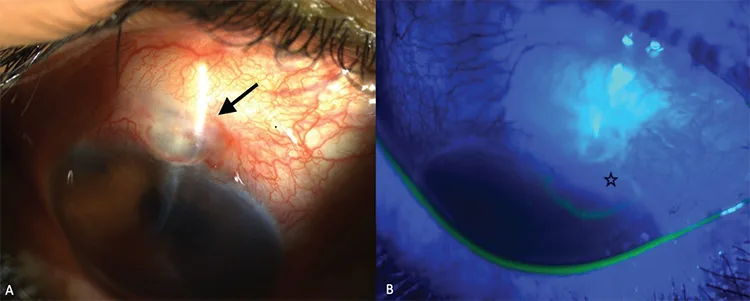
濾過胞漏出的Seidel陽性所見 Erişti Bölük C, et al. Surgical Treatment of a Patient with Recurrent Bleb Leak and Glaucoma: Bleb Excision Combined with Gonioscopy-Assisted Transluminal Trabeculotomy. Turk J Ophthalmol. 2022. Figure 1. PM
CI D: PMC9631505. License: CC BY.
小樑切除術 10年後的濾過胞漏出,A為右眼
裂隙燈 照片顯示無血管性濾過胞(黑色箭頭),B顯示
結膜 缺損 及Seidel試驗顯示的漏出(黑色星號)。對應本文「2. 主要症狀與臨床所見」一節中處理的
房水 漏出。
布雷布漏本身通常無症狀,但可能伴隨以下症狀。
起床時淚液積聚 :反映布雷布壁薄,上眼瞼抬起時房水 滲出的現象2) 眼壓 下降引起的不適低眼壓 ,不少情況下也無症狀視力 下降低眼壓黃斑病變 時。由脈絡膜 皺褶或黃斑部 皺褶形成所致,持續可能導致永久性視力 障礙。常自覺為視物模糊充血 與刺激症狀結膜 可能伴隨輕度充血 。若出現明顯充血 或疼痛,需懷疑合併感染變視症 低眼壓黃斑病變 導致黃斑部 皺褶形成時,可能自覺直線扭曲等變視症
濾過泡外觀的觀察以裂隙燈顯微鏡檢查 為基礎,需確認以下五項。
濾過泡的範圍(擴散程度) :瀰漫性濾過泡比局限性濾過泡有更好的降眼壓 效果。手術時廣泛剝離結膜 以確保房水 擴散面積,有助於形成低而寬的濾過泡,並有助於預防滲漏濾過泡的高度 :低平且平坦的濾過泡可能暗示濾過功能下降。相反,高聳且緊張的局限性濾過泡對泡壁造成較大機械壓力,有滲漏風險濾過泡壁的厚度 :使用抗代謝藥物 的濾過手術 中,濾過泡壁變薄的情況較常見。壁變薄的濾過泡雖然降眼壓 效果通常較好,但容易發生房水 滲漏,需注意。用裂隙燈 的裂隙光從側面照射濾過泡壁,可較容易評估薄區的透光性血管分布 :無血管的濾過泡有較高的房水 滲漏風險。缺血性濾過泡的結膜 防禦功能減弱,感染風險也增加。相反,壁厚且有擴張血管侵入的濾過泡稱為包裹性濾過泡(encapsulated bleb),是導致眼壓 升高的另一種病理狀態Seidel試驗檢查有無房水 滲漏 :以螢光素 試紙染色後,在鈷藍光下觀察整個濾過泡。若有滲漏,房水 會稀釋螢光素 並形成流動(詳細請參閱「診斷與檢查方法」一節 )
持續性房水 滲漏會導致低眼壓 ,並可能出現以下表現1) 。
淺前房 與脈絡膜 剝離低眼壓黃斑病變 眼軸 長縮短、脈絡膜 皺褶、黃斑部 皺褶、視網膜 血管迂曲、視神經 盤水腫。好發於年輕近視 眼1)
前段OCT :可客觀評估濾過泡壁厚度及內腔結構4) 。配合裂隙燈顯微鏡檢查 綜合判斷濾過泡功能B型超音波 :有助於評估脈絡膜 剝離範圍
濾過泡滲漏的發生涉及多種因素。
代謝拮抗藥物(MMC・5-FU)的使用 :最重要的風險因子。導致濾過泡壁變薄及無血管化。杯狀細胞減少使黏蛋白產生降低,結膜 的物理及免疫學防禦壁減弱。術後5-FU結膜 下注射已被證實會增加房水 滲漏的頻率1) 鞏膜 瓣縫合不全結膜 閉合不全結膜 切口縫合不充分或組織脆弱導致房水 滲漏
濾過泡壁變薄 :變薄的濾過泡通常眼壓 下降良好,但容易發生滲漏無血管濾過泡 :存在缺乏血管分布區域的濾過泡滲漏風險高下方濾過泡 :暴露於淚液積聚較多,且無上眼瞼保護。機械刺激也增加滲漏風險緊張性侷限性濾過泡 :小而高的濾過泡對泡壁造成較大的機械應力
年輕、近視 眼 :低眼壓黃斑病變 的風險較高1) 。眼球壁彈性較大,容易受到低眼壓 引起的眼軸 縮短影響結膜 瘢痕化傾向結膜 組織脆弱且修復能力下降合併眼瞼炎 、結膜炎 :眼表面慢性發炎會降低結膜 的屏障功能,增加滲漏和感染的風險糖尿病 :可能導致傷口癒合延遲
青光眼 濾過手術 後,應定期回診檢查濾過泡的狀況如果起床時出現淚水積聚、視力 模糊等新症狀,請儘早就醫
請遵照主治醫師指示,持續使用抗生素眼藥水或藥膏。若有滲漏,預防感染尤其重要
Q
為什麼使用抗代謝藥物容易發生濾過泡滲漏?
A
絲裂黴素C(MMC)或5-FU等抗代謝藥物 用於抑制濾過泡周圍的瘢痕形成,以長期維持眼壓 下降效果。但同時會促進濾過泡壁變薄、無血管化,並因杯細胞減少導致黏蛋白分泌下降。這些變化削弱結膜 的防禦屏障,增加房水 滲漏的風險。
濾過泡滲漏的確診採用Seidel試驗。建議在小樑切除術 後的每次門診常規執行,以評估有無滲漏。操作步驟如下:
試紙準備 :將浸有表面麻醉藥的螢光素 試紙輕輕塗抹於濾過泡表面。避免試紙過度壓迫結膜 ,以免人為造成滲漏,僅需輕觸即可觀察條件 :在鈷藍光(藍色濾光片)下觀察整個濾過泡。降低周圍照明可提高微小滲漏的檢出率閉瞼/開瞼法 :先讓患者閉眼,睜眼後立即觀察濾過泡數秒,較易判斷。閉眼時眼瞼壓迫可暫時促進滲漏陽性判定 :若濾過泡有房水 滲漏,可見到被房水 稀釋的螢光素 流動(Seidel試驗陽性)。特徵為滲漏處流出發出綠色螢光的稀釋液,周圍則呈橘色染色滲漏記錄 :記錄滲漏位置(濾過泡頂端、邊緣、結膜 縫合處等)及範圍在臨床上很重要。記錄滲漏量大小有助於決定治療方針
外觀上的濾過泡分類以Moorfields bleb grading system(MBGS)和Indiana bleb appearance grading scale(IBAGS)為代表。這些分類將濾過泡的範圍、高度、壁的血管性、壁厚度等進行評分,用於評估濾過泡功能及分層滲漏風險。定期記錄評分可客觀追蹤濾過泡形態變化及變薄的進展。
前段OCT 可斷層評估濾過泡壁厚度、內腔狀態及結膜 下組織特性4) 。有助於檢出裂隙燈 顯微鏡難以判斷的細微壁變薄,以及評估治療效果的變化。
需要與濾過泡滲漏鑑別的疾病如下所示。
鑑別疾病 Seidel試驗 特徵 濾過泡滲漏 陽性 確認房水 流出 濾過泡感染 陽性至陰性 充血 、白濁(white-on-red)、疼痛過度濾過 陰性 低眼壓 但無結膜 滲漏結膜鬆弛症 陰性 結膜 鬆弛導致流淚
濾過胞感染時,碎屑可能暫時阻塞滲漏部位,導致Seidel試驗呈陰性。若發現被充血 結膜 包圍的不透明白濁濾過胞(即所謂「白上紅」),應懷疑感染,並進行結膜 拭子及前房 水培養等詳細檢查。過度濾過是指房水 經鞏膜 瓣過度流出,導致低眼壓 及淺前房 ,但無結膜 滲漏,可與濾過泡滲漏區別。
濾過泡滲漏的治療取決於滲漏程度、濾過泡血管狀況及有無併發症。房水 滲漏是濾過泡感染的重大危險因子,需迅速控制2) 。
發生於血管豐富結膜 的滲漏,經保守治療後閉合的可能性相對較高。
非侵入性治療
加壓眼墊 :用紗布等準確加壓鞏膜 瓣。對改善過度濾過也有效。
繃帶式隱形眼鏡(BCL) :配戴18mm大直徑軟式隱形眼鏡,促進傷口閉合。
房水 生成抑制劑房水 生成量,以減輕滲漏。
阿托品硫酸鹽水合物點眼液 :放鬆睫狀體 以抑制房水 生成,並預期有抗發炎效果1) 。
低侵入性處置
自體血注射 :將患者自體血液注射至濾過泡內及周圍。已有報告顯示可改善低眼壓黃斑病變 3) 。
氰基丙烯酸酯組織膠 :局部塗抹於小的滲漏部位以封閉之。
黏彈性物質 或空氣注入前房 前房 ,暫時抑制滲漏。
若保守治療無改善,或續發低眼壓黃斑病變 ,則進行外科介入。
經結膜 鞏膜 瓣縫合 :從結膜 上方直接用尼龍線縫合鞏膜 瓣的方法,長期以來已被證明對治療低眼壓 黃斑部 病變有效3) 。也用於抑制過度濾過直視下鞏膜 瓣縫合 :若經結膜 方式無法處理,則採開放式手術打開結膜 ,在直視下縫合鞏膜 瓣。若伴有明顯脈絡膜 剝離,則合併施行鞏膜 開窗術引流1) 無血管濾過泡切除合併結膜 前徙術 :切除有房水 滲漏的無血管濾過泡,並將後方正常結膜 及Tenon囊向前徙動。一次手術約可停止90%病例的房水 滲漏,且據報告包括再次手術病例在內無復發3) 羊膜合併Tenon前徙術 :在結膜 前徙的基礎上合併使用羊膜的手術方式,據報告對結膜 組織不足或復發病例有效3)
輕度、暫時性滲漏且眼壓 維持正常 → 嘗試保守治療2至4週。血管豐富的結膜 發生的滲漏可能自行閉合
持續性滲漏導致低眼壓 → 在保守治療基礎上考慮外科介入
續發低眼壓 黃斑部 病變 → 迅速進行積極的外科閉合。在視功能障礙固定前處理至關重要
感染伴隨 → 需要緊急抗菌藥物治療和外科處理(詳情請參閱濾過泡相關感染症 )
青光眼 診療指引(第5版)對於小樑切除術 後的抗生素使用建議如下1) 2) 。
術後早期 :建議持續使用新型氟喹諾酮類抗生素眼藥水1至3個月(建議強度:強烈建議「應執行」,證據強度:C)術後長期 :若發現濾過泡滲漏,應積極考慮睡前使用新型氟喹諾酮類抗生素眼藥膏。長期使用可顯著延緩濾過泡感染的發生(未使用組3.9年 vs 長期使用組6.4年 vs 藥膏組10.5年)2)
自體血注射雖能改善低眼壓黃斑病變 ,但可能導致眼壓 急遽上升,因此需謹慎追蹤觀察3)
過度的雷射縫線切斷(LSL )可能在血塊溶解後引發低眼壓 的風險
術後抗菌藥物的長期使用需注意結膜 細菌叢的變化及抗藥性菌株的出現1)
低眼壓黃斑病變 多見於年輕近視 眼,若持續存在可能導致永久性視功能障礙,因此早期處理至關重要
Q
什麼是自體血注射治療?
A
自體血注射是採集患者自身的血液,注射到濾過泡內及其周圍的治療方法3) 。血液的凝固作用可促進滲漏部位的閉合。雖然有報告指出其能改善低眼壓黃斑病變 ,但也可能引起眼壓 急劇升高3) ,因此術後需嚴格監測眼壓 。
Q
濾過泡滲漏可以通過手術治癒嗎?
A
若保守治療無效,則進行外科治療。切除無血管濾過泡並進行結膜 前徙術,約九成病例在一次手術後滲漏停止,且復發率低3) 。也有報告指出聯合羊膜移植的方法有效3) 。手術適應症需根據滲漏程度、濾過泡性狀及有無併發症來判斷。
線維柱帯切除術是在輪部強角膜 開窗,建立一條從前房 到結膜 下組織的非生理性房水 流出通道的手術1) 。術後眼壓 取決於房水 生成量與經由鞏膜 瓣流向濾過泡的流出量之間的平衡。
術後傷口癒合過程中,結膜 下組織會形成疤痕。這種疤痕形成會導致濾過泡功能下降(眼壓 升高),因此標準做法是併用MMC來抑制早期過度的組織反應,提高長期維持濾過泡的機率1) 。然而,MMC同時會引起以下變化。
結膜 變薄房水 滲透和滲漏。術中MMC塗布濃度(一般為0.2~0.4 mg/mL)和塗布時間會影響變薄的程度無血管化 :結膜 的血管新生受到抑制,修復能力下降。無血管濾過泡也會減少結膜 上皮的營養供應,導致上皮更新延遲杯細胞減少 :黏蛋白產生減少,損害結膜 表面的防禦功能。黏蛋白層有助於穩定淚液並作為微生物的物理屏障,其喪失會增加滲漏和感染的風險纖維母細胞抑制 :傷口修復的主要細胞——纖維母細胞減少,濾過泡壁的自我修復能力下降
這些變化綜合作用,使濾過泡滲漏的風險在術後早期至晚期持續存在。特別是在疤痕形成快速進展的術後數月內,鞏膜 瓣的流出阻力與濾過泡形態不斷變化,需要在適當的時機進行干預。
早期滲漏主要源於手術創口的機械性缺陷。鞏膜 瓣縫合不全、結膜 切口裂開,或房水 生成與流出平衡急遽變化導致的過度濾過是主要原因。術後追加5-FU結膜 下注射,除了角膜上皮 損傷外,也會增加房水 滲漏的頻率1) 。
晚期滲漏是抗代謝藥物 導致慢性組織變性的結果。長期進行的濾過泡壁逐漸變薄,在某個時間點超過臨界值,房水 經壁滲漏便會顯現。機械性外傷(如揉眼睛)也可能成為誘因。
持續房水 滲漏導致的低眼壓 可能引發以下一系列變化1) :
眼球壁收縮與鞏膜 皺縮
眼軸 長縮短脈絡膜 皺褶形成黃斑部 皺褶與視網膜 血管迂曲視神經 盤水腫
這些因素合併導致嚴重的視功能下降(低眼壓黃斑病變 )。短暫的術後低眼壓 不影響長期眼壓 ,但持續的低眼壓 可能導致不可逆的黃斑 變化。
濾過泡的房水 滲漏成為淚液及眼周正常菌群經由滲漏部位進入眼內的路徑2) 。正常結膜 具有上皮緊密連接、杯細胞來源的黏蛋白、淚液中的溶菌酶和IgA等多層防禦機制,但在使用抗代謝藥物 後這些機制減弱的濾過泡中,細菌可能輕易經由滲漏部位侵入。
滲漏持續時間越長,感染風險越高。一旦發生感染,可能經歷濾過泡炎(侷限於濾過泡的感染)階段,進而擴散至前房 ,甚至玻璃體 (濾過泡相關眼內炎 )2) 。有報告指出,濾過泡相關眼內炎 即使積極治療,仍有94%的患者視力 降至0.1以下,因此在濾過泡滲漏階段及時處理對預後影響重大。
對於出現滲漏或低眼壓 的濾過泡,可通過無血管濾過泡切除或結膜 前徙術等外科修復,同時達到封閉滲漏和眼壓 控制的目標3) 。
在健康結膜 不足的再次手術案例中,有時會考慮將結膜 前徙與羊膜等輔助材料結合的修復方法3) 。
近年來日益普及的微創青光眼手術 (MIGS ),與傳統的小梁切除術不同,多數裝置不形成濾過泡。由於其設計是經由Schlemm管或脈絡膜 上腔排出房水 ,因此不形成結膜 下濾過泡,從結構上避免了術後低眼壓 和濾過泡滲漏的風險。不過,其降眼壓 效果較小梁切除術有限,適應症多僅限於中度以下的青光眼 。雖然也存在形成結膜 下濾過泡的MIGS 裝置,但由於不使用抗代謝藥物 ,與傳統小梁切除術相比,滲漏風險已降低。
Kojima等人(2015)報告了使用前段OCT 評估濾過泡內部結構的研究4) 。由於可以定量評估囊壁厚度、腔內低反射區域以及結膜 下組織的性質,此方法有望應用於預測Seidel試驗難以察覺的微小滲漏或滲漏風險。未來,透過人工智慧輔助OCT 影像分析,可望自動檢測濾過泡壁變薄的進展,並預測滲漏前預防性介入的適當時機。
除了羊膜移植外,使用膠原蛋白基質和纖維蛋白膠等生物材料修復濾過泡的報告逐漸累積。對於傳統結膜 前徙術中健康結膜 不足的病例,利用組織工程方法開發結膜 替代材料仍處於研究階段。
日本緑内障学会. 緑内障診療ガイドライン(第5版). 日眼会誌. 2022;126(2):85-177.
Soltau JB, Rothman RF, Budenz DL, et al. Risk factors for glaucoma filtering bleb infections. Arch Ophthalmol. 2000;118(3):338-342. doi:10.1001/archopht.118.3.338. https://doi.org/10.1001/archopht.118.3.338
American Academy of Ophthalmology Preferred Practice Pattern Glaucoma Panel. Primary Open-Angle Glaucoma Preferred Practice Pattern. Ophthalmology. 2021;128(1):P71-P150. doi:10.1016/j.ophtha.2020.10.022. https://doi.org/10.1016/j.ophtha.2020.10.022
Kojima S, Inoue T, Kawaji T, Tanihara H. Risk factors for hypotony after trabeculectomy with mitomycin C: anterior segment optical coherence tomography study. JAMA Ophthalmol. 2015;133(2):148-156. doi:10.1001/jamaophthalmol.2014.4855. https://doi.org/10.1001/jamaophthalmol.2014.4855
開啟下方的 AI 助手,並將複製的內容貼到聊天欄。