یافتههای معمول
سلول و فلر اتاق قدامی: یافته التهابی در اتاق قدامی. شدت معمولاً خفیف تا متوسط است.
رسوبات اندوتلیال (KP): اغلب KPهای ریز نقطهای، اما گاهی KPهای چرب دیده میشود.
سینشیای خلفی: در موارد مزمن ظاهر میشود.

سندرم نفریت توبولواینترستیشیال و یووئیت (TINU) یک بیماری التهابی سیستمیک نادر است که با نفریت توبولواینترستیشیال حاد (TIN) و یووئیت دوطرفه همراه است. اولین بار در سال 1975 توسط Dobrin و همکاران گزارش شد1). در اوایل قرن بیست و یکم، تنها حدود 133 مورد در جهان گزارش شده بود، اما پس از آن تعداد موارد گزارش شده افزایش یافته و به حدود 600 مورد رسیده است1).
تصور میشود که یک بیماری ایمنیمحور با دخالت آنتیژنهای خودی مشترک در کلیه و چشم باشد و در زنان نوجوان شایعتر است. علائم کلیوی و چشمی اغلب با فاصله زمانی ظاهر میشوند و تشخیص اغلب به تأخیر میافتد.
بروز سالانه 1 تا 2 مورد در هر میلیون نفر تخمین زده میشود1). نسبت بیماران مبتلا به یووئیت 0.1 تا 2٪ است و حدود 5٪ از موارد بیوپسی TIN با این سندرم همراه هستند2). در کودکان، یکی از علل اصلی یووئیت همراه با سارکوئیدوز چشمی و ایریدوسیکلیت مزمن نوجوانان است.
از نظر اپیدمیولوژیک، در زنان جوان شایعتر است. در یک مرور سیستماتیک در سال 2022، میانه سن شروع 17 سال و نسبت زن به مرد 1.8:1 گزارش شده است1). با این حال، گزارشهای اخیر نشان میدهد که با افزایش آگاهی تشخیصی، موارد تشخیص در بزرگسالان و سالمندان نیز افزایش یافته است1)3). یک مطالعه در ایرلند شمالی میانگین سن تشخیص را 43 سال گزارش کرده است3). ارتباط خاصی با قومیت، نژاد یا عوامل جغرافیایی ثابت نشده است.
برآورد میشود میزان بروز سالانه ۱ تا ۲ مورد در هر میلیون نفر باشد. این سندرم تنها ۰.۱ تا ۲٪ از کل موارد یووئیت را تشکیل میدهد و تصور میشود تعداد قابل توجهی از موارد تشخیصدادهنشده وجود دارد که بهعنوان ایدیوپاتیک تشخیص داده میشوند1).
مکانیسم دقیق بروز سندرم TINU ناشناخته است، اما تصور میشود یک بیماری خودایمنی باشد که هم ایمنی هومورال و هم ایمنی سلولی در آن نقش دارند1)4).
یافتههای بافتشناسی بیوپسی کلیه نشان میدهد که سلولهای نفوذی عمدتاً از زیرمجموعه سلولهای T کمککننده/القاگر هستند3). این نشان میدهد که ایمنی سلولی نقش اصلی را در پاتوژنز ایفا میکند.
نقش ایمنی هومورال نیز گزارش شده است. Tan و همکاران آنتیبادیهای ضد CRP اصلاحشده (mCRP) سرم را در درصد بالایی از ۹ بیمار مبتلا به سندرم TINU تشخیص دادند و نشان دادند که mCRP ممکن است یک آنتیژن خودی مشترک در بافت کلیه و چشم باشد4).
اپیتلیوم توبولار کلیه و اپیتلیوم جسم مژگانی چشم از نظر جنینشناسی ساختارهای مشابهی دارند. اختلال عملکرد آنزیمهای مشترک در هر دو بافت یا تخریب هدف پاسخ ایمنی بهعنوان مکانیسم آسیب همزمان کلیه و چشم فرض میشود.
ارتباط قوی با ژنوتیپهای خاص HLA گزارش شده است. Levinson و همکاران هاپلوتیپ HLA-DQA1*01/DQB1*05/DRB1*01 را در ۱۳ نفر از ۱۸ بیمار شناسایی کردند1). در ژاپنیها، ارتباط با HLA-A2، HLA-A24، HLA-A31 و HLA-DR4 ذکر شده است4). تصور میشود این مولکولهای HLA کلاس II در ارائه آنتیژنهای خودی و فعالسازی سلولهای T خودواکنشگر نقش دارند.
نفریت توبولواینترستیشیال ناشی از دارو ممکن است محرک بروز TINU باشد. در مرور Mandeville و همکاران، حدود ۲۴٪ از موارد گزارششده سابقه مصرف آنتیبیوتیک و ۱۸٪ سابقه مصرف NSAIDs داشتند4). داروهای گزارششده بهعنوان عامل عبارتند از:
ارتباط با عفونتهای قبلی مانند ویروس اپشتین-بار، ویروس واریسلا-زوستر و کلامیدیا مطرح شده است1). مواردی نیز از ارتباط با عفونت SARS-CoV-2 گزارش شده است که در آن پروتئین اسپایک ویروس در بافت کلیه تشخیص داده شده است5). همچنین همراهی با بیماریهای خودایمنی مانند پرکاری تیروئید و آرتریت روماتوئید گزارش شده است1)4).
کونا و همکاران (2026) یک سری 4 موردی را گزارش کردند که در یک مورد سابقه آرتریت روماتوئید و مصرف NSAIDs و در مورد دیگر گاستروانتریت ویروسی پیش از آن وجود داشت. این گزارش تنوع عوامل محیطی را نشان میداد1).
در سندرم TINU، علائم سیستمیک، کلیوی و چشمی ظاهر میشوند. زمان بروز این سه گروه اغلب با فاصله زمانی همراه است که تشخیص را دشوار میکند.
علائم سیستمیک غیراختصاصی هستند و قبل یا همزمان با نفریت ظاهر میشوند.
منعکسکننده نفریت توبولواینترستیشیال حاد است و ممکن است بدون علامت باشد. اغلب با افزایش کراتینین سرم، پروتئیناوری، پیوری استریل و گلیکوزوری تشخیص داده میشود. موارد شدید ممکن است به نارسایی حاد کلیه منجر شده و نیاز به دیالیز داشته باشند، اما به طور کلی پیشآگهی کلیوی خوب است.
علائم چشمی به صورت یووئیت قدامی کلاسیک ظاهر میشوند.
حدود ۸۰٪ موارد به صورت یووئیت قدامی غیرگرانولوماتوز دوطرفه با شروع حاد تظاهر میکنند1). یووئیت همراه با سلول و فلر در اتاق قدامی است، ۶۵٪ دوطرفه و ۸۸٪ قدامی است1). در موارد عودکننده یا مزمن، ممکن است رسوبات اندوتلیال چرب، فیبرین، سینشیای خلفی و هیپوپیون دیده شود.
یافتههای معمول
سلول و فلر اتاق قدامی: یافته التهابی در اتاق قدامی. شدت معمولاً خفیف تا متوسط است.
رسوبات اندوتلیال (KP): اغلب KPهای ریز نقطهای، اما گاهی KPهای چرب دیده میشود.
سینشیای خلفی: در موارد مزمن ظاهر میشود.
یافتههای بخش خلفی چشم
تورم سر عصب بینایی: در حدود 33٪ موارد دیده میشود و نشاندهنده پیشرفت به یووئیت خلفی است6).
کدورت زجاجیه: در حدود 22٪ موارد سلولهای زجاجیه مشاهده میشود6).
لکههای ترشحی شبکیه: در حدود 11٪ موارد ظاهر میشود6).
بین زمان بروز علائم چشمی و کلیوی فاصله زمانی وجود دارد. در 65٪ موارد، علائم چشمی پس از علائم کلیوی ظاهر میشود، در 21٪ موارد پیش از آن و در 15٪ موارد همزمان رخ میدهد. علائم چشمی ممکن است تا 14 ماه پس از تشخیص کلیوی ظاهر شوند1) و این فاصله زمانی عامل اصلی دشواری تشخیص است.
حدود 20٪ موارد با یووئیت میانی، خلفی یا پان یووئیت تظاهر میکنند. گزارشهایی از تورم سر عصب بینایی، کدورت زجاجیه، عروق جدید مشیمیه و نورورتینیت وجود دارد6)7)2). اگرچه نادر است، اما میتواند منجر به اختلال شدید بینایی شود، بنابراین بررسی بخش خلفی چشم توصیه میشود.
سندرم TINU یک تشخیص افتراقی است و باید سایر بیماریهای سیستمیک که هم کلیه و هم چشم را درگیر میکنند، رد شوند1).
معیارهای تشخیصی Mandeville و همکاران (2001) به طور گسترده استفاده میشود4).
| طبقهبندی | شرایط |
|---|---|
| مورد قطعی | تأیید TIN با بیوپسی کلیه + یووئیت |
| مورد احتمالی | یافتههای بالینی معمول + بتا-2 میکروگلوبولین ادراری بالا |
در هر دو مورد، حذف سایر بیماریها مانند سارکوئیدوز، SLE، سندرم شوگرن و سل پیشنیاز است1).
یافتههای آزمایشگاهی مهم برای ارزیابی نفریت به شرح زیر است:
تشخیص قطعی TIN تنها با بیوپسی کلیه امکانپذیر است4). یافتههای بافتشناسی معمول به شرح زیر است:
برای تشخیص قطعی، بیوپسی کلیه لازم است، اما در موارد خفیف بیماری کلیوی، ممکن است خطرات بیش از فواید باشد. در صورت وجود سطح بالای β2-میکروگلوبولین ادرار و یووئیت قدامی دوطرفه معمول، میتوان به عنوان «مورد مشکوک» تشخیص داد7). این تصمیم با مشورت نفرولوژیست گرفته میشود.
بیماریهای زیادی وجود دارند که هم علائم کلیوی و هم یووئیت را نشان میدهند و تشخیص افتراقی مهم است.
درمان سندرم TINU هم برای التهاب چشم و هم برای التهاب کلیه انجام میشود. همکاری بین چشمپزشک و نفرولوژیست مهم است. در راهنمای بالینی یووئیت نیز، برای سندرم TINU به عنوان تشخیص افتراقی یووئیت کودکان، همکاری با نفرولوژیست توصیه میشود 8).
برای یووئیت قدامی، درمانهای موضعی زیر انجام میشود:
اگر عملکرد کلیه به سرعت عادی نشود، کورتیکواستروئیدهای سیستمیک تجویز میشود.
در صورت وجود داروهای محرک مانند ریفامپین یا سولفونامیدها، مصرف آنها قطع میشود.
در صورت غیرقابل قبول بودن عوارض استروئید یا مقاومت به درمان، داروهای سرکوبکننده ایمنی در نظر گرفته میشود 1).
برای یووئیت، در صورت عدم پاسخ به قطرههای استروئیدی یا مشکل در کاهش دوز استروئید، استفاده از مهارکنندههای TNFα (آدالیموماب) نیز گزارش شده است1)7). در موارد شدید همراه با واسکولیت شبکیه یا عود، مصرف خوراکی استروئیدها یا داروهای سرکوبکننده ایمنی ضروری است.
تفاوت پاسخ به درمان و پیشآگهی بین نفریت و التهاب چشمی یکی از ویژگیهای مهم مدیریت این بیماری است.
نفریت معمولاً سیر خوبی دارد. درمان استروئیدی برای نفریت به طور متوسط پس از حدود ۸ ماه قابل قطع است7). در بسیاری از موارد، عملکرد کلیه به طور کامل بهبود مییابد، اما در برخی موارد پیشرفت به سمت نارسایی مزمن کلیه گزارش شده است.
درمان یووئیت به طور متوسط ۱۸ ماه طول میکشد که طولانیتر از نفریت است7). تا ۴۰٪ موارد عود میکنند و تمایل به مزمن شدن دارند. در هنگام عود، ممکن است عوارضی مانند التهاب مجدد اتاق قدامی، چسبندگی عنبیه به عدسی، گلوکوم ثانویه و آب مروارید ایجاد شود. پیگیری طولانی مدت برای آمادگی در برابر عود توصیه میشود.
در دوره طولانی، عوارض زیر گزارش شده است.
درمان استروئیدی برای نفریت به طور متوسط حدود ۸ ماه قابل قطع است. از سوی دیگر، درمان یووئیت به طور متوسط ۱۸ ماه طول میکشد که طولانیتر از نفریت است 7). پیگیری طولانیمدت برای آمادگی در برابر عود توصیه میشود.
García-Fernández و همکاران (2023) در یک مورد TINU در دختر ۱۲ ساله، پروتئین اسپایک SARS-CoV-2 را در بافت بیوپسی کلیه با روش ایمونوفلورسانس تشخیص دادند 5). پروتئین ویروسی در دو بیوپسی کلیه در ۳ ماه و ۱۰ ماه پس از شروع علائم به طور مداوم شناسایی شد. احتمال میرود که تمایل SARS-CoV-2 به کلیه در بروز و تشدید TINU نقش داشته باشد.
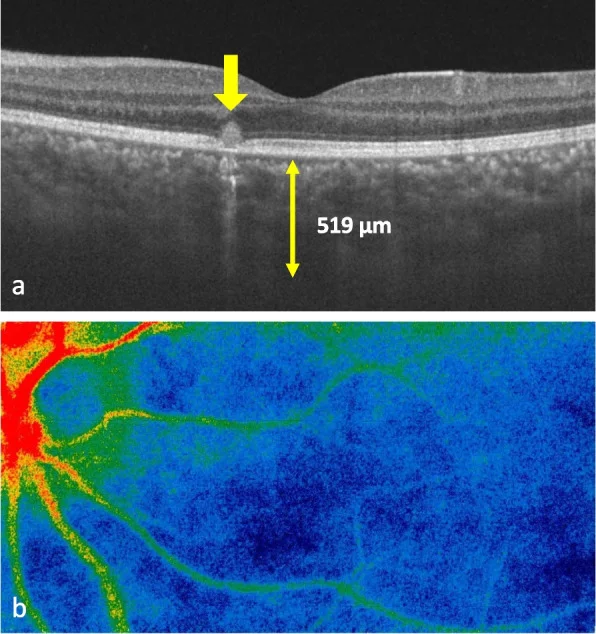
آریتا و همکاران (2023) در یک پسر 12 ساله مبتلا به TINU، کوریورتینیت نهفتهای را که با معاینه معمول فوندوس قابل تشخیص نبود، با تصویربرداری چندوجهی (آنژیوگرافی فلورسین با ICG، OCT، و جریاننگاری لکهای لیزری) شناسایی کردند 6). این نشان میدهد که در سندرم TINU نیز ممکن است التهاب نهفته در بخش خلفی چشم وجود داشته باشد و از نظر پیشگیری از عروق جدید مشیمیه (CNV)، تصویربرداری دقیق توصیه میشود.
وازکز و همکاران (2024) یک دختر 12 ساله را گزارش کردند که 21 ماه پس از تشخیص TINU، با وجود درمان با متوترکسات و آدالیموماب، دچار نورورتینیت شد 7). با استروئید با دوز بالا و تغییر به اینفلیکسیماب، دید به 20/20 بازگشت. این مورد نشان میدهد که عوارض جدید چشمی حتی تحت سرکوب ایمنی نیز ممکن است رخ دهد.
پروتئین کموتاکتیک مونوسیت-1 (MCP-1) در ادرار بیماران TIN افزایش یافته و با فعالیت بیماری همبستگی دارد 4). انتظار میرود که در آینده برای پایش و ارزیابی شدت سندرم TINU به کار رود.
ژانگ و همکاران (2025) یک زن 74 ساله را با سندرم TINU و گاموپاتی مونوکلونال با اهمیت نامشخص (MGUS) گزارش کردند 3). بیوپسی کلیه نفریت بینابینی حاد را تأیید کرد و رسوب زنجیره سبک κ در دیواره عروق مشاهده شد، اما رسوب MIg در گلومرول یا توبول وجود نداشت. درمان با گلوکوکورتیکوئید آسیب کلیوی ناشی از TINU را بهبود بخشید.