典型表現
前房細胞和閃輝:前房內的發炎表現。程度多為輕度至中度。
角膜後沉著物(KP):多為細小點狀KP,但也有表現為羊脂狀KP的病例。
虹膜後粘連:在慢性病例中出現。

腎小管間質性腎炎伴葡萄膜炎症候群(TINU)是一種罕見的全身性發炎疾病,合併急性腎小管間質性腎炎(TIN)和雙眼葡萄膜炎。1975年由Dobrin等人首次報告1)。21世紀初全球僅報告約133例,此後病例報告增加,已達約600例1)。
被認為是一種免疫介導疾病,涉及腎臟和眼睛的共同自體抗原,好發於青春期女性。腎臟和眼部症狀常不同時出現,容易導致診斷延遲。
年發生率估計為每百萬人1-2例1)。在葡萄膜炎患者中占0.1-2%,約5%的TIN切片病例存在此症候群2)。在兒童中,它是葡萄膜炎的主要原因之一,與眼類肉瘤病和青少年慢性虹膜睫狀體炎並列。
流行病學上好發於年輕女性。2022年的一項系統性回顧報告發病年齡中位數為17歲,女性與男性比為1.8:11)。但近期報告顯示,隨著診斷意識的提高,成人和老年人的診斷病例也在增加1)3)。北愛爾蘭的一項研究報告平均診斷年齡為43歲3)。尚未確定與特定民族、種族或地理因素的關聯。
年發生率估計為每百萬人1-2例。僅佔所有葡萄膜炎的0.1-2%,實際上,相當數量的未確診病例可能被診斷為特發性1)。
TINU症候群的确切發病機制尚不清楚,但被認為是一種涉及體液免疫和細胞免疫的自身免疫性疾病1)4)。
腎活檢的組織學發現顯示,浸潤細胞主要是輔助/誘導T細胞亞群3)。這表明細胞免疫在發病機制中起核心作用。
體液免疫的參與也有報導。Tan等人在9例TINU症候群患者中高頻率檢測到血清抗修飾CRP(mCRP)抗體,提示mCRP可能是腎和眼組織的共同靶自身抗原4)。
腎小管上皮和眼睫狀體上皮在胚胎學上具有相似的結構。兩種組織共有的酶功能障礙或免疫應答的靶向破壞被認為是同時累及腎和眼的機制。
已報導與特定HLA基因型有強烈關聯。Levinson等人在18例患者中的13例中鑑定出HLA-DQA101/DQB105/DRB1*01單倍型1)。在日本患者中,已指出與HLA-A2、HLA-A24、HLA-A31和HLA-DR4的關聯4)。推測這些HLA II類分子參與自身抗原的呈遞並激活自身反應性T細胞。
藥物性腎小管間質性腎炎可觸發TINU的發病。Mandeville等人的綜述中,約24%的報告病例有抗生素使用史,18%有NSAIDs使用史4)。已報導的致病藥物如下:
EB病毒、水痘帶狀疱疹病毒、披衣菌等先前感染被認為與發病相關1)。也有報告指出與SARS-CoV-2感染相關,有病例在腎組織中檢測到病毒棘蛋白5)。此外,有報告指出與甲狀腺功能亢進症、類風濕性關節炎等自體免疫疾病合併發生1)4)。
Cunha等人(2026年)報告了4例病例系列,其中1例有類風濕性關節炎病史並使用NSAIDs,另1例有病毒性胃腸炎前驅症狀。該報告顯示了環境因素的多樣性1)。
TINU症候群可出現全身症狀、腎臟症狀和眼部症狀。三者出現的時間常有差異,使診斷變得困難。
全身症狀為非特異性,可在腎炎之前或同時出現。
反映急性腎小管間質性腎炎,可能無症狀。常透過血清肌酸酐升高、蛋白尿、無菌性膿尿、糖尿等檢查異常發現。重症病例可能導致需要透析的急性腎損傷,但腎臟預後通常良好。
眼部症狀表現為典型的前葡萄膜炎。
約80%表現為急性發作的雙眼非肉芽腫性前葡萄膜炎1)。葡萄膜炎伴有前房細胞和閃輝,65%為雙眼性,88%為前葡萄膜炎1)。在復發或遷延病例中,可能出現羊脂狀KP、纖維素滲出、虹膜後粘連和前房蓄膿。
典型表現
前房細胞和閃輝:前房內的發炎表現。程度多為輕度至中度。
角膜後沉著物(KP):多為細小點狀KP,但也有表現為羊脂狀KP的病例。
虹膜後粘連:在慢性病例中出現。
後眼部所見
視神經乳頭腫脹:約33%的患者出現,暗示可能進展為後葡萄膜炎6)。
玻璃體混濁:約22%的患者可見玻璃體細胞6)。
視網膜滲出斑:約11%的患者出現6)。
眼部症狀和腎臟症狀的出現時間存在時間差。65%的病例眼部症狀出現在腎臟症狀之後,21%先於腎臟症狀,15%同時出現。眼部症狀可能在腎臟診斷後長達14個月才出現1),這種時間差是導致診斷困難的主要原因。
約20%的病例表現為中間葡萄膜炎、後葡萄膜炎或全葡萄膜炎。有視神經乳頭腫脹、玻璃體混濁、脈絡膜新生血管、視神經視網膜炎等的報告6)7)2)。雖然罕見,但可能導致嚴重的視功能損害,因此建議對後眼部進行詳細檢查。
TINU症候群是排除性診斷,需要排除其他同時累及腎臟和眼部的全身性疾病1)。
Mandeville等人的診斷標準(2001年)被廣泛使用4)。
| 分類 | 要求 |
|---|---|
| 確定病例 | 腎臟切片證實TIN + 葡萄膜炎 |
| 推定病例 | 典型臨床表現 + 尿中β2微球蛋白升高 |
無論哪種情況,前提是排除其他疾病,如類肉瘤病、全身性紅斑狼瘡、修格連氏症候群和結核病1)。
評估腎炎的重要檢查結果如下。
TIN的確診只能透過腎臟切片來達成4)。典型的組織學發現如下:
確診需要腎臟切片,但在腎臟疾病較輕微的情況下,風險可能大於益處。如果尿液β2微球蛋白升高且伴有典型的雙側前葡萄膜炎,可診斷為「疑似病例」7)。需與腎臟內科討論後決定。
許多疾病同時表現腎臟症狀和葡萄膜炎,鑑別診斷很重要。
TINU症候群的治療需同時針對眼部與腎臟發炎。眼科與腎臟內科的協作至關重要。葡萄膜炎診療指引也建議將TINU症候群作為兒童葡萄膜炎的鑑別診斷,並與腎臟內科協作8)。
對於前葡萄膜炎,進行以下局部治療。
如果腎功能未能迅速恢復正常,則進行全身性皮質類固醇給藥。
如果存在可能誘發的藥物,如利福平或磺胺類藥物,應停用。
如果類固醇副作用不可接受或治療抵抗,可考慮免疫抑制劑1)。
對於葡萄膜炎,在類固醇眼藥水無效或類固醇減量困難的情況下,也有使用TNFα抑制劑(阿達木單抗)的報告1)7)。當伴有視網膜血管炎而重症化或復發時,需要口服類固醇或使用免疫抑制劑。
腎炎和眼部炎症在治療反應和預後上存在差異,這是本病管理上的重要特徵。
腎炎通常預後良好。腎炎的類固醇治療中位時間約為8個月後可停藥7)。大多數病例腎功能完全恢復,但也有部分病例進展為慢性腎損傷。
葡萄膜炎的治療中位時間為18個月,比腎炎更長7)。高達40%的病例會復發並趨於慢性化。復發時可能出現前房炎症再燃、虹膜後粘連、繼發性青光眼、白內障等併發症。建議進行長期追蹤以應對復發。
長期病程中報告了以下併發症。
腎炎的類固醇治療中位數約8個月可停藥。而葡萄膜炎的治療中位數為18個月,比腎炎更長7)。建議長期追蹤以防復發。
García-Fernández等人(2023)在一例12歲女性TINU患者的腎活檢組織中,通過免疫螢光法檢測到SARS-CoV-2棘蛋白5)。在症狀出現後3個月和10個月的兩次腎活檢中持續檢測到病毒蛋白。提示SARS-CoV-2的腎嗜性可能參與TINU的發生和加重。
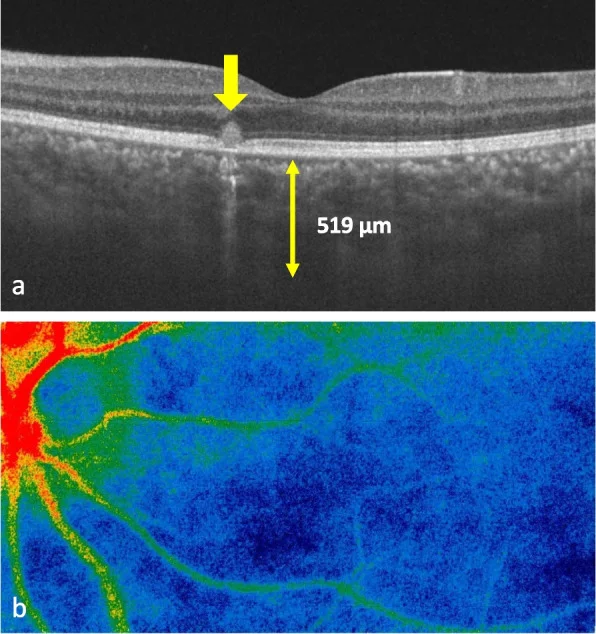
Arita等人(2023)利用多模態影像(ICG螢光血管造影、OCT、雷射斑點血流成像)在一名12歲男性TINU病例中檢測到常規眼底檢查難以發現的潛伏性脈絡膜炎6)。這表明TINU症候群中可能存在後段潛在發炎,從預防脈絡膜新生血管(CNV)的角度建議進行詳細影像檢查。
Vazquez等人(2024)報告了一名12歲女性,在TINU診斷後21個月,儘管接受methotrexate和adalimumab治療,仍發生神經視網膜炎7)。改用高劑量類固醇和infliximab後視力恢復至20/20。該病例顯示即使在免疫抑制下仍可能出現新的眼部併發症。
單核球趨化蛋白-1(MCP-1)在TIN患者尿液中升高,並據報導與疾病活動性相關4)。未來有望應用於TINU症候群的監測和嚴重度評估。
Zhang等人(2025)報告了一名74歲女性TINU症候群合併意義未明的單株丙種球蛋白病(MGUS)病例3)。腎臟切片證實急性間質性腎炎,血管壁有κ輕鏈沉積,但腎小球和腎小管無MIg沉積。糖皮質類固醇治療改善了TINU相關的腎損傷。