视神经系统

COVID-19的神经眼科征象
一目了然的要点
Section titled “一目了然的要点”1. 什么是COVID-19的神经眼科征象
Section titled “1. 什么是COVID-19的神经眼科征象”COVID-19的神经眼科体征是指与SARS-CoV-2感染(COVID-19)相关的、累及视神经、脑神经、视路、瞳孔通路等神经眼科系统的多种临床体征的总称。
SARS-CoV-2于2019年在中国武汉首次报告病例,2020年3月WHO宣布大流行。随后蔓延至223个以上国家,导致超过7.7亿确诊病例和约700万人死亡(WHO)。2020年在美国成为仅次于心脏病和癌症的第三大死因。约4%的重症COVID-19患者报告有神经系统并发症1),重症风险在60岁以上且有基础疾病的人群中最高。
约4%的重症COVID-19患者报告有神经系统并发症1)。头痛见于高达71%的SARS-CoV-2阳性患者,眼痛见于34%。视神经炎和脑神经麻痹等神经眼科体征可在感染期间或恢复后出现。
2. 主要症状与临床所见
Section titled “2. 主要症状与临床所见”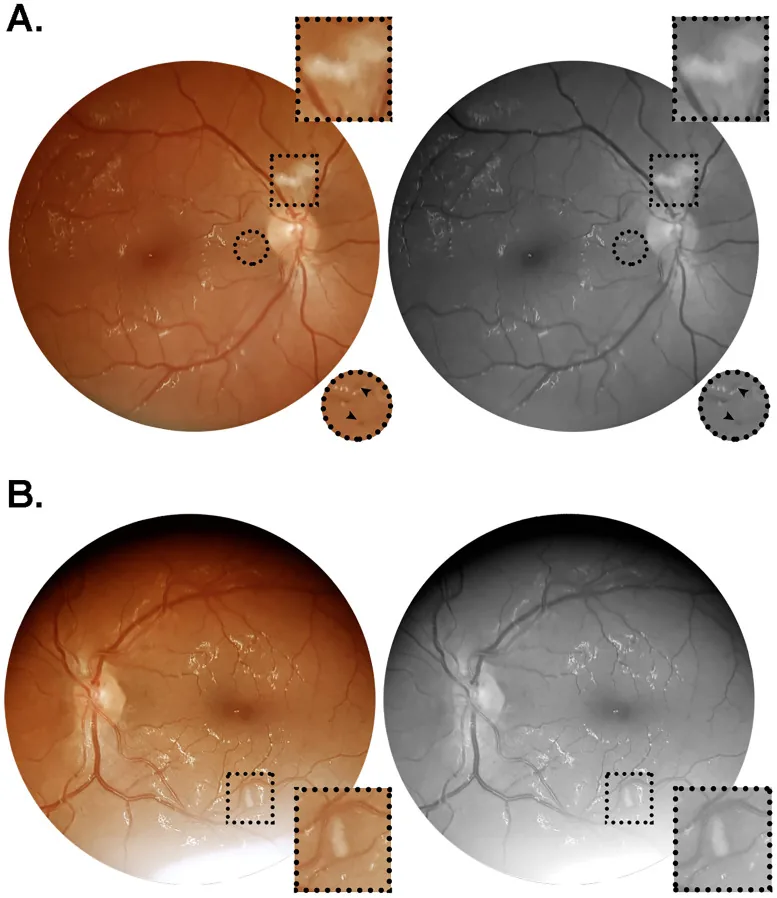
- 头痛:高达71%的SARS-CoV-2阳性患者报告此症状。
- 眼痛:34%的患者出现。
- 视力下降:由视神经炎、视神经梗死、可逆性后部脑病综合征(PRES)等引起的急性视力下降。
- 复视:由第3、4、6脑神经麻痹引起。
- 视振荡(oscillopsia):免疫介导性脑炎相关症状。
与COVID-19相关的神经眼科体征多种多样。主要类别如下所示。
脑神经与眼球运动系统
视路及其他
3. 原因与风险因素
Section titled “3. 原因与风险因素”SARS-CoV-2的特性与神经组织入侵
Section titled “SARS-CoV-2的特性与神经组织入侵”SARS-CoV-2属于冠状病毒科,是一种有包膜的正链单链RNA病毒。刺突(S)蛋白与ACE2受体结合,侵入宿主细胞。ACE2受体不仅在呼吸道上皮细胞中表达,也在脑神经元和胶质细胞中表达。
目前认为其侵入神经组织的途径如下:
- 嗅神经途径:通过嗅神经直接侵入中枢神经系统。
- 脑膜/脉络丛途径:不通过血脑屏障的侵入途径。
- 血行性途径:通过病毒血症经全身循环侵入。
- 直接神经损伤:病毒直接侵袭神经细胞。
- 细胞因子风暴:单核细胞、中性粒细胞、T淋巴细胞的免疫激活引发局部和全身炎症,导致血管通透性增加。
- 异常自身抗体产生:抗MOG抗体阳性等免疫介导的神经损伤。
- 血液高凝状态:促炎状态导致脑静脉窦血栓形成(CVST)和卒中风险增加。
- 60岁以上、基础疾病(如高血压、糖尿病)
- 重症COVID-19(多器官功能衰竭)
- 大剂量类固醇使用(毛霉菌病发病风险)
与NA-AION的关联
Section titled “与NA-AION的关联”SARS-CoV-2感染已被报道为非动脉炎性前部缺血性视神经病变(NA-AION)的风险因素。2)其发病机制推测为炎症性/自身免疫性血栓性微血管病变。COVID-19疫苗接种后也有NA-AION的报道。2)
4. 诊断与检查方法
Section titled “4. 诊断与检查方法”COVID-19的确定诊断
Section titled “COVID-19的确定诊断”COVID-19的诊断方法如下所示。
| 检测方法 | 特点 | 适用时机 |
|---|---|---|
| PCR(鼻咽拭子) | 金标准 | 感染第1周 |
| 血清学检查 | 检测病毒抗原的抗体 | 感染第2周及以后 |
灵敏度并非完美,需结合临床数据和流行病学史进行诊断。
神经眼科评估
Section titled “神经眼科评估”检查时应确认以下体征。
视野及电生理检查
Section titled “视野及电生理检查”- 视野检查:视神经炎典型表现为(旁)中心暗点,缺血性视神经病变(AION)典型表现为水平半盲。
- 视觉诱发电位(VEP):脱髓鞘疾病表现为潜伏期延长,缺血性疾病仅表现为振幅降低。
- 光学相干断层扫描(OCT):对视神经损伤进行定量评估有用。
- 眼眶MRI:有助于识别与视神经炎相关的异常增强效应。冠状位脂肪抑制STIR序列和增强T1加权序列尤其有用。
- FLAIR图像:用于评估脱髓鞘病变(多发性硬化合并评估)。
- DWI(弥散加权成像):有助于评估卒中及视神经缺血。
视神经炎的鉴别诊断需排除缺血性、压迫性、肿瘤性、鼻源性、中毒性及遗传性视神经病变。非典型视神经炎的特征包括以下内容。
- 发病年龄不在15-45岁之间
- 双眼发病
- 发病后2周以上仍进展
- 激素依赖性
- 全身症状的合并
抗AQP4抗体和抗MOG抗体的评估对鉴别诊断也很重要。与NA-AION的鉴别可参考年龄、有无疼痛、视野模式及VEP结果。2)
5. 标准治疗方法
Section titled “5. 标准治疗方法”COVID-19的全身管理包括抗SARS-CoV-2单克隆抗体、抗病毒药物、免疫调节剂和肾上腺皮质激素。对于呼吸衰竭,基本措施是通过脉搏血氧仪监测并维持血氧饱和度在92-96%。
据报道,地塞米松或瑞德西韦与降低神经系统并发症(包括卒中、癫痫和脑膜炎)的发生率相关。两药联用具有协同效应,在非低氧性COVID-19中,地塞米松也降低了神经系统并发症的风险。1)
视神经炎的治疗
Section titled “视神经炎的治疗”视神经炎的治疗如下。
| 病型 | 一线治疗 | 备注 |
|---|---|---|
| 典型视神经炎 | 类固醇脉冲疗法 | 加速视力恢复(对最终视力的影响有限) |
| 非典型视神经炎 | 类固醇冲击疗法 | 必须适应症。疑似NMO/胶原病时需专科协作 |
- 类固醇冲击疗法:甲泼尼龙1000mg/日,静脉滴注3天。
- 脉冲治疗后不口服泼尼松龙(基于ONTT的研究结果)。
- 若怀疑NMO、胶原病或血管炎综合征,需与神经内科等科室协作。
缺血性视神经病变(AION)的治疗
Section titled “缺血性视神经病变(AION)的治疗”- 动脉炎性AION(GCA相关):大剂量糖皮质激素静脉滴注1g/日×3
5天,之后口服泼尼松龙1mg/kg/日,在46个月内逐渐减量。 - 非动脉炎性AION(NA-AION):目前对于改善急性期视功能损害和预防对侧眼发病,均无明确有效的治疗方法。
神经眼科体征的总体管理
Section titled “神经眼科体征的总体管理”基本处理包括针对炎症、缺血、高凝状态及全身异常(高血压、低氧血症)的干预。对于脑卒中相关病例,可选择治疗性抗凝、静脉溶栓或机械取栓。使用免疫抑制剂时,需注意活动性感染患者的感染并发症风险。目前尚无标准的筛查方案或既定的决策算法。
视神经炎的基本治疗是类固醇脉冲疗法(甲泼尼龙1000mg/日×3天静脉滴注)。非典型视神经炎(双眼性、类固醇依赖性、全身并发症等)中,该治疗是必须的适应症。若怀疑NMO谱系障碍或胶原病,需要与神经内科等协作。
6. 病理生理学·详细发病机制
Section titled “6. 病理生理学·详细发病机制”SARS-CoV-2的刺突(S)蛋白与ACE2受体结合侵入宿主细胞。ACE2受体广泛分布于呼吸道上皮、食管、心肌细胞、膀胱尿路上皮、肾近端肾小管、脑(神经元、胶质细胞)。
神经眼科体征的发病机制被认为涉及以下途径的复合作用。
- 直接神经损伤:病毒通过嗅神经、脑膜、脉络丛、血行途径侵入中枢神经系统,直接损伤神经元和胶质细胞。
- 细胞因子风暴:单核细胞、中性粒细胞、T淋巴细胞的激活引发局部和全身炎症,导致血管通透性增加和肺水肿。这种全身炎症进一步导致神经组织的继发性损伤。
- 免疫介导机制:诱导异常自身抗体产生(如抗MOG抗体),引起视神经炎和NMO谱系障碍。
- 血液高凝状态:持续存在的促炎状态增加脑静脉窦血栓形成(CVST)和脑卒中的风险。
神经眼科体征与全身症状同时出现,或在数天至数周后出现。
NA-AION的推测机制是SARS-CoV-2感染引起的炎症性/自身免疫性血栓性微血管病变。2)在疫苗相关的神经眼科并发症中,已报道因脉络膜毛细血管微血管缺血导致的急性黄斑神经视网膜病变(AMN)。
长COVID中的神经眼科症状被认为是由慢性炎症和细胞因子持续增加所维持的。
7. 最新研究与未来展望(研究阶段报告)
Section titled “7. 最新研究与未来展望(研究阶段报告)”抗病毒药物预防神经系统并发症
Section titled “抗病毒药物预防神经系统并发症”Grundmann等人(2022)在一项针对重症COVID-19患者的分析中报告,使用地塞米松或瑞德西韦治疗与包括卒中、癫痫和脑膜炎在内的神经系统并发症发生率降低相关1)。两种药物联用显示出协同效应,且在非低氧性COVID-19中,地塞米松也降低了神经系统并发症风险。从预防神经系统并发症的角度来看,这两种药物的定位需要进一步研究。
疫苗接种后的神经眼科并发症
Section titled “疫苗接种后的神经眼科并发症”COVID-19疫苗接种后已有神经眼科并发症的报道。
- 颅内出血·脑静脉血栓症
- 脑神经病变·瞳孔异常(霍纳综合征、霍姆斯-阿迪瞳孔、瞳孔缩小、瞳孔散大)
- 双侧AION·急性缺血性脑卒中
- 视神经炎·BPPV
- 急性黄斑神经视网膜病变(AMN):可能与感染或疫苗接种直接相关
长COVID的神经眼科症状
Section titled “长COVID的神经眼科症状”在COVID-19康复后神经眼科症状持续存在的长COVID中,报告了以下情况。
- 持续性头痛和视神经炎
- 角膜神经损伤
- 眼球运动的变化
- 视神经乳头静脉炎
- 炎症性视网膜血管闭塞
巨细胞动脉炎(GCA)的相关性
Section titled “巨细胞动脉炎(GCA)的相关性”已有报道指出COVID-19感染和疫苗接种均与巨细胞动脉炎(GCA)相关,期待未来积累更多证据。
8. 参考文献
Section titled “8. 参考文献”- Grundmann A, et al. Fewer COVID-19 neurological complications with dexamethasone and remdesivir. Ann Neurol. 2022. doi:10.1002/ana.26536
- Salvetat ML, et al. Non-Arteritic Anterior Ischemic Optic Neuropathy. Vision. 2023;7:72.
