視神經系統

COVID-19的神經眼科徵候
一目瞭然的重點
Section titled “一目瞭然的重點”1. 什麼是COVID-19的神經眼科徵兆
Section titled “1. 什麼是COVID-19的神經眼科徵兆”COVID-19的神經眼科徵候是指伴隨SARS-CoV-2感染(COVID-19)而出現的視神經、腦神經、視路、瞳孔路徑等神經眼科系統受損的多種臨床徵候的總稱。
SARS-CoV-2於2019年在中國武漢首次報告病例,2020年3月WHO宣布大流行。隨後擴散至223個以上國家,造成超過7.7億確診病例及約700萬人死亡(WHO)。2020年在美國成為僅次於心臟病和癌症的第三大死因。重症COVID-19患者中約4%出現神經學併發症1),重症風險在60歲以上且有基礎疾病者中最高。
重症COVID-19中約4%報告有神經學併發症1)。頭痛見於最多71%的SARS-CoV-2陽性者,眼痛見於34%。視神經炎或腦神經麻痺等神經眼科徵候可能在感染期間或恢復後出現。
2. 主要症狀與臨床表現
Section titled “2. 主要症狀與臨床表現”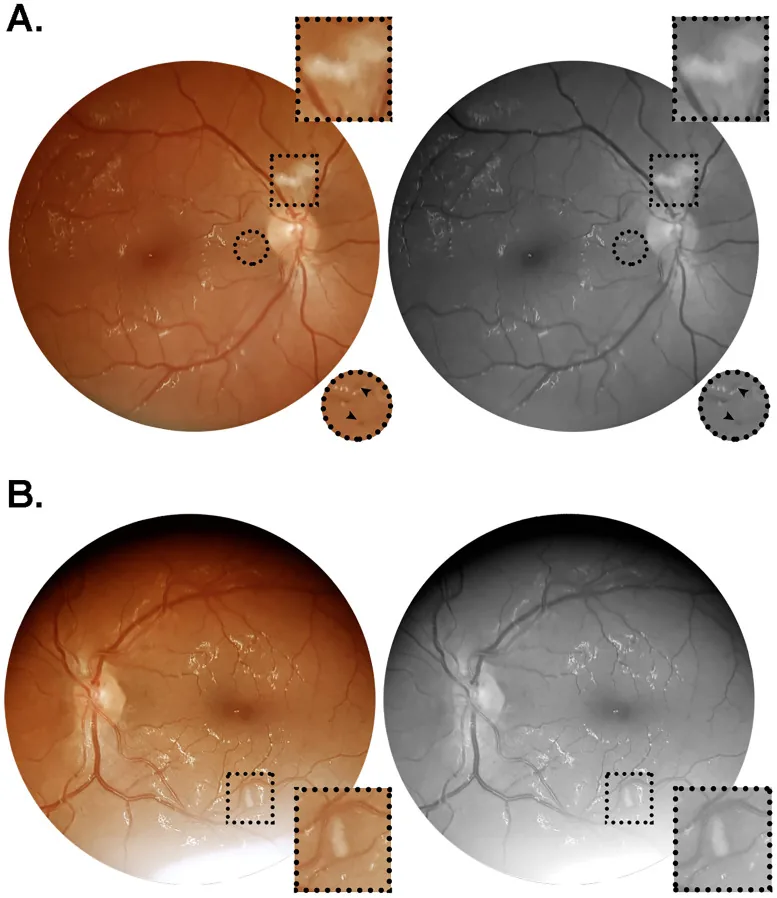
- 頭痛:高達71%的SARS-CoV-2陽性患者會出現。
- 眼痛:34%的患者會出現。
- 視力下降:因視神經炎、視神經梗塞、後可逆性腦病症候群(PRES)等引起的急性視力下降。
- 複視:伴隨第3、4、6對腦神經麻痺而出現。
- 視搖晃(oscillopsia):免疫介導性腦炎相關症狀。
與COVID-19相關的神經眼科徵象多種多樣。主要類別如下所示。
腦神經與眼球運動系統
視路及其他
COVID-19後的複視主要由第3、4、6對腦神經麻痺引起。也可能發生在費雪症候群(以眼肌麻痺、運動失調、腱反射消失為三大主徵)、格林-巴利症候群、重症肌無力的背景下。也有報告指出伴隨腦靜脈竇血栓(CVST)的情況。
3. 原因與風險因素
Section titled “3. 原因與風險因素”SARS-CoV-2的特性與神經組織侵入
Section titled “SARS-CoV-2的特性與神經組織侵入”SARS-CoV-2屬於冠狀病毒科,是一種具有包膜的正鏈單股RNA病毒。棘突(S)蛋白與ACE2受體結合,進入宿主細胞。ACE2受體不僅存在於呼吸道上皮,也存在於腦神經元和神經膠質細胞中。
目前認為以下途徑可侵入神經組織:
- 嗅神經途徑:通過嗅神經直接侵入中樞神經系統。
- 腦膜/脈絡叢途徑:不經由血腦屏障的侵入。
- 血行性途徑:透過病毒血症引起的全身循環侵入。
- 直接神經損傷:病毒直接侵襲神經細胞。
- 細胞激素風暴:單核球、嗜中性球、T淋巴球的免疫活化引發局部及全身性發炎,導致血管通透性增加。
- 異常自體抗體產生:抗MOG抗體陽性等免疫介導的神經損傷。
- 血液高凝固狀態:因發炎促進狀態導致腦靜脈竇血栓(CVST)及中風風險增加。
- 60歲以上、患有基礎疾病(如高血壓、糖尿病等)
- 重症COVID-19(多重器官衰竭)
- 高劑量類固醇使用(增加罹患毛黴菌症風險)
與NA-AION的關聯
Section titled “與NA-AION的關聯”SARS-CoV-2感染已被報告為非動脈炎性前部缺血性視神經病變(NA-AION)的危險因子。2)其致病機轉被認為是發炎性、自體免疫性的血栓性微血管病變。COVID-19疫苗接種後也有NA-AION的案例報告。2)
4. 診斷與檢查方法
Section titled “4. 診斷與檢查方法”COVID-19的確定診斷
Section titled “COVID-19的確定診斷”COVID-19的診斷方法如下所示。
| 檢查方法 | 特徵 | 適用時機 |
|---|---|---|
| PCR(鼻咽拭子) | 黃金標準 | 感染第一週 |
| 血清學檢查 | 檢測病毒抗原的抗體 | 感染第二週以後 |
敏感性並非完全,需結合臨床數據和流行病學史進行診斷。
神經眼科評估
Section titled “神經眼科評估”檢查時需確認以下發現:
視野與電生理檢查
Section titled “視野與電生理檢查”- 視野檢查:視神經炎典型表現為(旁)中心暗點,缺血性視神經病變(AION)則為水平半盲。
- 視覺誘發電位(VEP):脫髓鞘疾病顯示潛時延長,缺血性疾病僅顯示振幅下降。
- 光學同調斷層掃描(OCT):有助於定量評估視神經病變。
- 眼眶MRI:有助於識別與視神經炎相關的異常增強效應。冠狀斷面脂肪抑制STIR影像和顯影T1加權影像特別有用。
- FLAIR影像:用於評估脫髓鞘病變(合併多發性硬化症的評估)。
- DWI(擴散加權影像):有助於評估中風及視神經缺血。
視神經炎的鑑別診斷需排除缺血性、壓迫性、腫瘤性、鼻源性、中毒性及遺傳性視神經病變。非典型視神經炎的特徵包括以下幾點。
- 發病年齡不在15至45歲之間
- 雙眼發病
- 發病後兩週以上仍持續進展
- 類固醇依賴性
- 全身症狀的合併
抗AQP4抗體與抗MOG抗體的評估對鑑別診斷也很重要。與NA-AION的鑑別需參考年齡、有無疼痛、視野型態及VEP檢查結果。2)
5. 標準治療方法
Section titled “5. 標準治療方法”COVID-19的全身管理包括使用抗SARS-CoV-2單株抗體、抗病毒藥物、免疫調節劑和皮質類固醇。對於呼吸衰竭,基本措施是通過脈搏血氧儀監測並維持血氧飽和度在92-96%。
據報導,地塞米松或瑞德西韋與降低神經系統併發症(包括中風、癲癇和腦膜炎)的發生率相關。兩藥聯合使用具有協同作用,即使在非低氧性COVID-19中,地塞米松也降低了神經系統併發症的風險。1)
視神經炎的治療
Section titled “視神經炎的治療”視神經炎的治療如下:
| 病型 | 第一線用藥 | 備註 |
|---|---|---|
| 典型視神經炎 | 類固醇脈衝療法 | 加速視力恢復(對最終視力影響有限) |
| 非典型視神經炎 | 類固醇脈衝療法 | 必須適應症。疑似NMO或膠原病時需專科合作 |
- 類固醇脈衝療法:甲基潑尼松龍每日1000mg,連續3天靜脈滴注。
- 脈衝治療後不口服prednisolone(根據ONTT研究結果)。
- 若懷疑NMO、膠原病或血管炎症候群,需與神經內科等專科合作。
缺血性視神經病變(AION)的治療
Section titled “缺血性視神經病變(AION)的治療”- 動脈炎性AION(GCA相關):大量皮質類固醇靜脈注射1g/日×3~5天,之後口服prednisolone 1mg/kg/日,並在4~6個月內逐漸減量。
- 非動脈炎性AION(NA-AION):目前對於急性期視功能障礙改善及預防對側眼發作,均無明確有效的治療。
神經眼科徵候的整體管理
Section titled “神經眼科徵候的整體管理”基本處理原則為針對發炎、缺血、高凝血狀態及全身異常(高血壓、低氧血症)進行處置。若與腦中風相關,可考慮治療性抗凝血治療、靜脈血栓溶解治療及機械性血栓移除術。使用免疫抑制劑時,需注意活動性感染病例的感染併發症風險。目前尚無標準篩檢或確立的決策演算法。
視神經炎的基本治療是類固醇脈衝療法(甲基潑尼松龍1000毫克/日×3天靜脈滴注)。非典型視神經炎(雙眼性、類固醇依賴性、全身併發症等)則必須採用此治療。若懷疑是NMO譜系疾病或膠原病,需與神經內科等部門合作。
6. 病理生理學・詳細發病機制
Section titled “6. 病理生理學・詳細發病機制”SARS-CoV-2的棘突蛋白(S蛋白)與ACE2受體結合後侵入宿主細胞。ACE2受體廣泛分布於呼吸道上皮、食道、心肌細胞、膀胱尿路上皮、腎近曲小管、腦部(神經元、神經膠質細胞)。
神經眼科徵象的發病機制被認為涉及以下多重路徑的綜合作用。
- 直接神經損傷:病毒經由嗅神經、腦膜、脈絡叢、血行路徑侵入中樞神經系統,直接損害神經元和神經膠質細胞。
- 細胞激素風暴:單核球、嗜中性球、T淋巴球的活化引發局部及全身性發炎,導致血管通透性增加和肺水腫。此全身性發炎進一步造成神經組織的二次損傷。
- 免疫媒介機制:誘發異常自體抗體產生(如抗MOG抗體),引起視神經炎及NMO譜系疾病。
- 血液高凝固狀態:持續的促發炎狀態增加腦靜脈竇血栓(CVST)及中風的風險。
神經眼科徵候與全身症狀同時出現,或在數日至數週後出現。
NA-AION的推測機轉為SARS-CoV-2感染引起的發炎性、自體免疫性血栓性微血管病變。2)在疫苗相關的神經眼科併發症中,已有報告指出脈絡膜微血管缺血導致急性黃斑神經視網膜病變(AMN)。
長新冠中的神經眼科症狀被認為是由慢性發炎和持續增加的細胞激素產生所維持。
7. 最新研究與未來展望(研究階段報告)
Section titled “7. 最新研究與未來展望(研究階段報告)”抗病毒藥物預防神經學併發症
Section titled “抗病毒藥物預防神經學併發症”Grundmann等人(2022)在一項針對重症COVID-19患者的分析中報告,使用地塞米松或瑞德西韋治療與降低包括中風、癲癇和腦膜炎在內的神經學併發症的發生率相關1)。兩種藥物聯合使用具有協同效應,且在非低氧性COVID-19中,地塞米松也降低了神經學併發症的風險。從預防神經學併發症的角度來看,這兩種藥物的定位仍需進一步探討。
疫苗接種後的神經眼科併發症
Section titled “疫苗接種後的神經眼科併發症”COVID-19疫苗接種後已有神經眼科併發症的報告。
- 顱內出血、腦靜脈血栓
- 腦神經病變・瞳孔異常(霍納氏症候群、霍姆斯-艾迪瞳孔、縮瞳、散瞳)
- 雙側AION・急性缺血性腦中風
- 視神經炎・良性陣發性姿勢性眩暈(BPPV)
- 急性黃斑神經視網膜病變(AMN):可能與感染或疫苗接種有直接關聯
長新冠的神經眼科症狀
Section titled “長新冠的神經眼科症狀”在COVID-19康復後仍持續出現神經眼科症狀的長新冠中,已報告以下情況。
- 持續頭痛、視神經炎
- 角膜神經損傷
- 眼球運動的變化
- 視神經乳頭靜脈炎
- 發炎性視網膜血管阻塞
巨細胞動脈炎(GCA)的相關性
Section titled “巨細胞動脈炎(GCA)的相關性”COVID-19感染和疫苗接種兩者均被報告與巨細胞動脈炎(GCA)相關,未來期待更多證據累積。
8. 參考文獻
Section titled “8. 參考文獻”- Grundmann A, et al. Fewer COVID-19 neurological complications with dexamethasone and remdesivir. Ann Neurol. 2022. doi:10.1002/ana.26536
- Salvetat ML, et al. Non-Arteritic Anterior Ischemic Optic Neuropathy. Vision. 2023;7:72.
