阿迪瞳孔
病灶:睫狀神經節(周邊)
瞳孔大小:中度散大,不規則圓形
側別:多為單側(約80%)
緊張性:有(縮瞳持續較長時間)
毛果芸香鹼反應:低濃度時縮瞳

Adie緊張性瞳孔(Adie tonic pupil)是由於副交感神經去神經支配,導致患側瞳孔對光反射消失或減弱,而近反射(近見反應)則表現出良好且緊張性的縮瞳的疾病。
疾病名稱來源於William John Adie,1931年由Adie、Morgan、Symons和Holmes幾乎同時獨立報導。患病率為每1000人2例,男女比為2.6:1,女性居多(約70%為女性),平均發病年齡為32歲。約80%為單側,每年有4%的病例進展為雙側。
相關症候群包括以下兩種重要情況:
約80%為單側發病。但每年有4%的病例進展為雙側,因此在追蹤期間也應注意對側瞳孔的變化。
初期患眼散瞳,與對側瞳孔不等明顯,但慢性病程中患眼瞳孔反而有縮小的趨勢。這被認為是睫狀體來源的副交感神經纖維異常再生支配了瞳孔括約肌所致。
大部分為特發性(原因不明),責任病灶位於周邊睫狀神經節和短後睫狀神經。
可確定的原因包括以下:
關於Ross症候群的病因,有學說認為遺傳易感性與環境因素(如病毒感染)共同作用。有同卵雙胞胎Ross症候群的報導以及巨細胞病毒感染後發病的病例,提示遺傳和感染因素可能都參與其中3)。
關於COVID-19感染後的緊張性瞳孔,自COVID-19流行以來,已有多個免疫介導機製發病的報導,作為感染後的神經眼科併發症已得到廣泛認識1, 2)。
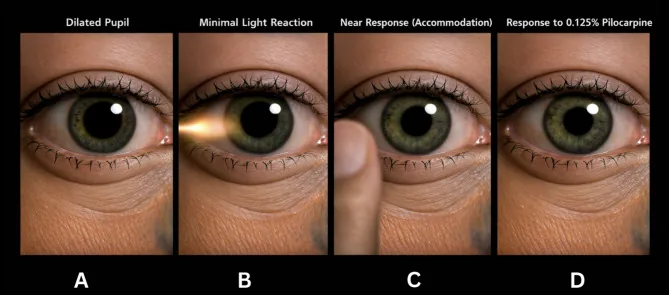
當出現典型症狀(節段性麻痺、蠕蟲樣運動、光-近反射分離)時,診斷很容易。
低濃度毛果芸香鹼點眼試驗應用最廣泛。
需要以出現光-近反射分離的疾病為中心進行鑑別。
阿迪瞳孔
病灶:睫狀神經節(周邊)
瞳孔大小:中度散大,不規則圓形
側別:多為單側(約80%)
緊張性:有(縮瞳持續較長時間)
毛果芸香鹼反應:低濃度時縮瞳
阿蓋爾·羅伯遜瞳孔
病灶:中腦頂蓋前區(梅毒)
瞳孔大小:雙側嚴重縮瞳
側別:雙側
緊張性:無
毛果芸香鹼反應:低濃度無反應
頂蓋瞳孔
病灶:中腦背側(如松果體腫瘤)
瞳孔大小:中度散大
側別:雙側
帕里諾症候群:常合併出現
緊張性:無
其他鑑別診斷包括動眼神經麻痺後的異常再生、眼眶外傷/腫瘤、水痘-帶狀疱疹感染、Fisher症候群、Charcot-Marie-Tooth病、神經結節病。
梅毒血清學檢查(RPR)、糖尿病、外傷、神經疾病的病史有助於診斷。若懷疑羅斯症候群,可用Minor試驗(碘澱粉試驗)檢測無汗區域3)。
不能排除。急性期時,去神經超敏反應尚未建立,因此可能出現陰性結果。若臨床體徵(蠕蟲樣運動、節段性麻痺)典型,即使試驗陰性也可臨床診斷為艾迪瞳孔。定期複查也有幫助。
艾迪瞳孔是一種良性病程的疾病,對大多數患者,充分解釋「其為良性疾病」後,基本策略是追蹤觀察。
關於病程:調節麻痺可能在數月到數年內改善。然而,瞳孔對光反射通常不會恢復。合併全身性疾病時預後不一定良好,原發疾病的管理很重要。
羅斯症候群代償性多汗症的治療:使用外用格隆溴銨、氯化鋁乳膏、肉毒桿菌毒素注射。對於重症且希望手術的患者,胸部交感神經切除術也是一種選擇3)。
調節麻痺引起的視物模糊和近距離視力障礙可能在數月到數年內改善。但瞳孔對光反射通常不會恢復,因此不能期望瞳孔對光反應正常化。該病很少導致嚴重視力障礙,是一種可以安心追蹤的良性疾病。
Adie瞳孔的發病機轉中,「去神經過敏」和「異常再生」兩個機制扮演核心角色。
副交感神經解剖學背景:從動眼神經的Edinger-Westphal(EW)核發出的副交感神經纖維中,95%到達睫狀肌(參與調節),5%到達瞳孔括約肌(參與光反射)。睫狀神經節中與光反射和調節反應相關的神經元比例為3:97,特點是參與光反射的纖維原本就很少。
發病過程按以下順序進展:
光近反射分離的神經解剖學解釋:近反應到EW核的核上纖維走行於中腦頂蓋前區和後連合的腹側,而光反射的傳入纖維通過該區域。因此,頂蓋前區損傷(中樞性)也可引起類似的分離,但Adie瞳孔的病灶位於睫狀神經節(周邊),這是鑑別的關鍵。
COVID-19相關機制:在SARS-CoV-2感染後的緊張性瞳孔中,提出了三種機制:病毒直接神經侵入、內皮功能障礙、以及過度炎症和細胞因子釋放導致的神經毒性1)。
Ross症候群的病理:後根神經節神經元和副交感神經系統被認為共同起源於神經嵴細胞,這一觀點被提出作為解釋Ross症候群中腱反射消失的假說3)。
自COVID-19流行以來,感染後緊張性瞳孔作為神經眼科併發症的病例報告相繼出現。
Quijano-Nieto等人(2021年)報告了一例36歲女性在COVID-19感染(PCR陽性)17天後出現雙側緊張性瞳孔的病例1)。腦部MRI、血液檢查和腦脊液檢查均正常。0.125%毛果芸香鹼眼藥水證實雙眼強烈縮瞳。推測為免疫介導機制。
Gopal等人(2021年)報告了一例37歲女性在COVID-19感染3週後出現右眼緊張性瞳孔的病例2)。右眼瞳孔直徑5.5毫米,可見蠕蟲樣運動和節段性收縮。0.1%毛果芸香鹼眼藥水證實縮瞳。腦部和眼眶MRI無顯著發現,推測感染後免疫反應為原因。
Ahmad等人(2022年)報告了同一機構一個月內診斷的兩例羅斯症候群3)。病例1(24歲女性)表現為左緊張性瞳孔、右踝反射消失和T4水平以下節段性無汗三聯徵。病例2(42歲女性)為「羅斯症候群plus」,合併雙側緊張性瞳孔、下肢腱反射消失和霍納氏症候群。
有觀點認為羅斯症候群可能與帕金森氏症、路易體失智症和多系統萎縮症一樣屬於突觸核蛋白病3)。此外,羅斯症候群、霍姆斯-阿迪症候群和哈勒昆症候群可能是同一疾病過程的不同表型,未來有望整合這些疾病概念。
Quijano-Nieto BA, Córdoba-Ortega CM. Tonic pupil after COVID-19 infection. Arch Soc Esp Oftalmol. 2021;96(7):353-355.
Gopal M, Ambika S, Padmalakshmi K. Tonic Pupil Following COVID-19. J Neuroophthalmol. 2021;41:e764-e766.
Ahmad R, Saurabh K. Two Cases of Tonic Pupil: Ross and Ross Syndrome Plus. Cureus. 2022;14(2):e22305.