Pupila de Adie
Lesão: Gânglio ciliar (periférico)
Diâmetro pupilar: Midríase moderada, irregular
Lateralidade: Frequentemente unilateral (cerca de 80%)
Tonicidade: Presente (miose prolongada)
Resposta à pilocarpina: Miose em baixa concentração

A pupila tônica de Adie (Adie tonic pupil) é uma doença causada por denervação parassimpática, na qual o reflexo fotomotor da pupila afetada está ausente ou diminuído, enquanto o reflexo de acomodação (para perto) mostra miose boa e tônica.
O nome da doença deriva de William John Adie, e foi relatada independentemente quase ao mesmo tempo em 1931 por Adie, Morgan, Symons e Holmes. A prevalência é de 2 por 1000 pessoas, razão sexual 2,6:1 (cerca de 70% mulheres), e idade média de início aos 32 anos. Cerca de 80% são unilaterais, e a progressão para bilateral ocorre a uma taxa de 4% ao ano.
Síndromes relacionadas importantes:
Cerca de 80% dos casos são unilaterais. No entanto, a progressão para bilateral ocorre a uma taxa de 4% ao ano, portanto, durante o acompanhamento, é necessário observar alterações pupilares no olho contralateral.
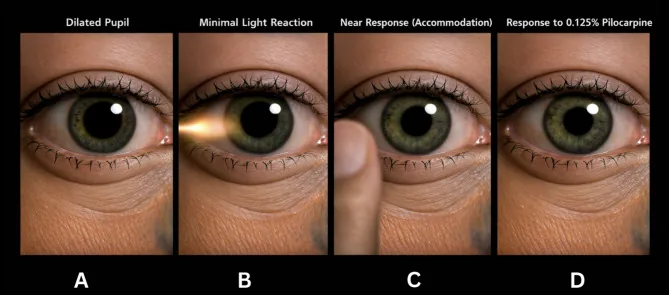
Inicialmente, a pupila do olho afetado dilata e a anisocoria com o lado contralateral é evidente, mas no curso crônico, a pupila afetada tende a contrair, ao contrário. Acredita-se que isso ocorre porque as fibras nervosas parassimpáticas do corpo ciliar controlam o esfíncter da pupila devido à regeneração anormal.
A maioria é idiopática (causa desconhecida), e a lesão responsável é o gânglio ciliar periférico e os nervos ciliares curtos posteriores.
As causas identificáveis incluem:
Sobre a etiologia da síndrome de Ross, foi proposta a teoria de que a predisposição genética somada a fatores ambientais (como infecção viral) contribui. Há relatos de síndrome de Ross em gêmeos idênticos e casos de início após infecção por citomegalovírus, sugerindo que fatores genéticos e infecciosos podem estar envolvidos 3).
Sobre a pupila tônica após infecção por COVID-19, desde a pandemia de COVID-19, vários casos de início por mecanismo imune foram relatados, e é reconhecida como uma complicação neuro-oftalmológica pós-infecção 1, 2).
Se os sintomas típicos (paralisia segmentar, movimento vermicular, dissociação luz-perto) estiverem presentes, o diagnóstico é fácil.
Teste de instilação de pilocarpina em baixa concentração é o mais utilizado.
É necessário diferenciar de doenças que apresentam dissociação luz-perto.
Pupila de Adie
Lesão: Gânglio ciliar (periférico)
Diâmetro pupilar: Midríase moderada, irregular
Lateralidade: Frequentemente unilateral (cerca de 80%)
Tonicidade: Presente (miose prolongada)
Resposta à pilocarpina: Miose em baixa concentração
Pupila de Argyll Robertson
Lesão: Área pré-tetal do mesencéfalo (sífilis)
Diâmetro pupilar: Miose intensa bilateral
Lateralidade: Bilateral
Tonicidade: Ausente
Resposta à pilocarpina: Sem resposta em baixa concentração
Pupila tectal
Lesão: Mesencéfalo dorsal (tumor pineal, etc.)
Diâmetro pupilar: Midríase moderada
Lateralidade: Bilateral
Síndrome de Parinaud: Frequentemente associada
Tonicidade: Ausente
Outros diagnósticos diferenciais incluem: regeneração neural anômala após paralisia do nervo oculomotor, trauma ou tumor orbitário, infecção por varicela-zóster, síndrome de Fisher, doença de Charcot-Marie-Tooth, sarcoidose neurológica.
O teste sorológico para sífilis (RPR) e a verificação de histórico de diabetes, trauma ou doenças neurológicas auxiliam no diagnóstico. Se houver suspeita de síndrome de Ross, use o teste de Minor (teste de iodo-amido) para detectar áreas de anidrose 3).
Não pode ser descartada. Na fase aguda, a hipersensibilidade por desnervação ainda não está estabelecida, portanto o resultado pode ser negativo. Se os achados clínicos (movimento vermiforme, paralisia segmentar) forem típicos, é possível diagnosticar clinicamente a pupila tônica de Adie mesmo com teste negativo. O reexame periódico também é útil.
A pupila tônica de Adie é uma doença de curso benigno. Para a maioria dos pacientes, a conduta básica é explicar que é uma doença benigna e realizar acompanhamento.
Sobre o curso: A paralisia de acomodação pode melhorar em meses a anos. Por outro lado, o reflexo pupilar à luz geralmente não se recupera. O prognóstico em casos com doença sistêmica não é necessariamente bom, e o manejo da doença primária é importante.
Tratamento da hiperidrose compensatória na síndrome de Ross: Glicopirrolato tópico, creme de cloreto de alumínio e injeção de toxina botulínica são utilizados. Em casos graves que desejam cirurgia, a simpatectomia torácica também é uma opção 3).
A visão turva e a dificuldade para perto devido à paralisia de acomodação podem melhorar em meses a anos. No entanto, o reflexo pupilar à luz geralmente não se recupera, portanto a normalização da resposta pupilar à luz não é esperada. Frequentemente não leva a comprometimento visual grave, sendo uma doença benigna que pode ser acompanhada com segurança.
Dois mecanismos principais desempenham um papel central na patogênese da pupila de Adie: “hipersensibilidade por desnervação” e “regeneração anormal”.
Contexto Anatômico Parassimpático: 95% das fibras parassimpáticas do núcleo de Edinger-Westphal (EW) do nervo oculomotor vão para o músculo ciliar (envolvido na acomodação) e 5% para o esfíncter da pupila (envolvido no reflexo fotomotor). A proporção de neurônios envolvidos no reflexo fotomotor e na acomodação no gânglio ciliar é de 3:97, sendo característico que as fibras do reflexo fotomotor sejam originalmente poucas.
O curso da patogênese progride na seguinte ordem:
Explicação neuroanatômica da dissociação luz-perto: As fibras supranucleares para o núcleo de EW para o reflexo de acomodação percorrem ventralmente em relação às fibras aferentes do reflexo fotomotor que passam pela área pré-tetal do mesencéfalo e comissura posterior. Portanto, lesões na área pré-tetal (centrais) também podem causar dissociação semelhante, mas na pupila de Adie, a lesão está no gânglio ciliar (periférico), sendo este o ponto chave para a diferenciação.
Mecanismo relacionado à COVID-19: Na pupila tônica pós-infecção por SARS-CoV-2, três mecanismos foram propostos: invasão neural direta do vírus, disfunção endotelial e neurotoxicidade devido à inflamação excessiva e liberação de citocinas1).
Fisiopatologia da síndrome de Ross: Acredita-se que os neurônios do gânglio da raiz dorsal e o sistema parassimpático compartilhem uma origem comum a partir das células da crista neural, o que explica a perda dos reflexos tendinosos na síndrome de Ross3).
Desde a pandemia de COVID-19, relatos de casos de pupila tônica como complicação neuro-oftalmológica pós-infecção têm surgido.
Quijano-Nieto et al. (2021) relataram o caso de uma mulher de 36 anos que desenvolveu pupila tônica bilateral 17 dias após infecção por COVID-19 (PCR positiva)1). Ressonância magnética cerebral, exames de sangue e líquido cefalorraquidiano estavam normais. Miose intensa em ambos os olhos foi confirmada com colírio de pilocarpina a 0,125%. Mecanismo imunomediado é presumido.
Gopal et al. (2021) relataram o caso de uma mulher de 37 anos que desenvolveu pupila tônica no olho direito 3 semanas após infecção por COVID-192). Diâmetro pupilar do olho direito de 5,5 mm, com movimentos vermiculares e contração segmentar observados. Miose confirmada com colírio de pilocarpina a 0,1%. Ressonância magnética cerebral e orbitária sem achados significativos, e a resposta imune pós-infecção é sugerida como causa.
Ahmad et al. (2022) relataram dois casos de síndrome de Ross diagnosticados na mesma instituição em um mês3). Caso 1 (mulher de 24 anos) apresentou a tríade: pupila tônica esquerda, perda do reflexo do tendão de Aquiles direito e anidrose segmentar até o nível T4. Caso 2 (mulher de 42 anos) foi “Ross syndrome plus” com pupila tônica bilateral, perda de reflexos nos membros inferiores e síndrome de Horner associada.
A síndrome de Ross é proposta como uma sinucleinopatia, assim como a doença de Parkinson, demência com corpos de Lewy e atrofia de múltiplos sistemas3). Além disso, sugere-se que a síndrome de Ross, síndrome de Holmes-Adie e síndrome de Arlequim podem ser fenótipos diferentes do mesmo processo patológico, e espera-se a integração futura desses conceitos.
Quijano-Nieto BA, Córdoba-Ortega CM. Tonic pupil after COVID-19 infection. Arch Soc Esp Oftalmol. 2021;96(7):353-355.
Gopal M, Ambika S, Padmalakshmi K. Tonic Pupil Following COVID-19. J Neuroophthalmol. 2021;41:e764-e766.
Ahmad R, Saurabh K. Two Cases of Tonic Pupil: Ross and Ross Syndrome Plus. Cureus. 2022;14(2):e22305.