Đồng tử Adie
Tổn thương: Hạch mi (ngoại vi)
Đường kính đồng tử: Giãn vừa, không tròn
Bên: Thường một bên (khoảng 80%)
Trương lực: Có (co đồng tử kéo dài)
Đáp ứng pilocarpine: Co đồng tử ở nồng độ thấp

Đồng tử trương lực Adie (Adie tonic pupil) là bệnh do mất chi phối thần kinh phó giao cảm, khiến phản xạ ánh sáng của đồng tử bị ảnh hưởng mất hoặc giảm, trong khi phản xạ điều tiết (nhìn gần) cho thấy co đồng tử tốt và có tính trương lực.
Tên bệnh bắt nguồn từ William John Adie, và được báo cáo độc lập gần như cùng lúc vào năm 1931 bởi Adie, Morgan, Symons và Holmes. Tỷ lệ hiện mắc là 2 trên 1000 người, tỷ lệ giới tính 2,6:1 (khoảng 70% là nữ), và tuổi khởi phát trung bình là 32. Khoảng 80% là một bên, và tiến triển thành hai bên xảy ra với tỷ lệ 4% mỗi năm.
Các hội chứng liên quan sau đây quan trọng:
Khoảng 80% trường hợp là một bên. Tuy nhiên, tiến triển thành hai bên xảy ra với tỷ lệ 4% mỗi năm, do đó trong quá trình theo dõi cần chú ý đến thay đổi đồng tử ở mắt đối diện.
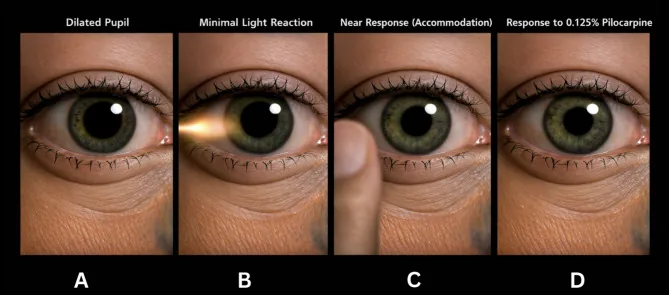
Ban đầu, đồng tử mắt bị ảnh hưởng giãn ra và sự bất đẳng đồng tử với bên đối diện rõ rệt, nhưng trong diễn tiến mạn tính, đồng tử bị ảnh hưởng có xu hướng co lại ngược lại. Điều này được cho là do các sợi thần kinh phó giao cảm từ thể mi chi phối cơ thắt đồng tử do tái tạo bất thường.
Phần lớn là vô căn (không rõ nguyên nhân), và tổn thương chịu trách nhiệm là hạch mi ngoại vi và các dây thần kinh mi ngắn sau.
Các nguyên nhân xác định được bao gồm:
Về căn nguyên của hội chứng Ross, giả thuyết cho rằng yếu tố di truyền kết hợp với yếu tố môi trường (như nhiễm virus) góp phần gây bệnh. Có báo cáo về hội chứng Ross ở cặp song sinh cùng trứng và các trường hợp khởi phát sau nhiễm cytomegalovirus, cho thấy cả yếu tố di truyền và nhiễm trùng có thể liên quan 3).
Về đồng tử trương lực sau nhiễm COVID-19, kể từ đại dịch COVID-19, một số trường hợp khởi phát do cơ chế qua trung gian miễn dịch đã được báo cáo, và được công nhận là biến chứng thần kinh nhãn khoa sau nhiễm trùng 1, 2).
Nếu có các triệu chứng điển hình (liệt phân đoạn, cử động giun, phản xạ ánh sáng-gần phân ly), chẩn đoán dễ dàng.
Thử nghiệm nhỏ pilocarpine nồng độ thấp được sử dụng rộng rãi nhất.
Cần phân biệt với các bệnh có biểu hiện phản xạ ánh sáng-gần phân ly.
Đồng tử Adie
Tổn thương: Hạch mi (ngoại vi)
Đường kính đồng tử: Giãn vừa, không tròn
Bên: Thường một bên (khoảng 80%)
Trương lực: Có (co đồng tử kéo dài)
Đáp ứng pilocarpine: Co đồng tử ở nồng độ thấp
Đồng tử Argyll Robertson
Tổn thương: Vùng trước mái não giữa (giang mai)
Đường kính đồng tử: Co đồng tử nặng hai bên
Tính bên: Hai bên
Trương lực: Không
Đáp ứng pilocarpine: Không đáp ứng ở nồng độ thấp
Đồng tử mái
Tổn thương: Lưng não giữa (u tuyến tùng, v.v.)
Đường kính đồng tử: Giãn đồng tử mức độ vừa
Tính bên: Hai bên
Hội chứng Parinaud: Thường đi kèm
Trương lực: Không
Các chẩn đoán phân biệt khác bao gồm: tái tạo thần kinh bất thường sau liệt dây thần kinh vận nhãn, chấn thương hoặc u hốc mắt, nhiễm varicella zoster, hội chứng Fisher, bệnh Charcot-Marie-Tooth, sarcoid thần kinh.
Xét nghiệm huyết thanh giang mai (RPR) và kiểm tra tiền sử đái tháo đường, chấn thương hoặc bệnh thần kinh hỗ trợ chẩn đoán. Nếu nghi ngờ hội chứng Ross, hãy sử dụng nghiệm pháp Minor (nghiệm pháp iốt-tinh bột) để phát hiện vùng vô mồ hôi 3).
Không thể loại trừ. Trong giai đoạn cấp, hiện tượng mẫn cảm do mất thần kinh chưa được thiết lập, do đó kết quả có thể âm tính. Nếu các dấu hiệu lâm sàng (vận động giống sâu, liệt phân đoạn) điển hình, có thể chẩn đoán lâm sàng đồng tử Adie ngay cả khi nghiệm pháp âm tính. Kiểm tra lại định kỳ cũng hữu ích.
Đồng tử Adie là bệnh có diễn tiến lành tính. Đối với đa số bệnh nhân, giải thích rằng đây là bệnh lành tính và theo dõi là nguyên tắc cơ bản.
Về diễn tiến: Liệt điều tiết có thể cải thiện trong vài tháng đến vài năm. Mặt khác, phản xạ đồng tử với ánh sáng thường không hồi phục. Tiên lượng trong trường hợp có bệnh toàn thân không nhất thiết tốt, và việc quản lý bệnh nguyên phát là quan trọng.
Điều trị chứng tăng tiết mồ hôi bù trừ trong hội chứng Ross: Glycopyrrolat bôi ngoài da, kem nhôm clorua và tiêm độc tố botulinum được sử dụng. Trong trường hợp nặng muốn phẫu thuật, cắt hạch giao cảm ngực cũng là một lựa chọn 3).
Nhìn mờ và khó nhìn gần do liệt điều tiết có thể cải thiện trong vài tháng đến vài năm. Tuy nhiên, phản xạ ánh sáng thường không hồi phục, do đó không thể mong đợi bình thường hóa đáp ứng đồng tử với ánh sáng. Thường không dẫn đến suy giảm thị lực nghiêm trọng, và là bệnh lành tính có thể theo dõi an toàn.
Hai cơ chế chính đóng vai trò trung tâm trong cơ chế bệnh sinh của đồng tử Adie: “mẫn cảm sau hủy thần kinh” và “tái sinh bất thường”.
Bối cảnh giải phẫu phó giao cảm: 95% sợi phó giao cảm từ nhân Edinger-Westphal (EW) của thần kinh vận nhãn đi đến cơ thể mi (tham gia điều tiết), 5% đến cơ thắt đồng tử (tham gia phản xạ ánh sáng). Tỷ lệ tế bào thần kinh liên quan đến phản xạ ánh sáng và điều tiết tại hạch mi là 3:97, đặc trưng bởi số lượng sợi phản xạ ánh sáng vốn đã ít.
Diễn tiến bệnh sinh tiến triển theo thứ tự sau:
Giải thích giải phẫu thần kinh về phân ly phản xạ ánh sáng-điều tiết: Các sợi trên nhân đến nhân EW cho phản xạ điều tiết chạy ở phía bụng so với các sợi hướng tâm của phản xạ ánh sáng đi qua vùng tiền thị giữa não và mép sau. Do đó, tổn thương vùng tiền thị (trung ương) cũng có thể gây phân ly tương tự, nhưng ở đồng tử Adie, tổn thương nằm ở hạch mi (ngoại biên), đây là điểm mấu chốt để phân biệt.
Cơ chế liên quan đến COVID-19: Trong đồng tử trương lực sau nhiễm SARS-CoV-2, ba cơ chế đã được đề xuất: xâm nhập thần kinh trực tiếp của virus, rối loạn chức năng nội mô, và độc tính thần kinh do viêm quá mức và giải phóng cytokine1).
Sinh lý bệnh hội chứng Ross: Các tế bào thần kinh hạch rễ lưng và hệ phó giao cảm được cho là có chung nguồn gốc từ tế bào mào thần kinh, điều này giải thích sự mất phản xạ gân xương trong hội chứng Ross3).
Kể từ đại dịch COVID-19, các báo cáo ca bệnh về đồng tử trương lực như một biến chứng thần kinh nhãn khoa sau nhiễm trùng đã liên tiếp xuất hiện.
Quijano-Nieto và cộng sự (2021) báo cáo trường hợp một phụ nữ 36 tuổi bị đồng tử trương lực hai bên 17 ngày sau khi nhiễm COVID-19 (PCR dương tính)1). MRI não, xét nghiệm máu và dịch não tủy đều bình thường. Co đồng tử mạnh ở cả hai mắt được xác nhận bằng nhỏ pilocarpine 0,125%. Cơ chế qua trung gian miễn dịch được cho là nguyên nhân.
Gopal và cộng sự (2021) báo cáo trường hợp một phụ nữ 37 tuổi bị đồng tử trương lực mắt phải 3 tuần sau khi nhiễm COVID-192). Đường kính đồng tử mắt phải 5,5 mm, quan sát thấy chuyển động ngoằn ngoèo và co thắt phân đoạn. Co đồng tử được xác nhận bằng nhỏ pilocarpine 0,1%. MRI não và hốc mắt không có phát hiện đáng kể, và đáp ứng miễn dịch sau nhiễm trùng được cho là nguyên nhân.
Ahmad và cộng sự (2022) báo cáo hai trường hợp hội chứng Ross được chẩn đoán tại cùng một cơ sở trong vòng một tháng3). Trường hợp 1 (nữ 24 tuổi) biểu hiện bộ ba: đồng tử trương lực trái, mất phản xạ gân Achilles phải và vô tiết mồ hôi phân đoạn đến mức T4. Trường hợp 2 (nữ 42 tuổi) là “Ross syndrome plus” với đồng tử trương lực hai bên, mất phản xạ chi dưới và hội chứng Horner kèm theo.
Hội chứng Ross được cho là một bệnh lý synuclein giống như bệnh Parkinson, sa sút trí tuệ thể Lewy và teo đa hệ thống3). Ngoài ra, hội chứng Ross, hội chứng Holmes-Adie và hội chứng Harlequin có thể là các kiểu hình khác nhau của cùng một quá trình bệnh, và sự hợp nhất các khái niệm bệnh trong tương lai được kỳ vọng.
Quijano-Nieto BA, Córdoba-Ortega CM. Tonic pupil after COVID-19 infection. Arch Soc Esp Oftalmol. 2021;96(7):353-355.
Gopal M, Ambika S, Padmalakshmi K. Tonic Pupil Following COVID-19. J Neuroophthalmol. 2021;41:e764-e766.
Ahmad R, Saurabh K. Two Cases of Tonic Pupil: Ross and Ross Syndrome Plus. Cureus. 2022;14(2):e22305.