阿迪瞳孔
病灶:睫状神经节(外周)
瞳孔大小:中度散大,不规则圆形
侧别:多为单侧(约80%)
紧张性:有(缩瞳持续较长时间)
毛果芸香碱反应:低浓度时缩瞳

Adie紧张性瞳孔(Adie tonic pupil)是由于副交感神经失神经支配,导致患侧瞳孔对光反射消失或减弱,而近反射(近见反应)则表现出良好且紧张性的缩瞳的疾病。
疾病名称来源于William John Adie,1931年由Adie、Morgan、Symons和Holmes几乎同时独立报道。患病率为每1000人2例,男女比为2.6:1,女性居多(约70%为女性),平均发病年龄为32岁。约80%为单侧,每年有4%的病例进展为双侧。
相关综合征包括以下两种重要情况:
约80%为单侧发病。但每年有4%的病例进展为双侧,因此在随访期间也应注意对侧瞳孔的变化。
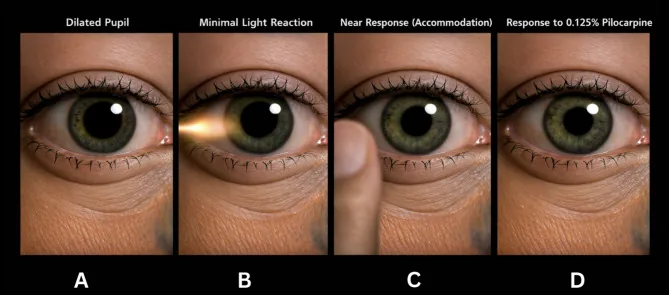
初期患眼散瞳,与对侧瞳孔不等明显,但慢性病程中患眼瞳孔反而有缩小的趋势。这被认为是由于睫状体来源的副交感神经纤维异常再生支配了瞳孔括约肌所致。
大部分为特发性(原因不明),责任病灶位于外周睫状神经节和短后睫状神经。
可确定的原因包括以下:
关于Ross综合征的病因,有学说认为遗传易感性与环境因素(如病毒感染)共同作用。有同卵双胞胎Ross综合征的报道以及巨细胞病毒感染后发病的病例,提示遗传和感染因素可能都参与其中3)。
关于COVID-19感染后的紧张性瞳孔,自COVID-19流行以来,已有多个免疫介导机制发病的报道,作为感染后的神经眼科并发症已得到广泛认识1, 2)。
当出现典型症状(节段性麻痹、蠕虫样运动、光-近反射分离)时,诊断很容易。
低浓度毛果芸香碱滴眼试验应用最广泛。
需要以出现光-近反射分离的疾病为中心进行鉴别。
阿迪瞳孔
病灶:睫状神经节(外周)
瞳孔大小:中度散大,不规则圆形
侧别:多为单侧(约80%)
紧张性:有(缩瞳持续较长时间)
毛果芸香碱反应:低浓度时缩瞳
阿盖尔·罗伯逊瞳孔
病灶:中脑顶盖前区(梅毒)
瞳孔大小:双侧严重缩瞳
侧别:双侧
紧张性:无
毛果芸香碱反应:低浓度无反应
顶盖瞳孔
病灶:中脑背侧(如松果体肿瘤)
瞳孔大小:中度散大
侧别:双侧
帕里诺综合征:常合并出现
紧张性:无
其他鉴别诊断包括动眼神经麻痹后的异常再生、眼眶外伤/肿瘤、水痘-带状疱疹感染、Fisher综合征、Charcot-Marie-Tooth病、神经结节病。
梅毒血清学检查(RPR)、糖尿病、外伤、神经系统疾病的病史有助于诊断。若怀疑罗斯综合征,可用Minor试验(碘淀粉试验)检测无汗区域3)。
不能排除。急性期时,去神经超敏反应尚未建立,因此可能出现阴性结果。若临床体征(蠕虫样运动、节段性麻痹)典型,即使试验阴性也可临床诊断为阿迪瞳孔。定期复查也有帮助。
阿迪瞳孔是一种良性病程的疾病,对大多数患者,充分解释“其为良性疾病”后,基本策略是随访观察。
关于病程:调节麻痹可能在数月到数年内改善。然而,瞳孔对光反射通常不会恢复。合并全身性疾病时预后不一定良好,原发病的管理很重要。
罗斯综合征代偿性多汗症的治疗:使用外用格隆溴铵、氯化铝乳膏、肉毒毒素注射。对于重症且希望手术的患者,胸部交感神经切除术也是一种选择3)。
调节麻痹引起的视物模糊和近视力障碍可能在数月到数年内改善。但瞳孔对光反射通常不会恢复,因此不能期望瞳孔对光反应正常化。该病很少导致严重视力障碍,是一种可以安心随访的良性疾病。
Adie瞳孔的发病机制中,“去神经超敏”和“异常再生”两个机制起核心作用。
副交感神经解剖学背景:从动眼神经的Edinger-Westphal(EW)核发出的副交感神经纤维中,95%到达睫状肌(参与调节),5%到达瞳孔括约肌(参与光反射)。睫状神经节中与光反射和调节反应相关的神经元比例为3:97,特点是参与光反射的纤维原本就很少。
发病过程按以下顺序进展:
光近反射分离的神经解剖学解释:近反应到EW核的核上纤维走行于中脑顶盖前区和后连合的腹侧,而光反射的传入纤维通过该区域。因此,顶盖前区损伤(中枢性)也可引起类似的分离,但Adie瞳孔的病灶位于睫状神经节(外周),这是鉴别的关键。
COVID-19相关机制:在SARS-CoV-2感染后的紧张性瞳孔中,提出了三种机制:病毒直接神经侵入、内皮功能障碍、以及过度炎症和细胞因子释放导致的神经毒性1)。
Ross综合征的病理:后根神经节神经元和副交感神经系统被认为共同起源于神经嵴细胞,这一观点被提出作为解释Ross综合征中腱反射消失的假说3)。
自COVID-19流行以来,感染后紧张性瞳孔作为神经眼科并发症的病例报告相继出现。
Quijano-Nieto等人(2021年)报告了一例36岁女性在COVID-19感染(PCR阳性)17天后出现双侧紧张性瞳孔的病例1)。脑MRI、血液检查和脑脊液检查均正常。0.125%毛果芸香碱滴眼液证实双眼强烈缩瞳。推测为免疫介导机制。
Gopal等人(2021年)报告了一例37岁女性在COVID-19感染3周后出现右眼紧张性瞳孔的病例2)。右眼瞳孔直径5.5毫米,可见蠕虫样运动和节段性收缩。0.1%毛果芸香碱滴眼液证实缩瞳。脑和眼眶MRI无显著发现,推测感染后免疫反应为原因。
Ahmad等人(2022年)报告了同一机构一个月内诊断的两例罗斯综合征3)。病例1(24岁女性)表现为左紧张性瞳孔、右踝反射消失和T4水平以下节段性无汗三联征。病例2(42岁女性)为“罗斯综合征plus”,合并双侧紧张性瞳孔、下肢腱反射消失和霍纳综合征。
有观点认为罗斯综合征可能与帕金森病、路易体痴呆和多系统萎缩一样属于突触核蛋白病3)。此外,罗斯综合征、霍姆斯-阿迪综合征和哈勒昆综合征可能是同一疾病过程的不同表型,未来有望整合这些疾病概念。
Quijano-Nieto BA, Córdoba-Ortega CM. Tonic pupil after COVID-19 infection. Arch Soc Esp Oftalmol. 2021;96(7):353-355.
Gopal M, Ambika S, Padmalakshmi K. Tonic Pupil Following COVID-19. J Neuroophthalmol. 2021;41:e764-e766.
Ahmad R, Saurabh K. Two Cases of Tonic Pupil: Ross and Ross Syndrome Plus. Cureus. 2022;14(2):e22305.