中枢性(第一级神经元)
通路:下丘脑至Budge中枢(C8-T2)
常见原因:脑干梗死(Wallenberg综合征)、脑干肿瘤、多发性硬化
伴随表现:下丘脑病变→对侧偏瘫和感觉减退;脑桥病变→外展神经麻痹;延髓病变→Wallenberg综合征(同侧面部感觉异常、对侧温痛觉减退、侧倾、斜视偏差)

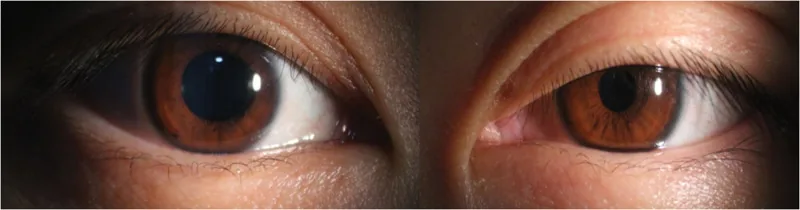
霍纳综合征是由于眼交感神经系统受损,导致眼部及全身出现多种症状的综合征。三大主征为瞳孔缩小、上睑下垂和出汗减少,病变可发生在中枢、节前或节后任何部位。
该病以Claude Bernard(1852年)和Johann Friedrich Horner(1869年)的名字命名,也称为Bernard-Horner综合征。眼交感神经通路从下丘脑经三个神经元到达瞳孔开大肌,路径长,病变部位不同,病因和紧急程度差异很大。
瞳孔缩小为中度,在暗处患眼与健眼瞳孔不等大最为明显。对光反射保持正常,这是与Adie瞳孔和动眼神经麻痹的重要鉴别点。上眼睑Müller肌失神经支配导致约2mm的轻度上睑下垂,下眼睑Müller肌受累导致下眼睑轻度上抬(反向性上睑下垂)。两者共同导致睑裂狭窄和外观上的眼球内陷。
| 病变部位 | 出汗减少范围 |
|---|---|
| 中枢性(第一级神经元) | 全身半侧 |
| 节前性(第二级神经元) | 面部半侧 |
| 节后性(第三级神经元) | 前额内侧和鼻尖(也可能正常) |
如果先天性或出生后一年内发病,则伴有虹膜色素减退(虹膜异色)。原因包括产钳分娩等出生时颈部外伤,但也有许多原因不明的病例。
眼交感神经通路由三个神经元链组成,根据病变部位不同,病因也不同。
中枢性(第一级神经元)
通路:下丘脑至Budge中枢(C8-T2)
常见原因:脑干梗死(Wallenberg综合征)、脑干肿瘤、多发性硬化
伴随表现:下丘脑病变→对侧偏瘫和感觉减退;脑桥病变→外展神经麻痹;延髓病变→Wallenberg综合征(同侧面部感觉异常、对侧温痛觉减退、侧倾、斜视偏差)
节前性(二级神经元)
通路:Budge中枢至星状神经节(颈上神经节)
常见原因:Pancoast肿瘤(肺尖肿瘤)、臂丛神经麻痹、锁骨下动脉瘤、颈部手术后
特点:由于通路经过肺尖和纵隔,应优先排除肺癌和纵隔肿瘤
节后性(三级神经元)
通路:星状神经节至瞳孔开大肌
常见原因:颈内动脉夹层、甲状腺手术后、颈动脉内膜剥脱术后、外伤性颈内动脉夹层
特点:急性发作伴颈部疼痛或头痛强烈提示夹层,属于急症
GCA是一种发生于50岁以上人群的中大型血管肉芽肿性血管炎,已有报道可并发霍纳综合征1)。一项针对GCA患者的病例系列分析显示,53例中有2例(约4%)出现霍纳综合征1)。
病例报告中,一名67岁男性出现右滑车神经麻痹和左霍纳综合征,ESR 70mm/hr、CRP 10mg/L升高。开始使用泼尼松60mg后复视消失,但霍纳综合征持续存在1)。另一名71岁男性出现双侧头痛、下颌痛、左霍纳综合征和skew deviation,ESR 68mm/hr、CRP 46mg/L。开始使用泼尼松60mg后3天,包括霍纳综合征在内的所有症状消失1)。两例均通过颞动脉活检确诊GCA,MRI/MRA未发现异常1)。
将1%盐酸阿普可乐定(Iopidine®)滴入双眼(超说明书使用)。
使用5%可卡因滴眼抑制去甲肾上腺素再摄取,判断散瞳情况。正常眼在90-120分钟后出现散瞳(++),而霍纳眼散瞳不良。
| 滴眼液 | 判定时间 | 正常 | 中枢性 | 节前性 | 节后性 |
|---|---|---|---|---|---|
| 5%可卡因 | 90~120分钟 | ++ | + | − | − |
| 5%酪胺 | 45分钟 | + | + | + | − |
| 1.25%肾上腺素 | 60分钟 | − | − | + | ++ |
酪胺能促使神经末梢释放去甲肾上腺素。节前病变时,神经末梢仍有去甲肾上腺素残留,因此瞳孔散大。节后病变时无残留,因此瞳孔不散大。
羟苯丙胺(1%)滴眼液也可用于鉴别节前和节后病变:节前病变表现为瞳孔散大(+),节后病变表现为瞳孔不散大(−)2)。
由于去神经超敏反应在发病后至少3天才能充分建立,因此在急性期(发病3天内)可能出现假阴性。急性期推荐使用可卡因滴眼试验,但在日本可卡因滴眼液可能难以获得。
根据病变部位进行相应的影像学检查。需要针对各病变部位进行相应的影像学检查,但优先进行胸部影像学检查以排除肺癌和纵隔肿瘤。
对于50岁及以上的新病例,测量ESR和CRP 1)。疑似GCA时,进行颞动脉活检 1)。
原发病的治疗是首要任务。如果没有其他全身性表现且判断为良性,则进行观察。
如果原发病得到治疗,恢复的可能性因损伤部位和原因而异。医源性(手术后)和特发性病例通常预后良好。颈动脉夹层经紧急治疗后症状可能改善。肿瘤性原因取决于肿瘤本身的预后。GCA病例有使用泼尼松后症状改善的报道,但部分病例霍纳综合征可能持续存在。
由于该通路较长,从脑干到肺尖和颈部的多种原因都可能涉及。
上眼睑的Müller肌(参与约2 mm的眼睑上提)和下眼睑的Müller肌受交感神经支配。去神经支配导致上睑下垂(约2 mm)和下眼睑上提(反向性上睑下垂),引起睑裂缩小和外观上的眼球内陷。
在节后性病变中,神经末梢释放去甲肾上腺素中断。这导致瞳孔开大肌的α1受体代偿性上调。即使微弱的α1作用(如阿可乐定的α1作用)也能引起瞳孔散大,这是药理学诊断的原理。这种超敏性的获得至少需要3天以上。
推测GCA的血管炎波及椎动脉穿通支,导致脑干血流减少,引起第一级神经元损伤1)。或者,颈内动脉血管壁的肉芽肿性炎症直接损伤交感神经丛,引起节后性损伤1)。文献综述中既有中枢性也有节后性的报道,损伤部位因病例而异1)。
GCA相关霍纳综合征的报道病例在文献中不足10例,十分罕见,其发病机制的细节尚未阐明1)。在既往报道的8例中,所有患者使用泼尼松60mg/天(约1mg/kg/天)后全身症状均得到改善。霍纳综合征的恢复因病例而异,有在治疗开始后3天完全消失的病例,也有残留症状的病例1)。中枢性病变(第一级神经元)很可能由脑干缺血引起,常合并滑车神经麻痹或skew deviation1)。许多病例在MRI/MRA上无法检测到异常,因此基于临床表现和炎症标志物的诊断被认为很重要1)。
Sverdlichenko I, Lam C, Donaldson L, Margolin E. Horner Syndrome in Giant Cell Arteritis: Case Series and Review of the Literature. J Neuroophthalmol.
Martin TJ. Horner syndrome: a clinical review. ACS Chem Neurosci. 2018;9:177-186.