รูม่านตา Adie
รอยโรค: ปมประสาทซิลิอารี (ส่วนปลาย)
ขนาดรูม่านตา: ขยายปานกลาง ไม่กลม
ข้างที่พบ: มักเป็นข้างเดียว (ประมาณ 80%)
ภาวะตึงตัว: มี (ม่านตาหดตัวนาน)
การตอบสนองต่อพิโลคาร์พีน: ม่านตาหดตัวที่ความเข้มข้นต่ำ

รูม่านตาตึงตัวของ Adie (Adie tonic pupil) เป็นโรคที่เกิดจากการสูญเสียเส้นประสาทพาราซิมพาเทติก ทำให้รีเฟล็กซ์แสงของรูม่านตาที่ได้รับผลกระทบหายไปหรือลดลง ในขณะที่รีเฟล็กซ์การมองใกล้ (ใกล้) แสดงการหดตัวของม่านตาที่ดีและแบบตึงตัว
ชื่อโรคมาจาก William John Adie และถูกรายงานอย่างอิสระเกือบพร้อมกันในปี 1931 โดย Adie, Morgan, Symons และ Holmes ความชุกคือ 2 ต่อ 1000 คน อัตราส่วนเพศ 2.6:1 (ประมาณ 70% เป็นหญิง) และอายุเริ่มต้นเฉลี่ย 32 ปี ประมาณ 80% เป็นข้างเดียว และการลุกลามเป็นสองข้างเกิดขึ้นในอัตรา 4% ต่อปี
กลุ่มอาการที่เกี่ยวข้อง ต่อไปนี้มีความสำคัญ:
ประมาณ 80% ของกรณีเป็นข้างเดียว อย่างไรก็ตาม การลุกลามเป็นสองข้างเกิดขึ้นในอัตรา 4% ต่อปี ดังนั้นในระหว่างการติดตามผล ควรสังเกตการเปลี่ยนแปลงของรูม่านตาข้างตรงข้ามด้วย
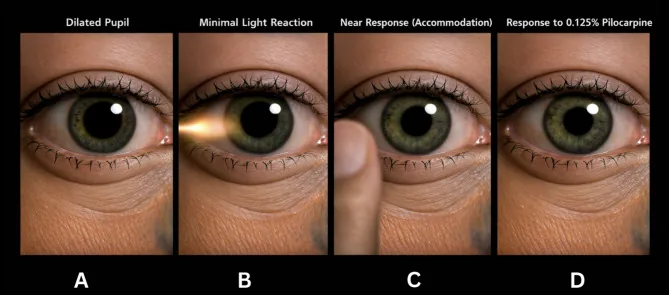
ในระยะแรก รูม่านตาของตาที่ได้รับผลกระทบขยายออกและความแตกต่างของขนาดรูม่านตากับข้างตรงข้ามชัดเจน แต่ในระยะเรื้อรัง รูม่านตาที่ได้รับผลกระทบมีแนวโน้มที่จะหดตัวในทางตรงกันข้าม เชื่อว่าเกิดจากเส้นใยประสาทพาราซิมพาเทติกจากซิลิอารีบอดีควบคุมกล้ามเนื้อหูรูดของรูม่านตาเนื่องจากการสร้างใหม่ผิดปกติ
ส่วนใหญ่เป็น ไม่ทราบสาเหตุ และรอยโรคที่รับผิดชอบคือปมประสาทซิลิอารีส่วนปลายและเส้นประสาทซิลิอารีสั้นส่วนหลัง
สาเหตุที่ระบุได้รวมถึง:
เกี่ยวกับสาเหตุของกลุ่มอาการรอสส์ มีการเสนอทฤษฎีว่าปัจจัยทางพันธุกรรมร่วมกับปัจจัยสิ่งแวดล้อม (เช่น การติดเชื้อไวรัส) มีส่วนเกี่ยวข้อง มีรายงานกลุ่มอาการรอสส์ในฝาแฝดเหมือนกันและกรณีที่เกิดหลังการติดเชื้อไซโตเมกาโลไวรัส ซึ่งบ่งชี้ว่าปัจจัยทางพันธุกรรมและการติดเชื้ออาจเกี่ยวข้อง 3)
เกี่ยวกับรูม่านตาตึงตัวหลังการติดเชื้อโควิด-19 ตั้งแต่การระบาดของโควิด-19 มีรายงานหลายกรณีที่เกิดจากกลไกทางภูมิคุ้มกัน และได้รับการยอมรับว่าเป็นภาวะแทรกซ้อนทางประสาทจักษุวิทยาหลังการติดเชื้อ 1, 2)
หากมีอาการทั่วไป (อัมพาตแบบปล้อง, การเคลื่อนไหวแบบหนอน, การแยกของรีเฟล็กซ์แสงและการปรับระยะใกล้) การวินิจฉัยทำได้ง่าย
การทดสอบหยด pilocarpine ความเข้มข้นต่ำ เป็นวิธีที่ใช้กันอย่างแพร่หลายที่สุด
จำเป็นต้องแยกโรคที่มีการแยกของรีเฟล็กซ์แสงและการปรับระยะใกล้
รูม่านตา Adie
รอยโรค: ปมประสาทซิลิอารี (ส่วนปลาย)
ขนาดรูม่านตา: ขยายปานกลาง ไม่กลม
ข้างที่พบ: มักเป็นข้างเดียว (ประมาณ 80%)
ภาวะตึงตัว: มี (ม่านตาหดตัวนาน)
การตอบสนองต่อพิโลคาร์พีน: ม่านตาหดตัวที่ความเข้มข้นต่ำ
ม่านตาอาร์ไกลล์ โรเบิร์ตสัน
รอยโรค: บริเวณพรีเทกตัลของสมองส่วนกลาง (ซิฟิลิส)
ขนาดม่านตา: ม่านตาหดตัวรุนแรงทั้งสองข้าง
ข้างที่พบ: ทั้งสองข้าง
ภาวะตึงตัว: ไม่มี
การตอบสนองต่อพิโลคาร์พีน: ไม่ตอบสนองที่ความเข้มข้นต่ำ
ม่านตาเทกตัล
รอยโรค: ด้านหลังของสมองส่วนกลาง (เนื้องอกไพเนียล ฯลฯ)
ขนาดม่านตา: ม่านตาขยายปานกลาง
ข้างที่พบ: ทั้งสองข้าง
กลุ่มอาการพาริโนด์: มักพบร่วม
ภาวะตึงตัว: ไม่มี
การวินิจฉัยแยกโรคอื่นๆ ได้แก่: การสร้างเส้นประสาทใหม่ผิดปกติหลังอัมพาตเส้นประสาทกล้ามเนื้อตา, การบาดเจ็บหรือเนื้องอกในเบ้าตา, การติดเชื้อวาริเซลลาซอสเตอร์, กลุ่มอาการฟิชเชอร์, โรคชาร์โก-มารี-ทูธ, ซาร์คอยโดซิสทางระบบประสาท
การตรวจซีรั่มซิฟิลิส (RPR) และการตรวจสอบประวัติโรคเบาหวาน การบาดเจ็บ หรือโรคทางระบบประสาทช่วยในการวินิจฉัย หากสงสัยกลุ่มอาการรอสส์ ให้ใช้การทดสอบไมเนอร์ (การทดสอบไอโอดีน-แป้ง) เพื่อตรวจหาบริเวณที่ไม่มีการขับเหงื่อ 3)
ไม่สามารถตัดออกได้ ในระยะเฉียบพลัน ภาวะไวเกินจากการเสียเส้นประสาทยังไม่เกิดขึ้น ดังนั้นผลอาจเป็นลบ หากอาการทางคลินิก (การเคลื่อนไหวแบบหนอน, อัมพาตแบบปล้อง) มีลักษณะเฉพาะ ก็สามารถวินิจฉัยรูม่านตาเอดี้อาทางคลินิกได้แม้การทดสอบจะให้ผลลบ การตรวจซ้ำเป็นระยะก็มีประโยชน์
รูม่านตาเอดีโอเป็นโรคที่มีแนวทางไม่ร้ายแรง สำหรับผู้ป่วยส่วนใหญ่ การอธิบายว่าเป็นโรคไม่ร้ายแรงและการติดตามผลเป็นแนวทางพื้นฐาน
เกี่ยวกับแนวทาง: อัมพาตของการปรับตาอาจดีขึ้นภายในไม่กี่เดือนถึงหลายปี ในทางกลับกัน ปฏิกิริยารูม่านตาต่อแสงมักไม่ฟื้นตัว การพยากรณ์โรคในกรณีที่มีโรคทางระบบไม่จำเป็นต้องดี และการจัดการโรคปฐมภูมิมีความสำคัญ
การรักษาภาวะเหงื่อออกมากชดเชยในกลุ่มอาการรอสส์: ใช้ไกลโคไพร์โรเลตทาเฉพาะที่ ครีมอะลูมิเนียมคลอไรด์ และการฉีดโบทูลินัมทอกซิน ในกรณีรุนแรงที่ต้องการผ่าตัด การตัดเส้นประสาทซิมพาเทติกบริเวณทรวงอกก็เป็นทางเลือกหนึ่ง 3)
ตามัวและมองใกล้ลำบากจากอัมพาตของการปรับตาอาจดีขึ้นภายในไม่กี่เดือนถึงหลายปี อย่างไรก็ตาม ปฏิกิริยารูม่านตาต่อแสงมักไม่ฟื้นตัว ดังนั้นจึงไม่สามารถคาดหวังการกลับมาเป็นปกติของการตอบสนองของรูม่านตาต่อแสง มักไม่ทำให้เกิดความบกพร่องทางการมองเห็นอย่างรุนแรง และเป็นโรคไม่ร้ายแรงที่สามารถติดตามผลได้อย่างปลอดภัย
กลไกหลักสองประการมีบทบาทสำคัญในการเกิดรูม่านตา Adie: “ภาวะไวเกินหลังเสียประสาท” และ “การงอกใหม่ผิดปกติ”
พื้นฐานทางกายวิภาคของระบบประสาทพาราซิมพาเทติก: เส้นใยประสาทพาราซิมพาเทติก 95% จากนิวเคลียส Edinger-Westphal (EW) ของเส้นประสาทกล้ามเนื้อตาไปยังกล้ามเนื้อซิลิอารี (เกี่ยวข้องกับการปรับตา) และ 5% ไปยังกล้ามเนื้อหูรูดม่านตา (เกี่ยวข้องกับรีเฟล็กซ์แสง) อัตราส่วนของเซลล์ประสาทที่เกี่ยวข้องกับรีเฟล็กซ์แสงและการปรับตาที่ปมประสาทซิลิอารีคือ 3:97 ซึ่งเป็นลักษณะเฉพาะที่เส้นใยรีเฟล็กซ์แสงมีจำนวนน้อยตั้งแต่แรก
การดำเนินของโรค ดำเนินไปตามลำดับดังนี้:
คำอธิบายทางประสาทกายวิภาคของการแยกตัวของรีเฟล็กซ์แสงและการปรับตา: เส้นใยเหนือนิวเคลียสไปยังนิวเคลียส EW สำหรับรีเฟล็กซ์การปรับตาจะวิ่งอยู่ทางด้านท้องมากกว่าเส้นใยนำเข้าของรีเฟล็กซ์แสงที่ผ่านบริเวณพรีเทกตัลของสมองส่วนกลางและคอมมิสชัวร์หลัง ดังนั้น รอยโรคที่บริเวณพรีเทกตัล (ส่วนกลาง) ก็สามารถทำให้เกิดการแยกตัวที่คล้ายกันได้ แต่ในรูม่านตา Adie รอยโรคอยู่ที่ปมประสาทซิลิอารี (ส่วนปลาย) ซึ่งเป็นจุดสำคัญในการแยกความแตกต่าง
กลไกที่เกี่ยวข้องกับ COVID-19: ในรูม่านตาตึงตัวหลังการติดเชื้อ SARS-CoV-2 มีการเสนอสามกลไก: การบุกรุกเส้นประสาทโดยตรงของไวรัส ความผิดปกติของเยื่อบุผนังหลอดเลือด และความเป็นพิษต่อระบบประสาทจากการอักเสบมากเกินไปและการปล่อยไซโตไคน์1)
พยาธิสรีรวิทยาของกลุ่มอาการ Ross: เชื่อกันว่าเซลล์ประสาทปมประสาทรากหลังและระบบประสาทพาราซิมพาเทติกมีต้นกำเนิดร่วมกันจากเซลล์คริสตาประสาท ซึ่งอธิบายการสูญเสียรีเฟล็กซ์เอ็นในกลุ่มอาการ Ross3)
นับตั้งแต่การระบาดของโควิด-19 มีรายงานผู้ป่วยรูม่านตาหดเกร็ง (tonic pupil) ซึ่งเป็นภาวะแทรกซ้อนทางจักษุประสาทหลังการติดเชื้อเพิ่มขึ้นอย่างต่อเนื่อง
Quijano-Nieto และคณะ (2021) รายงานผู้ป่วยหญิงอายุ 36 ปี ที่มีรูม่านตาหดเกร็งทั้งสองข้าง 17 วันหลังติดเชื้อโควิด-19 (PCR positive)1) ผล MRI สมอง การตรวจเลือด และน้ำไขสันหลังปกติทั้งหมด การหดตัวของรูม่านตาอย่างรุนแรงในทั้งสองข้างได้รับการยืนยันด้วยยาหยด pilocarpine 0.125% สันนิษฐานว่ากลไกที่เกิดจากภูมิคุ้มกันเป็นสาเหตุ
Gopal และคณะ (2021) รายงานผู้ป่วยหญิงอายุ 37 ปี ที่มีรูม่านตาหดเกร็งที่ตาขวา 3 สัปดาห์หลังติดเชื้อโควิด-192) รูม่านตาขวาขนาด 5.5 มม. พบการเคลื่อนไหวแบบตัวหนอนและการหดตัวแบบเป็นปล้อง การหดตัวของรูม่านตาได้รับการยืนยันด้วยยาหยด pilocarpine 0.1% MRI สมองและเบ้าตาไม่พบสิ่งผิดปกติที่สำคัญ และคาดว่าการตอบสนองทางภูมิคุ้มกันหลังการติดเชื้อเป็นสาเหตุ
Ahmad และคณะ (2022) รายงานผู้ป่วย Ross syndrome 2 รายที่ได้รับการวินิจฉัยในสถานพยาบาลเดียวกันภายในหนึ่งเดือน3) รายที่ 1 (หญิงอายุ 24 ปี) แสดงสามอาการ: รูม่านตาหดเกร็งซ้าย, หมดรีเฟล็กซ์เอ็นร้อยหวายขวา, และเหงื่อออกน้อยแบบเป็นปล้องจนถึงระดับ T4 รายที่ 2 (หญิงอายุ 42 ปี) เป็น “Ross syndrome plus” โดยมีรูม่านตาหดเกร็งทั้งสองข้าง, หมดรีเฟล็กซ์ขาส่วนล่าง, และร่วมกับ Horner syndrome
Ross syndrome ถูกเสนอว่าเป็น synucleinopathy เช่นเดียวกับโรคพาร์กินสัน, ภาวะสมองเสื่อมจาก Lewy body, และ multiple system atrophy3) นอกจากนี้ยังมีข้อเสนอว่า Ross syndrome, Holmes-Adie syndrome, และ Harlequin syndrome อาจเป็นฟีโนไทป์ที่แตกต่างกันของกระบวนการโรคเดียวกัน ซึ่งคาดว่าจะมีการรวมแนวคิดโรคในอนาคต
Quijano-Nieto BA, Córdoba-Ortega CM. Tonic pupil after COVID-19 infection. Arch Soc Esp Oftalmol. 2021;96(7):353-355.
Gopal M, Ambika S, Padmalakshmi K. Tonic Pupil Following COVID-19. J Neuroophthalmol. 2021;41:e764-e766.
Ahmad R, Saurabh K. Two Cases of Tonic Pupil: Ross and Ross Syndrome Plus. Cureus. 2022;14(2):e22305.