后弹力层膨出是由于角膜基质 缺损 导致完整的后弹力层向前膨隆,是穿孔的前兆。
角膜 穿孔是超过后弹力层的全层缺损 ,导致房水 渗漏和前房 消失,是一种眼科急症 。病因多样,包括感染性(细菌、真菌、病毒)、炎症性(类风湿关节炎、蚕蚀性角膜溃疡 )和外伤等。
诊断中Seidel试验(荧光素 确认房水 渗漏)很有用。
根据穿孔大小逐步选择治疗:组织粘合剂(<3mm)、羊膜移植、全层角膜移植 (>3mm)。
据报道,组织粘合剂(氰基丙烯酸酯)的成功率为86%,羊膜移植的成功率为70-90%。
后弹力层膨出是指通过角膜基质 和上皮层的缺损 ,完整的后弹力层(DM)呈疝状向前膨隆的状态1) 。DM是一种透明、有弹性、无细胞的膜,厚8-10μm,由内皮细胞分泌1) 。它对蛋白水解和生物力学应力相对有抵抗力,在基质破坏过程中保护内皮1) 。
后弹力层膨出按位置分类如下1) :
中央型 :距角膜 中心5mm以内旁中央型 :5-8mm周边型 :8mm以上(包括角膜缘 )
按大小分类根据最大直径:小(<3mm)、中(3-6mm)、大(>6mm)1) 。
当角膜溃疡 深入基质层并超过后弹力层(DM)时,会导致角膜 穿孔。房水 漏出,前房 消失。原因包括感染性、非感染性和外伤性因素。
根据穿孔创口的大小、位置、发生时间以及角膜 状况,选择保守治疗或手术治疗。
Q
后弹力层膨出和角膜穿孔有什么区别?
A
后弹力层膨出是后弹力层保持完整但向前膨出的状态,相当于穿孔的“前一步”。角膜 穿孔是后弹力层也破裂,房水 漏出的状态。后弹力层膨出穿孔风险高,需要紧急干预。
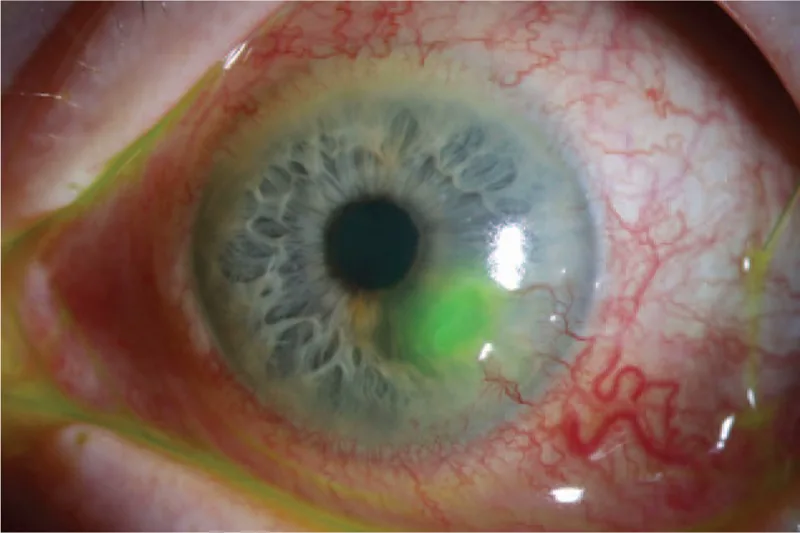
后弹力层膨出和角膜穿孔的管理图片 Tobias Röck, Karl Ulrich Bartz-Schmidt, Daniel Röck Management of a neurotrophic deep corneal ulcer with amniotic membrane transplantation in a patient with functional monocular vision: A case report 2017 Dec 15 Medicine (Baltimore). 2017 Dec 15; 96(50):e8997 Figure 1. PM
CI D: PMC5815707. License: CC BY.
荧光素染色 显示荧光
角膜溃疡 ,伴有
角膜 周边
新生血管 和
结膜 充血 的临床照片
急剧视力 下降 :伴随穿孔或后弹力层膨出形成而发生眼痛 过度流泪 :可能伴随房水 漏出
后弹力层膨出
后弹力层皱襞 :在溃疡底部可见DM皱襞。
中央透明区 :变薄区域的中央存在透明区域。
前凸 :后弹力层可能呈囊样突出1) 。
角膜穿孔
葡萄膜脱出 :虹膜 嵌顿于缺损 处。
Seidel试验阳性 :观察到荧光素 的稀释和流出。
浅前房 或前房 消失房水 渗漏,前房 消失。
葡萄膜脱出或Seidel试验阳性是角膜 穿孔的确诊依据。但如果葡萄膜脱出堵塞了缺损 ,Seidel试验可能呈假阴性。
诊断延迟可能导致角膜 损伤扩大、眼内炎 、继发性青光眼 或白内障 ,甚至眼球丧失。
角膜溃疡 大致分为中央部和周边部。中央部溃疡多为感染性,周边部溃疡多为非感染性。
分类 主要致病微生物 细菌性 铜绿假单胞菌、葡萄球菌、肺炎链球菌、莫拉菌、淋病奈瑟菌 真菌性 镰刀菌、曲霉菌、念珠菌 病毒性 单纯疱疹、带状疱疹
佩戴隐形眼镜(CL)是美国微生物性角膜 炎的最大风险因素7) 。过夜佩戴(包括角膜 塑形镜)是主要的感染风险7) 。CL佩戴者中革兰氏阴性菌(铜绿假单胞菌、莫拉菌、沙雷菌)常见。
铜绿假单胞菌角膜炎 角膜 溶解。
真菌性角膜炎 前房积脓 和角膜内皮 斑6) 。感染扩散后,最终可能导致严重溶解和穿孔6) 。
淋球菌 引起的结膜炎 并发角膜 炎时,角膜 穿孔发生率很高,需注意5) 。
这是诊断角膜 穿孔必不可少的检查。用少量无菌生理盐水浸湿的无菌荧光素 试纸涂抹于可疑穿孔部位,在钴蓝光下观察。如果荧光素 被稀释并流出,则判定为阳性。
对眼球施加压力有扩大穿孔的风险,因此检查时应尽量减少压力。
该检查有助于详细评估角膜 结构1) 。即使临床观察因坏死物质或黏液性分泌物受阻,它也能显示基质的真实厚度和DM膨隆1) 。连续扫描可监测愈合过程。
如果病因是感染性角膜 炎,必须进行病灶刮片的涂片镜检和分离培养。理想情况下,应在使用抗菌药物前采集标本。
涂片镜检 :通过革兰染色评估细菌的形态和染色特性6) 分离培养 :接种于血琼脂平板、巧克力琼脂平板和沙氏琼脂平板(用于真菌)6) 真菌培养 :需在37℃和室温两种条件下培养至少2周6) 真菌荧光Y染色 :对真菌的特异性染色有用
Q
什么是Seidel试验?
A
这是一种使用荧光素 染料检查角膜 房水 渗漏的检查。荧光素 被房水 稀释后流出的现象(阳性结果)可在钴蓝光下观察到。这是角膜 穿孔确诊最重要的检查之一。
治疗方法的选择基于穿孔的大小、范围、部位、实质浸润程度、视力 预后和基础疾病。在许多情况下,多种治疗同时或分阶段进行。
绷带式角膜 接触镜(BCL) :对非感染性即将穿孔或没有葡萄膜脱出的小穿孔有用房水 生成抑制剂低眼压 ,减少缺损 处的流出频繁润滑滴眼液、泪点栓塞、眼睑缝合术 :促进泪液分泌减少型干眼相关溃疡的再上皮化抗胶原酶药物 :全身性四环素类药物通过抑制黏膜类天疱疮来抑制胶原降解维生素C :刺激胶原蛋白生成,对碱性损伤 尤其有用PROSE(巩膜 镜) :在高手术风险病例中,巩膜 镜的非手术管理是一种选择4)
Tseng等人(2024)报道,对继发于眼GVHD的后弹力层膨出使用PROSE疗法成功进行了7年的非手术管理,维持矫正视力 20/504) 。oGVHD 相关的角膜 穿孔发生率估计为1-4%4) 。
如果感染性角膜溃疡 是原因,则基础疾病的感染控制是首要任务。
细菌性 :以氟喹诺酮类滴眼液(如左氧氟沙星、莫西沙星)为基础,重症病例可联用万古霉素+头孢他啶6) 7) 真菌性 :丝状真菌首选匹马霉素(5%滴眼液、1%眼膏)6) 。对于镰刀菌属以外的丝状真菌,推荐使用伏立康唑1%滴眼液6) 。重症病例可联合结膜 下注射或基质内注射6) 淋菌性 :CDC推荐首选头孢曲松1g单次肌内注射5)
Che Ku Amran等人(2024)报道,使用氰基丙烯酸酯粘合剂+BCL+头孢曲松1g肌内注射处理淋菌性角结膜炎 导致的角膜 穿孔,2个月后感染得到控制5) 。
穿孔大小 推荐治疗 <3mm 组织粘合剂或AMT >3mm PKP 或补片移植全角膜 角膜 巩膜 移植1)
氰基丙烯酸酯粘合剂 :适用于<3mm的穿孔。具有抑菌作用,持续时间比纤维蛋白胶长。被认为能抑制多形核白细胞和胶原酶的产生,从而停止角膜 融解过程。对于<3mm穿孔的成功率为86%。羊膜移植(AMT) :用于即将穿孔或<3mm的穿孔。促进上皮愈合、减轻炎症和瘢痕形成。成功率为70-90%,平均上皮愈合时间为3-4周。全层角膜移植术 (PKP ) :适用于>3mm的穿孔、伴有虹膜 脱出的前房 消失、以及其他治疗失败的病例。90%的眼可改善视力 。排斥率约为20%。
Kusano等人(2023)报告了一例严重微生物性角膜 炎导致整个角膜 形成后弹力层膨出(全角膜后弹力层 膨出)的病例1) 。前段OCT 确认角膜 厚度为37μm,实施了角膜 巩膜 移植术,成功保留了眼球1) 。这被认为是报道中最大的后弹力层膨出1) 。
Tenon囊补片移植 :据报道可用于最大6mm的角膜 穿孔3)
Shekhawat等人(2022)报告了一种使用Tenon囊补片移植联合血管化结膜 瓣治疗旁中心角膜 穿孔(1mm)的技术3) 。术后4个月,裸眼视力 达到20/25,散光 最小3) 。Tenon囊成纤维细胞引起的旺盛伤口愈合反应以及结膜 瓣的血液供应促进了愈合3) 。该手术即使在角膜 供体组织获取受限的环境中也可实施3) 。
单针微型角膜移植术 :对于约1mm的小穿孔,使用单针缝合植入角膜 补片的技术2)
Kato等人(2021)报告了对金属异物引起的旁中心角膜 穿孔(1mm)实施单针微型角膜移植术 的良好结果,术后矫正视力 达到180/200,角膜 散光 0.6屈光 度2) 。17个月后再次穿孔时也采用相同技术处理,维持了2年以上的良好视功能2) 。
结膜 瓣结膜 瓣如Gundersen瓣适用于视力 预后不良的眼。结膜 切除术角膜溃疡 。
Q
应该选择粘合剂还是手术?
A
对于小于3mm、远离角膜缘 且前房 存在的穿孔,氰基丙烯酸酯粘合剂可作为首选。粘合剂也可作为穿透性角膜移植术 (PKP )前的临时措施。对于大于3mm的穿孔或前房 消失的情况,粘合剂难以处理,应选择PKP 。治疗方案根据穿孔的大小、部位和基础疾病个体化决定。
Q
角膜穿孔需要紧急手术吗?
A
角膜 穿孔是眼科急症 。如果置之不理,可能导致眼内炎 、继发性青光眼 、白内障 和失明。但并非所有病例都需要紧急手术。小穿孔可通过绷带型角膜 接触镜或粘合剂处理,感染性穿孔可先进行24-48小时抗菌治疗,再计划穿透性角膜移植术 (PKP )。
角膜溃疡 始于上皮缺损 ,并向基质层进展。当角膜基质 溶解深入并暴露后弹力层(DM)时,形成后弹力层膨出,DM进一步破裂则导致穿孔。
在铜绿假单胞菌引起的实验性角膜 炎中,后弹力层膨出的形成与碱性蛋白酶、总蛋白酶和弹性蛋白酶活性直接相关1) 。高产蛋白酶菌株(102、115、118株)在Ca²⁺和Mg²⁺存在下,即使少量炎症细胞也能诱导基质的大规模破坏、后弹力层膨出形成和穿孔1) 。白细胞蛋白酶也参与角膜 变性,但仅其存在并不一定导致后弹力层膨出1) 。
DM具有抵抗蛋白水解和生物力学应力的能力,因此即使周围基质溶解,也能在一定时间内保持完整1) 。这一特性产生了“穿孔前阶段”——后弹力层膨出。然而,由于缺乏足够的抗张强度,DM最终向前疝出1) 。
丝状真菌不仅停留在角膜 表层,还容易向深层进展6) 。当菌丝突破DM到达角膜 后表面时,形成角膜 后斑块(内皮斑)6) 。进展时,严重溶解导致穿孔。
淋病奈瑟菌(Neisseria gonorrhoeae)通过菌毛粘附并侵入角膜上皮 5) 。接种后1小时内,被摄入上皮细胞的空泡内,24小时后上皮厚度显著减少5) 。这一过程经过上皮性、基质性和溃疡性角膜 炎,最终导致穿孔5) 。
已有报道将Tenon囊补片移植与带血管蒂结膜 瓣相结合的技术3) 。结膜 瓣的血管供应使得愈合速度比传统的Tenon囊补片移植更快(6周时角膜基质 厚度完全恢复)3) 。预计在无法获得角膜 供体组织的低资源环境中具有应用价值3) 。
One-bite mini-keratoplasty是一种针对约1mm小穿孔的简便技术,通过单根10-0尼龙缝线植入角膜移植 物2) 。据报道,与传统板层角膜移植 相比,其引起的散光 更少2) 。
PROSE(人工替代眼表生态系统)疗法作为手术高风险患者中后弹力层膨出的长期管理选择而受到关注4) 。其设计跨越角膜 穹窿,保护角膜 并提供持续的润滑和氧气供应4) 。在角膜扩张症 中,有报道称PROSE组在平均视力 和视力 恢复速度方面优于角膜移植 组4) 。
Kusano M, Mohamed YH, Uematsu M, et al. Whole Corneal Descemetocele. Medicina. 2023;59:1780.
Kato Y, Nagasato D, Nakakura S, et al. A Case of Paracentral Corneal Perforation Treated with One-Bite Mini-Keratoplasty. Turk J Ophthalmol. 2021;51:55-57.
Shekhawat NS, Kaur B, Edalati A, et al. Tenon patch graft with vascularized conjunctival flap for management of corneal perforation. Cornea. 2022;41:1465-1470.
Tseng AM, Heur M, Chiu GB. Sustained descemetocele management with Prosthetic Replacement of the Ocular Surface Ecosystem (PROSE) treatment. Am J Ophthalmol Case Rep. 2024;36:102092.
Che Ku Amran CKH, Ngoo QZ, Awis Qarni F. A Rare Case of Corneal Perforation Secondary to Gonococcal Keratoconjunctivitis. Cureus. 2024;16(11):e74312.
感染性角膜 炎診療ガイドライン(第3版)作成委員会. 感染性角膜 炎診療ガイドライン(第3版). 日眼会誌. 2024.
American Academy of Ophthalmology Cornea/External Disease Preferred Practice Pattern Panel. Bacterial Keratitis Preferred Practice Pattern. Ophthalmology. 2024.
复制全文后,可以粘贴到你常用的 AI 助手中提问。
打开下面的 AI 助手,并把复制的内容粘贴到聊天框。