穿透性角膜移植术(PKP)
排斥反应率:约4.9~28.9%7)
失败主要原因:排斥反应(早期)+ 内皮功能衰竭(晚期)3)
特点:包含全层供体组织,抗原性最高

角膜移植是成功率最高的器官移植之一。低风险眼的首次穿透性角膜移植术(PKP)5年存活率达95%。这一高成功率得益于角膜的免疫特权。
构成角膜免疫特权的因素如下:
然而,在伴有角膜新生血管的高风险眼中,3年时的失败率可能超过35%。即使在免疫特权下,移植失败的最常见原因也是不可逆的免疫排斥反应1)。
“移植排斥反应”是指宿主对供体角膜的特异性免疫反应。原发性移植失败(primary graft failure)是由于供体组织本身的缺陷、手术创伤或保存不当导致术后8周内未能透明化,并非免疫介导的3)。PKP中约0.1%发生此情况。
排斥反应的诊断仅针对术后至少维持透明2周的移植片。半数以上病例集中在术后1年内,尤其在术后6个月至1年期间达到高峰。但术后20年以上也可能发生。据报道,从排斥反应进展为失败的比例约为49%。
角膜移植是全球最常实施的组织移植,2012年的国际调查显示PKP约占角膜移植总数的70%1)。近年来,针对内皮疾病的DSAEK和DMEK迅速普及,针对圆锥角膜和角膜炎后瘢痕的DALK也成为标准选择,手术方式的构成比发生了显著变化。然而,PKP对于广泛的角膜混浊和畸形仍然不可或缺,并且是排斥反应风险最高的术式1)。
穿透性角膜移植术(PKP)
排斥反应率:约4.9~28.9%7)
失败主要原因:排斥反应(早期)+ 内皮功能衰竭(晚期)3)
特点:包含全层供体组织,抗原性最高
深板层角膜移植术(DALK)
排斥反应率:1~24%4)
优点:消除内皮排斥反应的风险
挑战:仍可能发生基质排斥反应4)
角膜内皮移植术(DSAEK)
Descemet膜内皮角膜移植术(DMEK)
排斥反应率:平均1.9%(范围0~5.9%)7)
原发性失败率:1.7%
特点:抗原性最低,排斥率低3)
大规模队列研究表明,DMEK的排斥反应风险显著低于PKP和DSAEK3)。比较UT-DSAEK和DMEK的荟萃分析显示,术后12个月的排斥反应风险无显著差异2)。一项针对54只眼睛的荷兰多中心随机对照试验显示,DMEK组术后12个月达到20/25或以上视力的比例显著高于DSAEK组(66% vs 33%,P=0.02),而内皮细胞密度和屈光变化无显著差异11)。
半数以上发生在术后1年内,尤其是术后6个月至1年期间。但排斥反应也可能在长期后发生,因此术后多年出现充血、视物模糊、视力下降等症状时,需及时就医。有报告称术后20年以上因疫苗接种诱发排斥反应的病例10)。
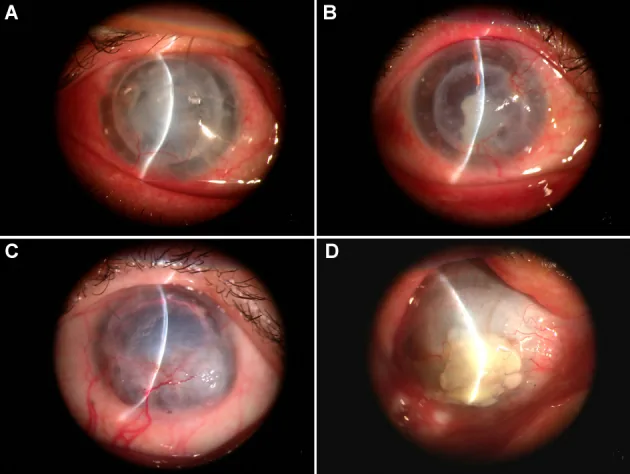
患者表现为视物模糊、充血、眼痛、异物感和视力下降。术后3个月和1年有两个发病高峰。出现自觉症状后需立即就医。
排斥反应的诊断标准包括以下任一表现:充血、畏光、视力下降、前房细胞、角膜后沉着物(KP)、内皮或上皮排斥线、上皮下浸润、局限性移植片水肿1)。
移植片局限性的KP具有特征性,受体角膜上不出现KP。Khodadoust线是线状的角膜后沉着物,代表内皮排斥反应的前进前沿。
排斥反应根据受累层次分为上皮型、实质型和内皮型三种。内皮型对移植片预后影响最大,治疗延迟会导致不可逆的内皮功能衰竭和视力下降。
| 排斥反应类型 | 频率 | 主要表现 |
|---|---|---|
| 上皮型 | 约2% | 从角膜缘移行的线状隆起(上皮排斥线) |
| 实质型 | — | 实质水肿是唯一表现 |
| 内皮型 | 约50% | KP、Khodadoust线、水肿 |
上皮型排斥反应(epithelial rejection)发生率低,约占所有排斥反应的2%。前驱病变为Bowman膜下0.2~0.5mm的圆形上皮下浸润。进展时形成水肿性隆起的线状病变(上皮排斥线)。对移植片的透明愈合本身影响很小,但可能诱发内皮型排斥反应。
实质型排斥反应(stromal rejection)的唯一表现是实质水肿。在DALK中,实质免疫排斥反应可表现为实质浸润和界面新生血管4)。与PKP眼中内皮型排斥反应引起的角膜水肿难以鉴别。
内皮型排斥反应(endothelial rejection)约占所有排斥反应的50%,临床最重要。移植片内局限的角膜后沉着物是重要表现,形成Khodadoust线时伴有同部位实质水肿。混合型(上皮型+内皮型等)约占30%。
Khodadoust线是内皮型排斥反应特征性的线状角膜后沉着物。代表排斥反应进行前沿在移植片内皮面上渐进移动,线经过的区域内皮细胞受损,导致该部位实质水肿。发现Khodadoust线时需立即开始强效类固醇治疗。
| 所见 | 排斥反应 | HSV/VZV内皮炎 | CMV内皮炎 |
|---|---|---|---|
| KP的分布 | 局限于移植片内 | 移植片外也有附着 | 移植片外也有附着 |
| KP的色调 | 白色至灰白色 | 褐色 | 褐色至白色 |
| 特征性所见 | Khodadoust线 | Arlt三角 | 硬币样病变 |
排斥反应的最大特征是局限于移植片内的KP,而病毒性内皮炎在移植片外也可见KP,以此进行鉴别。此外,角膜后沉着物有时在角膜移植时来自供体,因此在日常检查中记录KP的分布对鉴别有用。
PKP容易发生排斥反应的病例称为高风险眼,包括以下因素。
在DMEK中,类固醇减量时可能诱发排斥反应。有病例在DMEK术后15个月从倍他米松换用氟米龙时发生排斥反应7)。周边虹膜前粘连(PAS)也被报道为DMEK排斥的风险因素7)。
虽然HLA配型在器官移植中的益处明确,但在角膜移植中结果不一致1)。英国进行的**角膜移植随访研究II(CTFS II)**是一项前瞻性大型临床试验,旨在评估高风险PKP中HLA II类(HLA-DR)配型的影响1)。从1998年至2011年,共纳入1133例移植,在HLA I类错配≤2个抗原的条件下,按HLA-DR错配0、1、2个进行分层1)。供体和受体的组织分型采用基于DNA的PCR-SSP/PCR-SSO方法,以避免血清学方法的误差1)。
在CTFS II中,HLA-DR错配数与排斥反应发生率之间未发现明确关系1)。正如啮齿动物模型所示,角膜移植排斥反应涉及多种不同的免疫途径,这种免疫应答的冗余性被认为是HLA配型研究结果不一致的部分原因1)。
已有多个关于COVID-19疫苗接种后角膜移植排斥反应的报道。mRNA疫苗(BNT162b2)、病毒载体疫苗(ChAdOx1)和灭活疫苗(国药)均可引发。
有报道称,两例患者在首次接种BNT162b2疫苗2周后出现PKP急性排斥反应6)。两者均无既往排斥反应史,并对局部和全身类固醇治疗反应良好6)。
还有一例在接种ChAdOx1疫苗2周后发生飞秒激光角膜移植内皮排斥反应的病例8)。观察到Khodadoust线和前房炎症,经类固醇治疗5周后恢复8)。
接种国药灭活疫苗后也报告了两例排斥反应9)。文献综述显示至少已积累20例以上疫苗相关排斥反应,大多数通过类固醇治疗恢复9)。
有一例术后20年以上的PKP在接种BNT162b2后10天发生排斥反应10)。
虽然因果关系尚未确定,但有假说认为疫苗接种可能通过诱导MHC II类抗原呈递细胞引发排斥反应9)。
COVID-19疫苗接种后的角膜移植排斥反应在mRNA、载体和灭活疫苗中均有报道。通常在接种后1-3周内发生,大多数对类固醇治疗有反应。荟萃分析已排除实体器官移植中疫苗引起的排斥反应,但角膜移植的病例正在积累中。由于因果关系未确定,建议角膜移植患者在接种前增加类固醇用量,并在接种后尽早就医。
检查移植物局部的KP、Khodadoust线、角膜水肿和前房细胞。上皮排斥线从充血的角膜缘血管附近开始,越过移植物边界移动。
需要与内皮型排斥反应鉴别的主要疾病如下。
排斥反应中KP局限于移植片内,眼压升高少见。HSV/VZV内皮炎中KP也附着于移植片外,并伴有急性眼压升高。CMV内皮炎的特征是硬币样KP和慢性持续性眼压升高。若难以确诊,需综合前房水PCR、血清抗体检查和对类固醇的治疗反应进行判断。
排斥反应的治疗以类固醇消炎为基础。
轻度(上皮型/实质型)
重度(内皮型,Khodadoust线阳性)
急性排斥反应若早期治疗,50%以上可恢复;但治疗延迟会导致不可逆的内皮细胞丢失,进而导致移植失败。患者教育很重要:应让患者了解术后自觉症状(充血、视物模糊、眼痛、畏光),并在出现异常时尽早就医。
角膜移植术后排斥反应的预防管理采用基于风险分层的两步方案。
常规风险眼的术后管理
类固醇滴眼液:Rinderon滴眼液0.01%(倍他米松)每日5次→切换为Flumetholon滴眼液0.1%(氟米龙)每日2-3次(半年内逐渐减量)
全身给药:泼尼松20 mg数日,或不给药
CsA:联合滴眼,持续数月
高危眼的术后管理
类固醇滴眼液:倍他米松0.1%×每日4次→持续1年以上
全身类固醇:Rinderon注射液0.4%每次2mg每日1次静脉滴注,从手术日起3天,之后Rinderon片0.5mg 2片分1次,2周内逐渐减量
CsA:新山地明胶囊25mg 3mg/kg/日,谷浓度70-100 ng/mL
**环孢素A(CsA)**用于2个象限以上角膜基质血管侵入、再次移植、有排斥反应史等高危病例。全身给药时维持谷浓度70-100 ng/mL,监测包括肾功能在内的全身副作用。术后持续约半年。
在一例18岁PKP患者出现双侧同时排斥反应时,经IV甲泼尼龙脉冲诱导缓解后,因出现类固醇反应,切换为CsA 1%滴眼液并成功维持5)。CsA 1%滴眼液可使类固醇反应者早期减量强效类固醇,有助于长期维持移植片5)。
他克莫司用于口服环孢素期间发生排斥反应的病例作为切换药物。术后2个月内目标谷浓度8-10 ng/mL,之后5-6 ng/mL(普乐可复0.05-0.1 mg/kg/日)。有报道称0.03%他克莫司滴眼液对预防高危角膜移植排斥反应有效。
缝线松动或断裂可诱发排斥反应和晚期感染,因此发现后应立即拆线。拆线后暂时加强类固醇和抗生素滴眼治疗。缓解后长期持续类固醇滴眼有望抑制复发3)。
从倍他米松0.1%开始,首先每日4次维持数月至1年,然后切换为氟米龙0.1%等低浓度类固醇,每日1-2次长期维持。若眼压升高,考虑更换为氯替泼诺或联合使用青光眼滴眼液。
如果因类固醇反应导致眼压升高,可考虑将醋酸泼尼松龙更换为对眼压影响较小的氯替泼诺,或联合使用CsA 1%滴眼液。CsA 1%滴眼液可早期减少类固醇用量,有助于兼顾眼压管理和抑制排斥反应。必要时也可联合使用青光眼滴眼液。
角膜通过前房相关免疫偏离(ACAID)维持生理性免疫耐受。在ACAID中,抗原呈递细胞在TGF-β主导的环境中成为耐受原性,抑制针对供体抗原的迟发型超敏反应和补体结合抗体产生。然而,当存在新生血管、炎症、缝线松动等高风险因素时,这种免疫特权容易遭到破坏。
排斥反应的核心机制是迟发型超敏反应,主要效应细胞是CD4+ Th1细胞。活化的Th1细胞产生IFN-γ,诱导移植角膜全层出现MHC II类抗原呈递细胞,从而推进细胞免疫反应8)。近年来,抗体介导机制的参与也受到关注,提示抗HLA抗体可能通过补体激活引起慢性内皮细胞损伤1)。
不同术式的排斥反应率差异主要源于移植的供体组织量和抗原性不同3)。
周边虹膜前粘连(PAS)被认为是DMEK术后排斥反应的危险因素。在小鼠角膜移植模型中,存在PAS的组排斥反应显著增加7)。PAS导致虹膜与供体内皮直接接触,可能诱导细胞毒性T淋巴细胞活性,从而促进排斥反应7)。
角膜移植排斥反应主要由细胞免疫介导,但啮齿类动物研究已确认存在多种不同的免疫途径导致排斥1)。这种免疫应答的冗余性被认为是HLA配型研究结果不一致的原因之一1)。近年来,抗HLA抗体和抗体介导的排斥反应的作用也受到关注,可能有助于阐明晚期内皮衰竭的机制1)。
COVID-19疫苗接种会引发全身性免疫反应,诱导产生SARS-CoV-2中和抗体以及抗原特异性CD8+和Th1型CD4+ T细胞应答6)。这种免疫增强可能通过交叉反应或非特异性免疫激活诱发移植角膜的排斥反应6)。对于灭活疫苗(国药),佐剂氢氧化铝的免疫原性被认为是排斥反应的可能主要原因9)。然而,在荟萃分析层面,尚未确认实体器官移植中COVID-19疫苗接种后排斥反应增加,角膜移植中的因果关系目前也尚未确定。
与COVID-19疫苗相关的角膜移植排斥反应病例报告在全球范围内不断积累9)。文献综述已收集20多例,显示大多数为再次移植病例,接种后1-2周发病,且大多数通过类固醇治疗恢复9)。有人提出接种前预防性使用类固醇,但尚无随机对照试验,需根据具体病例个体化判断8)9)。
关于HLA匹配的有效性,CTFS II试验进行了前瞻性研究,但目前尚未显示角膜移植中HLA-DR匹配的明确临床益处1)。然而,抗HLA抗体和抗体介导的排斥反应的作用正逐渐明确,可能有助于阐明晚期内皮衰竭的机制1)。
在UT-DSAEK与DMEK的比较中,Sela 2023荟萃分析2)和Dunker 2020多中心RCT11)均显示12个月排斥反应率无显著差异,而DMEK组可获得更好的矫正视力。但DMEK组移植失败率略高2),术式选择应综合考虑患者个体眼部病变、病史及机构经验。
以下方向备受关注。