การปลูกถ่ายกระจกตาทะลุทะลวง (PKP)
อัตราการปฏิเสธ: ประมาณ 4.9-28.9% 7)
สาเหตุหลักของความล้มเหลว: การปฏิเสธ (ระยะแรก) + ความล้มเหลวของเยื่อบุผนังกระจกตา (ระยะหลัง) 3)
ลักษณะ: มีเนื้อเยื่อผู้บริจาคเต็มความหนา ดังนั้นจึงมีแอนติเจนสูงที่สุด

การปลูกถ่ายกระจกตาเป็นการปลูกถ่ายอวัยวะที่มีอัตราความสำเร็จสูงที่สุดชนิดหนึ่ง ในการปลูกถ่ายกระจกตาแบบทะลุทะลวง (PKP) ครั้งแรกในตาที่มีความเสี่ยงต่ำ อัตราการรอดชีวิตที่ 5 ปีสูงถึง 95% ความสำเร็จสูงนี้ได้รับการสนับสนุนจากเอกสิทธิ์ทางภูมิคุ้มกันของกระจกตา
ปัจจัยที่ประกอบเป็นเอกสิทธิ์ทางภูมิคุ้มกันของกระจกตามีดังนี้:
อย่างไรก็ตาม ในดวงตาที่มีความเสี่ยงสูงซึ่งมีเส้นเลือด新生ที่กระจกตา อัตราความล้มเหลวที่ 3 ปีอาจเกิน 35% แม้ภายใต้สภาวะเอกสิทธิ์ทางภูมิคุ้มกัน สาเหตุที่พบบ่อยที่สุดของความล้มเหลวของการปลูกถ่ายคือการปฏิเสธทางภูมิคุ้มกันแบบไม่สามารถย้อนกลับได้ 1)
“การปฏิเสธการปลูกถ่าย” หมายถึงการตอบสนองทางภูมิคุ้มกันจำเพาะของโฮสต์ต่อกระจกตาผู้บริจาค ความล้มเหลวของการปลูกถ่ายปฐมภูมิคือภาวะที่กระจกตาไม่ใสภายใน 8 สัปดาห์หลังการผ่าตัดเนื่องจากความบกพร่องของเนื้อเยื่อผู้บริจาคเอง การบาดเจ็บจากการผ่าตัด หรือการเก็บรักษาที่ไม่เหมาะสม และไม่ได้เกิดจากภูมิคุ้มกัน 3) เกิดขึ้นในประมาณ 0.1% ของ PKP
การวินิจฉัยการปฏิเสธจะทำเฉพาะกับ graft ที่คงความใสไว้อย่างน้อย 2 สัปดาห์หลังการผ่าตัด มากกว่าครึ่งหนึ่งของกรณีการปฏิเสธเกิดขึ้นภายในปีแรกหลังการผ่าตัด โดยมีจุดสูงสุดระหว่าง 6 เดือนถึง 1 ปี อย่างไรก็ตาม การปฏิเสธอาจเกิดขึ้นหลังจาก 20 ปีหลังการผ่าตัด อัตราการดำเนินจากปฏิเสธไปสู่ความล้มเหลวรายงานประมาณ 49%
การปลูกถ่ายกระจกตาเป็นการปลูกถ่ายเนื้อเยื่อที่ทำบ่อยที่สุดในโลก และในการสำรวจระหว่างประเทศปี 2012 PKP คิดเป็นประมาณ 70% ของการปลูกถ่ายกระจกตาทั้งหมด 1) ในช่วงไม่กี่ปีที่ผ่านมา DSAEK และ DMEK สำหรับโรคเยื่อบุผนังกระจกตาได้แพร่กระจายอย่างรวดเร็ว และ DALK สำหรับโรคกระจกตารูปกรวยและแผลเป็นหลังเยื่อบุกระจกตาอักเสบได้กลายเป็นทางเลือกมาตรฐาน ดังนั้นสัดส่วนของเทคนิคการผ่าตัดจึงเปลี่ยนแปลงไปอย่างมาก อย่างไรก็ตาม PKP ยังคงจำเป็นสำหรับกระจกตาขุ่นกว้างและความผิดปกติ และมีความเสี่ยงต่อการปฏิเสธสูงที่สุด 1)
การปลูกถ่ายกระจกตาทะลุทะลวง (PKP)
อัตราการปฏิเสธ: ประมาณ 4.9-28.9% 7)
สาเหตุหลักของความล้มเหลว: การปฏิเสธ (ระยะแรก) + ความล้มเหลวของเยื่อบุผนังกระจกตา (ระยะหลัง) 3)
ลักษณะ: มีเนื้อเยื่อผู้บริจาคเต็มความหนา ดังนั้นจึงมีแอนติเจนสูงที่สุด
การปลูกถ่ายกระจกตาชั้นลึก (DALK)
อัตราการปฏิเสธ: 1-24% 4)
ข้อดี: ขจัดความเสี่ยงของการปฏิเสธเยื่อบุผนังกระจกตา
ความท้าทาย: การปฏิเสธชั้นสโตรมายังสามารถเกิดขึ้นได้ 4)
การปลูกถ่ายเยื่อบุผนังกระจกตา (DSAEK)
อัตราการปฏิเสธ: เฉลี่ย 10% (ช่วง 0-45%)
อัตราความล้มเหลวปฐมภูมิ: เฉลี่ย 5% (ช่วง 0-29%)
ลักษณะเฉพาะ: ไม่มีความแตกต่างอย่างมีนัยสำคัญเมื่อเทียบกับ PKP ตามรายงาน3)
การปลูกถ่ายเยื่อหุ้มเดสเซเม็ทและเซลล์บุผนังกระจกตา (DMEK)
อัตราการปฏิเสธ: เฉลี่ย 1.9% (ช่วง 0-5.9%)7)
อัตราความล้มเหลวปฐมภูมิ: 1.7%
ลักษณะเฉพาะ: มีแอนติเจนต่ำที่สุดและอัตราการปฏิเสธต่ำที่สุด3)
DMEK ได้รับการพิสูจน์แล้วว่ามีความเสี่ยงต่อการปฏิเสธต่ำกว่า PKP และ DSAEK อย่างมีนัยสำคัญในการศึกษาแบบกลุ่มใหญ่3) ในการวิเคราะห์อภิมานเปรียบเทียบระหว่าง UT-DSAEK และ DMEK ไม่มีความแตกต่างอย่างมีนัยสำคัญในความเสี่ยงต่อการปฏิเสธที่ 12 เดือนหลังผ่าตัด2) ในการทดลองแบบสุ่มที่มีกลุ่มควบคุมหลายศูนย์ในเนเธอร์แลนด์ใน 54 ตา อัตราการบรรลุการมองเห็น 20/25 หรือดีกว่าที่ 12 เดือนหลังผ่าตัดสูงกว่าอย่างมีนัยสำคัญในกลุ่ม DMEK เมื่อเทียบกับกลุ่ม DSAEK (66% เทียบกับ 33%, P=0.02) ในขณะที่ไม่มีความแตกต่างอย่างมีนัยสำคัญในความหนาแน่นของเซลล์บุผนังกระจกตาหรือการเปลี่ยนแปลงค่าสายตา11)
มากกว่าครึ่งหนึ่งของกรณีเกิดขึ้นภายในปีแรกหลังการผ่าตัด โดยเฉพาะระหว่าง 6 เดือนถึง 1 ปี อย่างไรก็ตาม การปฏิเสธสามารถเกิดขึ้นได้แม้หลังจากเวลาผ่านไปนาน ดังนั้นหากมีอาการเช่น ตาแดง มองเห็นไม่ชัด หรือการมองเห็นลดลงหลังจากผ่าตัดหลายปี ผู้ป่วยควรไปพบแพทย์ทันที มีรายงานกรณีการปฏิเสธที่เกิดจากการฉีดวัคซีนหลังจากผ่าตัดมากกว่า 20 ปี10)
อัตราการปฏิเสธของ PKP อยู่ระหว่าง 4.9% ถึง 28.9% ในขณะที่ DMEK เฉลี่ย 1.9% (ช่วง 0-5.9%) ซึ่งต่ำกว่าอย่างมีนัยสำคัญ ความแตกต่างนี้ส่วนใหญ่เกิดจากปริมาณเนื้อเยื่อผู้บริจาคที่ปลูกถ่าย PKP ปลูกถ่ายเยื่อบุผิวและสโตรมาที่มีเซลล์เดนไดรต์ ทำให้มีแอนติเจนสูง ในทางตรงกันข้าม DMEK ปลูกถ่ายเฉพาะเยื่อหุ้มเดสเซเม็ทและเซลล์บุผนังกระจกตา ซึ่งมีแอนติเจนต่ำและไม่ต้องใช้ไหมเย็บ จึงลดความเสี่ยง อย่างไรก็ตาม หลังจากหยุดสเตียรอยด์ การปฏิเสธอาจเกิดขึ้นได้ประมาณ 6% ของกรณี DMEK ดังนั้นการรักษาด้วยสเตียรอยด์ในระยะยาวจึงมีความสำคัญ
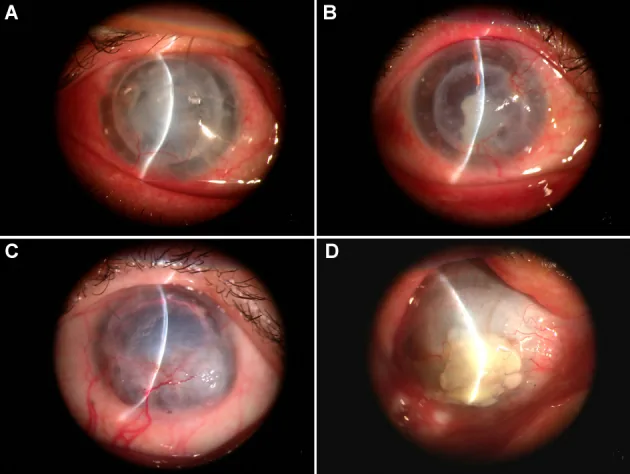
มีอาการตามัว ตาแดง ปวดตา รู้สึกมีสิ่งแปลกปลอม และการมองเห็นลดลง จุดสูงสุดของการเกิดอาการคือ 3 เดือนและ 1 ปีหลังผ่าตัด เมื่อมีอาการควรไปพบแพทย์ทันที
เกณฑ์การวินิจฉัยการปฏิเสธรวมถึง: ตาแดง กลัวแสง การมองเห็นลดลง เซลล์ในช่องหน้าตา ตะกอนที่ผิวด้านหลังกระจกตา (KP) เส้นการปฏิเสธของเอ็นโดทีเลียมหรือเอพิทีเลียม การแทรกซึมใต้เอพิทีเลียม และอาการบวมเฉพาะที่ของ graft1).
KP ที่จำกัดเฉพาะ graft เป็นลักษณะเฉพาะ และไม่พบ KP ที่กระจกตาของผู้รับ เส้น Khodadoust คือตะกอนเป็นเส้นตรงที่ผิวด้านหลังกระจกตา ซึ่งแสดงถึงแนวหน้าของการดำเนินไปของการปฏิเสธชนิดเอ็นโดทีเลียม
การปฏิเสธแบ่งเป็น 3 ชนิดตามชั้นที่ถูกกระทบ: ชนิดเอพิทีเลียม ชนิดสโตรมา และชนิดเอ็นโดทีเลียม ชนิดเอ็นโดทีเลียมมีผลต่อพยากรณ์โรคของ graft มากที่สุด การรักษาที่ล่าช้าทำให้เกิดความล้มเหลวของเอ็นโดทีเลียมแบบถาวรและการมองเห็นลดลง
| ชนิดการปฏิเสธ | ความถี่ | อาการแสดงหลัก |
|---|---|---|
| เอพิทีเลียม | ประมาณ 2% | เส้นนูนที่เคลื่อนจากลิมบัส (epithelial rejection line) |
| สโตรมา | — | อาการบวมของสโตรมาเป็นอาการแสดงเพียงอย่างเดียว |
| ชนิดเยื่อบุโพรง | ประมาณ 50% | KP • เส้น Khodadoust • บวมน้ำ |
การปฏิเสธเยื่อบุผิว (epithelial rejection) พบได้น้อย คิดเป็นประมาณ 2% ของการปฏิเสธทั้งหมด รอยโรคก่อนเกิดคือการแทรกซึมใต้เยื่อบุผิวรูปกลมขนาด 0.2–0.5 มม. ใต้เยื่อบาวแมน เมื่อดำเนินไปจะเกิดรอยโรคเส้นนูนบวมน้ำ (เส้นปฏิเสธเยื่อบุผิว) แทบไม่มีผลต่อการหายใสของ graft แต่สามารถกระตุ้นให้เกิดการปฏิเสธเยื่อบุโพรงได้
การปฏิเสธสโตรมา (stromal rejection) มีเพียงอาการบวมน้ำของสโตรมาเท่านั้น ใน DALK อาจพบการแทรกซึมของสโตรมาและเส้นเลือด新生ที่รอยต่อเป็นการปฏิเสธภูมิคุ้มกันสโตรมา 4) แยกยากจากอาการบวมน้ำของกระจกตาจากการปฏิเสธเยื่อบุโพรงในตา PKP
การปฏิเสธเยื่อบุโพรง (endothelial rejection) คิดเป็นประมาณ 50% ของการปฏิเสธทั้งหมด และสำคัญที่สุดทางคลินิก การเกาะที่ผิวด้านหลังกระจกตาที่จำกัดอยู่ภายใน graft เป็นสิ่งสำคัญ และเมื่อเกิดเป็นเส้น Khodadoust จะมีอาการบวมน้ำของสโตรมาร่วมด้วยในบริเวณนั้น พบชนิดผสม (เยื่อบุผิว + เยื่อบุโพรง) ประมาณ 30%
เส้น Khodadoust คือการเกาะที่ผิวด้านหลังกระจกตาเป็นเส้น ซึ่งเป็นลักษณะเฉพาะของการปฏิเสธเยื่อบุโพรง แสดงถึงแนวหน้าของการดำเนินไปของการปฏิเสธที่เคลื่อนที่ไปเรื่อยๆ บนผิวเยื่อบุโพรงของ graft ในบริเวณที่เส้นผ่าน เซลล์เยื่อบุโพรงจะถูกทำลายทำให้เกิดอาการบวมน้ำของสโตรมา เมื่อพบเส้น Khodadoust ต้องเริ่มการรักษาด้วย steroid ขนาดสูงทันที
| ลักษณะ | การปฏิเสธ | เยื่อบุโพรงอักเสบจาก HSV/VZV | เยื่อบุโพรงอักเสบจาก CMV |
|---|---|---|---|
| การกระจายของ KP | จำกัดอยู่ภายใน graft | เกาะนอก graft ด้วย | เกาะนอก graft ด้วย |
| สีของ KP | ขาวถึงขาวเทา | น้ำตาล | น้ำตาลถึงขาว |
| ลักษณะเฉพาะ | เส้น Khodadoust | สามเหลี่ยมของ Arlt | รอยโรคเหรียญ |
ปฏิกิริยาการปฏิเสธมีลักษณะเด่นคือ KP ที่จำกัดอยู่เฉพาะใน graft ในขณะที่ viral endothelitis จะพบ KP นอก graft ด้วย ซึ่งช่วยในการแยกโรค อย่างไรก็ตาม สารตกตะกอนที่ผิวด้านหลังของกระจกตาอาจมาจาก donor ระหว่างการปลูกถ่ายกระจกตา ดังนั้นการบันทึกการกระจายของ KP ในการตรวจประจำวันจึงมีประโยชน์ในการวินิจฉัยแยกโรค
กรณีที่เกิดปฏิกิริยาการปฏิเสธได้ง่ายหลัง PKP เรียกว่าตาที่มีความเสี่ยงสูง โดยมีปัจจัยดังนี้:
ใน DMEK การปฏิเสธอาจเกิดขึ้นเมื่อลดสเตียรอยด์ ในกรณีหนึ่ง การปฏิเสธเกิดขึ้น 15 เดือนหลัง DMEK เมื่อเปลี่ยนจาก betamethasone เป็น fluorometholone7) การยึดติดของม่านตาส่วนหน้ารอบนอก (PAS) ก็ถูกรายงานว่าเป็นปัจจัยเสี่ยงของการปฏิเสธ DMEK7)
ในการปลูกถ่ายอวัยวะ ประโยชน์ของการจับคู่ HLA ชัดเจน แต่ในการปลูกถ่ายกระจกตา ผลลัพธ์ไม่สอดคล้องกัน1) การศึกษาติดตามผลการปลูกถ่ายกระจกตา II (CTFS II) ที่ดำเนินการในสหราชอาณาจักรเป็นการทดลองทางคลินิกแบบไปข้างหน้าขนาดใหญ่ที่ตรวจสอบผลของการจับคู่ HLA class II (HLA-DR) ใน PKP ความเสี่ยงสูง1) รวบรวมการปลูกถ่าย 1133 รายการตั้งแต่ปี 1998 ถึง 2011 และแบ่งชั้นเป็นกลุ่มที่ไม่ตรงกัน HLA-DR 0, 1 และ 2 ภายใต้เงื่อนไขที่ไม่ตรงกัน HLA class I ≤ 2 แอนติเจน1) ใช้วิธีที่ใช้ DNA (PCR-SSP/PCR-SSO) สำหรับการจำแนกเนื้อเยื่อของผู้บริจาคและผู้รับเพื่อหลีกเลี่ยงข้อผิดพลาดของวิธีทางซีรั่มวิทยา1)
ใน CTFS II ไม่พบความสัมพันธ์ที่ชัดเจนระหว่างจำนวนที่ไม่ตรงกัน HLA-DR กับอัตราการเกิดการปฏิเสธ1) ดังที่แสดงในแบบจำลองสัตว์ฟันแทะ มีวิถีภูมิคุ้มกันที่แตกต่างกันหลายวิถีที่เกี่ยวข้องกับการปฏิเสธการปลูกถ่ายกระจกตา และความซ้ำซ้อนของการตอบสนองทางภูมิคุ้มกันนี้เชื่อว่าเป็นสาเหตุส่วนหนึ่งของความไม่สอดคล้องกันของผลการศึกษาการจับคู่ HLA1)
มีรายงานกรณีการปฏิเสธการปลูกถ่ายกระจกตาหลังการฉีดวัคซีน COVID-19 หลายกรณี พบได้ทั้งในวัคซีน mRNA (BNT162b2) วัคซีนไวรัสเวกเตอร์ (ChAdOx1) และวัคซีนเชื้อตาย (Sinopharm)
มีรายงานผู้ป่วย 2 รายที่มีการปฏิเสธแบบเฉียบพลันของ PKP หลังจากได้รับวัคซีน BNT162b2 ครั้งแรก 2 สัปดาห์6) ทั้งสองรายไม่มีประวัติการปฏิเสธมาก่อน และตอบสนองต่อการรักษาด้วยสเตียรอยด์เฉพาะที่และทั่วร่างกายได้ดี6)
นอกจากนี้ยังมีกรณีการปฏิเสธชั้น内皮 (endothelial rejection) ในการปลูกถ่ายกระจกตาด้วยเลเซอร์ femtosecond หลังจากฉีดวัคซีน ChAdOx1 2 สัปดาห์8) พบ Khodadoust line และการอักเสบในช่องหน้าม่านตา และฟื้นตัวหลังจากรักษาด้วยสเตียรอยด์ 5 สัปดาห์8)
มีรายงานการปฏิเสธหลังจากวัคซีนเชื้อตาย Sinopharm 2 รายเช่นกัน9) การทบทวนวรรณกรรมพบว่ามีการรวบรวมกรณีการปฏิเสธที่เกี่ยวข้องกับวัคซีนอย่างน้อย 20 ราย และส่วนใหญ่ฟื้นตัวด้วยการรักษาด้วยสเตียรอยด์9)
แม้แต่ใน PKP ที่ผ่านการผ่าตัดมานานกว่า 20 ปี ก็เกิดการปฏิเสธ 10 วันหลังจากฉีดวัคซีน BNT162b210)
แม้ว่าความสัมพันธ์เชิงสาเหตุยังไม่ชัดเจน แต่มีสมมติฐานว่าการฉีดวัคซีนอาจกระตุ้นให้เกิดการปฏิเสธผ่านการเหนี่ยวนำเซลล์นำเสนอแอนติเจน MHC class II9)
มีการรายงานการปฏิเสธการปลูกถ่ายกระจกตาหลังการฉีดวัคซีน COVID-19 ทั้งในวัคซีน mRNA, เวกเตอร์ และเชื้อตาย มักเกิดขึ้นภายใน 1-3 สัปดาห์หลังฉีด และส่วนใหญ่ตอบสนองต่อการรักษาด้วยสเตียรอยด์ การวิเคราะห์อภิมานปฏิเสธการปฏิเสธการปลูกถ่ายอวัยวะแข็งเนื่องจากการฉีดวัคซีน แต่สำหรับการปลูกถ่ายกระจกตา ยังคงมีการรวบรวมกรณีศึกษา เนื่องจากความสัมพันธ์เชิงสาเหตุยังไม่แน่นอน ผู้ป่วยปลูกถ่ายกระจกตาควรเพิ่มขนาดสเตียรอยด์ก่อนฉีดวัคซีนและมาตรวจแต่เนิ่นๆ หลังฉีด
ยืนยันการมี KP เฉพาะที่บนเนื้อเยื่อปลูกถ่าย, Khodadoust line, กระจกตาบวมน้ำ และเซลล์ในช่องหน้าม่านตา เส้นการปฏิเสธของเยื่อบุผิวเริ่มต้นใกล้กับหลอดเลือดบริเวณลิมบัสที่คั่งและเคลื่อนผ่านขอบของเนื้อเยื่อปลูกถ่าย
ภาวะหลักที่ต้องแยกจากการปฏิเสธแบบเอ็นโดทีเลียมมีดังนี้
ในการปฏิเสธ ตะกอนจะจำกัดอยู่ภายในกราฟต์ และความดันลูกตาสูงขึ้นพบได้น้อย ในเอ็นโดทีเลียมอักเสบจาก HSV/VZV ตะกอนจะเกาะนอกกราฟต์ด้วย และมีความดันลูกตาสูงขึ้นเฉียบพลันร่วมด้วย ในเอ็นโดทีเลียมอักเสบจาก CMV ตะกอนรูปเหรียญและความดันลูกตาสูงขึ้นเรื้อรังแบบต่อเนื่องเป็นลักษณะเฉพาะ หากยืนยันได้ยาก ให้ทำการตรวจ PCR ของน้ำในช่องหน้า ตรวจแอนติบอดีในซีรั่ม และประเมินการตอบสนองต่อการรักษาด้วยสเตียรอยด์อย่างครอบคลุม
การรักษาภาวะปฏิเสธอาศัยการใช้สเตียรอยด์เพื่อลดการอักเสบ
ระดับเล็กน้อย (ชนิดเยื่อบุผิวหรือเนื้อเยื่อ)
ระดับรุนแรง (ชนิดเยื่อบุผนังหลอดเลือดหรือเส้น Khodadoust บวก)
ด้วยการรักษาตั้งแต่เนิ่นๆ ผู้ป่วยภาวะปฏิเสธแบบเฉียบพลันมากกว่า 50% จะฟื้นตัว ในขณะที่การรักษาที่ล่าช้าจะนำไปสู่การสูญเสียเซลล์เยื่อบุผนังหลอดเลือดอย่างถาวรและ graft ล้มเหลว การให้ความรู้ผู้ป่วยเกี่ยวกับอาการหลังผ่าตัด (ตาแดง ตาพร่า ปวดตา กลัวแสง) และความสำคัญของการมาตรวจแต่เนิ่นๆ เมื่อมีอาการผิดปกติเป็นสิ่งสำคัญ
การจัดการป้องกันภาวะปฏิเสธหลังปลูกถ่ายกระจกตาใช้แนวทางสองขั้นตอนตามการแบ่งระดับความเสี่ยง
การจัดการหลังผ่าตัดสำหรับตาที่มีความเสี่ยงปกติ
ยาหยอดตาสเตียรอยด์: Lindelon 0.01% (betamethasone) 5 ครั้ง/วัน → เปลี่ยนเป็น Flumetron 0.1% (fluorometholone) 2-3 ครั้ง/วัน (ลดขนาดลงทีละน้อยใน 6 เดือน)
การให้ทางระบบ: Prednisone 20 มก. เป็นเวลาหลายวัน หรือไม่ให้
CsA: ใช้ยาหยอดตาร่วม ต่อเนื่องหลายเดือน
การจัดการหลังผ่าตัดสำหรับตาที่มีความเสี่ยงสูง
ยาหยอดตาสเตียรอยด์: Betamethasone 0.1% × 4 ครั้ง/วัน → ต่อเนื่องนานกว่า 1 ปี
สเตียรอยด์ทางระบบ: ฉีด Lindelon 0.4% 2 มก. วันละครั้งทางหลอดเลือดดำเป็นเวลา 3 วันนับจากวันผ่าตัด จากนั้นยาเม็ด Lindelon 0.5 มก. 2 เม็ดแบ่งให้ 2 ครั้ง ลดขนาดลงทีละน้อยใน 2 สัปดาห์
CsA: แคปซูล Neoral 25 มก. 3 มก./กก./วัน ระดับ trough 70-100 นาโนกรัม/มล.
Cyclosporin A (CsA) ใช้ในกรณีที่มีความเสี่ยงสูง เช่น การบุกรุกของหลอดเลือดในสโตรมาของกระจกตาตั้งแต่ 2 ควอดแรนต์ขึ้นไป กรณีปลูกถ่ายซ้ำ และประวัติการปฏิเสธ graft เมื่อให้ทางระบบ ให้รักษาระดับ trough ที่ 70-100 นาโนกรัม/มล. และติดตามผลข้างเคียงทางระบบรวมถึงการทำงานของไต ต่อเนื่องประมาณ 6 เดือนหลังผ่าตัด
ในกรณี PKP ในผู้ป่วยอายุ 18 ปีที่มีการปฏิเสธ graft พร้อมกันทั้งสองข้าง หลังจาก remission ด้วย methylprednisolone ทางหลอดเลือดดำ เนื่องจากมีการตอบสนองต่อสเตียรอยด์ จึงเปลี่ยนเป็นยาหยอดตา CsA 1% และรักษา graft ได้สำเร็จ5) ยาหยอดตา CsA 1% ช่วยให้ลดขนาดสเตียรอยด์ชนิดแรงได้เร็วในผู้ที่ตอบสนองต่อสเตียรอยด์ และมีประโยชน์ในการรักษา graft ในระยะยาว5)
Tacrolimus ใช้เป็นยาทดแทนในกรณีที่เกิดการปฏิเสธ graft ขณะรับประทาน cyclosporin ระดับ trough เป้าหมาย 8-10 นาโนกรัม/มล. จนถึง 2 เดือนหลังผ่าตัด จากนั้น 5-6 นาโนกรัม/มล. (Prograf 0.05-0.1 มก./กก./วัน) มีรายงานว่ายาหยอดตา tacrolimus 0.03% มีประสิทธิภาพในการป้องกันการปฏิเสธ graft ในการปลูกถ่ายกระจกตาที่มีความเสี่ยงสูง
ไหมเย็บที่หลวมหรือขาดอาจกระตุ้นให้เกิดทั้งการปฏิเสธ graft และการติดเชื้อระยะหลัง ดังนั้นควรตัดไหมทันทีเมื่อพบ หลังตัดไหม ให้เพิ่มการรักษาด้วยยาหยอดตาสเตียรอยด์และยาปฏิชีวนะชั่วคราว แม้หลัง remission การใช้ยาหยอดตาสเตียรอยด์ต่อเนื่องระยะยาวสามารถยับยั้งการกลับเป็นซ้ำได้3)
เมื่อเริ่มด้วย betamethasone 0.1% ให้คงระยะ maintenance 4 ครั้ง/วันเป็นเวลาหลายเดือนถึง 1 ปี จากนั้นเปลี่ยนเป็นสเตียรอยด์ความเข้มข้นต่ำ เช่น fluorometholone 0.1% วันละ 1-2 ครั้งเพื่อ maintenance ระยะยาว หากมีความดันลูกตาสูง ให้พิจารณาเปลี่ยนเป็น loteprednol หรือเพิ่มยาหยอดตาต้อหิน
หากมีความดันลูกตาสูงจากการตอบสนองต่อสเตียรอยด์ ให้พิจารณาเปลี่ยนจากเพรดนิโซโลนอะซิเตตเป็นโลเทรดนอลซึ่งมีผลต่อความดันลูกตาน้อยกว่า หรือใช้ร่วมกับยาหยอดตา CsA 1% ยาหยอดตา CsA 1% ช่วยให้ลดสเตียรอยด์ได้เร็ว มีประโยชน์ในการควบคุมความดันลูกตาและระงับการปฏิเสธ นอกจากนี้ยังใช้ยาหยอดตารักษาต้อหินตามความจำเป็น
กระจกตารักษาความทนทานต่อภูมิคุ้มกันทางสรีรวิทยาผ่านการเบี่ยงเบนภูมิคุ้มกันที่เกี่ยวข้องกับช่องหน้าม่านตา (ACAID) ใน ACAID เซลล์นำเสนอแอนติเจนจะกลายเป็นเซลล์ที่ก่อให้เกิดความทนทานในสภาพแวดล้อมที่ TGF-β มีมาก ซึ่งยับยั้งปฏิกิริยาภูมิไวเกินชนิดล่าช้าและการผลิตแอนติบอดีที่จับกับคอมพลีเมนต์ต่อต้านแอนติเจนของผู้บริจาค อย่างไรก็ตาม การมีปัจจัยเสี่ยง เช่น หลอดเลือดใหม่ การอักเสบ และการหย่อนของไหมเย็บ สามารถทำลายเอกสิทธิ์ทางภูมิคุ้มกันนี้ได้ง่าย
กลไกหลักของการปฏิเสธคือ ปฏิกิริยาภูมิไวเกินชนิดล่าช้า และเซลล์เอฟเฟกเตอร์หลักคือ เซลล์ Th1 CD4+ เซลล์ Th1 ที่ถูกกระตุ้นจะผลิต IFN-γ ซึ่งเหนี่ยวนำให้เกิดเซลล์นำเสนอแอนติเจน MHC คลาส II ทั่วทุกชั้นของกระจกตาที่ปลูกถ่าย ทำให้การตอบสนองทางภูมิคุ้มกันแบบเซลล์ดำเนินไป8) บทบาทของกลไกที่อาศัยแอนติบอดีก็ได้รับความสนใจเมื่อเร็วๆ นี้ โดยมีหลักฐานว่าแอนติบอดีต่อต้าน HLA อาจทำให้เกิดความเสียหายต่อเซลล์เอนโดทีเลียมเรื้อรังผ่านการกระตุ้นคอมพลีเมนต์1)
ความแตกต่างของอัตราการปฏิเสธระหว่างเทคนิคการผ่าตัดส่วนใหญ่มาจากปริมาณเนื้อเยื่อผู้บริจาคที่ปลูกถ่ายและความแตกต่างของแอนติเจน3)
การยึดติดของม่านตาส่วนหน้ารอบนอก (PAS) ถูกระบุว่าเป็นปัจจัยเสี่ยงต่อการปฏิเสธหลัง DMEK ในแบบจำลองการปลูกถ่ายกระจกตาในหนู พบว่าการปฏิเสธเพิ่มขึ้นอย่างมีนัยสำคัญในกลุ่มที่มี PAS 7) การสัมผัสโดยตรงระหว่างม่านตาและเอ็นโดทีเลียมของผู้บริจาคจาก PAS เชื่อว่ากระตุ้นการทำงานของลิมโฟไซต์ทีชนิดเป็นพิษต่อเซลล์ และส่งเสริมการปฏิเสธ 7)
การปฏิเสธการปลูกถ่ายกระจกตาส่วนใหญ่ mediated โดยภูมิคุ้มกันแบบเซลล์ แต่การศึกษาในสัตว์ฟันแทะระบุวิถีภูมิคุ้มกันที่แตกต่างกันหลายวิถีที่นำไปสู่การปฏิเสธ 1) ความซ้ำซ้อนของการตอบสนองทางภูมิคุ้มกันนี้เชื่อว่าเป็นสาเหตุหนึ่งที่ทำให้ผลการศึกษาการจับคู่ HLA ไม่สอดคล้องกัน 1) ในระยะหลัง บทบาทของแอนติบอดีต่อต้าน HLA และการปฏิเสธที่ mediated โดยแอนติบอดีได้รับความสนใจ ซึ่งอาจช่วยอธิบายกลไกของความล้มเหลวของเอ็นโดทีเลียมระยะปลาย 1)
การฉีดวัคซีน COVID-19 กระตุ้นการตอบสนองทางภูมิคุ้มกันทั่วร่างกาย ทำให้เกิดแอนติบอดีที่ทำให้ SARS-CoV-2 เป็นกลาง รวมถึงการตอบสนองของเซลล์ T CD8+ และ Th1 CD4+ ที่จำเพาะต่อแอนติเจน 6) การเพิ่มขึ้นของภูมิคุ้มกันนี้อาจกระตุ้นการปฏิเสธต่อกระจกตาที่ปลูกถ่ายผ่านปฏิกิริยาข้ามหรือการกระตุ้นภูมิคุ้มกันแบบไม่จำเพาะ 6) สำหรับวัคซีนเชื้อตาย (Sinopharm) มีข้อเสนอว่าความสามารถในการกระตุ้นภูมิคุ้มกันของอะลูมิเนียมไฮดรอกไซด์ (สารเสริม) เป็นสาเหตุหลักของการปฏิเสธ 9) อย่างไรก็ตาม ในระดับการวิเคราะห์อภิมาน ยังไม่มีการยืนยันการเพิ่มขึ้นของการปฏิเสธหลังการฉีดวัคซีน COVID-19 ในการปลูกถ่ายอวัยวะแข็ง และความสัมพันธ์เชิงสาเหตุในการปลูกถ่ายกระจกตาก็ยังไม่ได้รับการยืนยันในปัจจุบัน
รายงานผู้ป่วยเกี่ยวกับการปฏิเสธการปลูกถ่ายกระจกตาที่เกี่ยวข้องกับวัคซีน COVID-19 สะสมทั่วโลก 9) การทบทวนวรรณกรรมรวบรวมมากกว่า 20 ราย ซึ่งส่วนใหญ่เป็นการปลูกถ่ายซ้ำ เกิดขึ้นภายใน 1-2 สัปดาห์หลังการฉีดวัคซีน และส่วนใหญ่ฟื้นตัวด้วยการรักษาด้วยสเตียรอยด์ 9) มีการเสนอประโยชน์ของการให้สเตียรอยด์ป้องกันก่อนการฉีดวัคซีน แต่ไม่มีการทดลองแบบสุ่มที่มีกลุ่มควบคุม และต้องตัดสินใจเป็นรายกรณี 8)9)
เกี่ยวกับประสิทธิภาพของการจับคู่ HLA การทดลอง CTFS II ได้ตรวจสอบไปข้างหน้า แต่ในปัจจุบันยังไม่มีประโยชน์ทางคลินิกที่ชัดเจนของการจับคู่ HLA-DR ในการปลูกถ่ายกระจกตา 1) อย่างไรก็ตาม บทบาทของแอนติบอดีต่อต้าน HLA และการปฏิเสธที่อาศัยแอนติบอดีกำลังชัดเจนขึ้น ซึ่งอาจช่วยอธิบายกลไกของความล้มเหลวของเอ็นโดทีเลียมระยะหลัง 1)
ในการเปรียบเทียบ UT-DSAEK และ DMEK ทั้งการวิเคราะห์อภิมานของ Sela 2023 2) และการทดลองแบบสุ่มหลายศูนย์ของ Dunker 2020 11) แสดงให้เห็นว่าไม่มีความแตกต่างอย่างมีนัยสำคัญในอัตราการปฏิเสธที่ 12 เดือน ในขณะที่กลุ่ม DMEK มีค่าสายตาที่ดีขึ้น อย่างไรก็ตาม ความล้มเหลวของ graft มีแนวโน้มสูงกว่าเล็กน้อยในกลุ่ม DMEK 2) และการเลือกเทคนิคควรขึ้นอยู่กับสภาพตาของผู้ป่วยแต่ละราย ประวัติ และประสบการณ์ของศูนย์
แนวโน้มในอนาคตต่อไปนี้กำลังได้รับความสนใจ: