رأب القرنية النافذ (PKP)
معدل الرفض: حوالي 4.9-28.9% 7)
السبب الرئيسي للفشل: الرفض (مبكرًا) + فشل البطانة (متأخرًا) 3)
الخصائص: يحتوي على نسيج مانح كامل السمك، وبالتالي أعلى مستضدية

زرع القرنية هو واحد من أكثر عمليات زرع الأعضاء نجاحًا. في زرع القرنية النافذ الأولي (PKP) للعين منخفضة الخطورة، يصل معدل البقاء لمدة 5 سنوات إلى 95%. يرجع هذا النجاح العالي إلى الامتياز المناعي للقرنية.
العوامل المكونة للامتياز المناعي للقرنية هي كما يلي:
ومع ذلك، في العيون عالية الخطورة المصحوبة بتوعية القرنية، قد يتجاوز معدل الفشل في 3 سنوات 35%. حتى في ظل الامتياز المناعي، السبب الأكثر شيوعًا لفشل الطعم هو الرفض المناعي غير القابل للعكس 1).
يشير مصطلح “رفض الطعم” إلى الاستجابة المناعية النوعية للمضيف تجاه القرنية المانحة. فشل الطعم الأولي هو حالة لا تصبح فيها القرنية شفافة خلال 8 أسابيع بعد الجراحة بسبب عيوب في النسيج المانح نفسه، أو صدمة جراحية، أو حفظ غير مناسب، وهو ليس بوساطة مناعية 3). يحدث في حوالي 0.1% من عمليات رأب القرنية النافذ.
يتم تشخيص الرفض فقط للطعم الذي حافظ على شفافيته لمدة أسبوعين على الأقل بعد الجراحة. أكثر من نصف حالات الرفض تحدث خلال السنة الأولى بعد الجراحة، مع ذروة خاصة بين 6 أشهر وسنة واحدة. ومع ذلك، يمكن أن يحدث الرفض بعد أكثر من 20 عامًا من الجراحة. يُبلغ عن معدل التقدم من الرفض إلى الفشل بحوالي 49%.
زرع القرنية هو أكثر أنواع زرع الأنسجة شيوعًا على مستوى العالم، وفي مسح دولي عام 2012، شكل رأب القرنية النافذ حوالي 70% من جميع عمليات زرع القرنية 1). في السنوات الأخيرة، انتشرت عمليات DSAEK و DMEK لأمراض البطانة بسرعة، وأصبح DALK للقرنية المخروطية والندبات بعد التهاب الحمة خيارًا قياسيًا، مما غير نسب العمليات الجراحية بشكل كبير. ومع ذلك، لا يزال رأب القرنية النافذ ضروريًا لعتمات القرنية الواسعة والتشوهات، ويحمل أعلى خطر للرفض 1).
رأب القرنية النافذ (PKP)
معدل الرفض: حوالي 4.9-28.9% 7)
السبب الرئيسي للفشل: الرفض (مبكرًا) + فشل البطانة (متأخرًا) 3)
الخصائص: يحتوي على نسيج مانح كامل السمك، وبالتالي أعلى مستضدية
رأب القرنية الطبقي العميق (DALK)
معدل الرفض: 1-24% 4)
الميزة: يزيل خطر رفض البطانة
التحدي: قد يحدث رفض الحمة 4)
زرع بطانة القرنية (DSAEK)
معدل الرفض: متوسط 10% (نطاق 0-45%)
معدل الفشل الأولي: متوسط 5% (نطاق 0-29%)
الخصائص: لا يوجد فرق كبير مقارنة بـ PKP وفقًا للتقارير3)
زراعة الغشاء الداخلي للقرنية (DMEK)
معدل الرفض: متوسط 1.9% (نطاق 0-5.9%)7)
معدل الفشل الأولي: 1.7%
الخصائص: أقل مستضدية وأقل معدل رفض3)
أظهرت دراسة جماعية كبيرة أن DMEK لديه خطر رفض أقل بكثير مقارنة بـ PKP و DSAEK3). في تحليل تلوي مقارن بين UT-DSAEK و DMEK، لم يكن هناك فرق كبير في خطر الرفض بعد 12 شهرًا من الجراحة2). في تجربة عشوائية متعددة المراكز في هولندا شملت 54 عينًا، كان معدل تحقيق رؤية 20/25 أو أفضل بعد 12 شهرًا أعلى بكثير في مجموعة DMEK مقارنة بمجموعة DSAEK (66% مقابل 33%، P=0.02)، بينما لم يكن هناك فرق كبير في كثافة الخلايا البطانية أو التغير الانكساري11).
أكثر من نصف الحالات تحدث خلال السنة الأولى بعد الجراحة، خاصة بين 6 أشهر وسنة. ومع ذلك، يمكن أن يحدث الرفض حتى بعد فترة طويلة، لذلك إذا ظهرت أعراض مثل الاحمرار أو عدم وضوح الرؤية أو انخفاض حدة البصر بعد سنوات من الجراحة، يجب مراجعة الطبيب فورًا. هناك تقارير عن حالات رفض حدثت بعد أكثر من 20 عامًا من الجراحة بسبب التطعيم10).
معدل الرفض في PKP يتراوح بين 4.9% و 28.9%، بينما في DMEK يبلغ متوسطه 1.9% (نطاق 0-5.9%)، وهو أقل بكثير. يرجع هذا الاختلاف بشكل أساسي إلى كمية الأنسجة المزروعة. في PKP، تُزرع أيضًا الظهارة والسدى التي تحتوي على خلايا شجرية، مما يزيد من المستضدية. في المقابل، في DMEK، يُزرع فقط الغشاء الداخلي والبطانية، مما يقلل المستضدية ولا حاجة للخيوط الجراحية، مما يقلل الخطر. ومع ذلك، بعد إيقاف الستيرويدات، قد يحدث رفض في حوالي 6% من حالات DMEK، لذا فإن الاستمرار في استخدام الستيرويدات على المدى الطويل مهم.
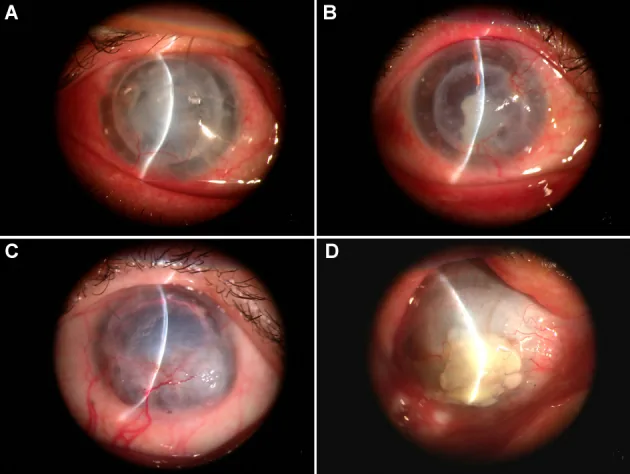
يظهر ضباب الرؤية، احمرار العين، ألم العين، الإحساس بوجود جسم غريب، وانخفاض حدة البصر. توجد ذروتان للإصابة بعد 3 أشهر وسنة واحدة من الجراحة. عند ظهور الأعراض، يجب مراجعة الطبيب فورًا.
تشمل معايير تشخيص الرفض: احمرار العين، رهاب الضوء، انخفاض حدة البصر، خلايا في الغرفة الأمامية، ترسبات على السطح الخلفي للقرنية (KP)، خط رفض البطانة أو الظهارة، ارتشاح تحت الظهارة، وذمة الطعم الموضعية1).
تعتبر ترسبات KP الموضعية في الطعم مميزة، ولا توجد KP في قرنية المتلقي. خط خودادوست (Khodadoust line) هو ترسبات خطية على السطح الخلفي للقرنية، ويمثل جبهة تقدم رفض البطانة.
يصنف الرفض إلى ثلاثة أنواع حسب الطبقة المصابة: الظهاري، اللحمي، البطاني. النوع البطاني هو الأكثر تأثيرًا على بقاء الطعم، وتأخير العلاج يؤدي إلى فشل بطاني لا رجعة فيه وانخفاض حدة البصر.
| نوع الرفض | التكرار | العلامات الرئيسية |
|---|---|---|
| الظهاري | حوالي 2% | خط مرتفع يتحرك من الحوف (خط رفض ظهاري) |
| اللحمي | — | الوذمة اللحمية هي العلامة الوحيدة |
| نوع بطاني | حوالي 50% | KP • خط خودادوست • وذمة |
رفض ظهاري (epithelial rejection) نادر الحدوث، حيث يمثل حوالي 2% من حالات الرفض. كآفة أولية، تُلاحظ ارتشاحات تحت ظهارية دائرية بقطر 0.2-0.5 مم تحت غشاء بومان. مع التقدم، تتشكل آفة خطية مرتفعة وذمية (خط الرفض الظهاري). لا تؤثر بشكل كبير على شفاء الطعم نفسه، ولكنها قد تكون محفزًا للرفض البطاني.
رفض سدوي (stromal rejection) يتمثل العرض الوحيد فيه في وذمة السدى. في عملية رأب القرنية العميق (DALK)، قد يُلاحظ ارتشاح سدوي وأوعية دموية جديدة في الواجهة كرفض مناعي سدوي 4). يصعب تمييزه عن وذمة القرنية الناتجة عن الرفض البطاني في عين خضعت لعملية رأب القرنية النافذ (PKP).
رفض بطاني (endothelial rejection) يمثل حوالي 50% من حالات الرفض، وهو الأهم سريريًا. الترسبات الخلفية للقرنية المحدودة داخل الطعم هي علامة مهمة، وعندما تشكل خط خودادوست، تكون مصحوبة بوذمة سدوية في نفس المنطقة. يُلاحظ النوع المختلط (ظهاري + بطاني) في حوالي 30% من الحالات.
خط خودادوست هو ترسب خلفي للقرنية خطي مميز للرفض البطاني. يمثل جبهة تقدم الرفض التي تتحرك تدريجيًا عبر سطح بطانية الطعم، وفي المناطق التي يمر بها الخط، تتضرر الخلايا البطانية مما يسبب وذمة سدوية. عند ملاحظة خط خودادوست، يجب البدء فورًا بعلاج ستيرويدي قوي.
| العلامة | رفض | التهاب بطاني هربسي (HSV/VZV) | التهاب بطاني مضخم للخلايا (CMV) |
|---|---|---|---|
| توزع KP | محدود داخل الطعم | يترسب خارج الطعم أيضًا | يترسب خارج الطعم أيضًا |
| لون KP | أبيض إلى رمادي-أبيض | بني | بني إلى أبيض |
| العلامات المميزة | خط خدودوست | مثلث آرلت | آفة عملة |
إن رد الرفض يتميز بوجود KP مقتصر على الطعم، بينما يظهر التهاب البطانة الفيروسي KP خارج الطعم أيضًا، مما يساعد في التمييز. تجدر الإشارة إلى أن الترسبات الخلفية للقرنية قد تكون من المتبرع عند زرع القرنية، لذا فإن تسجيل توزيع KP أثناء الفحص اليومي مفيد في التشخيص التفريقي.
تسمى الحالات التي يحدث فيها رد رفض بسهولة بعد PKP بالعين عالية الخطورة، وتشمل العوامل التالية:
في DMEK، يمكن أن يحدث الرفض عند تقليل الستيرويدات. في إحدى الحالات، حدث الرفض بعد 15 شهرًا من DMEK عند التحول من البيتاميثازون إلى الفلوروميثولون7). كما تم الإبلاغ عن التصاق القزحية الأمامي المحيطي (PAS) كعامل خطر لرفض DMEK7).
في زراعة الأعضاء، تكون فائدة توافق HLA واضحة، لكن في زراعة القرنية، النتائج غير متسقة1). دراسة متابعة زراعة القرنية II (CTFS II) التي أجريت في المملكة المتحدة هي تجربة سريرية كبيرة استباقية فحصت تأثير توافق HLA class II (HLA-DR) في PKP عالي الخطورة1). جمعت 1133 عملية زرع من 1998 إلى 2011، وتم تقسيمها إلى مجموعات 0 و1 و2 عدم تطابق HLA-DR تحت شرط عدم تطابق HLA class I ≤ 2 مستضدات1). تم استخدام طرق قائمة على الحمض النووي (PCR-SSP/PCR-SSO) للتنميط النسيجي للمتبرع والمتلقي لتجنب أخطاء الطرق المصلية1).
في CTFS II، لم تظهر علاقة واضحة بين عدد عدم تطابق HLA-DR ومعدل حدوث الرفض1). كما هو موضح في نماذج القوارض، تشارك مسارات مناعية متعددة ومختلفة في رفض زراعة القرنية، ويعتقد أن هذه التكرارية في الاستجابة المناعية تفسر جزئيًا عدم اتساق نتائج دراسات توافق HLA1).
تم الإبلاغ عن عدة حالات من رفض زرع القرنية بعد التطعيم ضد كوفيد-19. لوحظ حدوث ذلك مع لقاح mRNA (BNT162b2)، ولقاح الناقل الفيروسي (ChAdOx1)، واللقاح المعطل (Sinopharm).
تم الإبلاغ عن حالتين من الرفض الحاد لزرع القرنية النافذ (PKP) بعد أسبوعين من الجرعة الأولى من لقاح BNT162b26). لم يكن لدى أي منهما تاريخ سابق للرفض، واستجابتا بشكل جيد للعلاج بالستيرويدات الموضعية والجهازية6).
هناك أيضًا حالة من رفض البطانة لزرع القرنية بليزر الفيمتو ثانية بعد أسبوعين من تلقي لقاح ChAdOx18). لوحظ خط خودادوست والتهاب في الغرفة الأمامية، وتعافت الحالة بعد 5 أسابيع من العلاج بالستيرويدات8).
تم الإبلاغ أيضًا عن حالتين من الرفض بعد لقاح Sinopharm المعطل9). تشير مراجعة الأدبيات إلى تجميع ما لا يقل عن 20 حالة من الرفض المرتبط باللقاح، وقد تعافت الغالبية العظمى بالعلاج بالستيرويدات9).
حتى في حالات زرع القرنية النافذ (PKP) التي مضى عليها أكثر من 20 عامًا، حدث رفض بعد 10 أيام من تلقي لقاح BNT162b210).
على الرغم من أن العلاقة السببية غير مؤكدة، فقد تم اقتراح فرضية أن التطعيم قد يحفز الرفض من خلال تحفيز الخلايا المقدمة للمستضد من الفئة الثانية من معقد التوافق النسيجي الرئيسي (MHC class II)9).
تم الإبلاغ عن رفض زرع القرنية بعد التطعيم ضد كوفيد-19 مع كل من لقاحات mRNA والناقل الفيروسي واللقاحات المعطلة. غالبًا ما يحدث بعد 1-3 أسابيع من التطعيم، وتستجيب الغالبية العظمى للعلاج بالستيرويدات. في التحليل التلوي، تم نفي رفض زرع الأعضاء الصلبة بسبب التطعيم، لكن بالنسبة لزرع القرنية، لا تزال الحالات قيد التجميع. نظرًا لأن العلاقة السببية غير مؤكدة، يُوصى لمرضى زرع القرنية بزيادة جرعة الستيرويدات قبل التطعيم والمراجعة المبكرة بعد التطعيم.
يتم تأكيد وجود الترسبات القرنية الموضعية في الطعم، وخط خودادوست، ووذمة القرنية، وخلايا في الغرفة الأمامية. يبدأ خط الرفض الظهاري بالقرب من الأوعية الليمبية المحتقنة ويتحرك عبر حدود الطعم.
الحالات الرئيسية التي تتطلب التمييز عن رفض البطانة هي كما يلي.
في الرفض، تكون الترسبات موضعية داخل الطعم، ومن غير المحتمل حدوث ارتفاع في ضغط العين. في التهاب بطانة القرنية بفيروس الهربس البسيط/النطاقي الحماقي، تلتصق الترسبات خارج الطعم أيضًا ويصاحبها ارتفاع حاد في ضغط العين. في التهاب بطانة القرنية بالفيروس المضخم للخلايا، تكون الترسبات على شكل عملة معدنية وارتفاع مزمن ومستمر في ضغط العين. إذا كان التأكيد صعبًا، يتم إجراء اختبار PCR لخلط الغرفة الأمامية واختبار الأجسام المضادة في الدم وتقييم الاستجابة للعلاج بالستيرويد بشكل شامل.
يعتمد علاج رفض الطعم على استخدام الستيرويدات لتخفيف الالتهاب.
الحالات الخفيفة (النوع الظهاري أو النسيجي)
الحالات الشديدة (النوع البطاني أو خط خودادوست الإيجابي)
مع العلاج المبكر، يتعافى أكثر من 50% من حالات رفض الطعم الحاد، بينما يؤدي التأخير في بدء العلاج إلى فقدان لا رجعة فيه للخلايا البطانية وفشل الطعم. من المهم تثقيف المرضى حول الأعراض الذاتية بعد الجراحة (احمرار، ضبابية الرؤية، ألم العين، رهاب الضوء) والتأكيد على ضرورة المراجعة المبكرة عند حدوث أي تغيير.
تستخدم بروتوكولات من مرحلتين للوقاية من رفض الطعم بعد زراعة القرنية، بناءً على تصنيف المخاطر.
إدارة ما بعد الجراحة للعين ذات المخاطر الطبيعية
قطرات الستيرويد: قطرات لينديرون 0.01% (بيتاميثازون) 5 مرات يوميًا → التحول إلى قطرات فوميترون 0.1% (فلوروميثولون) 2-3 مرات يوميًا (التقليل التدريجي على مدى 6 أشهر)
العلاج الجهازي: بريدنيزون 20 ملغ لعدة أيام، أو بدون علاج
CsA: استخدام قطرات العين بالتزامن، يستمر لعدة أشهر
إدارة ما بعد الجراحة للعين عالية الخطورة
قطرات الستيرويد: بيتاميثازون 0.1% × 4 مرات/يوم → يستمر لأكثر من عام
الستيرويد الجهازي: حقن لينديرون 0.4% 2 ملغ مرة واحدة يوميًا وريدياً لمدة 3 أيام من يوم الجراحة، ثم أقراص لينديرون 0.5 ملغ قرصين مقسمين على جرعتين مع التقليل التدريجي على مدى أسبوعين
CsA: كبسولات نيورال 25 ملغ 3 ملغ/كغ/يوم، مستوى القاع 70-100 نانوغرام/مل
السيكلوسبورين A (CsA) يُستخدم في الحالات عالية الخطورة مثل غزو الأوعية الدموية في سدى القرنية في رباعين أو أكثر، وحالات إعادة الزرع، وتاريخ رفض الطعم. عند تناوله جهازيًا، يُحافظ على مستوى القاع عند 70-100 نانوغرام/مل، وتتم مراقبة الآثار الجانبية الجهازية بما في ذلك وظائف الكلى. يستمر العلاج لمدة 6 أشهر تقريبًا بعد الجراحة.
في حالة PKP لمريض يبلغ من العمر 18 عامًا يعاني من رفض ثنائي متزامن، بعد الشفاء باستخدام جرعة ميثيل بريدنيزولون الوريدية، تم التحول إلى قطرات CsA 1% بسبب استجابة الستيرويد، ونجح الحفاظ على الطعم5). قطرات CsA 1% تسمح بالتقليل التدريجي المبكر للستيرويدات القوية لدى المستجيبين للستيرويد، وهي مفيدة للحفاظ على الطعم على المدى الطويل5).
التاكروليموس يُستخدم كدواء بديل للحالات التي تطور رفضًا أثناء تناول السيكلوسبورين الفموي. مستوى القاع المستهدف هو 8-10 نانوغرام/مل حتى شهرين بعد الجراحة، ثم 5-6 نانوغرام/مل بعد ذلك (بروغراف 0.05-0.1 ملغ/كغ/يوم). هناك تقارير تفيد بأن قطرات التاكروليموس 0.03% فعالة في الوقاية من رفض الطعم في زراعة القرنية عالية الخطورة.
ارتخاء الخيوط الجراحية أو كسرها يمكن أن يؤدي إلى كل من رفض الطعم والعدوى المتأخرة، لذلك يجب إزالتها فور اكتشافها. بعد إزالة الخيط، يتم تعزيز العلاج بقطرات الستيرويد والمضادات الحيوية مؤقتًا. حتى بعد الشفاء، يمكن أن يساعد الاستمرار طويل المدى في قطرات الستيرويد في منع الانتكاس3).
عند البدء بالبيتاميثازون 0.1%، تستمر مرحلة الصيانة 4 مرات يوميًا لعدة أشهر إلى عام، ثم يتم التحول إلى ستيرويد منخفض التركيز مثل فلوروميثولون 0.1% بجرعة 1-2 مرات يوميًا للصيانة طويلة المدى. في حالة ارتفاع ضغط العين، يُنظر في التبديل إلى لوتيبريدنول أو إضافة قطرات الجلوكوما.
في حالة ارتفاع ضغط العين بسبب الاستجابة للستيرويدات، يُنظر في التحول من بريدنيزولون أسيتات إلى لوتيبردنول الأقل تأثيرًا على ضغط العين، أو استخدامه مع قطرات السيكلوسبورين 1%. قطرات السيكلوسبورين 1% تسمح بتقليل الستيرويدات مبكرًا، مما يساعد في التحكم بضغط العين وقمع الرفض. كما تُستخدم قطرات الجلوكوما حسب الحاجة.
تحافظ القرنية على التحمل المناعي الفسيولوجي من خلال انحراف المناعة المرتبط بالغرفة الأمامية (ACAID). في ACAID، تصبح الخلايا المقدمة للمستضد مولدة للتسامح في بيئة يغلب عليها TGF-β، مما يثبط فرط الحساسية المتأخر وإنتاج الأجسام المضادة المثبتة للمتممة ضد مستضدات المتبرع. لكن وجود عوامل خطر مثل الأوعية الدموية الجديدة والالتهاب وارتخاء الغرز يؤدي بسهولة إلى انهيار هذا الامتياز المناعي.
الآلية المركزية للرفض هي فرط الحساسية المتأخر، والخلايا المستجيبة الرئيسية هي خلايا Th1 CD4+. تنتج خلايا Th1 المنشطة IFN-γ، مما يحفز ظهور خلايا مقدمة للمستضد من الفئة الثانية MHC في جميع طبقات القرنية المزروعة، ويتقدم الاستجابة المناعية الخلوية8). كما أن دور الآليات الوسيطة بالأجسام المضادة يحظى باهتمام مؤخرًا، حيث تشير الأدلة إلى أن الأجسام المضادة لـ HLA قد تسبب تلفًا بطانيًا مزمنًا عبر تنشيط المتممة1).
يعود اختلاف معدلات الرفض بين التقنيات الجراحية بشكل رئيسي إلى كمية الأنسجة المزروعة من المتبرع واختلاف مستضديتها3).
يُعتبر التصاق القزحية الأمامي المحيطي (PAS) عامل خطر لرفض الطعم بعد DMEK. في نموذج زرع القرنية في الفئران، زاد الرفض بشكل ملحوظ في المجموعة التي تعاني من PAS 7). يُعتقد أن الاتصال المباشر بين القزحية وبطانة المتبرع الناتج عن PAS يحفز نشاط الخلايا اللمفاوية التائية السامة للخلايا، مما يعزز رفض الطعم 7).
رفض زرع القرنية يتوسطه بشكل رئيسي المناعة الخلوية، لكن الدراسات على القوارض حددت مسارات مناعية متعددة تؤدي إلى الرفض 1). يُعتقد أن هذا التكرار في الاستجابة المناعية هو أحد أسباب عدم اتساق نتائج دراسات مطابقة HLA 1). في الآونة الأخيرة، يزداد الاهتمام بدور الأجسام المضادة لـ HLA والرفض بوساطة الأجسام المضادة، مما قد يساعد في فهم آليات فشل البطانة المتأخر 1).
يحفز التطعيم ضد COVID-19 استجابة مناعية جهازية، مما يؤدي إلى إنتاج أجسام مضادة معادلة لـ SARS-CoV-2 بالإضافة إلى استجابات الخلايا التائية CD8+ و Th1 CD4+ الخاصة بالمستضد 6). يمكن أن يؤدي هذا التنشيط المناعي إلى تحفيز رفض الطعم عبر تفاعل تبادلي مع قرنية المتبرع أو تنشيط مناعي غير محدد 6). بالنسبة للقاح المعطل (Sinopharm)، يُقترح أن تكون المناعة الناتجة عن هيدروكسيد الألومنيوم (المادة المساعدة) هي السبب الرئيسي للرفض 9). ومع ذلك، لم يتم تأكيد زيادة رفض الطعم بعد التطعيم ضد COVID-19 في زراعة الأعضاء الصلبة على مستوى التحليل التلوي، كما أن العلاقة السببية في زرع القرنية لم تثبت بعد.
تراكمت تقارير الحالات العالمية حول رفض زراعة القرنية المرتبط بلقاح COVID-19 9). كشفت مراجعة الأدبيات عن تجميع أكثر من 20 حالة، معظمها حالات إعادة زرع، وتحدث في غضون 1-2 أسبوع بعد التطعيم، وتتعافى معظمها بالعلاج بالستيرويدات 9). تم اقتراح فائدة العلاج الوقائي بالستيرويدات قبل التطعيم، لكن لا توجد تجارب عشوائية محكومة، ويجب اتخاذ القرار بشكل فردي لكل حالة 8)9).
أما بالنسبة لفعالية توافق HLA، فقد فحصتها تجربة CTFS II بشكل استباقي، لكن في الوقت الحالي لم تظهر فائدة سريرية واضحة لتوافق HLA-DR في زراعة القرنية 1). ومع ذلك، يتضح دور الأجسام المضادة لـ HLA ورفض الوساطة المضادة، مما قد يساهم في توضيح آلية فشل البطانة المتأخر 1).
في مقارنة UT-DSAEK و DMEK، أظهر كل من التحليل التلوي لـ Sela 2023 2) والتجربة العشوائية متعددة المراكز لـ Dunker 2020 11) عدم وجود فرق كبير في معدل الرفض لمدة 12 شهرًا، بينما أظهرت مجموعة DMEK حدة بصرية مصححة أفضل. ومع ذلك، كان فشل الطعم أكثر شيوعًا في مجموعة DMEK 2)، ويجب أن يعتمد اختيار التقنية على حالة العين الفردية والتاريخ وخبرة المركز.
الاتجاهات المستقبلية التالية تحظى بالاهتمام: